ņä£ ļĪĀ
AcetazolamideļŖö Ēāäņé░ĒāłņłśĒÜ©ņåī ņ¢ĄņĀ£ņĀ£(carbonic anhydrase inhibitor)ļĪ£, ņŗĀļć©ņäĖĻ┤ĆņŚÉņä£ ņżæĒāäņé░Ļ│╝ ļéśĒŖĖļź©ņØś ņ×¼ĒØĪņłśņŚÉ Ļ┤ĆņŚ¼ĒĢśļŖö Ēāäņé░ĒāłņłśĒÜ©ņåīļź╝ ņ¢ĄņĀ£ĒĢśņŚ¼ ņØ┤ļć©ņĀ£ņØś ĻĖ░ļŖźņØä ĒĢ£ļŗż[1]. ļśÉĒĢ£, ļģ╣ļé┤ņן ĒÖśņ×ÉņØś ņĢłņĢĢņØä ļ¢©ņ¢┤ļ£©ļ”¼ĻĖ░ ņ£äĒĢ┤ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ņ£╝ļ®░, Ļ░äņ¦ł ļ░£ņ×æ, ņ¢æņä▒ ļæÉĻ░£ ļé┤ņĢĢ ĒĢŁņ¦ä, Ļ│Āņé░ļ│æ, ņłśļ®┤ ļ¼┤ĒśĖĒØĪņ”Ø ļō▒ņØä ņ╣śļŻīĒĢśļŖö ļŹ░ņŚÉļÅä ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŗż[1,2]. ļČĆņ×æņÜ®ņ£╝ļĪ£ Ļ░ÉĻ░ü ļ¦łļ╣ä, ņåÉĻ░ĆļØĮņØ┤ļéś ļ░£Ļ░ĆļØĮņØś ņĀĆļ”░Ļ░É, Ļ▓░ņäØ ļō▒ņØä ņØ╝ņ£╝Ēé¼ ņłś ņ׳ņ£╝ļ®░, ņŗĀņןĻĖ░ļŖźņØ┤ ņĀĆĒĢśļÉ£ ĒÖśņ×ÉņŚÉņä£ ļīĆņé¼ņä▒ ņé░ņ”ØņØ┤ļéś ĻĖēņä▒ņŗĀļČĆņĀäņØä ņØ╝ņ£╝Ēé¼ ņłś ņ׳ņ£╝ļ»ĆļĪ£ ņŻ╝ņØśĒĢ┤ņä£ ņé¼ņÜ®ĒĢ┤ņĢ╝ ĒĢśļŖö ņĢĮļ¼╝ņØ┤ļŗż[3,4]. ĻĘĖļ¤¼ļéś ņĢäņ¦üĻ╣īņ¦Ć ņØ┤ ņĢĮļ¼╝ņŚÉ ņØśĒĢ┤ ņĀĢņāü ņŗĀĻĖ░ļŖźņŚÉņä£ ĻĖēņä▒ņŗĀļČĆņĀäņØä ņØ╝ņ£╝Ēé© ņśłļŖö ĻĄŁļé┤ņŚÉ Ļ▒░ņØś ņĢīļĀżņĀĖ ņ׳ņ¦Ć ņĢŖļŗż. ņØ┤ņŚÉ ņĀĆņ×ÉļōżņØĆ ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ ņĢłņĢĢņØä ņĪ░ņĀłĒĢśĻĖ░ ņ£äĒĢ┤ ņ£Āņ¦Ć ņÜ®ļ¤ēņØś acetazolamideļź╝ ņé¼ņÜ®Ē¢łļŹś ĒÖśņ×ÉņŚÉņä£ Ēśłņןļ¤ēņØś ņŗ¼ĒĢ£ Ļ░Éņåī ņŚåņØ┤ ļīĆņé¼ņä▒ņé░ņ”ØĻ│╝ ĒĢ©Ļ╗ś ĒĢŹļć©ņä▒ ĻĖēņä▒ņŗĀļČĆņĀäņØ┤ ļ░£ņāØĒĢśņŚ¼ ĒśłņĢĪĒł¼ņäØņ£╝ļĪ£ ņ╣śļŻīĒĢ£ ņśłļź╝ Ļ▓ĮĒŚśĒĢśņśĆĻĖ░ņŚÉ ņØ┤ļź╝ ļ¼ĖĒŚīĻ│Āņ░░Ļ│╝ ĒĢ©Ļ╗ś ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ņ”Ø ļĪĆ
ĒÖś ņ×É: 55ņäĖ, ņŚ¼ņ×É
ņŻ╝ ņåī: 3ņØ╝ ņĀäļČĆĒä░ ņŗ£ņ×æļÉ£ ņĀäņŗĀ ņćĀņĢĮĻ░É ļ░Å ņśżņŗ¼, ĻĄ¼ĒåĀ
Ēśäļ│æļĀź: ĒÅēņåīņŚÉ ņŗĀĻĖ░ļŖźņØĆ ņĀĢņāüņØ┤ņŚłņ£╝ļ®░, ļé┤ņøÉ ĒĢ£ ļŗ¼ ņĀä ļŗżļŗłļŹś ļ│æņøÉņŚÉņä£ ņĖĪņĀĢĒĢ£ BUN/CrļÅä 14/1.0 mg/dLņśĆļŗż. 2ņŻ╝ ņĀä ļČĆĒä░ļŖö ļģ╣ļé┤ņןņØä ņ¦äļŗ©ļ░øĻ│Ā acetazolamideļź╝ 250 mgņö® ĒĢśļŻ©ņŚÉ ļæÉ ļ▓ł ļ│ĄņÜ®ĒĢśņśĆļŗż. ļ│ĄņÜ® ņØ╝ņŻ╝ņØ╝ ĒøäļČĆĒä░ ņŗØņÜĢņØ┤ ļ¢©ņ¢┤ņ¦ĆĻ│Ā ņś©ļ¬ĖņŚÉ ĒלņØ┤ ņŚåņŚłņ£╝ļ®░, ļ│æņøÉ ļ░®ļ¼Ė 3ņØ╝ ņĀäļČĆĒä░ļŖö ņåīļ│Ć ņ¢æņØ┤ ņżäņ¢┤ļōżļ®┤ņä£ ņśżņŗ¼Ļ│╝ ĻĄ¼ĒåĀĻ░Ć ļÅÖļ░śļÉśņŚłĻ│Ā ļ░®ļ¼Ė ļŗ╣ņØ╝ņŚÉļŖö ņŚēļÜ▒ĒĢ£ ļ¦ÉņØä ĒĢśņŚ¼ ņÖĖļČĆ ļ│æņøÉņŚÉ ļ░®ļ¼ĖĒĢśņśĆĻ│Ā, ĻĖēņä▒ņŗĀļČĆņĀäĻ│╝ ņÜöļÅģņ”ØņØä ņ¦äļŗ©ļ░øĻ│Ā ņØæĻĖē ĒśłņĢĪĒł¼ņäØņØä ņŗ£Ē¢ēĒĢ£ Ēøä ļ│ĖņøÉņ£╝ļĪ£ ņĀäņøÉļÉśņŚłļŗż.
Ļ│╝Ļ▒░ļĀź: 20ļģä ņĀä ļŗ╣ļć©ļ│æņØä ņ¦äļŗ©ļ░øņĢśņ£╝ļ®░ Ļ▓ĮĻĄ¼ Ēśłļŗ╣ Ļ░ĢĒĢśņĀ£(glimepiride 2 mg/day, metformin 1,700 mg/day)ļź╝ ļ│ĄņÜ®ĒĢśņśĆļŗż.
Ļ░ĆņĪ▒ļĀź: ĒŖ╣ņØ┤ņé¼ĒĢŁņØĆ ņŚåņŚłļŗż.
ņ¦äņ░░ ņåīĻ▓¼: ĒśłņĢĢ 140/90 mmHg, ļ¦źļ░Ģņłś 78ĒÜī/ļČä, ĒśĖĒØĪ 20ĒÜī/ļČä, ņ▓┤ņś© 37.1ŌäāņśĆļŗż. ĻĖēņä▒ ļ│æņāēņØä ļ│┤ņśĆņ£╝ļ®░ ņÖĖļČĆ ļ│æņøÉņŚÉņä£ļŖö ņØśņŗØņĀĆĒĢśĻ░Ć ņ׳ņŚłņ£╝ļéś ļ│ĖņøÉņŚÉ ļÅäņ░®ĒĢ┤ņä£ļŖö ņØśņŗØņØ┤ ļ¬ģļŻīĒĢśņśĆļŗż. Ēö╝ļČĆĻĖ┤ņןļÅäļŖö ņĀĢņāüņØ┤ņŚłĻ│Ā, ĻĄ¼Ļ░ĢņĀÉļ¦ēļÅä ņĀĢņāüņØ┤ņŚłļŗż. Ēö╝ļČĆ ļ│æļ│ĆņØĆ ņŚåņŚłņ£╝ļ®░, Ļ▓ĮļČĆ ļ”╝ĒöäņĀłņØĆ ļ¦īņĀĖņ¦Ćņ¦Ć ņĢŖņĢśĻ│Ā Ļ▓░ļ¦ēņØĆ ņ░Įļ░▒ĒĢśņ¦Ć ņĢŖņĢśĻ│Ā Ļ│Ąļ¦ēņŚÉ ĒÖ®ļŗ¼ņåīĻ▓¼ņØĆ ņŚåņŚłļŗż. ņĀäņŗĀņŚÉ ļČĆņóģļÅä ņŚåņŚłņ£╝ļ®░ Ļ░ĆņŖ┤ņ¦äņ░░ņŚÉņä£ļÅä ņŗ¼ņØīņØ┤ļéś ĒÅÉņØīņØĆ ņĀĢņāüņØ┤ņŚłĻ│Ā ļ│ĄļČĆ ņ¦äņ░░ņŚÉņä£ļÅä ņןņØīņØĆ ņĀĢņāüņĀüņØ┤ņŚłĻ│Ā Ļ░äņØ┤ļéś ļ╣äņןņØĆ ļ¦īņĀĖņ¦Ćņ¦Ć ņĢŖņĢśņ£╝ļ®░ ņĢĢĒåĄņØ┤ļéś ļ░śņé¼ĒåĄļÅä ņŚåņŚłļŗż. ļŖæĻ│©ņ▓ÖņČöĻ░üņĢĢĒåĄ ļ░Å ņĀĢĻ░ĢņØ┤ ņĢ×ņ¬Į ļČĆņ£äņØś ļČĆņóģļÅä ņŚåņŚłļŗż.
Ļ▓Ćņé¼ ņåīĻ▓¼: ņÖĖļČĆ ļ│æņøÉņŚÉņä£ ņŗ£Ē¢ēĒĢ£ Ļ▓Ćņé¼ļŖö Ēśłņ▓Ł ļéśĒŖĖļź© 132 mEq/L, ņ╣╝ļź© 8.3 mEq/L, ņŚ╝ņåī 103 mEq/LņśĆĻ│Ā, ļÅÖļ¦źĒśł Ļ░ĆņŖżļČäņäØ Ļ▓Ćņé¼ Ļ▓░Ļ│╝ pH 7.02, PCO2 27 mmHg, PO2 135 mmHg, HCO3- 7.0 mmol/LņśĆĻ│Ā, Ēśłņ▓Ł ņØīņØ┤ņś©ņ░©ļŖö 22 mEq/LņśĆļŗż. ĒÖöĒĢÖĻ▓Ćņé¼ Ļ▓░Ļ│╝ Ēśłņ▓Ł ņ╣╝ņŖśĻ│╝ ņØĖņØ┤ 8.2 mg/dL, 9.4 mg/dLņśĆĻ│Ā, ĒśłņżæņÜöņåīņ¦łņåīļŖö 65 mg/dL, Ēü¼ļĀłņĢäĒŗ░ļŗīņØĆ 9.1 mg/dLņśĆĻ│Ā, ņ┤Ø ļŗ©ļ░▒ņ¦łĻ│╝ ņĢīļČĆļ»╝ņØĆ 6.2 g/dL, 4.1 g/dLņśĆņ£╝ļ®░, AST 28 IU/L, ALT 9 IU/L, ņ┤Ø ļ╣īļ”¼ļŻ©ļ╣łņØĆ 0.8 mg/dL, ņĢīņ╣╝ļ”¼ņä▒ ĒāłņØĖņé░ĒÖöĒÜ©ņåīļŖö 41 IU/LņśĆĻ│Ā, Ēśłņ▓Ł ĒżļÅäļŗ╣ņØĆ 198 mg/dLņśĆļŗż. ņØ╝ļ░śĒśłņĢĪĻ▓Ćņé¼ņŚÉņä£ ļ░▒ĒśłĻĄ¼ 9,990/uL, Ēśłņāēņåī 10.2 g/dL, ĒŚżļ¦łĒåĀĒü¼ļ”┐ 31.3%, ĒśłņåīĒīÉ 276,000/╬╝LņØ┤ņŚłļŗż. ņÜöĻ▓Ćņé¼ Ļ▓░Ļ│╝ ļ╣äņżæņØĆ 1.020, pH 5.0, ņĀüĒśłĻĄ¼ 3+, ĒżļÅäļŗ╣ 3+, ļ░▒ĒśłĻĄ¼ ┬▒ņØ┤ņŚłĻ│Ā, ņÜöļŗ©ļ░▒ņØĆ ņØīņä▒ņØ┤ņŚłļŗż. ņåīļ│Ćļ░░ņ¢æņŚÉņä£ļŖö E.coliĻ░Ć ļÅÖņĀĢļÉśņŚłļŗż.
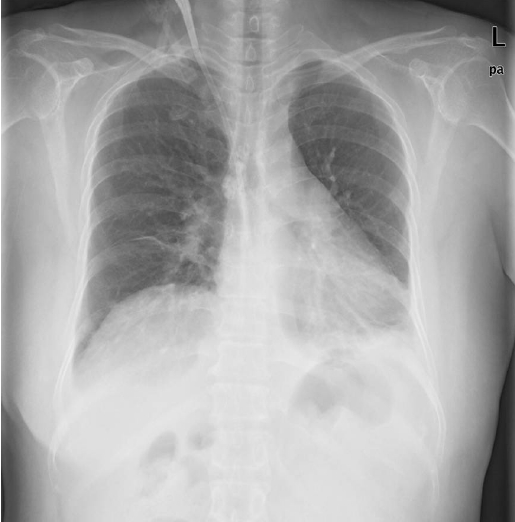
ļ░®ņé¼ņäĀ ņåīĻ▓¼: ĒØēļČĆ X-rayņŚÉņä£ļŖö ņ¢æņ¬Į ĒÅÉņŚÉ ĒØēņłśļĪ£ ņØśņŗ¼ļÉśļŖö ņåīĻ▓¼ņØ┤ ņ׳ņŚłņ£╝ļ®░ ņ¢æņ¬Į ĒÅÉ ĒĢśņŚĮņŚÉ ļ¼┤ĻĖ░ĒÅÉ ņåīĻ▓¼ņØ┤ ņ׳ņŚłļŗż(Fig. 1). ņÖĖļČĆļ│æņøÉņŚÉņä£ ņŗ£Ē¢ēĒĢ£ CTņŚÉņä£ļŖö ņ¢æņ¬Į ņŗĀņןņŚÉ ļČłĻĘ£ņ╣ÖĒĢ£ ņĪ░ņśüņ”ØĻ░ĢņØ┤ Ļ┤Ćņ░░ļÉśņŚłņ£╝ļéś ļ¦īņä▒ņŗĀļČĆņĀäņØś ņåīĻ▓¼ņØĆ ņŚåņŚłļŗż.
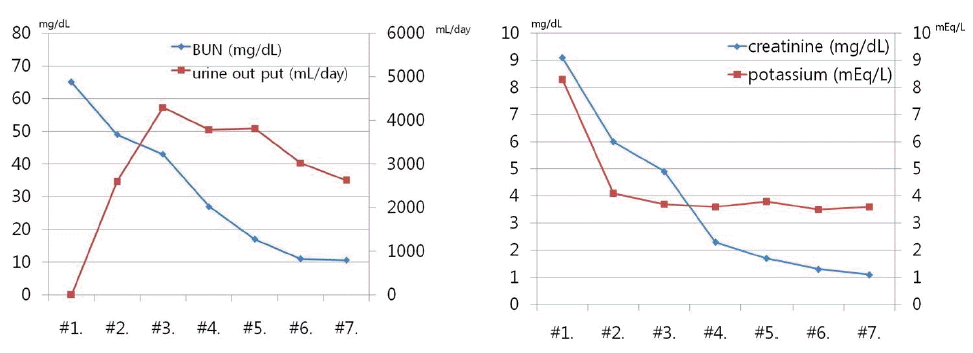
ņ╣śļŻī ļ░Å Ļ▓ĮĻ│╝: ņÖĖļČĆļ│æņøÉņŚÉņä£ ņŗ¼ĒĢ£ ļīĆņé¼ņä▒ ņé░ņ”ØĻ│╝ Ļ│Āņ╣╝ļź© Ēśłņ”Øņ£╝ļĪ£ ĒśłņĢĪ Ēł¼ņäØņØä 2ĒÜī ņŗ£Ē¢ēĒĢ£ ļÆżņŚÉ ļ│ĖņøÉņ£╝ļĪ£ ņĀäņøÉļÉśņŚłļŗż. ļ│ĖņøÉņŚÉņä£ ĒśłņĢĪĒł¼ņäØņØä ņ¦ĆņåŹĒĢśņŚ¼ ņÜöļÅģņ”ØĻ│╝ ļīĆņé¼ņä▒ņé░ņ”ØņØä ĻĄÉņĀĢĒĢśņśĆĻ│Ā, ņłśņĢĪĻ│ĄĻĖē, Ēśłļŗ╣ ņĪ░ņĀł, ņĢłĻ│╝ ņ¦äļŻī Ēøä ņ×ģņøÉ 2ņØ╝ņ¦ĖļČĆĒä░ ĒĢśļŻ© ņåīļ│Ćļ¤ēņØ┤ 2,000 mL ņØ┤ņāüņ£╝ļĪ£ ļŖśņ¢┤ļéśļ®┤ņä£ ņĀäņŗĀņāüĒā£ņÖĆ Ļ▓Ćņé¼Ļ▓░Ļ│╝Ļ░Ć ĒśĖņĀäļÉśņ¢┤ ņłśņĢĪĻ│ĄĻĖēņØä ņŗ£Ē¢ēĒĢśļ®┤ņä£ ĒśłņĢĪĒł¼ņäØņØä ņżæļŗ©ĒĢśņśĆļŗż. ņØ┤Ēøä Ēśłņ▓Ł ņĀäĒĢ┤ņ¦łĻ│╝ ņÜöņåīņ¦łņåī ļ░Å Ēü¼ļĀłņĢäĒŗ░ļŗīņØä Ļ┤Ćņ░░ĒĢśņśĆĻ│Ā ņ╣śļŻī 7ņØ╝ņ¦ĖļČĆĒä░ļŖö ņĀĢņāü Ēü¼ļĀłņĢäĒŗ░ļŗī ņłśņ╣śļź╝ ļ│┤ņØ┤ĻĖ░ ņŗ£ņ×æĒĢśĻ│Ā ņĀäņŗĀ ņāüĒā£Ļ░Ć ĒśĖņĀäļÉśņ¢┤ Ēć┤ņøÉĒĢśņśĆļŗż(Fig. 2).
Ļ│Ā ņ░░
ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ ņĢłņĢĢņØä ņĪ░ņĀłĒĢśĻĖ░ ņ£äĒĢ┤ acetazolamideļź╝ ņé¼ņÜ® Ēøä ļīĆņé¼ņä▒ ņé░ņ”Ø, Ļ│Āņ╣╝ļź©Ēśłņ”ØĻ│╝ ĒĢ©Ļ╗ś ļ░£ņāØĒĢ£ ĒĢŹļć©ņä▒ ĻĖēņä▒ņŗĀļČĆņĀäņØä ĻĖ░ņłĀĒĢśņśĆļŗż.
AcetazolamideļŖö ņĢłĻĄ¼ņŚÉņä£ ņ▓┤ņĢĪņØś ņāØņä▒ņØä Ļ░Éņåīņŗ£ņ╝£ ņĢłņĢĢņØä ļ¢©ņ¢┤ļ£©ļ”¼ļ»ĆļĪ£ ļģ╣ļé┤ņן ņ╣śļŻīņŚÉ ņé¼ņÜ®ļÉśļŖöļŹ░[2], ĒŖ╣Ē׳ Ļ░£ļ░®Ļ░ü ļģ╣ļé┤ņן ĒÖśņ×ÉņŚÉņä£ Ēāäņé░ĒāłņłśĒÜ©ņåī ņ¢ĄņĀ£ņĀ£ ņĀÉņĢłņĀ£ļ¦īņØä ņé¼ņÜ®ĒĢśļŖö ĒÖśņ×ÉņŚÉĻ▓ī acetazolamideļź╝ ņČöĻ░ĆļĪ£ Ļ▓ĮĻĄ¼Ēł¼ņŚ¼ĒĢśļŖö Ļ▓āņØ┤ ļŹö ĒÜ©Ļ│╝ņĀüņØ┤ļØ╝ļŖö ņŚ░ĻĄ¼Ļ▓░Ļ│╝ļÅä ņ׳ņ¢┤ņä£ ļŗżļźĖ ļ░®ļ▓Ģņ£╝ļĪ£ ņĢłņĢĢņĪ░ņĀłņØ┤ Ēלļōż Ļ▓ĮņÜ░ņŚÉ ņØ┤ņÜ®ĒĢ£ļŗż. AcetazolamideļŖö ņŗĀņןņØś ĻĘ╝ņ£äņäĖļć©Ļ┤ĆņāüĒö╝ņäĖĒżņŚÉņä£ Ēāäņé░ĒāłņłśĒÜ©ņåīļź╝ ņ¢ĄņĀ£ĒĢśņŚ¼ ņØ┤ļć©ņ×æņÜ®ņØä ņØ╝ņ£╝ĒéżļŖöļŹ░, ņØ┤ ņĢĮļ¼╝ņØĆ ņŗĀņןņØä ĒåĄĒĢ┤ ļ░░ņäżļÉśĻ│Ā ļČĆņ×æņÜ®ņ£╝ļĪ£ Ļ░ÉĻ░üļ¦łļ╣ä, ņåÉĻ░ĆļØĮņØ┤ļéś ļ░£Ļ░ĆļØĮņØś ņĀĆļ”░Ļ░É ļō▒ņØä ņØ╝ņ£╝Ēé¼ ņłś ņ׳ņ£╝ļ®░ ļō£ļ¼╝Ļ▓ī ļīĆņé¼ņä▒ņé░ņ”ØņØä ņØ╝ņ£╝Ēé©ļŗż. ĒŖ╣Ē׳ Ļ│ĀļĀ╣ņØ┤ļéś Ļ░äļČĆņĀä, ņŗĀļČĆņĀäņØä ļÅÖļ░śĒĢśĻ│Ā ņ׳ļŖö ĒÖśņ×ÉņŚÉņä£ ļīĆņé¼ņä▒ņé░ņ”ØņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[4].
Acetazolamide Ēł¼ņŚ¼ņŚÉ ņØśĒĢ£ ļīĆņé¼ņä▒ ņé░ņ”Ø ļ░Å ĻĖēņä▒ņŗĀļČĆņĀäņØś ņé¼ļĪĆļŖö ņØ┤ņĀäļČĆĒä░ ņĢīļĀżņĀĖ ņ׳ņŚłļŗż. Maisey ļō▒[4]ņØĆ ļģ╣ļé┤ņןņØś ņ╣śļŻīļź╝ ņ£äĒĢ┤ ļ│Ė ņ”ØļĪĆņÖĆ ļ╣äņŖĘĒĢ£ ĻĖ░Ļ░ä ļÅÖņĢł ļÅÖņØ╝ ņÜ®ļ¤ēņØś acetazolamideļź╝ ļ│ĄņÜ®ĒĢ£ ĒÖśņ×ÉņŚÉņä£ ļ░£ņāØĒĢ£ ļīĆņé¼ņä▒ ņé░ņ”ØņØä ļ│┤Ļ│ĀĒĢśņśĆļŗż. ĒĢśņ¦Ćļ¦ī ņØ┤ ĒÖśņ×ÉļŖö 82ņäĖļĪ£ Ļ│ĀļĀ╣ņØ┤ņŚłĻ│Ā, Ļ▓Įņ”ØņØś ņŗĀĻĖ░ļŖź ņןņĢĀĻ░Ć ņ׳ņŚłĻ│Ā Ļ│Āņ╣╝ļź©Ēśłņ”ØņØ┤ ņŚåņŚłņ£╝ļ®░ ņłśņĢĪņÜöļ▓Ģļ¦īņ£╝ļĪ£ ĒÖśņ×ÉĻ░Ć ĒśĖņĀäļÉśņŚłļŗżļŖö ņĀÉņŚÉņä£ ļ│Ė ņ”ØļĪĆņÖĆļŖö ņ░©ņØ┤Ļ░Ć ņ׳ņŚłļŗż[4]. Heller ļō▒ņØĆ ļģ╣ļé┤ņן ĒÖśņ×Éļōż ņżæ acetazolamideļź╝ Ēł¼ņŚ¼ĒĢ£ ĒÖśņ×ÉņŚÉņä£ Ēł¼ņŚ¼ĒĢśņ¦Ć ņĢŖņØĆ ĒÖśņ×ÉņŚÉ ļ╣äĒĢ┤ ļīĆņé¼ņä▒ ņé░ņ”ØņØ┤ ļŹö ļ¦ÄņØ┤ ļ░£ņāØĒĢ£ļŗżļŖö Ļ▓░Ļ│╝ļź╝ ļ░£Ēæ£ĒĢśņśĆĻ│Ā[5], Higenbottam ļō▒ņŚÉ ņØśĒĢ┤ ļ│┤Ļ│ĀļÉ£ ļģ╣ļé┤ņן ļ░Å Ļ░äņ¦ł ĒÖśņ×ÉņŚÉņä£ņØś ĻĖēņä▒ņŗĀļČĆņĀä ņ”ØļĪĆļŖö acetazolamideņŚÉ ņØśĒĢ┤ ĒśĢņä▒ļÉ£ ņÜöņäØņŚÉ ņØśĒĢ£ ņÜöĻ┤ĆĒÅÉņćä ļĢīļ¼ĖņØ┤ļØ╝Ļ│ĀļÅä ĒĢśņśĆļŗż[6]. ĻĘĖļ¤¼ļéś Epelde ļō▒ņØĆ acetazolamideļź╝ Ēł¼ņŚ¼ĒĢ£ ĒÖśņ×ÉņŚÉņä£ ņÜöĻ┤ĆņØś ĒÅÉņćä ņŚåņØ┤ļÅä ĻĖēņä▒ ņŗĀļČĆņĀäņØ┤ ļ░£ņāØĒĢ£ ņé¼ļĪĆļź╝ ļ│┤Ļ│ĀĒĢśņśĆĻ│Ā[7], Ļ▓Įņ”ØņØś ņŗĀļČĆņĀäņØ┤ ņ׳Ļ▒░ļéś Ļ│ĀļĀ╣ņŚÉņä£ acetazolamideņŚÉ ņØśĒĢ£ ĻĖēņä▒ ņŗĀļČĆņĀäĻ│╝ ļīĆņé¼ņä▒ņé░ņ”ØļōżņØ┤ ļ│┤Ļ│ĀļÉśņŚłņ£╝ļéś[3-6], ņĢäņ¦üĻ╣īņ¦Ć ĒśłņĢĪĒł¼ņäØĻ╣īņ¦Ć ĒĢäņÜöĒĢĀ ņĀĢļÅäļĪ£ ņŗ¼ĒĢ£ ņŗĀļČĆņĀäĻ│╝ ļīĆņé¼ ņä▒ņé░ņ”ØņØ┤ ņ¦äĒ¢ēĒĢ£ Ļ▓ĮņÜ░ļŖö ņ░ŠņĢäļ│┤ĻĖ░ ņ¢┤ļĀżņÜ░ļ®░, ļö░ļØ╝ņä£ ļ│Ė ņ”ØļĪĆļź╝ ĒåĄĒĢ┤ ņŗĀĻĖ░ļŖźņØ┤ ņĀĢņāüņØ┤ļŹś ĒÖśņ×ÉņŚÉņä£ļÅä acetazolamideņŚÉ ņØśĒĢ┤ ĻĖēņä▒ņŗĀļČĆņĀäņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ņØīņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłļŗż. ņØ┤ņĀäņØś ņ”ØļĪĆļōżņŚÉņä£ ļ│┤Ļ│ĀĒĢśļŖö acetazolamideņŚÉ ņØśĒĢ£ ļīĆņé¼ņä▒ ņé░ņ”ØņØĆ ĻĘ╝ņ£äņäĖļć©Ļ┤ĆņŚÉņä£ ņżæĒāäņé░ņŚ╝ņØś ņ×¼ĒØĪņłś ņןņĢĀ ļĢīļ¼ĖņŚÉ ļ░£ņāØĒĢśļŖö ņĀĢņāü ņØīņØ┤ņś©ņ░©ņØś ļīĆņé¼ņä▒ ņé░ņ”ØņØ┤ļ®░, Ēśłņ▓Ł ņ╣╝ļź© ļåŹļÅäļŖö ņĀĢņāüņØ┤ņŚłļŗż[4]. ĻĘĖļ¤¼ļéś ļ│Ė ņ”ØļĪĆņŚÉņä£ļŖö Ēśłņ▓Ł ņØīņØ┤ņś©ņ░©Ļ░Ć 22 mEq/LņśĆĻ│Ā, ņĀĆņ╣╝ļź©Ēśłņ”ØņØ┤ ņĢäļŗī ņŗ¼ĒĢ£ Ļ│Āņ╣╝ļź©Ēśłņ”ØņØä ļ│┤ņŚ¼, acetazolamide ņ×Éņ▓┤ņŚÉ ņØśĒĢ£ ļīĆņé¼ņä▒ ņé░ņ”Øļ│┤ļŗżļŖö acetazolamideņŚÉ ņØśĒĢ£ ĻĖēņä▒ ņäĖļć©Ļ┤ĆĻ┤┤ņé¼ņÖĆ ĻĖēņä▒ņŗĀļČĆņĀäņŚÉ ņØśĒĢ£ ļīĆņé¼ņä▒ņé░ņ”ØņØ┤ ņØśņŗ¼ļÉ£ļŗż. ļśÉĒĢ£ ĻĖēņä▒ņŗĀļČĆņĀäņØś ņøÉņØĖņ£╝ļĪ£ļÅä Ļ│╝ļÅäĒĢ£ ņØ┤ļć©ņŚÉ ņØśĒĢ£ ņŗĀļČĆņĀäļ│┤ļŗżļŖö ņĢĮņĀ£ņŚÉ ņØśĒĢ£ ĻĖēņä▒ ņäĖļć©Ļ┤ĆĻ┤┤ņé¼ņÖĆ ņłśļČäņäŁņĘ© ļČĆņĪ▒ņ£╝ļĪ£ ņØĖĒĢ£ ĻĖēņä▒ ĒśĆĒśłņä▒ ņŗĀļČĆņĀäņØ┤ ņØśņŗ¼ļÉśņŚłļŗż. ĒÖśņ×ÉļŖö 20ļģä ņĀäļČĆĒä░ ļŗ╣ļć©ļ│æņØ┤ ņ׳ņ¢┤ ĻĖēņä▒ ņäĖļć©Ļ┤ĆĻ┤┤ņé¼ņØś ņ£äĒŚśņä▒ņØ┤ ļåÆņØĆ ņāüĒā£ņśĆņ£╝ļ®░, Siklos ļō▒ņØĆ ļŗ╣ļć©ļ│æņä▒ ņŗĀņ”ØņØ┤ ļÅÖļ░śļÉ£ ņäĖļć©Ļ┤Ć ĻĖ░ļŖźņØ┤ņāüņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░ ļīĆņé¼ņä▒ ņé░ņ”ØļÅä ļŹö ņēĮĻ▓ī ļ░£ņāØĒĢĀ Ļ▓āņØ┤ļØ╝Ļ│Ā ņĀ£ņĢłĒĢśĻĖ░ļÅä ĒĢśņśĆļŗż[8]. ļśÉĒĢ£ acetazolamideĻ░Ć ņŗĀņןņäĖļÅÖļ¦źņØś ņĀĆĒĢŁņä▒ņØä ņ”ØĻ░Ćņŗ£ņ╝£ņä£ ņŗĀ Ēśłļźś Ļ░Éņåī ļ░Å ņé¼ĻĄ¼ņ▓┤ ņŚ¼Ļ│╝ņ£©ņØś Ļ░Éņåīļź╝ ņØ╝ņ£╝ņ╝£ ĻĖēņä▒ ņäĖļć©Ļ┤ĆĻ┤┤ņé¼ļź╝ ļ░£ņāØņŗ£Ēé¼ ņłś ņ׳ļŗżļŖö ļÅÖļ¼╝ ņŗżĒŚś Ļ▓░Ļ│╝Ļ░Ć ņ׳ņ£╝ļ®░, ņØ┤ ņŗżĒŚśņŚÉņä£ ņŗĀ ĒśłļźśņØś ņĀĆĒĢŁņä▒ņØś ņ”ØĻ░ĆļŖö acetazolamideĻ░Ć ņ¦üņĀæņĀüņ£╝ļĪ£ ņŗĀ Ēśłļźś ņł£ĒÖśņŚÉ ņśüĒ¢źņØä ņŻ╝Ļ▒░ļéś ĻĘ╝ņ£äņäĖļć©Ļ┤ĆņØś ņ×¼ĒØĪņłśļź╝ Ļ░Éņåīņŗ£Ēéżļ®┤ņä£ ņØ┤ņ░©ņĀüņ£╝ļĪ£ ļ░£ņāØĒĢ£ ņŗĀņןļé┤ ņĢĢļĀźņØś ļ│ĆĒÖöļĪ£ ņäżļ¬ģĒĢśņśĆļŗż[9]. ņØ┤ ĒÖśņ×ÉņØś Ļ▓ĮņÜ░ļÅä ņŗĀ Ēśłļźś ņĀĆĒĢŁņä▒ņØś ņ”ØĻ░ĆļĪ£ ņØĖĒĢ┤ ņé¼ĻĄ¼ņ▓┤ Ēśłļźśļ¤ēņØ┤ Ļ░æņ×ÉĻĖ░ Ļ░ÉņåīĒĢśļ®┤ņä£ ĻĖēņä▒ ņäĖļć©Ļ┤ĆĻ┤┤ņé¼Ļ░Ć ļ░£ņāØĒ¢łņØä Ļ░ĆļŖźņä▒ņØä ņāØĻ░üĒĢ┤ ļ│╝ ņłś ņ׳ļŗż. ļśÉĒĢ£ ņØ┤ ņ”ØļĪĆņŚÉņä£ ļīĆņé¼ņä▒ ņé░ņ”ØņØś ņøÉņØĖņ£╝ļĪ£ ņÜöļĪ£Ļ░ÉņŚ╝ņŚÉņØśĒĢ£ Ēī©Ēśłņ”ØņØ┤ļéś metforminņØś ļ│ĄņÜ®ļÅä Ļ│ĀļĀżĒĢśņŚ¼ņĢ╝ ĒĢśņ¦Ćļ¦ī, ĻĖēņä▒ņŗĀļČĆņĀäņŚÉņä£ļÅä Ēśłļć©ņÖĆ ļåŹļć©Ļ░Ć ļ░£Ļ▓¼ļÉĀ ņłś ņ׳Ļ│Ā[10] ņ×äņāü ņ”ØņāüļÅä ņŚåņ¢┤ņä£ ņÜöļĪ£Ļ░ÉņŚ╝ņØś Ļ░ĆļŖźņä▒ņØĆ ļé«ņ£╝ļ®░, 10ļģä ņØ┤ņāü ņ£Āņ¦Ć ņÜ®ļ¤ēņ£╝ļĪ£ ļ│ĄņÜ®ĒĢ£ metformin ļĢīļ¼ĖņŚÉ Ēł¼ņäØņØ┤ ĒĢäņÜöĒĢĀ ņĀĢļÅäņØś ņŗ¼ĒĢ£ ņŗĀļČĆņĀäĻ│╝ ļīĆņé¼ņä▒ņé░ņ”ØņØ┤ ļ░£ņāØĒĢĀ Ļ░ĆļŖźņä▒ļ│┤ļŗżļŖö ņĄ£ĻĘ╝ ļ│ĄņÜ®ņØä ņŗ£ņ×æĒĢ£ acetazolamideļź╝ ņøÉņØĖņ£╝ļĪ£ ņāØĻ░üĒĢśņśĆļŗż.
ļ│Ė ņŚ░ĻĄ¼ņØś ņĀ£ĒĢ£ņĀÉ ņżæ ĒĢśļéśļŖö ĒÖśņ×ÉĻ░Ć ņÖĖļČĆļ│æņøÉņŚÉņä£ ĒśłņĢĪĒł¼ņäØ Ēøä ņØ┤ņåĪļÉśņ¢┤ Ēśłņżæ ņĢĮļ¼╝ ļåŹļÅäļź╝ ņĖĪņĀĢĒĢśņ¦Ć ļ¬╗ĒĢ£ Ļ▓āņØĖļŹ░, ņĢ×ņ£╝ļĪ£ ļŹö ļ¦ÄņØĆ ņ”ØļĪĆĻ░Ć ĒÖĢņØĖļÉ£ļŗżļ®┤ acetazolamideņÖĆ ņŗĀļČĆņĀä ļ░Å ļīĆņé¼ņä▒ņé░ņ”ØņØś Ļ┤ĆĻ│äļź╝ ļ░ØĒ׳ļŖö ļŹ░ ļÅäņøĆņØ┤ ļÉĀ ņłś ņ׳ņØä Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
ņĀĆņ×ÉļōżņØĆ ņŗĀņן ĻĖ░ļŖźņØ┤ ņĀĢņāüņ£╝ļĪ£ ņ£Āņ¦ĆļÉśļŹś ĒÖśņ×ÉņŚÉņä£ ņ£Āņ¦ĆņÜ®ļ¤ēņ£╝ļĪ£ acetazolamideļź╝ ņé¼ņÜ®ĒĢ£ ĒÖśņ×ÉņŚÉņä£ ļ░£ņāØĒĢ£ ņŗ¼ĒĢ£ ļīĆņé¼ņä▒ ņé░ņ”ØĻ│╝ ņŗĀļČĆņĀäņØä ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļ®░, ļö░ļØ╝ņä£ ļģ╣ļé┤ņןĒÖśņ×Éļź╝ ļ╣äļĪ»ĒĢ┤ņä£ acetazolamideļź╝ Ēł¼ņĢĮĒĢśļŖö ĒÖśņ×ÉņŚÉ ļīĆĒĢ┤ņä£ļŖö ĻĖēņä▒ņŗĀļČĆņĀäņØś Ļ░ĆļŖźņä▒ļÅä ņāØĻ░üĒĢśņŚ¼ ņĢĮļ¼╝ņØä ņé¼ņÜ®ĒĢĀ ļĢī ļŹö ņŻ╝ņØśļź╝ ĻĖ░ņÜĖņŚ¼ņĢ╝ ĒĢĀ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






