서 론
약물 용출성 스텐트(drug-eluting stent)는 기존 단순 금속 스텐트(bare metal stent)에 비하여 신생내막(neointima)과 반흔(scar) 형성이 적어 재협착을 감소시킨다고 알려져 있고[1-4], 2002년 약물 용출성 스텐트가 도입되면서부터 많은 양의 수요가 있어 왔다. 이에 따라 현재 관상동맥 내로 삽입된 약물 용출성 스텐트의 경과 및 신생내막 형성에 대한 연구가 혈관내초음파(intravascular ultrasonography, IVUS)와 광결합단층촬영(optical coherence tomography, OCT) 등을 통하여 이루어지고 있다. 저자들은 ST 분절상승 심근경색으로 경피적 관상동맥 조영술을 시행하여 약물 용출성 스텐트를 삽입한 환자에게서 4년 뒤 혈관내초음파를 시행하여 발견된 흔하지 않은 석회침착(calcification)을 경험하였기에 보고하는 바이다.
증 례
70세 남자 환자가 내원 3시간 전부터 시작된 흉통을 주소로 응급실 내원하였다. 고혈압, 당뇨로 경구약 복용 중이었으며, 4년 전 ST 분절 상승 심근경색으로 인근 대학병원에서 경피적 관상동맥 조영술을 시행하여 우관상동맥 근위부의 완전폐쇄 및 좌전하관상동맥 중간부위에 80%의 협착소견 발견되어 우관상동맥 근위부로 Paclitacel 용출성 스텐트(Taxus, Boston Scientific, Natick, MA, USA)를 삽입하고 5일 후 이차 관상동맥조영술 시행하여 좌전하관상동맥 중간부위에도 같은 용출성 스텐트를 삽입하였으며, 이후 연고지 관계로 본원으로 의뢰되어 외래에서 경과관찰 중이었던 분이다. 응급실에 내원하여 당시 시행한 심전도상 ST 분절에 이상소견 관찰되지 않고, 심근효소수치 정상으로 불안정성협심증 진단하에 내원한 다음날 관상동맥조영술을 시행하였다.
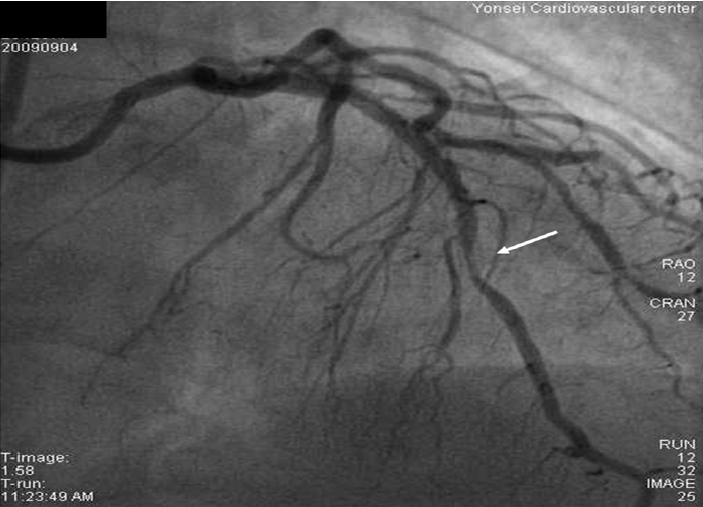
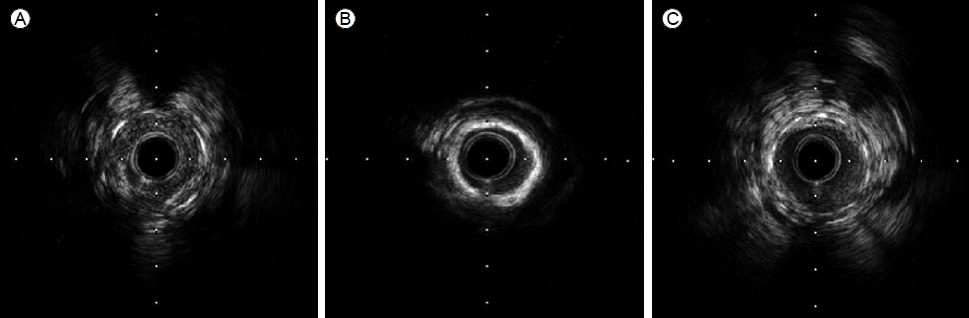
조영술 소견상 좌전하관상동맥의 중간부위에서 4년 전 삽입하였던 스텐트의 원위부에 80%의 재협착 소견(Fig. 1) 및 우관상동맥 원위부로 새로이 90%의 협착소견이 관찰되었다. 또한 4년 전 우관상동맥 원위부로 삽입하였던 스텐트에는 신생내막 과증식으로 인하여 20% 정도의 협착소견이 확인되었다. 좌전하관상동맥의 4년 전 스텐트 삽입한 부위에 혈관내초음파(IVUS)를 시행한 결과 스텐트 내강 안쪽을 둘러싼 원형의 두꺼운 석회침착소견이 관찰되었다(Fig. 2B). 좌전하관상동맥 스텐트 내강으로 협착된 소견 보인 부위와 우관상동맥 원위부에 새로 발견된 협착부위로 각각 Everolimus 용출성 스텐트(Xience, Abbott Vascular, Santa Clara, CA, USA)를 삽입하고 시술을 마쳤으며, 현재 환자 외래에서 흉통 없이 경과관찰 중으로 새로운 스텐트 삽입 후 9개월 뒤에 추적관찰을 위한 관상동맥조영술을 시행 예정이다.
고 찰
관상동맥에서 칼슘이 침착되는 현상은 20-30대 이후부터 일어나는 것으로 되어있으며 유전적 소인 및 임상적인 소인들이 작용하는 것으로 되어있다[5,6]. 관상동맥의 석회화는 관상동맥의 죽상동맥경화반의 총량과 비례하고 관상동맥의 협착을 예측하는 지표가 되며 허혈성 심장질환 발생의 독립적인 위험인자가 되는 것으로 알려져 있다[7-9].
1986년 관상동맥 질환에 처음으로 스텐트가 사용되면서 풍선확장술 후 심각한 합병증이었던 급성 또는 아급성 폐쇄를 현격히 감소시켰으며[10], 이에 따라 스텐트 삽입술 후 재협착을 감소시키는 데 초점이 모아졌다. 재협착의 주요 기전으로 1) 조기 탄력성 재수축(early elastic recoil) 2) 신생내막 과형성(neointimal hyperplasia) 및 3) 늦은 혈관 개형(late vessel remodeling)의 세 가지를 들 수 있는데 이 중 스텐트 삽입술 후에는 신생내막 과형성이 가장 중요한 재협착의 기전으로 알려져 있다. 신생내막 과형성은 시술 후 주로 6개월 내에 발생하며 proteoglycan matrix 내에 평활근 세포(smooth muscle cell)가 과도하게 증식하여 혈관을 재협착시키는 과정으로 이 과정의 촉발은 풍선확장술로 혈관 내막이 손상을 받은 직후부터 발생하는 염증단계에서 병변 내로 분비된 각종 염증세포, 혈소판 및 cytokine 들이 주 요인이라고 여겨진다[11-13]. 2007년 Doyle 등[14]이 4500여 명의 단순 금속 스텐트를 삽입한 환자를 대상으로 조사한 논문에 따르면 10년 내에 임상적으로 의미 있는 스텐트 재협착은 18.1%였으며, 그중 심근경색은 2.1%로 조사되었다.
하지만 Agostoni 등[15]은 11년 전 불안정성 협심증으로 단순 금속 스텐트를 삽입한 환자에게 운동부하검사 도중 발생한 ST 분절상승 심근경색으로 관상동맥조영술을 통해 이전 스텐트 삽입부위가 협착되어 흡착(aspiration)을 시행하였고, 흡착물에서 죽상동맥경화반(atherosclerotic plaque) 조각들을 발견하여 스텐트 주위로 새로운 죽상동맥경화증(de novo atherosclerosis)이 생겼음을 시사한다고 하였다. 또한 Fineschi 등[16]은 이전에 단순 금속 스텐트를 삽입한 안정성협심증 환자에게서 혈관내초음파를 시행하여 파열된 반(ruptured plaque)를 발견하여, 이를 스텐트내 협착증이 아닌 신생내막과 관련하여 생긴 죽상동맥증으로 추정하였다. 그리고 Appleby [17]는 안정성 협심증으로 단순 금속 스텐트를 삽입한 환자에게서 8년 뒤 협심증 증상으로 관상동맥조영술 재시행하면서 혈관내초음파로 스텐트 내강의 신생내막의 일부에서 석회화를 발견하였다고 보고하였으며 새로운 죽상동맥경화증이 스텐트와 관련하여 드물게 생긴 것으로 판단하였다.
본 증례의 경우 단순 금속 스텐트를 삽입한 위의 경우들과는 달리 약물 용출성 스텐트를 삽입한 환자의 혈관내초음파를 통해 스텐트 내강을 원형으로 둘러싼 특이한 형태의 석회화 소견을 찾아냈다. 이는 약물 용출성 스텐트를 삽입함으로써 발생빈도가 적을 것으로 받아들여졌던 신생내막 증식 및 새로운 죽상동맥경화증이 약물 용출성 스텐트와 관련하여 나타난 것으로 생각되고, 상기 병변에 대한 추적관찰이 필요할 것으로 생각한다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






