서 론
비인두암은 중국 광동지방, 홍콩 등에서 빈도가 높은 것으로 알려져 있지만 대부분의 나라에서는 약 10만 명 중의 1명이 발병하는 비교적 드물게 발생하는 암으로[1], 우리나라에서는 전체 악성 종양의 1% 미만을 차지하고 두경부 종양의 약 2-15%를 차지하는 것으로 보고되고 있다[2]. 비인두암은 비교적 방사선 요법과 항암화학요법에 잘 반응하여 병기에 따라 일차적 치료로서 방사선 요법 또는 동시 항암화학방사선요법을 시도하게 되나 치료실패의 원인으로 원격전이가 많다고 알려져 있다[3]. 폐는 비인두암의 전이가 가장 많이 나타나는 곳이지만 폐 단독으로 전이가 있을 때에는 비교적 양호한 예후를 보인다[4,5]. 폐 단독 전이가 있을 때 동시 항암방사선요법이 효과가 있다는 보고가 있으나 이에 대해서는 아직 논란의 여지가 많다[5]. 두경부암의 폐전이에 대한 폐전이절제술을 시행하여 양호한 결과를 보인다는 보고가 있지만[6,7] 비인두암에서의 폐전이절제술에 대해서는 아직 보고된 바 없다. 따라서 저자들은 비인두암의 폐전이절제술을 시행한 4예를 문헌고찰과 함께 보고하는 바이다.
증 례
증례 1
환 자: 남자, 50세
주 소: 우상엽 폐 종괴
현병력: 환자는 경부 종괴로 내원하여 WHO 제3형의 미분화성 비인두암 T3N3M0 (Stage IVB)로 진단되어 유도 항암화학요법(cisplatin 20 mg/m2, 5-FU 1,000 mg/m2 D1-D41주기) 후에 동시 항암방사선요법(cisplatin 20 mg/m2 3주 간격 D1-D4 2주기, 방사선요법 200 cGy × 35회, 총 7,000 cGy) 시행하였고 이후 완전관해 소견을 보였다. 1년 뒤 시행한 양전자 방출 단층촬영(PET-CT)에서 폐우상엽의 18F-Flurodeoxyglcuose (18F-FDG) 섭취 증가 소견 보여 폐전이로 판단, 수술 위해 입원하였다.
영상학적 소견: 흉부 전산화 단층촬영에서 우상엽 전구역(right upper lung, anterior segment)의 조영 증강되는 종괴 보였고, 양전자 방출 단층촬영상에서 우상엽의 18F-FDG 섭취 증가(maximum SUV [SUVmax] = 4.9) 보였다.
치료 및 경과: 비디오 흉강경을 이용한 쐐기 절제술 시행하였다. 술 후 2일째 흉관 제거하였고 합병증 없이 퇴원하였다. 수술 후 보조 항암화학요법으로 경구 S-1을 6주 간격으로(4주 투약, 2주 휴약) 4주기 시행하였고 현재 수술 후 50개월로 재발 소견 없이 외래 추적관찰 중이다.
병리결과: 1.5 cm의 회색의 둥근 종괴 보였고 절제연은 음성이었다. 미분화성 암종으로 비인두암과 같은 조직 소견 보였다.
증례 2
환 자: 남자, 57세
주 소: 좌상엽 폐 종괴
현병력: 환자는 WHO 제3형의 미분화성 비인두암, T2N3bM0 (Stage IV)로 진단되어 동시 항암방사선요법(cisplatin 100 mg/m2, D1, D22. 방사선요법 200 cGy × 35회, 총 7,000 cGy) 후 완전관해 소견을 보였다. 완전관해 후 1년 4개월째 시행한 양전자 방출 단층촬영에서 폐좌상엽과 폐문 부위 림프절에 새로운 18F-FDG 섭취 증가 발견되어 폐전이로 의심하고 폐 종괴에 대해 경피적 폐 생검 시행하였지만 결과는 음성이었다. 추후 시행한 흉부 전산화 단층촬영에서 폐문 부위 림프절 크기 점차 증가하여 폐전이를 배제할 수 없어 조직학적 확진 및 종괴 절제술을 위해 입원하였다.
방사선 소견: 흉부 전산화 단층촬영에서 약 0.9 cm 크기의 좌상엽 전구역의 조영 증강되는 종괴와 폐문, 대동맥-폐동맥 창(aortopulmonary window)의 림프절 비대 소견 보였다. 양전자방출단층촬영에서 좌상엽에 18F-FDG 섭취 증가(SUVmax = 3.2) 보였고 대동맥-폐동맥 창의 림프절 섭취 증가(SUVmax = 9.2) 보였다.
치료 및 경과: 개흉 좌상엽 쐐기절제술 및 폐문 림프절 박리술 진행하였다. 수술적 소견으로 약 1 cm 크기의 좌상엽 종괴가 보였으며 폐문 주위 림프절 비대소견이 보였다. 술 후 2일째 흉관 제거하였고 합병증 없이 퇴원하였다. 수술 후 보조 항암화학요법으로 경구 S-1을 6주 간격으로(4주 투약, 2주 휴약) 6주기 시행하였고 현재 수술 후 25개월로 재발소견 없이 외래 추적관찰 중이다.
병리 소견: 회백색의 둥근 1 cm의 종괴가 보였다. 미분화성 비인두암과 일치하는 결과를 얻었다. 림프절은 3개 중 1개(대동맥-폐동맥 창의 림프절)가 양성이었다.
증례 3
환 자: 남자, 69세
주 소: 좌상엽 폐 종괴
현병력: 환자는 양측 귀밑 통증 및 부종으로 내원하여 WHO 제3형의 미분화성 비인두암, T2aN2M0 (Stage III)로 진단되어 동시 항암방사선요법(cisplatin 100 mg/m2 D1, cisplatin 75 mg/m2 D22, 방사선요법 200 cGy × 35회, 총 7,000 cGy) 후 완전관해 소견을 보였다. 관해 후 9개월째 시행한 양전자 방출 단층촬영에서 폐좌상엽에 새로운 18F-FDG 섭취 증가 발견되어 폐전이 의심하에 경피적 폐 생검을 시행하였고 결과는 미분화성암으로 비인두암과 일치하는 소견 보여 수술 위해 입원하였다.
방사선 소견: 흉부 전산화 단층촬영에서 2 cm 크기의 좌상엽 전구역의 조영 증강되는 종괴와 폐문, 종격동의 림프절 비대 보였다. 우상엽에 양성육아종으로 생각되는 0.6 cm의 종괴가 보였다. 양전자 방출 단층촬영에서 폐좌상엽에 18F-FDG 섭취 증가(SUVmax = 10.8) 보였고 우측상부 기관옆(paratracheal) 림프절 섭취 증가(SUVmax = 3.5) 보였다.
치료 및 경과: 흉강경을 이용한 폐 좌상엽 절제술 및 폐문 림프절 박리술 시행하였다. 수술적 소견은 국소적으로 흉막유착이 관찰되었으며 다수의 림프절 비대 소견을 보였다. 술 후 6일째 흉관 제거하였고 합병증 없이 퇴원하였다. 수술 후 종격동 방사선요법(200 cGy × 30회, 총 6,000 cGy)를 시행한 후, 보조 항암화학요법으로 경구 S-1을 6주 간격으로(4주 투약, 2주 휴약) 3주기 시행하였다. 환자는 현재 수술 후 20개월째 재발소견 없이 외래 추적관찰 중이다.
병리결과: 경계가 불명확한 폐실질에 둘러싸인 3.3 × 2.7 cm 크기의 종괴가 보였고 절제연은 음성이었다. 미분화성 비인두암과 일치하는 결과 보였고 림프절은 18개 중 2개(종격동, 기관지 주변 림프절)에서 양성소견 보였다. 면역 조직화학 염색을 통한 면역표지자 검사상 Cytokeratin 염색에 음성, TTF-1염색에 음성이었다.
증례 4
환 자: 남자, 35세
주 소: 좌상엽 폐 종괴
현병력: 환자는 경부 종괴로 내원하여 WHO 제3형의 미분화성 비인두암, T3N1M0 (StageⅢ)로 진단 후, 동시 항암방사선요법(cisplatin 100 mg/m2, D1, D22, D43, 방사선요법 200 cGy × 35회, 총 7,000 cGy) 시행하여 완전관해 소견 보였다. 관해 후 3년 11개월째 시행한 양전자 방출 단층촬영에서 폐좌상엽에 18F-FDG 섭취 증가 소견보여 폐전이로 판단, 수술 위해 입원하였다.
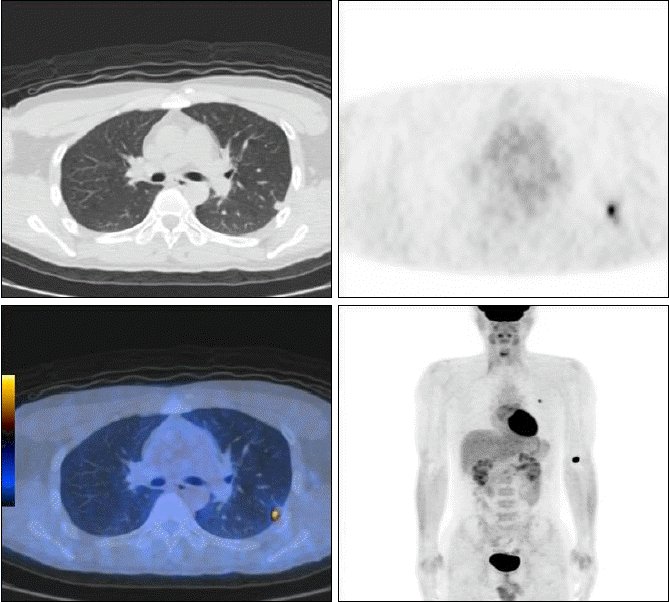
영상학적 소견: 흉부 전산화 단층촬영에서 폐흉막에 둘러싸인 좌상엽에 0.9 cm의 종괴가 보였고 좌하엽의 석회화된 육아종이 보였다(Fig. 1). 양전자 방출 단층촬영에서 폐좌상엽의 강한 18F-FDG 섭취 증가(SUVmax = 3.1) 보였으며 좌측 경부 제IB군 림프절에 반응성 림프절로 생각되는 18F-FDG (SUVmax = 3.5) 섭취 증가 보였다(Fig. 2).
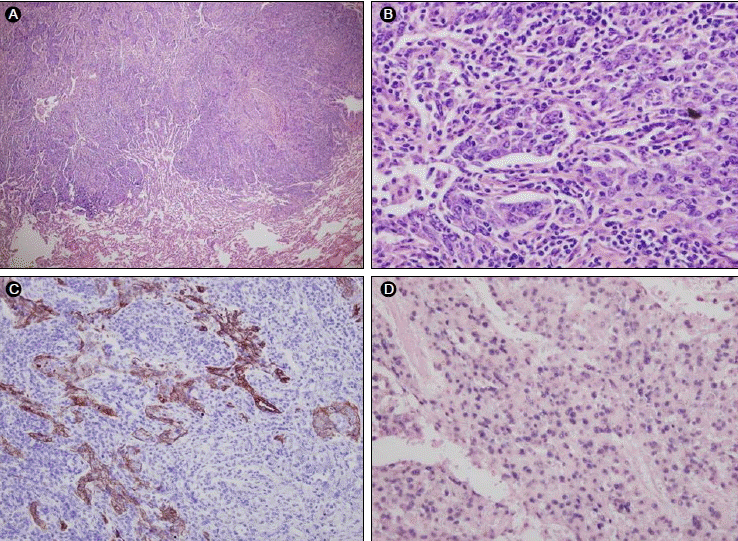
치료 및 경과: 비디오 흉강경을 이용한 쐐기 절제술 시행하였다. 술 후 2일째 흉관 제거하였고 합병증 없이 퇴원하였다. S-1으로 보조 항암화학요법 2주기 시행하였고 현재 수술 후 8개월째 재발소견 없이 외래 추적관찰 중이다.병리 소견: 1.4 cm의 회백색의 종괴로 폐흉막을 침범하고 있었다. 절제연은 음성이었다. 미분화성 암종으로 비인두암과 같은 조직 소견보였으며(Fig. 3A and 3B), 면역 조직화학 염색을 통한 면역표지자 검사에서 Cytokeratin염색에 양성(Fig. 3C), EBV-encoded small nuclear RNA (EBER)에 대한 In situ hybridization이 양성이었다(Fig. 3D).
고 찰
비인두암은 증상이 경미하고 발현증상 및 증후가 다양하기 때문에 초기에 진단이 어렵고, 비교적 조기에 경부 임파선으로 전이하며, 진단 당시에 이미 상당한 진행된 병기를 보이는 경우가 많아, 예후가 불량한 것으로 알려져 있다[3]. 비인두암은 방사선요법에 잘 반응하여 방사선 치료는 비인두암의 치료의 근간을 이루고 있으며 조기 비인두암에서 방사선요법 시 5년 생존율이 95%에 이른다. 또한 비인두암은 항암화학요법에 좋은 반응률을 보여 국소적 또는 국지적 진행암(III, IV기)에서는 동시 항암화학방사선요법이 표준치료이며, 50-70%의 5년 생존율을 보인다[8]. 본 증례에서도 4명의 경우 모두 진행된 병기(III, IV기)에서 진단이 되었고, 일차적 치료로 동시 항암화학방사선요법을 하여 완전관해를 이루었다.
비인두암에서의 원격전이가 있을 시 5년 생존율이 약 15%로 원격전이는 비인두암 치료의 실패와 사망의 주요한 원인으로 생각되고 있다. Hui 등은 방사선 요법 후 원격전이가 나타나는 장기에 따라서 생존기간의 차이를 조사하여 폐 단독일 때 중앙생존기간이 3.9년, 간 단독일 때 1.9년, 뼈 단독일 때 1.7년으로 폐 단독 전이가 비교적 양호한 예후를 보인다고 보고하였다[4]. 또한 Cao 등은 폐 단독 전이가 있는 환자들을 항암화학요법 단독 환자들과 동시 항암방사선요법을 시행한 환자들을 비교하였을 때 평균생존기간이 26.8개월에서 46.2개월로 유의한 향상을 보였다고 보고하였으며, 무병기간을 비교하였을 때에는 1년 이상인 환자에서 동시 항암방사선요법을 하였을 때 예후가 더욱 좋은 것으로 나타났다[5]. 이러한 연구들의 결과로 미루어 볼 때 폐 단독 전이가 있을 때에는 항암화학요법 단독보다는 다학제적 치료를 고려해야 할 것으로 생각된다.
폐전이절제술은 대장암, 유방암, 골육종 등에서 나타난 폐전이에서 표준치료로 받아들여지고 있으며, 두경부암의 폐전이절제술을 시행한 경우에서도 비교적 양호한 생존율을 보여주는 몇몇 보고가 있다[6,7]. Shiono 등은 두경부 편평세포암에서의 폐전이절제술을 시행하였을 때, 5년 생존율을 26.5%, 비강(Nasal cavity)의 편평세포암의 경우는 47.6%로 보고하였다[6]. 또한 Winter 등은 두경부암의 폐전이 환자에서 폐전이절제술을 시행한 경우, 중앙 생존값과 5년 생존율이 각각 19.4개월과 20.9%로 보고하였고, 이는 보존적 치료군의 중앙 생존값인 5개월에 비해 유의한 향상(p< 0.01)을 보여주는 결과이다[7]. Ma 등은 비인두암의 폐전이 환자 105명을 대상으로 항암화학요법 단독군, 방사선요법 ± 항암화학요법군 그리고 폐전이절제술 ± 항암화학요법군을 비교한 후향적연구를 보고하였다[8]. 방사선요법 ± 항암화학요법과 폐전이절제술 ± 항암화학요법을 시행한 군이 항암화학요법 단독군(53.8%)에 비해 국소재발률 방지(local control rate)에서 각각 88.0%, 96.4%로 우월한 결과를 보여 주었고 특히 폐전이절제술 ± 항암화학요법군이 다른 두 군들에 비해 1년, 3년, 5년 무진행생존율 및 전체생존율에서 향상된 결과(p< 0.01)를 보고하였다. 또한 방사선요법 ± 항암화학요법군 역시 항암화학요법 단독군에 비해 생존율을 향상시키는 것(p< 0.001)으로 보고하였다. 이러한 연구 결과로 미루어 볼 때 후향적 연구이기는 하나 두경부암의 폐단독 전이가 있을 때에도 다른 고형종양에서와 마찬가지로 폐전이절제술을 적극적으로 고려해야 한다고 생각된다.
일반적으로, 악성 고형종양에서 폐전이의 수술적 절제가 가능한 최소한의 기준은 다음과 같다. 1) 전이의 원인이 되는 원발성 종양은 조절되었거나 또는 폐수술 후 조절될 수 있어야 한다. 2) 폐 이외의 다른 장기에 전이가 없어야 한다. 전이가 있더라도 수술로 제거할 수 있거나 다른 방법으로 제거할 수 있어야 한다. 3) 전이에 합당한 방사선적 소견을 보여야 한다. 4) 환자의 전신상태가 계획된 폐절제술을 감당할 수 있으며, 폐절제술 후 적절한 폐기능이 유지되어야 한다. 5) 폐전이암의 완전 제거가 가능해야 한다. 6) 비수술적 방법으로 수술과 같거나 보다 좋은 치료 효과를 기대할 수 있을 때는 수술을 시행하지 않고, 수술 이외에 다른 효과적인 치료방법이 없는 경우에만 수술을 시행한다[9]. 본 증례의 환자들은 모두 위의 조건을 고려한 후 수술을 결정하였다. 4명 중 2명에서 수술 전 영상학적 검사에서 림프절 비대가 나타났으나 영상학적 검사만으로는 림프절 전이인지 양성 림프절 비대인지 구별할 수 없었기 때문에 조직 확인이 필요했으며 근치적 절제가 가능하다고 판단하여 림프절 박리술을 함께 시행하였다.
본 증례의 환자들의 술 후 현재까지의 중앙생존기간은 22.5개월(범위: 8-50개월)로 모두 현재까지 재발 소견이 없는 상태이다. 하지만 단일 기관의 보고이고, 추적관찰 기간이 짧아 다른 치료방법 즉, 보존적 치료, 항암화학요법, 항암방사선요법과 비교하여 생존율 향상을 입증할 수 없다는 한계가 있다. 또한 폐전이절제술을 시행하기 위해서는 환자를 선별하는 데 있어 선택 치우침(selectioin bias)이 있을 수밖에 없고 이러한 선택 치우침이 폐전이절제술을 시행한 환자의 결과나 예후에 영향을 미칠 수도 있다. 그러나 여러 문헌에서 환자를 잘 선별하여 폐전이절제술을 시행할 경우 두경부암에서도 국소재발률 조절 및 생존율에서 우월한 결과를 보이고 있어 기준에 부합하는 환자에서는 폐전이절제술을 고려해야 할 것으로 생각된다.
아직까지 폐전이 절제술 후의 보조적인 치료에 대한 기준은 정립되어 있지 않다. 비인두암은 수술로 전이부위를 제거했다 하더라도 미세전이의 가능성이 높고 항암화학요법에 잘 반응하므로, 수술 후 보조 항암화학요법이 무병생존기간 향상에 도움이 될 것으로 생각된다. 본 증례들은 1예를 제외하고는 5-FU를 사용하지 않았고 cisplatin을 이미 사용한 점을 고려하여 두경부암에 효과적인 TS-1을 사용하였다[10].




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






