서 론
최근에 개발된 나트륨-포도당 공동수송체 2 (sodium-glucose cotransporter 2, SGLT2) 억제제는 경구용 혈당 강하제로서, 현재 dapagliflozin, empagliflozin, ipragliflozin, canagliflozin, luseogloflozin, tofogliflozin 등이 사용되고 있다. 이 약물은 신장의 근위세뇨관에서 포도당의 재흡수를 막아 소변으로 배출시킴으로써, 혈압 강하, 체중감소 등을 동반하면서 혈당 조절에 기여한다[1]. SGLT2 억제제 투여 시 나타나는 부작용은 소변량 및 소변 횟수의 증가, 기립성 저혈압, 요로 감염 등이었다[1]. 혈중 크레아티닌의 증가 및 사구체 여과율의 감소도 관찰되었으나, 이는 대부분 가역적이었다고 보고되었다. 하지만 저자들은 급성 뇌경색으로 우측 반신마비, 운동 언어상실증, 연하불능증이 발생한 당뇨 환자에게 dapagliflozin 투여 후 발생한 급성 신손상을 경험하였기에 관련 문헌과 함께 보고하는 바이다.
증 례
환 자: 54세 남자
주 소: 갑자기 발생한 우측 반신마비
현병력: 과거 수술력이나 외상의 과거력이 없는 환자로 내원일에 갑자기 발생한 우측 반신마비, 운동 언어상실증이 있어 신경과로 입원하였다.
사회력: 특이 사항이 없었다.
가족력: 특이 사항이 없었다.
진찰 소견: 입원 당시 혈압 173/107 mmHg, 맥박수 106회/분, 호흡수 16회/분, 체온은 37.4℃였으며 급성 병색을 보였다. 흉부 청진에서 폐음이나 심음은 정상 소견을 보였다. 신경학적 검사에서 운동 언어상실증(motor aphasia), 오른쪽 상하지의 반신마비(Medical Research Council grade 2), 오른쪽 상하지의 경직 및 심부 건반사의 증가가 있었다.
검사실 소견: 입원 당시 시행한 말초혈액 검사에서 백혈구 13,800/mm3 (중성구 86.7%), 혈색소 16.3 g/dL, 혈소판 291,000/mm3였으며, C-반응성 단백(C-reactive protein)은 0.12 mg/dL였다. 전해질 검사에서 나트륨 136 mmol/L, 칼륨 4.7 mmol/L, 염소 98 mmol/L였다. 생화학 검사에서 혈청요소질소(blood urea nitrogen) 21.0 mg/dL, 크레아티닌(creatinine) 0.78 mg/dL로 정상이었고, 아스파르테이트 아미노 전달효소/알라닌 아미노 전달효소 17/15 IU/L, 총빌리루빈 0.51 mg/dL, 당화혈색소 9.9%였다. 혈액 응고 검사에서 프로트롬빈 시간(prothrombin time, PT) 11.1초, 활성화부분트롬보플라스틴 시간(activated partial thromboplastin time, aPTT) 25.3초로 정상이었다. 소변 검사에서 비중 1.029 pH 7.5, 단백뇨(±), 적혈구 5-9/high power field (HPF), 백혈구 0-1/HPF였다.
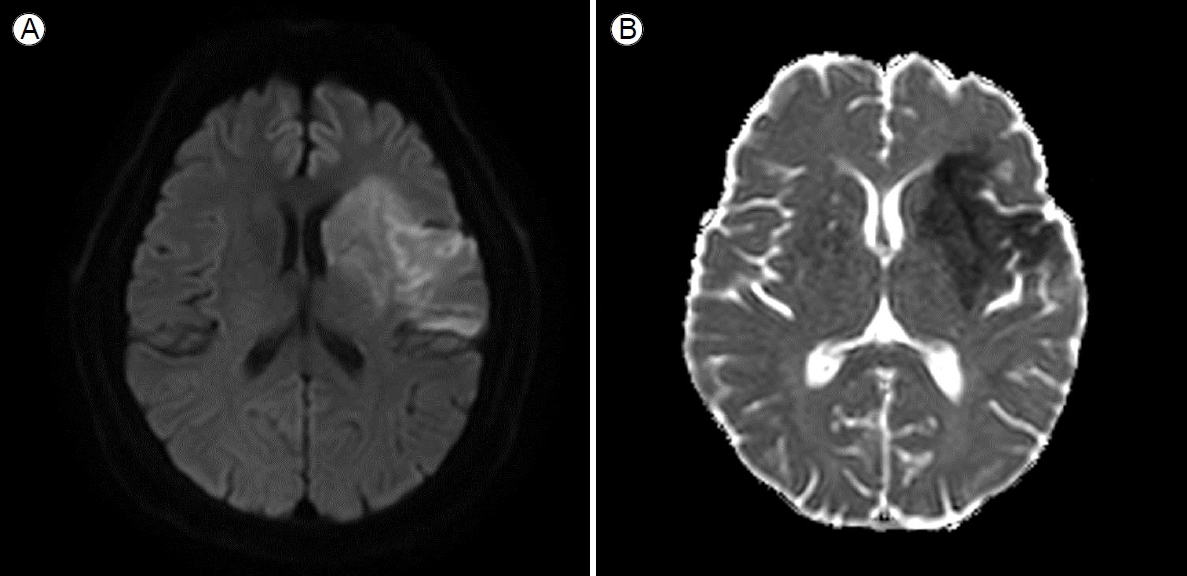
방사선 검사: 흉부 X선 촬영에서 양측 폐 음영은 정상이었고, 심장 비대는 보이지 않았다. 뇌졸중을 감별 진단하기 위해 시행한 뇌 자기공명영상에서 좌측 내경 동맥 근위부와 좌측 중대뇌동맥의 폐쇄를 동반한 좌측 전두엽 부위의 뇌경색이 관찰되었다(Fig. 1).
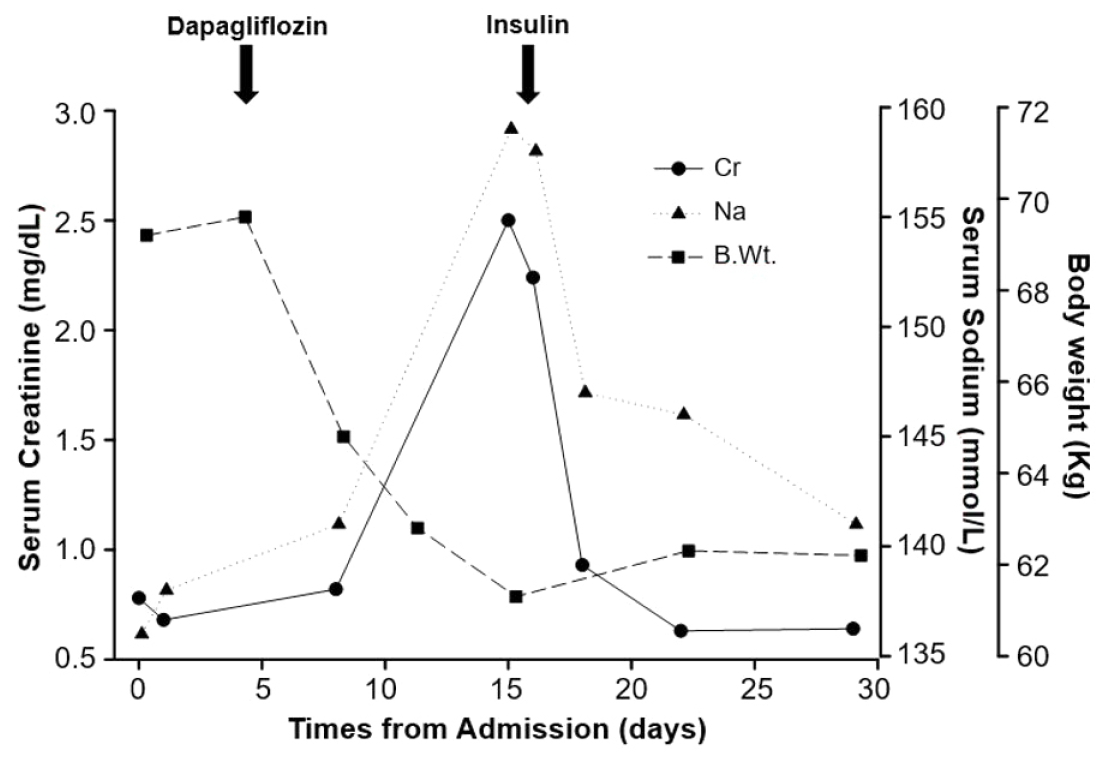
경과 및 치료: 환자는 좌측 전두엽 부위의 뇌경색 및 고혈압, 당뇨로 진단받고 신경과로 입원하여 항혈소판제제와 함께 피하 인슐린 주사, valsartan 40 mg을 포함한 항고혈압제를 투여 받았고, 입원 10일째 기존에 투여하던 피하 인슐린 주사를 중단한 뒤 dapagliflozin 10 mg을 포함한 경구혈당강하제로 변경하였다. 입원 이후 식이 처방은 경관 식이 하루 1,600 kcaL를 유지하였으며 생리식염수 시간당 40 mL의 속도로 정맥 내 투여 유지하고 있었으며 하루 총 섭취량 2,600 mL 정도였으며 총 배설량 1,500 mL로 안정적으로 유지되고 있었다. 그러나 당시 혈청요소질소 38.5 mg/dL, 혈청 크레아티닌 0.82 mg/dL였으며 체중은 64.8 kg으로 입원 당시 체중 69.2 kg보다 4.4 kg이 이미 감소한 상태였다. 입원 15일째 시행한 혈액 검사에서 혈청요소질소 100.5 mg/dL, 혈청 크레아티닌 2.50 mg/dL로 증가하였고 전해질 검사에서 나트륨 159 mEq/L로 증가한 소견이 관찰되었다. 환자는 급성 뇌경색으로 인해 발생한 운동 언어상실증으로 원활한 의사소통이 힘들었고, 오른쪽 상하지의 반신마비, 연하불능증으로 스스로 수분섭취를 하거나 식사를 할 수 없어 경관 식이를 유지하고 있었다. 입원 15일째 측정한 체중은 61.3 kg으로 입원 5일째 체중인 69.2 kg보다 7.9 kg이 감소된 상태이며 혈청요소질소/크레아티닌 비가 40에 이르는, 임상적으로 탈수에 의한 고나트륨혈증과 급성 신손상으로 진단하였다. 입원 이후 발열, 설사, 구토 또는 이뇨제 투여 등의 탈수를 일으킬만한 다른 원인은 찾을 수 없었다. Dapagliflozin을 포함한 경구혈당강하제를 인슐린 피하 주사 요법으로 다시 변경하였으며, 정맥을 통해 충분한 저장성 수액 공급을 시행하였다. 이후 혈청 나트륨이 서서히 감소하였고 입원 22일째 혈청 나트륨은 146 mmol/L, 혈청 크레아티닌 0.63 mg/dL, 체중 62.3 kg으로 회복되어 정맥을 통한 수액 공급을 중단하였다. 입원 29일째 혈청 나트륨은 141 mmol/L, 혈청 크레아티닌 0.64 mg/dL, 체중 62.2 kg이었으며 추가적인 고나트륨혈증과 급성 신손상의 재발은 발생하지 않았다(Fig. 2).
고 찰
본 증례는 SGLT2 억제제의 약물 부작용이 신장에 대해 비교적 가벼우면서 가역적이라 하더라도, 수분 섭취 의사를 충분히 표현할 수 없거나 수분의 자가 섭취가 어려운 환자의 경우에는 신전성 급성 신손상 및 고나트륨혈증을 동반한 탈수 등을 야기할 수 있으므로 주의를 기울여 사용해야 함을 교훈으로 한다는 데 그 의의가 있다고 하겠다.
Dapaglifozin은 SGLT2 억제제의 일종으로 DECLARE-TIMI 58이라는 대규모 임상 연구에서 주요 심혈관 질환을 유의하게 감소시킬 뿐만 아니라 알부민뇨의 감소를 통해 당뇨병성 콩팥 질환의 진행을 늦추는 장점이 입증되었다[2,3]. 단백뇨의 감소는, 사구체 되먹임(tubular glomerular feedback) 기전에 의해 수입 세동맥(afferent arteriole)의 긴장도가 증가하면서 생긴 사구체 내압의 감소가 당뇨병성 신병증의 진행을 늦추는 데에 기여하였을 것으로 추정되고 있다[4].
2013년 진행된 메타연구에서 dapagliflozin이 다른 혈당강하제에 비해 급성 신손상의 위험을 증가시키는 것으로 보고하였으나[5], DECLARE-TIMI 58 연구에서는 dapagliflozin이 급성 신손상의 위험을 낮추는 것으로 보고하였다[2]. Propensity score로 매칭한 두 개의 만성 질환 등록 연구(Mount Sinai CKD Registry and Geisinger Health System Cohort)에서는 SGLT2 억제제 사용군에서 다른 경구혈당강하제 사용군보다 급성 신손상의 발생 빈도가 더 적었다[6]. 따라서 SGLT2 억제제 사용과 관련된 급성 신손상의 빈도는 낮으며 드물게 발생하는 것으로 보인다. 그러나 Pleros 등[7]이 dapagliflozin 투여 후 발생한 급성 신손상을 보고한 것 이외에도 SGLT2 억제제 사용과 관련하여 급성 신손상의 보고가 지속적으로 있었고, SGLT2 억제제 사용 후 발생한 18,915건의 FDA 유해 사례 보고를 분석한 연구에서도 1,224건(6.4%)의 급성 신손상이 확인되어, SGLT2 억제제 사용이 다른 당뇨약제에 비해 급성 신손상의 발생이 3배 정도 높다는 보고도 있다[8].
Szalat 등[9]은 SGLT2 억제제가 급성 신손상을 일으키는 기전으로 1) 삼투성 이뇨에 의한 체액 용적의 고갈, 2) 세뇨관 사구체 되먹임(tubular glomerular feedback)에 의해 수입 세동맥(afferent arteriole)의 긴장도가 증가하면서 발생하는 사구체횡단압력(transglomerular pressure)의 감소, 3) 원위세뇨관으로의 용질부하로 인한 콩팥 수질의 허혈성 손상을 제시하였다. 또한 Perlman 등[8]은 SGLT2 억제제로 인한 급성 신손상이 탈수된 상태이거나 기저 신장기능에 장애가 있었던 경우에서 더 잘 발생하며, 특히 angiotensin converting enzyme (ACE) 억제제 또는 angiotensin II receptor blocker (ARB), 이뇨제를 SGLT2 억제제와 병용하여 사용한 군에서 SGLT2 억제제 단독 사용군보다 급성 신손상이 4배 더 많이 발생하였음을 보고하였다.
본 증례에서는 불행하게도 요중 나트륨 농도를 포함한 소변 검사가 진행되지 않았으나 1) 급성 신손상이 발견된 시점에서의 환자 체중은 이전보다 8 kg가량 감소되어 있었던 점, 2) 급성 뇌경색으로 인한 인지 및 운동 장애로 환자 스스로 수분이나 음식물을 섭취가 불가능한 상황이었던 점, 3) 수액 공급 후 신기능이 빠르게 회복되었던 점을 근거로 신전성 급성 신손상을 진단하였다. 환자에게 dapagliflozin이 투여된 시점에 크레아티닌 증가는 없었지만 이미 입원 시보다 4.4 kg의 체중감소가 있었던 것으로 보아 환자가 이미 탈수된 상태에서 dapagliflozin의 투여가 탈수를 더욱 조장하였을 것으로 생각된다. 급성 신손상이 발견된 시점까지 발열, 구토, 설사 및 이뇨제 투여 등의 탈수를 일으킬 만한 다른 원인은 없었고 dapagliflozin 중단 및 수액 요법으로 급성 신손상 회복 후 수액 요법 중단 및 종전 식이요법을 유지하였음에도 급성 신 손상 및 고나트륨혈증의 재발은 없어 환자가 가진 조건만으로 이 정도의 탈수를 유발하지 않았을 것으로 판단된다. 본 환자에게 조영제나 소염제와 같은 신독성 약물은 투여되지 않았으나, ARB 계열의 항고혈압제인 valsartan이 투여되고 있어 이에 의한 급성 신손상을 고려해볼 수 있었다. 그러나 ARB에 의한 전형적인 급성 신손상은 고칼륨혈증을 동반하지만 이 환자는 분명한 탈수에 의한 급성 신손상이었고 또한 체액량 회복 후 다시 나타난 고혈압에 valsartan 재투여에도 불구하고 급성 신손상은 재발하지 않았던 점으로 보아 ARB를 급성 신손상의 주요인으로 볼 수는 없다고 하겠다.
SGLT2 억제제의 작용 기전을 고려할 때, 이미 탈수되었거나 향후 탈수의 위험이 있는 환자에게는 SGLT2 억제제 투여에 주의해야 하며, ACE 억제제, ARB, 이뇨제, 신독성 약물 등을 병용하는 경우는 급성 신손상의 위험성이 더욱 증가함을 숙지해야 하겠다. 저자들은 스스로 수분 및 음식 섭취를 할 수 없었던 급성 뇌경색 환자에서 dapagliflozin 투여 후 발생한 급성 신손상을 진단한 후, dapagliflozin의 중단 및 수액 공급을 포함한 치료로 호전된 증례를 경험하였기에 문헌고찰과 함께 보고하는 바이다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






