서 론
관절 연골은 뼈 사이의 마찰을 줄여 통증이 없는 관절 운동을 가능하게 해주며, 외부 충격을 완화시켜준다. 관절 연골은 뼈 끝 관절면에 유리질 성분으로 구성되어 있다. 관절 연골의 1-5%를 차지하는 연골세포는 세포외기질(extracellular matrix, ECM)의 구성요소이며 프로테오클리칸, 콜라겐 등을 생산하여 연골의 성질을 유지한다[1]. 하지만 연골에는 혈관과 신경조직이 없기 때문에 외상, 노화, 유전적 요인 및 염증으로 인한 병리학적 변화에 의하여 손상을 받게 되면 손상된 연골이 자연 재생되지 않고 연골의 퇴화가 진행한다. 골관절염을 완치하는 근본적인 치료법은 현재까지 없고, 현대 의학의 치료 목적은 관절 손상요소를 줄이고 관절 운동 범위를 늘려서 환자가 느끼는 통증을 없애는데 집중해왔다. 체중 조절, 운동 치료, 온냉 치료, 초음파 치료와 같이 보존적 치료가 있으며, 타이레놀, 아스피린, 소염제와 같이 증상을 조절하는 약제도 사용한다. 이러한 치료법들은 질환의 진행을 막을 수 없어서 근본적인 치료제로 인정받지 못하고 있다.
본 론
연골 재생을 위한 치료 전략
현재까지 다양한 외과술기, 조직공학 치료법, 약제 등을 통해서 연골 재생을 위한 치료법이 시도 되어왔다. 지금까지 시도된 구체적인 치료법을 소개하고 장단점과 한계점을 기술하였다.
미세천공술(microfracture)
미세천공술은 뼈에 작은 구멍을 내, 골수 유래 중간엽줄기세포(bone marrow-derived mesenchymal stem cells, BMSCs)를 손상된 연골로 이동과 분화를 유도하여 연골의 재생을 돕는 방법이다[2]. 미세 천공술의 치료 효과를 보여주는 여러 임상연구들이 존재하지만[3-5] 단기간, 중기간 및 장기간의 연골 회복 효과가 일정하지 않으며 환자의 BMSCs의 양과 질도 치료 효과에 큰 영향을 준다[6]. 지속적인 관절 수동 운동 치료를 받은 환자가 미세천공술 이후 회복 정도가 더 좋았기 때문에 수술만큼이나 재활도 중요하다[7]. 하지만 이러한 미세천공술의 한계점은 미세 균열이 큰 병변(> 3 cm2)에는 적합하지 않으며, 유리질연골이 아닌 섬유연골로 분화가 되어질 좋은 연골을 재생하지 못한다는 단점을 가진다.
자가연골이식술(autologous chondrocyte implantation [ACI], matrix-induced ACI [MACI])
자가연골이식술(ACI)은 연골 재생법 중 하나로서, 관절의 물리적 부하가 덜 가는 부분에서 연골을 얻어 시험관 내에서 치료로 사용할 연골세포를 분리하고 증식 배양하여 연골 결손 부위에 사용하는 방법이다[8,9]. 미세천공술과 달리 ACI는 큰 연골 결함(> 3 cm2)의 치료에 효과적이며, 10년 이상 지속되는 장기간 연구에서 유리한 임상적 결과를 보였다[10-12]. 또한 환자 자신의 세포를 사용하기 때문에 잠재적인 면역 합병증을 피할 수 있다[13,14]. MACI는 ACI를 개량한 치료법이다. ACI와 달리 MACI는 제I형 콜라겐 또는 제III형 콜라겐 막에 연골세포를 배양한다. 장기간 배양하는 동안 관절 연골세포의 특성을 유지하는데 도움이 되며 연골세포의 소실을 방지하는 장점이 있다[15,16]. 하지만 ACI와 MACI의 한계점은 두 가지 방법 모두 환자에게서 연골세포를 얻어내어 환자에게 이식해야 하기 때문에 두 번의 수술이 필요하다는 점이다[8]. 또한 MACI에 사용되는 지지체가 콜라겐 및 히알루론산 지지체의 혼합물이기 때문에 면역 반응을 증가시킬 위험성도 가지고 있으며[17,18], 연골세포는 연골 조직의 5% 미만으로 구성되어있기 때문에 결국 치료제로 사용하기 위해서는 시험관 내 배양을 통한 세포 수 확보가 필요하다. 시험관 배양 과정에서 연골세포는 연골 특성을 상실하고 제I형 콜라겐과 같이 섬유아세포 마커 발현이 증가하게 된다. 따라서 순수한 유리질연골을 얻는 대신 섬유성 연골세포를 얻을 수 있다는 한계점을 가진다[19-21].
인공 지지체(scaffold)
인공 지지체(scaffold)는 조직 공학용 체외 연골 형성을 촉진하기 위하여 일반적으로 사용된다[21,22]. 연골세포와 골수 유래 중간엽줄기세포(BMSCs)는 연골 조직 공학에서 가장 일반적으로 사용되는 세포이며, 이 세포들의 세포 생존 및 연골 분화를 향상시키기 위하여 인공 지지체가 사용된다. 인공 지지체는 천연 생분해성 고분자(proteins, polysaccharides, and polynucleotides)와 합성 생분해성 고분자(poly-lactic acid, poly-glycolic acid, poly-lactic-co-glycolic acid [PLGA])가 있다. 인공 지지체는 흡수성이거나 생분해 성분으로 구성되어야 하며 연골 형성에 유리하게 설계가 되어야 한다. 인공 지지체는 세포 이동 촉진 및 기공 구조, 분자 이동도, 화학적 기능성, pH, 분해성, 탄력성 등이 고려되어야 한다. 이러한 조건이 고려가 되면 세포는 2D 형태보다 3D 구조에서 세포 응집이 잘 되고, ECM 생산을 향상시킨다[23,24]. 하지만 연골세포의 사멸 및 세포 누출, 조직과의 부적절한 integration이 문제가 되고 있다. 이러한 문제뿐만 아니라 다양한 이유로 인공 지지체의 한계점들이 발견이 되고 있다. 예를 들면 인공 지지체-PLGA를 이용한 연골 결손 치료의 경우에서 연골 치료의 효과를 볼 수는 있었지만, PLGA의 hydrophobicity 때문에 치료 효능이 제한적이었다. 따라서 지금도 끊임없이 인공 지지체뿐 아니라 세포의 부착, 분화를 개선하기 위한 다양한 노력이 이루어지고 있다[25-27].
무지지체 3D 배양(scaffold-free 3D culture)
연골 형성은 2D보다 3D 형태의 배양 시스템에서 더 효과적이다[28]. 2D 연골 배양법은 연골 특유의 성질을 잃기 쉽고 제II형 콜라겐이나 어그리칸(aggrecan)보다는 제I형 콜라겐 분비가 증가하며 유리질연골이 아닌 섬유연골이 된다[29,30]. 이러한 문제점을 해결하기 위하여 세포가 서로 상호 작용하며 3D 형태로 연골 분화를 할 수 있는 펠렛(Pellet) 배양과 마이크로 매스(micromass) 배양 기법이 있다. 이러한 방법은 밀도 및 기질 조성의 관점에서 본래의 관절 연골과 매우 유사하다[29,31]. 하지만 이러한 배양법도 3D 형태의 연골 펠렛의 중심 부분은 종종 미분화 및 괴사를 일으키는 단점이 있다[32,33]. 그리고 인공 지지체를 이용한 방법보다 연골 유사 구조물을 생성하기 위해서는 더 많은 수의 세포가 필요하다[34]. 그럼에도 불구하고 펠렛 배양과 마이크로 매스 배양은 시험관 내 연골 형성에 널리 사용되는 방법이다.
줄기세포를 이용한 연골 재생
골수 유래 중배엽줄기세포(bone marrow-derived mesenchymal stem cells, BMSCs)
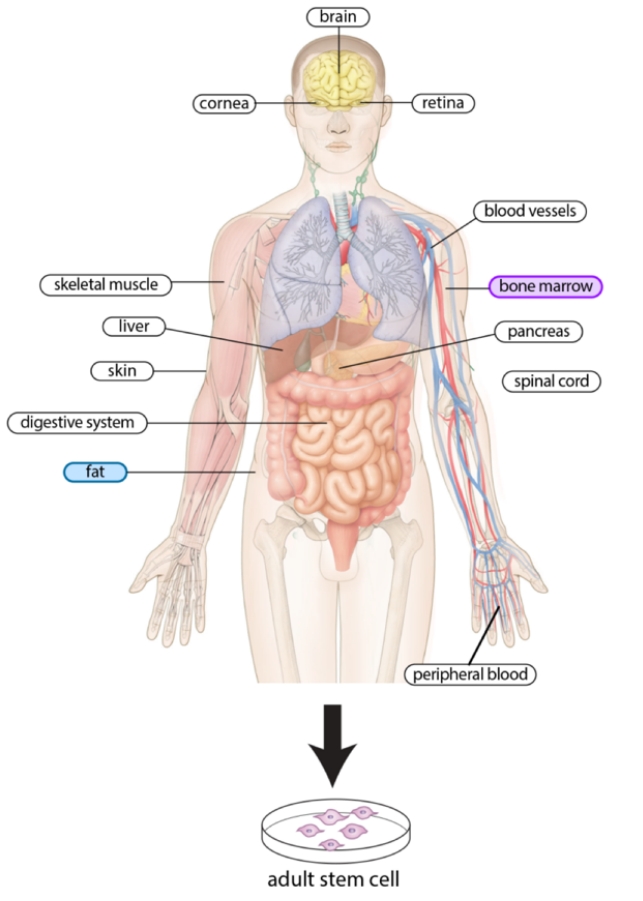
중배엽줄기세포는 다양한 조직에서 쉽게 얻을 수 있고, 그 중에서도 인간의 골수에서 가장 흔히 분리된다(Fig. 1) [35,36]. 골수 기질세포는 mesengenesis라고 불리는 과정을 통하여 지방세포와 골아세포를 포함한 중간엽세포로 분화하는 것으로 80년대 후반에 처음 제안되었으며, 이 세포들은 결과적으로 “BMSCs”로 명명되었다. 이 과정은 다양한 시험관내 분석법을 사용하여 연구되었다. 이러한 BMSCs는 여러 질병을 치료하는데 사용되어 왔으며 골관절염 환자에서 자가 BMSCs의 주입은 손상된 관절 연골의 회복에 도움이 된다. 주입된 BMSCs는 면역 조절 효과를 이끌어 낼 수도 있으며, 시험관 내에서 연골 분화를 할 수 있는 능력은 다양한 논문들로 증명이 되었다[37-39]. 하지만 이러한 BMSCs의 단점은 환자의 골수 체취 중 환자에게 통증을 유발하며, 소량의 골수를 얻기 때문에 BMSCs를 치료제로 사용하기 위해서는 in vitro 상에서 BMSCs 세포 수를 증가시켜야 한다. 연골세포와 유사하게, 대부분의 성체 줄기세포(ex, BMSCs)는 4-6 계대배양 후 감소된 분화능 및 증식을 보인다. BMSCs의 장점에도 불구하고, 배양된 BMSCs의 느린 증식 속도와 골수에서 얻은 적은 수의 세포가 해결되어야 한다[40-42].
지방 줄기세포(adipose tissue-derived stem cells, ASCs)
ASCs는 지방 조직의 stromal vascular fraction (SVF)을 분리함으로써 얻어진다. 이것은 지방 흡입 수술의 폐기물인 lipoaspirate가 collagenase로 효소 처리되어 생산되는 세포이다. 연속적인 계대배양 후, 부착 세포는 ASCs로 얻게 된다. SVF와 ASCs 모두 치료 가능성이 있으며 BMSCs에 비하여 덜 침습적이고 높은 수율 때문에 BMSCs의 대안으로 제시되고 있다[43-45]. 또한 ASCs는 BMSCs에 비하여 배양이 더 쉽고 빠르게 증식하며 노화되기 전에 장기간 배양될 수 있다[46,47]. ASCs는 다양한 연구에서 연골로 분화될 수 있음을 보여주었고, 임상시험에서 연골 재생에 사용되어 효과를 확인할 수 있었다[48,49]. 그러나 다른 연구들에서 BMSCs가 ASCs보다 COL2A1의 수준이 높고 인공 지지체 내에서 배양될 때 더 많은 ECM이 생성된다는 것을 확인하였다. 또한 3D 배양 시스템에서는 BMSCs가 ASCs보다 연골 형성능이 우수하였다. 하지만 BMP6의 성장인자를 이용한 연골 분화 조건 하에서는 ASCs가 BMSCs 연골 분화보다 aggrecan 발현이 높기도 하다. 여러 가지 조건 하에서 BMSCs와 ASCs 연골 분화능을 비교하는 연구들이 많이 진행되고 있다.
성체 줄기세포를 이용한 연골 재생
외과적인 방법(전방십자인대와 반월판을 제거)을 이용하여 연골 손상 동물모델을 만들고, BMSCs를 관절강내에 주사하면 BMSCs가 상대적으로 낮은 검출에도 불구하고 연골조직 재생을 촉진시킨다[50]. 화학적인 방법(ex, mono-iodoacetate-induced rat models)을 통하여 만들어진 연골 손상 쥐 모델에서 관절내 BMSCs의 투여는 동물이 몸의 하중을 견딜 때 체중을 분산시키는 것을 확인함으로써, 그 효과를 확인할 수 있었다. 하지만 이러한 기능적 향상에도 불구하고, 치료군과 대조군 간에 통계적, 유의적 차이는 나타나지 않았으며, BMSCs 주사로 치료한 군에서 연골 및 연골 하골의 병리학적 염증이 관찰되기도 한 연구도 있다[51,52]. 임상시험에서는 골관절염 치료에 ASCs를 사용한 임상 1상과 2상에서 연골 회복에 대한 MRI의 증거를 보였다. 제II형 콜라겐의 조직학적 평가에서 6개월간의 추적 관찰 결과 1억 개의 MSCs가 주입된 후 유리질연골이 재생됨을 확인하였다. 또한 관절 내 ASCs의 단일 주사가 연골 조직 재생뿐만 아니라, 운동 범위도 현저하게 개선시켜주는 것을 확인하였다. BMSCs와 ASCs를 사용하여 관찰된 긍정적인 전임상 결과들에 근거하여 미세 천공술과 함께 말초혈액 MSCs의 사용을 포함하는 다양한 실험을 진행해 보았을 때도, MSCs를 투여받은 환자에게서 연골 회복이 잘 되었음을 조직학적 분석 및 MRI 평가로 확인할 수 있었다[53]. 그 밖의 meniscectomy 후 MSCs의 효능을 평가하는 임상시험 결과에서도 대조군에 비하여 연골 손상 부위의 회복을 관찰할 수 있었으며, 반월판 부피의 재생에 대한 증거도 볼 수 있었다. 모든 전임상 결과들이 모두 일관성이 있지는 않지만 MSCs와 ASCs를 관절 내로 주사한 경우 치료 효과가 향상된다는 많은 연구 결과가 있다.
유도만능줄기세포(induced pluripotent stem cells)
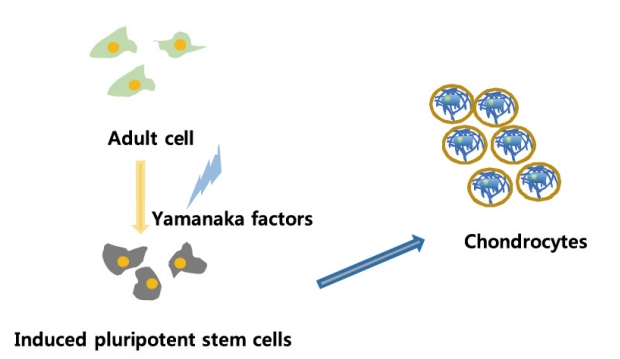
유도만능줄기세포는 4개의 Yamanaka factor (Klf4, Oct3/4, Sox2, c-Myc)로 마우스 섬유아세포를 형질 도입함으로써 2006년에 처음으로 소개되었다. 2007년에는 인간 체세포에 Klf4, Oct3/4, Sox2, c-Myc 또는 Sox2, Oct3/4, Nanog, Lin28을 도입하여 성공적으로 유도만능줄기세포를 생산하였다. 유도만능줄기세포는 사람의 배아줄기세포(embryonic stem cell, ESC)와 유사한 특성을 갖는다. 그러나 유도만능줄기세포는 무제한 증식이 가능하고 self-renew할 수 있으며 ESC와 같은 윤리적 문제는 피할 수 있다는 큰 장점이 있다. 따라서 유도만능줄기세포는 최근 재생의학의 주목받은 세포원으로써 각광받고 있다[38,54]. 유도만능줄기세포는 혈액세포, 소변세포 등등 유도만능줄기세포의 공급원이 되는 체세포를 쉽게 얻을 수 있다는 장점이 있다. 사람의 혈액 5 mL만 있다면, 30일 이내로 유도만능줄기세포를 만들 수 있다[55,56]. 또한 제대혈세포, 관절활막세포, 성체 줄기세포(ex, ASCs 및 MSCs), 신경세포, 연골세포, 골세포, 피부세포, 간세포, 심장세포, 근육세포 등 원하는 세포의 성질로 바꿀 수 있다는 점은 큰 장점이다(Fig. 2) [37,57-60]. 유도만능줄기세포 제작 초기프로토콜은 Yamanaka factor들의 통합을 촉진하기 위하여 렌티바이러스 혹은 레트로바이러스 형질 도입을 사용하였지만, 임상적 사용에 보다 더 적합한 방법들에 대한 여러 학계의 논의를 거쳐 현재는 센다이바이러스, 에피좀 벡터, 소분자, 단백질 등을 이용한 프로토콜로 변형되어 바이러스의 integration을 피하기 위한 방법들로 변하는 중이다[56,61]. 이렇게 생산된 유도만능줄기세포는 재생의학, 약물 스크리닝, 질환특이적 메커니즘 연구 등 다양한 용도로 이용되고 있다.
유도만능줄기세포를 이용한 연골 재생
유도만능줄기세포를 이용한 연골세포의 치료 효과는 최근 여러 동물모델에서 확인되었다. 2014년 배아체(embryonic body, EB) 배양과 Aliginate Beads를 이용한 연골 분화 유도, EB 세포를 분리하여 Micromass 방법 등을 이용하여 연골 펠렛을 만들고 이를 면역 결핍 렛트의 연골 손상 부위에 이식하였다. 12주 후, 섬유 조직이 있거나 거친 표면을 보이는 대조군에 비하여 연골 펠렛을 이식한 군에서의 결함은 매끄럽고 단단한 조직으로 채워졌고 조직학적 분석을 통해서도 손상연골의 회복을 입증하였다[63]. 유도만능줄기세포에서 유래된 연골세포를 monosodium iodoacetate induced cartilage damage 모델에 이식하여 연골 재생 효과를 확인하였다[64]. 유도만능줄기세포 유래 연골세포는 우수한 연골 재생 능력을 가졌고 연골 표면에서 프로테오글리칸의 레벨을 증가시켰다. 2015년에 유도만능줄기세포 유래 연골세포를 대동물에 이식하였다[65]. 연골세포가 연골 결손 부위에 이식되어 연골 손상된 부위가 회복되었으며, 그 부위에서 인간 vimentin의 발현을 관찰하여 투여된 연골 펠렛에 의한 직접 재생 치료 효과를 확인하였다.
결 론
연골의 손상은 관절의 통증과 심각한 기능 장애를 유발한다. 그러나 연골에는 혈관과 신경이 존재하지 않기 때문에 재생 능력이 제한되어 있어서 손상이 회복되지 않는다. 현재까지 개발된 화합물 기반 제제 및 생물학적 제제는 연골 회복을 촉진시키는 증거가 부족하다. 이에 세포 기반 치료법은 연골 재생을 위한 방법으로 관심을 받고 있다. 자가 연골세포 및 성체 줄기세포는 연골 재생에 사용되어 왔으나 다양한 제한점 때문에 유도만능줄기세포와 같이 분화능과 세포원 확보가 유리한 치료제가 한참 개발 중이다[38]. 세포 치료제의 재료의 관점뿐만 아니라 투여 형태, 지지체 응용 등에 대한 다양한 개발 전략이 진행되고 있어서[66] 고령화 시대를 맞이하여 노인 환자의 삶의 질에 큰 영향을 미치는 골관절염에 대한 연골 재생 치료가 실제로 진료실에서 사용될 날이 조만간 도래할 것으로 예측된다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






