 |
 |
| Korean J Med > Volume 93(4); 2018 > Article |
|
Abstract
Atrial fibrillation (AF) is the most common form of sustained arrhythmia in elderly patients. However, AF is often detected during health screening, or accidentally during testing for other diseases; some patients lack clinical symptoms. Nevertheless, AF increases the incidence of ischemic stroke and other thrombotic events, and compromises cardiovascular prognosis in terms of heart failure, dementia, and hospitalization. Therefore, initial AF management should be performed at the point of primary care, not only in specialized medical centers. We wish to propose a five-step management protocol for AF. We review the evidence supporting integrated management by primary care physicians new to AF, and by specialized physicians who often diagnose and manage AF. Further, we also outline a structured goal-based follow-up protocol; this is an important part of integrated management.
ņŗ¼ļ░®ņäĖļÅÖņØĆ ņŻ╝ļĪ£ Ļ│ĀļĀ╣ņŚÉņä£ ļ░£ņāØĒĢśļŖö ņ¦ĆņåŹņä▒ ļČĆņĀĢļ¦źņØś Ļ░Ćņן ĒØöĒĢ£ ĒśĢĒā£ņØ┤ļŗż. ĻĘĖļ¤¼ļéś ņØ┤ļ¤¼ĒĢ£ ņŗ¼ļ░®ņäĖļÅÖņØĆ ņ”ØņāüņØ┤ ņŚåļŖö Ļ▓ĮņÜ░Ļ░Ć ļ¦ÄņĢä, Ļ▒┤Ļ░ĢĻ▓Ćņ¦äņØä ĒåĄĒĢśņŚ¼ ļ░£Ļ▓¼ņØä ĒĢśĻ▒░ļéś, ļŗżļźĖ ņ¦łļ│æņŚÉ ļīĆĒĢ£ Ļ▓Ćņé¼ ļÅäņżæ ņŗ¼ņĀäļÅä Ļ▓Ćņé¼ļĪ£ ņÜ░ņŚ░Ē׳ ļ░£Ļ▓¼ļÉśļŖö Ļ▓ĮņÜ░Ļ░Ć ļ¦Äļŗż. ĻĘĖļ¤╝ņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ņŗ¼ļ░®ņäĖļÅÖņØĆ ĒŚłĒśłņä▒ ļćīņĪĖņżæņØä ļ╣äļĪ»ĒĢ£ ņāēņĀäņ”ØņØś ļ░£ņāØņØä ņ”ØĻ░Ćņŗ£Ēéżļ®░, ņŗ¼ļČĆņĀä, ņ╣śļ¦ż, ņ×ģņøÉņ£©ņØś ņ”ØĻ░Ć ļō▒ ĒÖśņ×ÉņØś ņŗ¼ĒśłĻ┤Ć Ļ┤ĆļĀ© ņśłĒøäļź╝ ņĢģĒÖöņŗ£ĒéżļŖö ņÜöņØĖņ£╝ļĪ£ ņ×æņÜ®ĒĢśĻ▓ī ļÉ£ļŗż[1,2]. ļö░ļØ╝ņä£ ņŗ¼ļ░®ņäĖļÅÖņØś ņ¦äļŗ©Ļ│╝ ņ╣śļŻīļŖö ĒÖśņ×Éļź╝ ņ▓śņØī ņĀæĒĢśĻ▓ī ļÉśļŖö ņØ╝ņ░© ņØśļŻīņØĖņŚÉņä£ļČĆĒä░ ņŗ£ņ×æļÉśņ¢┤ņĢ╝ ĒĢ£ļŗż. ĻĘĖļ¤¼ĒĢ£ ņØśļ»ĖņŚÉņä£ ņŗ¼ļ░®ņäĖļÅÖņØś ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīļź╝ ļŗżņØīĻ│╝ Ļ░ÖņØĆ ļŗżņä» Ļ░Ćņ¦ĆņØś ļŗ©Ļ│äļĪ£ ļéśļłäņ¢┤ ņäżļ¬ģĒĢśĻ│Āņ×É ĒĢ£ļŗż(Fig. 1). 1) ņŗ¼Ļ░üĒĢ£ Ļ┤ĆļĀ© ņ”ØņāüņØś ņĪ░ņĀł, 2) Ļ┤ĆļĀ© ņ£äĒŚśņÜöņØĖ(Ļ░æņāüņäĀĻĖ░ļŖźĒĢŁņ¦äņ”Ø, ņłśņłĀ Ēøä ņāüĒā£)ņŚÉ ļÅÖļ░śļÉ£ ņŗ¼ĒśłĻ┤Ćņ¦łĒÖśņØś Ļ┤Ćļ”¼, 3) ņŗ¼ļ░®ņäĖļÅÖņ£╝ļĪ£ ņØĖĒĢ£ ļćīņĪĖņżæņØś ņśłļ░®, 4) ļ░ĢļÅÖņłśņØś ņĪ░ņĀł, 5) ņ”Øņāü ņĪ░ņĀłņØä ņ£äĒĢ£ ļ”¼ļō¼ ņĪ░ņĀł.
ņØ┤ņÖĆ Ļ░ÖņØĆ ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīļŖö Ļ░ĆņØ┤ļō£ļØ╝ņØĖņŚÉ ĻĘ╝Ļ▒░ĒĢ£ ņŗ¼ļ░®ņäĖļÅÖņØś ņØ╝Ļ┤ĆņĀüņØĖ ņ╣śļŻīņØś ĻĘ╝Ļ░äņØ┤ ļÉśļ®░ ĒÖśņ×ÉņØś ņ╣śļŻī ņä▒ņĀüņØä Ē¢źņāüņŗ£ĒéżļŖöļŹ░ ļÅäņøĆņØä ņżĆļŗż(Fig. 2) [3-6]. ĻĘĖļ”¼Ļ│Ā ņØ┤ļ¤¼ĒĢ£ ņ╣śļŻīļ▓ĢņØĆ ņäĖĻ│äļ│┤Ļ▒┤ĻĖ░ĻĄ¼(World Health Organization)ņŚÉņä£ ļ¦īņä▒ ņ¦łĒÖśņŚÉ ļīĆĒĢ£ ņĀäņØĖņĀüņØĖ ņĀæĻĘ╝Ļ│╝ ņ╣śļŻīļź╝ ņ£äĒĢśņŚ¼ ņĀ£ņĢłĒĢ£ ļé┤ņÜ®Ļ│╝ ņØ╝ņ╣śĒĢ£ļŗż[7]. ņŗ¼ĒśłĻ┤Ćņ¦łĒÖśņŚÉ ļīĆĒĢ£ ņŗ¼ļ░®ņäĖļÅÖņØś ņśüĒ¢źņØä ņĀĢĒÖĢĒ׳ ĒÅēĻ░ĆĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö, ņ┤łĻĖ░ ņ¦äļŗ© Ēøä, ĒŖ╣Ē׳ Ēæ£ 1ņŚÉņä£ ĻĖ░ņłĀļÉ£ ņāüĒÖ®ņ▓śļ¤╝ ņŗĀņåŹĒĢ£ ņ╣śļŻīĻ░Ć ĒĢäņÜöĒĢ£ Ļ▓ĮņÜ░ ņŗ¼ņןļé┤Ļ│╝ ņĀäļ¼Ė ņØśļŻīņ¦äņŚÉĻ▓ī ņØśļó░ĒĢśļŖö Ļ▓āņØ┤ ĒĢäņÜöĒĢśļŗż.
ļ┐Éļ¦ī ņĢäļŗłļØ╝, ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīļŖö ĻĖ░ņĪ┤ņØś ĒåĄņāüņĀüņØĖ ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ņ╣śļŻīņŚÉņä£ ļ│┤ņŚ¼ņ¦ĆļŖö ĒĢŁņØæĻ│ĀņĀ£ņÖĆ ņ”Øņāü ņĪ░ņĀłņØä ņ£äĒĢ£ ņĢĮļ¼╝ņØś ļČĆņĀüņĀłĒĢ£ ņé¼ņÜ®ņØś ĒĢ£Ļ│äļź╝ ĻĘ╣ļ│ĄĒĢśĻ│Ā, Ļ┤ĆļĀ© ņŗ¼ĒśłĻ┤Ćņ¦łĒÖśņØś ņ£äĒŚśņØä Ļ░Éņåīņŗ£ĒéżļŖö ļŹ░ ļÅäņøĆņØä ņżä ņłś ņ׳ļŗż. ļö░ļØ╝ņä£ ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīļŖö ĒÖśņ×Éļź╝ ņ▓śņØī ņĀæĒĢśĻ▓ī ļÉśļŖö ņØ╝ņ░© ņØśļŻīņ¦äņØś ĒśæņĪ░ļź╝ ĒĢäņÜöļĪ£ ĒĢśĻ▓ī ļÉśļ®░, ņØ┤Ēøä ĒÖśņ×Éļź╝ ĒżĒĢ©ĒĢ£ ņŗ¼ņןļé┤Ļ│╝, ņÖĖĻ│╝, ļćīņĪĖņżæ ņĀäļ¼ĖņØśņŚÉ ņØ┤ļź┤ĻĖ░Ļ╣īņ¦Ć ņĀäļ¼ĖņĀüņØĖ ņ¦äļŻīņØśļōżņØś ļŗżĒĢÖņĀ£ņĀü ņĀæĻĘ╝ņØ┤ ļÆżļö░ļź┤Ļ▓ī ļÉ£ļŗż(Table 2). ņØ┤ņŚÉ ļ│Ė ņ¦äļŻī ņ¦Ćņ╣©ņŚÉņä£ļŖö ņŗ¼ļ░®ņäĖļÅÖņØś ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīņŚÉ ļīĆĒĢ£ ņØśĒĢÖņĀü ĻĘ╝Ļ▒░ļź╝ ņé┤ĒÄ┤ļ│┤Ļ│Ā, ņŗ¼ļ░®ņäĖļÅÖņØś ļ░£ņāØĻ│╝ ņśłĒøäņŚÉ ņśüĒ¢źņØä ņŻ╝ļŖö ņÜöņØĖļōżņŚÉ ļīĆĒĢ£ ņóģĒĢ®ņĀüņØĖ ņ¦äļŗ©Ļ│╝ ņ╣śļŻī ņøÉņ╣ÖņŚÉ ļīĆĒĢśņŚ¼ ņĢīņĢäļ│┤Ļ│Āņ×É ĒĢ£ļŗż. ĻĘĖļ”¼Ļ│Ā ņŗ¼ļ░®ņäĖļÅÖņØś ĒåĄĒĢ®ņĀü ņ╣śļŻīņŚÉņä£ ņżæņÜöĒĢ£ ņČĢņØä ņØ┤ļŻ©Ļ│Ā ņ׳ļŖö ĒÖśņ×É ĻĄÉņ£ĪĻ│╝ ņ░ĖņŚ¼ ĻĘĖļ”¼Ļ│Ā ĻĘĖļōżņŚÉ ļīĆĒĢ£ ņ▓┤Ļ│äņĀüņØĖ ņČöņĀü Ļ┤Ćņ░░ņŚÉ ļīĆĒĢśņŚ¼ ņé┤ĒÄ┤ļ│┤Ļ│Āņ×É ĒĢ£ļŗż.
ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīņŚÉļŖö ĒÖśņ×ÉņÖĆ ņØśļŻīņ¦ä ĻĘĖļ”¼Ļ│Ā ņØ┤ļź╝ ļÆĘļ░øņ╣©ĒĢśļŖö ļŗżņ¢æĒĢ£ ļ░®ņŗØņØś ņØśļŻī ĻĖ░ņłĀņĀüņØĖ ņÜöņåīļōżņØ┤ ĒżĒĢ©ļÉ£ļŗż. ņØ┤ļ¤░ ļ░®ņŗØņØś ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīļŖö Ļ░ĆņØ┤ļō£ļØ╝ņØĖņŚÉ ĻĘ╝Ļ▒░ĒĢ£ ņŗ¼ļ░®ņäĖļÅÖņØś ņØ╝Ļ┤ĆņĀüņØĖ ņ╣śļŻīņØś ĻĘ╝Ļ░äņØ┤ ļÉśļ®░ ĻČüĻĘ╣ņĀüņ£╝ļĪ£ ĒÖśņ×ÉņØś ņ╣śļŻī ņä▒ņĀüņØä Ē¢źņāüņŗ£ĒéżļŖöļŹ░ ļÅäņøĆņØä ņżĆļŗż[3-6]. ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ļ¼┤ņ×æņ£ä ļīĆņĪ░ ņŗżĒŚśņŚÉņä£, ĒåĄĒĢ®ņĀüņØĖ ņ¦łļ│æņØś ņ╣śļŻīļŖö ņØ╝ļ░śņĀüņØĖ ņ╣śļŻīņŚÉ ļ╣äĒĢśņŚ¼, ņŗ¼ĒśłĻ┤Ćņ¦łĒÖśņ£╝ļĪ£ ņØĖĒĢ£ ņ×ģņøÉĻ│╝ ņé¼ļ¦ØņØä 22Ļ░£ņøöĻ░ä 1/3Ļ╣īņ¦Ć Ļ░Éņåīņŗ£ņ╝░ļŗż[8]. ĻĘĖļ”¼Ļ│Ā ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīļŖö ļ╣äņÜ® ĒÜ©Ļ│╝ņĀüņØĖ ņĖĪļ®┤ņŚÉņä£ļÅä ĻĖŹņĀüņĀüņØĖ ĒÜ©Ļ│╝ļź╝ Ļ▒░ļæÉņŚłņ£╝ļ®░[9], ņØ┤ņŚÉ ļīĆĒĢ£ 2Ļ░£ņØś ļīĆĻĘ£ļ¬© Ļ┤Ćņ░░ ņŚ░ĻĄ¼ņŚÉņä£ļŖö ņØ╝ļ░śņĀüņØĖ ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ņ╣śļŻīņŚÉ ļ╣äĒĢśņŚ¼ ļé«ņØĆ ņ×ģņøÉņ£©[10,11], ļé«ņØĆ ļćīņĪĖņżæņØś ļ░£ņāØ[10]ņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗż. ĻĘĖļ”¼Ļ│Ā ņŗ¼ļ░®ņäĖļÅÖĻ│╝ Ļ┤ĆļĀ©ĒĢ£ ņØæĻĖēņŗż ļé┤ņøÉ ļ╣äņ£©ņØś Ļ░Éņåī, ņŗ¼ĒśłĻ┤ĆĻ│ä ņ×ģņøÉ ļ╣äņ£©ņØś Ļ░Éņåī, ņé¼ļ¦ØļźĀņØś Ļ░Éņåī ļō▒ņØś ĒÜ©Ļ│╝ļź╝ ļ│┤ņŚ¼ņŻ╝ņŚłļŗż[12]. ņØ┤ņ▓śļ¤╝, ņāłļĪŁĻ▓ī ļ░£ņāØĒĢ£ ņŗ¼ļ░®ņäĖļÅÖņØś ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīļŖö ļ░ĢļÅÖņłś ņĪ░ņĀłĻ│╝ ļ”¼ļō¼ ņĪ░ņĀł ĻĘĖļ”¼Ļ│Ā ĒĢŁņØæĻ│Ā ņ╣śļŻīņŚÉ ņ׳ņ¢┤ņä£ ļČĆņĀüņĀłĒĢ£ ņ╣śļŻīļĪ£ ņØĖĒĢ£ ņŗ¼ĒśłĻ┤Ć ņé¼Ļ▒┤ņØś ņ”ØĻ░Ćļź╝ ņśłļ░®ĒĢśļŖö ļŹ░ņŚÉļÅä ļÅäņøĆņØä ņŻ╝ņŚłļŗż.
ņŗ¼ļ░®ņäĖļÅÖĻ│╝ Ļ░ÖņØĆ ļ¦īņä▒ ņ¦łĒÖśņØĆ ĒÖśņ×É ņŖżņŖżļĪ£ ļ│æņŚÉ ļīĆĒĢ£ ņ¦ĆņŗØņØä ņל Ļ░¢ņČöĻ│Ā ņ╣śļŻī Ļ│╝ņĀĢņŚÉņä£ ņ×ÉņŗĀņØś ņ▒ģņ×äņØä ņØĖņ¦ĆĒĢśĻ│Ā ņ׳ļŖö Ļ▓ĮņÜ░ņŚÉ ļŹö ļéśņØĆ ņןĻĖ░ņĀü ņ╣śļŻī ĒÜ©Ļ│╝ļź╝ ĻĖ░ļīĆĒĢĀ ņłś ņ׳ļŗż[7]. ņ╣śļŻī Ļ▓░ņĀĢ ļŗ©Ļ│äņŚÉ ĒÖśņ×Éļź╝ ņ░ĖņŚ¼ņŗ£ĒéżļŖö ļō▒ ĒÖśņ×É ņżæņŗ¼ņØś ņ╣śļŻīļź╝ ĒĢśĻ▓ī ļÉśļ®┤ ņ╣śļŻīņł£ņØæļÅäļź╝ ļåÆņØ┤Ļ│Ā ĒÖśņ×É Ļ░£Ļ░£ņØĖņØś ņäĀĒśĖļÅäļéś ņÜöĻĄ¼ņé¼ĒĢŁ ļ░Å ņ×Éņ£©ĻČīņØä ņĪ┤ņżæĒĢĀ ņłś ņ׳ļŗż[13]. ņ╣śļŻī Ļ│╝ņĀĢņŚÉņä£ ĒÖśņ×ÉņØś ņŚŁĒĢĀņØä Ļ░ĢĒÖöĒĢśĻ│Ā ļŖźļÅÖņĀüņØĖ Ļ░£ņ×ģņØä ņŗ£ņ╝░ņØä ļĢī ņ╣śļŻī ņä▒ņĀüņØ┤ Ē¢źņāüļÉ©ņØ┤ ņ×ģņ”ØļÉ£ ļ░ö ņ׳ļŗż[14,15]. ĒÖśņ×É ņżæņŗ¼ ņ╣śļŻīļź╝ ņ£äĒĢ┤ņä£ļŖö ĒåĄĒĢ®ņĀü ĒÖśņ×É ĻĄÉņ£ĪņØä ĒåĄĒĢśņŚ¼ ĒÖśņ×É ņŖżņŖżļĪ£ ņ¦ĆņŗØņØä Ļ░¢ņČöļŖö Ļ▓āņØ┤ ļ░śļō£ņŗ£ ĒĢäņÜöĒĢśļŗż. ĻĘĖļ¤¼ļéś ņŗ¼ļ░®ņäĖļÅÖņ£╝ļĪ£ ņ╣śļŻīļ░øļŖö ĒÖśņ×ÉļōżņĪ░ņ░©ļÅä ņŚ¼ņĀäĒ׳ ņ¦łļ│æņŚÉ ļīĆĒĢ£ ņ¦ĆņŗØņØ┤ ļČĆņĪ▒ĒĢ£ Ļ▓āņØ┤ ĒśäņŗżņØ┤ļ®░[16], ļīĆĒĢ£ļČĆņĀĢļ¦źĒĢÖĒÜīņŚÉņä£ ņŗżņŗ£ĒĢ£ 2017ļģä ļīĆĻĄŁļ»╝ ļČĆņĀĢļ¦źņ¦łĒÖś ņØĖņŗØ ņĪ░ņé¼ ņé¼ņŚģņŚÉņä£ ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ņØĖņ¦Ćņ£©ņØĆ 10% ļ»Ėļ¦īņ£╝ļĪ£ ņ¦łĒÖśņŚÉ ļīĆĒĢ£ ĻĄÉņ£ĪņØ┤ ņŗ£ĻĖēĒĢ£ Ļ▓āņ£╝ļĪ£ ļéśĒāĆļé¼ļŗż. ņØ┤ņŚÉ ĒĢÖĒÜī ņĖĪņŚÉņä£ļŖö ņ¦łĒÖśņØś ņ£äĒŚśņØĖņ×É, Ļ┤ĆļĀ© ņ”ØņāüņØś ņØĖņ¦Ć, ņ╣śļŻī, ņ×ÉĻ░Ć Ļ┤Ćļ”¼ ļō▒ņØś ļé┤ņÜ®ņØä ĒżĒĢ©ĒĢśņŚ¼ ĒÖłĒÄśņØ┤ņ¦ĆņŚÉ Ļ░Ćņŗ£ņĀüņ£╝ļĪ£ ņĀĢļ│┤ļź╝ ņĀ£Ļ│ĄĒĢśĻ│Ā ļæÉĻĘ╝ļæÉĻĘ╝ ņ║ĀĒÄśņØĖ ļō▒ņØä ĒåĄĒĢśņŚ¼ ņØ╝ļ░śņØĖņØä ļīĆņāüņ£╝ļĪ£ ņØĖņ¦ĆļÅä Ē¢źņāüņØä ņ£äĒĢśņŚ¼ ļŗżĻ░üņĀü ļģĖļĀźņØä ĻĖ░ņÜĖņØ┤Ļ│Ā ņ׳ļŗż. ņ×ÉĻ░Ć Ļ┤Ćļ”¼ļŖö ņ╣śļŻī Ļ│╝ņĀĢņŚÉ ņל ņĀüņØæĒĢśĻ│Ā ĻĖłņŚ░ņØ┤ļéś ņ▓┤ņżæ ņĪ░ņĀł ļō▒ ņāØĒÖ£ ņŖĄĻ┤ĆņØä ļ│ĆĒÖöņŗ£ĒéżļŖö Ļ▓āņŚÉ ņØ╝ņ░©ņĀüņØĖ ļ¬®Ēæ£ļź╝ ļæÉļŖöļŹ░ ņØ┤ļź╝ ņ£äĒĢ┤ņä£ļŖö ņ╣śļŻī ļ░®ļ▓ĢņØ┤ļéś ļ¬®Ēæ£ņŚÉ ļīĆĒĢśņŚ¼ ĒÖśņ×É ņŖżņŖżļĪ£ ņל ņĢīĻ│Ā ņ׳ņ¢┤ņĢ╝ ĒĢ£ļŗż[17,18]. ņŗ¼ļ░®ņäĖļÅÖņØś ņ╣śļŻīņĀü ļ¬®Ēæ£ļŖö ļćīņĪĖņżæņØś ļ░£ņāØ ņ£äĒŚśņØä ļ¦ēĻ│Ā, Ļ┤ĆļĀ© ņ”ØņāüņØś ļ░£ĒśäņØä ņżäņØ┤ļ®░, ņŗ¼ĒśłĻ┤Ćņ¦łĒÖśņØś ļ░£ņāØņØä ņśłļ░®ĒĢśļŖöļŹ░ ņ׳ļŗż. ņØ┤ Ļ│╝ņĀĢņŚÉņä£ ņØśņé¼ļŖö ĒÖśņ×ÉņŚÉĻ▓ī ņ╣śļŻīņÖĆ Ļ┤ĆļĀ©ļÉ£ ĻĄ¼ņ▓┤ņĀüņØ┤Ļ│Ā ņĀĢĒÖĢĒĢ£ ņĀĢļ│┤ļź╝ ņĀ£Ļ│ĄĒĢśĻ│Ā, ĒÖśņ×ÉļŖö ņØ┤ņŚÉ ļīĆĒĢ£ ņČ®ļČäĒĢ£ ņØ┤ĒĢ┤ņÖĆ ņ×Éļ░£ņĀüņØĖ ņ╣śļŻīņØś ņ░ĖņŚ¼ļź╝ ĒåĄĒĢśņŚ¼ ļ│ĖņØĖņØś ņ¦łļ│æņŚÉ ļīĆĒĢ£ Ļ│ĄĒåĄņØś ņ▒ģņ×äņØśņŗØ(shared accountability)ņØä Ļ░Ćņ¦ĆļŖö Ļ▓āņØ┤ ņżæņÜöĒĢśļŗż[8,19,20].
ĒÖśņ×ÉņÖĆ ņ▓śņØī ņĀæĒĢśĻ▓ī ļÉśļŖö 1ņ░© ņØśļŻīņØĖ, ņŗ¼ņןļé┤Ļ│╝ ņĀäļ¼ĖņØś, ņŗ¼ĒśłĻ┤Ć ņÖĖĻ│╝ņØśņé¼, ļČĆņĀĢļ¦ź ņĀäļ¼ĖņØś, ļćīņĪĖņżæ ņĀäļ¼ĖņØśļź╝ ĒżĒĢ©ĒĢśļŖö ļŗżĒĢÖņĀ£ņĀü ņĀæĻĘ╝ņØĆ, ĒÖśņ×ÉĻ░Ć ņ╣śļŻīņŚÉ ņĀüĻĘ╣ņĀüņ£╝ļĪ£ ņ░ĖņŚ¼ĒĢĀ ņłś ņ׳ļÅäļĪØ ļÅäņÖĆņżä ņłś ņ׳ņ£╝ļ®░, ĒŖ╣Ē׳ ņ╣śļŻī Ļ▓░ņĀĢ ļŗ©Ļ│äņŚÉ ĒÖśņ×Éļź╝ ņ░ĖņŚ¼ņŗ£Ēé┤ņ£╝ļĪ£ņŹ© ĒÖśņ×ÉņØś ņ╣śļŻīņŚÉ ļīĆĒĢ£ ņł£ņØæļÅäļź╝ ļåÆņØ┤Ļ│Ā ņ╣śļŻī ĒÜ©Ļ│╝ļź╝ ļåÆņØ╝ ņłś ņ׳ļŗż[21,22]. ņĄ£ĻĘ╝ņŚÉļŖö ĒÖśņ×ÉņŚÉ ļīĆĒĢ£ ĻĄÉņ£Ī, ņ×ÉĻ░Ć Ļ┤Ćļ”¼ ļ░Å ņ╣śļŻī Ļ│╝ņĀĢ ņ░ĖņŚ¼ļź╝ ĒåĄĒĢ®ĒĢśļŖö ņ×äņāü ļ¬©ļŹĖņØ┤ ņĀ£ņŗ£ļÉśĻ│Ā ņ׳ņ£╝ļ®░ ņØ┤ļŖö ņŗ¼ļ░®ņäĖļÅÖņØś ņ╣śļŻīņŚÉ ņżæņÜöĒĢ£ Ļ░Ćņ╣śļź╝ ņ¦Ćļŗīļŗż[23]. ņØ┤ļĀćļō», ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ļŗżĒĢÖņĀ£ņĀü ņĀæĻĘ╝ņØĆ ņĀäļ¼ĖĒÖöļÉ£ ņØśĒĢÖņĀü ņ¦ĆņŗØļ┐Éļ¦ī ņĢäļŗłļØ╝, ĒÖśņ×ÉņÖĆ ņØśņé¼ ņé¼ņØ┤ņØś ņøÉĒÖ£ĒĢ£ ņØśņé¼ņåīĒåĄĻ│╝ ĻĄÉņ£ĪņØä ĒżĒĢ©ĒĢśļ®░, ņØ┤ Ļ│╝ņĀĢņŚÉņä£ ņØśņé¼ļź╝ ĒżĒĢ©ĒĢ£ ņĀäļ¼ĖĻ░ĆļōżņØś ņØśĒĢÖņĀü ņĪ░ņ¢Ėļ┐É ņĢäļŗłļØ╝, ļ╣äņØśļŻīņ¦äļōżņØś ĒÖśņ×ÉņŚÉ ļīĆĒĢ£ ņĀüĻĘ╣ņĀüņØĖ ĻĄÉņ£ĪĻ│╝ ĒśæņĪ░Ļ░Ć ĒĢäņÜöĒĢśļŗż.
ņŗ¼ļ░®ņäĖļÅÖņØä ņ▓śņØī ņ¦äļŗ©ĒĢśĻ│Ā ņĀæĒĢśĻ▓ī ļÉśļŖö ņØ╝ņ░© ņØśļŻīņØĖņØś Ļ▓ĮņÜ░, ņŗ¼ļ░®ņäĖļÅÖņØś ņ▓½ ņ╣śļŻīņÖĆ ļćīņĪĖņżæņØś ņśłļ░®ņŚÉ Ļ┤ĆĒĢ£ ņØśĒĢÖņĀüņØĖ ņ¦ĆņŗØņØ┤ ĒĢäņÜöĒĢśļŗż. ņØ┤ Ļ│╝ņĀĢņŚÉņä£ ĒåĄĒĢ®ņĀüņØĖ ņŗ¼ļ░®ņäĖļÅÖņØś ņ╣śļŻīņĀü ņŗ£ņŖżĒģ£ņØĆ ņ▓śņØī ņØ╝ņ░© ņØśļŻīĻĖ░Ļ┤ĆņŚÉņä£ ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ņĀüņĀłĒĢ£ ņ▓½ ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśĻ│Ā, ļČĆņĀĢļ¦ź ņĀäļ¼ĖĻ░ĆņŚÉĻ▓ī ņØśļó░ĒĢĀ ņłś ņ׳ļŖö ņ▓┤Ļ│äņĀüņØĖ ĻĖ░ļ░śņØä ņĀ£Ļ│ĄĒĢśĻ▓ī ļÉ£ļŗż[8,9,20].
ņŗ¼ļ░®ņäĖļÅÖņŚÉ Ļ┤ĆĒĢ£ ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīļź╝ ņ£äĒĢ┤ņä£ļŖö ĻĄ¼ņä▒ņøÉļōż Ļ░äņØś ņøÉĒÖ£ĒĢ£ ņØśņé¼ņåīĒåĄĻ│╝ ĻĄÉĒÖśņØ┤ ĒĢäņłśņĀüņØ┤ļŗż. ņØ┤ļź╝ ņ£äĒĢ┤ņä£ļŖö ĒÖśņ×ÉņÖĆ ņØśņé¼, ņØ╝ņ░© ņØśļŻīņØĖĻ│╝ ļČĆņĀĢļ¦ź ņĀäļ¼ĖĻ░Ć ņé¼ņØ┤ņØś ņ×Éņ£ĀļĪ£ņÜ┤ ņØśņé¼ ĻĄÉĒÖśņØä ņ£äĒĢ£ ĻĖ░ņłĀņĀü ņ¦ĆņøÉņØ┤ ĒĢäņÜöĒĢśļŗż. ņØ┤ Ļ│╝ņĀĢņŚÉņä£ ļööņ¦ĆĒäĖ ĒöäļĪ£ĻĘĖļשņØ┤ļéś ņŖżļ¦łĒŖĖĒÅ░ ņĢ▒ ļō▒ņØ┤ ļÅäņøĆņØä ņżä ņłś ņ׳ļŗż[24].
ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīļŖö ņØ┤ļźĖļ░ö ABC pathwayļĪ£ ņäżļ¬ģļÉśļŖöļŹ░, ļćīņĪĖņżæņØś ļ░£ņāØņØä Ēö╝ĒĢśĻ│Ā(Avoid stroke), Ļ┤ĆļĀ© ņ”ØņāüņØś ļ░£ņāØņØä ļ░®ņ¦ĆĒĢśļ®░(Better symptom management), ĻČüĻĘ╣ņĀüņ£╝ļĪ£ ņŗ¼ĒśłĻ┤Ćņ¦łĒÖśņØś ļ░£ņāØņØä ņżäņØ┤ĻĖ░(Cardiovascular and comorbidity risk reduction) ņ£äĒĢ£ Ļ▓āņØ┤ļŗż[25]. ņØ┤ļź╝ ņ£äĒĢ┤ņä£ļŖö ļ╣äļ¦ī, Ļ│ĀĒśłņĢĢ, ļŗ╣ļć©ņÖĆ Ļ░ÖņØĆ Ļ┤ĆļĀ© ņ¦łĒÖśņØś ņĀüĻĘ╣ņĀüņØĖ Ļ┤Ćļ”¼Ļ░Ć ņØ┤ļŻ©ņ¢┤ņĀĖņĢ╝ ĒĢśļ®░, ĒØĪņŚ░Ļ│╝ ņØīņŻ╝, ņÜ┤ļÅÖĻ│╝ Ļ░ÖņØĆ ņāØĒÖ£ņŖĄĻ┤Ć ĻĄÉņĀĢņØś ĻĄÉņĀĢņØ┤ ļÅÖņŗ£ņŚÉ ņØ┤ļŻ©ņ¢┤ņĀĖņĢ╝ ĒĢ£ļŗż(Table 2) [25-27].
ņŗ¼ļ░®ņäĖļÅÖņØś ņ¢æņāü, ņ”Øņāü ļ░Å ņ£Āļ░£ ņÜöņØĖņŚÉ ļīĆĒĢ£ ļ¼Ėņ¦ä ļ░Å ļćīĻ▓ĮņāēņØä ĒżĒĢ©ĒĢ£ ņĀäņŗĀņāēņĀäņ”ØņØś Ļ│╝Ļ▒░ļĀźņŚÉ ļīĆĒĢ£ ĒÅēĻ░ĆĻ░Ć ņłśĒ¢ēļÉśņ¢┤ņĢ╝ ĒĢ£ļŗż. ļŗ╣ļć©, Ļ│ĀĒśłņĢĢ, ļ¦īņä▒ĒÅÉņćäņä▒ĒÅÉņ¦łĒÖś, ļ╣äļ¦ī ļ░Å ņłśļ®┤ļ¼┤ĒśĖĒØĪņ”Ø, Ļ░æņāüņäĀĻĖ░ļŖźĒĢŁņ¦äĻ│╝ Ļ░ÖņØĆ ĻĖ░ņĀĆ ņ¦łĒÖś ļ░Å ņØīņŻ╝ļĀź Ēś╣ņØĆ ĒØĪņŚ░Ļ│╝ Ļ░ÖņØĆ ņāØĒÖ£ņŖĄĻ┤ĆņŚÉ ļīĆĒĢ£ ņ▓ĀņĀĆĒĢ£ ļ¼Ėņ¦äņØä ĒåĄĒĢśņŚ¼ ĻĄÉņĀĢ Ļ░ĆļŖźĒĢ£ ņøÉņØĖņØä ĒÅēĻ░ĆĒĢśņŚ¼ņĢ╝ ĒĢ£ļŗż[26-33]. ĻĄŁļé┤ ņĀä ĻĄŁļ»╝Ļ▒┤Ļ░ĢĻ▓Ćņ¦ä ņ×ÉļŻīņŚÉ ļīĆĒĢ£ Ēæ£ņżĆĒÖöļÉ£ ļŹ░ņØ┤Ēä░ļź╝ ĒåĄĒĢ£ ņ×ÉļŻī ļČäņäØņŚÉņä£ Ļ│ĀĒśłņĢĢņĀäļŗ©Ļ│ä, ļŗ╣ļć© ņĀäļŗ©Ļ│ä ĒÖśņ×ÉļōżņØś Ļ▓ĮņÜ░ ņāüņŖ╣ļÉ£ ĒśłņĢĢĻ│╝ Ļ│Ąļ│Ą Ēśłļŗ╣ļ¦īņ£╝ļĪ£ļÅä ņŗ¼ļ░®ņäĖļÅÖņØś ļ░£ņāØņØä ņ”ØĻ░Ćņŗ£ĒéżļŖö Ļ▓āņ£╝ļĪ£ ļéśĒāĆļé¼ņ£╝ļ®░[26], ļ╣äĻĄÉņĀü Ļ│ĀļÅä ļ╣äļ¦īņØ┤ ņĀüņØĆ ņĢäņŗ£ņĢä ĒÖśņ×ÉļōżņŚÉ ļīĆĒĢ£ ļČäņäØņŚÉņä£ļÅä ļ╣äļ¦īņØ┤ ļÅÖļ░śļÉĀ Ļ▓ĮņÜ░ ņŗ¼ļ░®ņäĖļÅÖņØś ļ░£ņāØņØ┤ ņ”ØĻ░ĆĒĢśĻ│Ā ņśłĒøäĻ░Ć ļéśņü£ Ļ▓āņ£╝ļĪ£ ņĪ░ņé¼ļÉśņŚłļŗż[27,34]. 12ņ£ĀļÅäņŗ¼ņĀäļÅäļź╝ ĒåĄĒĢśņŚ¼ ņŗ¼ņןņĀäļÅäņןņĢĀ, ĒŚłĒśłņä▒ņŗ¼ņ¦łĒÖś ļ░Å ĻĄ¼ņĪ░ņĀü ņŗ¼ņ¦łĒÖśņØś ņ£Āļ¼┤ļź╝ ĒÅēĻ░ĆĒĢśņŚ¼ņĢ╝ ĒĢ£ļŗż. Ļ▓ĮĒØēļČĆņŗ¼ņ┤łņØīĒīīļŖö ņŗ¼ļ░®ņäĖļÅÖņØś ņ╣śļŻī ļ░®ņ╣© Ļ▓░ņĀĢņØä ņ£äĒĢśņŚ¼ ļ¬©ļōĀ ĒÖśņ×ÉņŚÉĻ▓ī ņłśĒ¢ēļÉśņ¢┤ņĢ╝ ĒĢ£ļŗż.
ĒÖ£ļÅÖ ņżæ ņŗ¼ņĀäļÅäļŖö ņŗ¼ļ░®ņäĖļÅÖ ĒÖśņ×ÉņØś ļ¦źļ░Ģņłś ĒÅēĻ░Ć ļ░Å ņ”ØņāüĻ│╝ ņŗ¼ļ░®ņäĖļÅÖņØś Ļ┤ĆļĀ©ņä▒ņØä ĒÅēĻ░ĆĒĢśĻĖ░ņŚÉ ņ£ĀņÜ®ĒĢśļŗż. ĒŖ╣Ē׳ ĒÖ£ļÅÖ ņżæņŗ¼ņĀäļÅäĻ░Ć ņĀ£Ļ│ĄĒĢśļŖö ņÜ┤ļÅÖņØ┤ļéś ĒÖ£ļÅÖ ņżæņØś ļ¦źļ░ĢņłśņŚÉ ļīĆĒĢ£ ņĀĢļ│┤ļŖö ņĢĮļ¼╝ ņ╣śļŻīļź╝ ĒåĄĒĢ£ ļ¦źļ░Ģņłś ņĪ░ņĀłņØś ļ¬®Ēæ£Ļ░Ć ļŗ¼ņä▒ļÉśņŚłļŖöņ¦Ćļź╝ ĒÖĢņØĖĒĢśļŖöļŹ░ ņØ┤ņÜ®ļÉĀ ņłś ņ׳ļŗż. Ļ▓ĮņŗØļÅäņŗ¼ņ┤łņØīĒīīļŖö Ļ▓ĮĒØēļČĆņŗ¼ņ┤łņØīĒīīņŚÉ ļ╣äĒĢśņŚ¼ ņóīņŗ¼ļ░®ņØ┤ņØś ĻĖ░ļŖź ĒÅēĻ░Ć ļ░Å ņóīņŗ¼ļ░®ņØ┤ ļé┤ņØś ĒśłņĀä ņ£Āļ¼┤ ĒÅēĻ░ĆņŚÉ ņ£ĀņÜ®ĒĢśļŗż. ļö░ļØ╝ņä£ ņ╣©ņŖĄņĀüņØĖ ņ╣śļŻīņØĖ ļÅÖņ£©ļÅÖņĀäĒÖśņłĀņØ┤ļéś Ļ│ĀņŻ╝ĒīīņĀłņĀ£ņłĀņØä ņĢ×ļæö ĒÖśņ×ÉņŚÉņä£ Ļ▓ĮņŗØļÅäņ┤łņØīĒīīļź╝ ĒåĄĒĢ£ ņŗ¼ņןļé┤ ĒśłņĀäņØś ĒÅēĻ░ĆļŖö ĒĢäņłśņĀüņØ┤ļŗż(Table 3) [35,36]. ļćīĻ▓ĮņāēņØ┤ ņØśņŗ¼ļÉśļŖö ĒÖśņ×ÉļŖö ļćī ņĀäņé░ĒÖöļŗ©ņĖĄņ┤¼ņśü Ēś╣ņØĆ ļćī ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāüņØä ņØ┤ņÜ®ĒĢśņŚ¼ ļćīĻ▓Įņāē ņ£Āļ¼┤ļź╝ ĒÅēĻ░ĆĒĢśņŚ¼ņĢ╝ ĒĢśļ®░, ņØ┤ļź╝ ĒåĄĒĢśņŚ¼ ļćīĻ▓ĮņāēņØś ĻĖēņä▒ĻĖ░ ņ╣śļŻī ļ░Å ĒĢŁņØæĻ│ĀņĀ£ ņ╣śļŻī ļ░®ņ╣©ņØä ņłśļ”ĮĒĢśļŖöļŹ░ ļÅäņøĆņØä ļ░øņØä ņłś ņ׳ļŗż.
ļīĆļČĆļČäņØś ņŗ¼ļ░®ņäĖļÅÖ ĒÖśņ×ÉļōżņØĆ ņ¦ĆņåŹņĀüņØĖ ņĄ£ņĀüņØś ņ╣śļŻīļź╝ ņ£äĒĢśņŚ¼ ņĀĢĻĖ░ņĀüņØĖ ņČöņĀü Ļ┤Ćņ░░ņØ┤ ĒĢäņÜöĒĢśļŗż. ņČöņĀü Ļ┤Ćņ░░ņØĆ ņØ╝ņ░© ņ¦äļŻī, ņŗ¼ņןļé┤Ļ│╝ ņĀäļ¼ĖņØś ļśÉļŖö ļČĆņĀĢļ¦ź ņĀäļ¼ĖņØśņŚÉĻ▓ī ļ░øņØä ņłś ņ׳ņ£╝ļ®░, ņČöņĀü Ļ┤Ćņ░░ ļÅÖņĢł ņ╣śļŻī Ļ│äĒÜŹņØś ņłśĒ¢ē, ĒÖśņ×ÉņØś ņ¦ĆņåŹņĀüņØĖ ņ░ĖņŚ¼ ĻĘĖļ”¼Ļ│Ā ĒĢäņÜöĒĢĀ Ļ▓ĮņÜ░ ņ╣śļŻīņØś ļ│ĆĻ▓ĮņØ┤ ĒĢäņÜöĒĢśļŗż. ņŗ¼ļ░®ņäĖļÅÖņØś ņ╣śļŻīļŖö ņśłĒøäņÖĆ Ļ┤ĆļĀ©ļÉ£ ņ╣śļŻī(ĒĢŁņØæĻ│Ā ņ╣śļŻī ļ░Å ņŗ¼ĒśłĻ┤Ćņ¦łĒÖśņØś ņ╣śļŻī)ņÖĆ ņ”ØņāüņØä ņÖäĒÖöņŗ£ĒéżļŖö ņ╣śļŻī(ņŗ¼ļ░Ģņłś ļśÉļŖö ņŗ¼ņ£©ļÅÖ ņĪ░ņĀł; Table 4)ļź╝ ĒżĒĢ©ĒĢ£ļŗż[25,37]. ņśłĒøäļź╝ Ē¢źņāüņŗ£ĒéżļŖö ņ╣śļŻīņŚÉ ļīĆĒĢ┤ņä£ļŖö ņ╣śļŻīņØś ņØ┤ļōØņŚÉ ļīĆĒĢśņŚ¼ ņ¦üņĀæņĀüņ£╝ļĪ£ ļŖÉļéä ņłś ņŚåņ£╝ļ»ĆļĪ£ ĒÖśņ×ÉņŚÉĻ▓ī ņČ®ļČäĒ׳ ņØ┤ĒĢ┤ĒĢĀ ņłś ņ׳ļÅäļĪØ ņØ┤ņŚÉ ļīĆĒĢ£ ņŻ╝ņØś Ļ╣ŖņØĆ ņäżļ¬ģņØ┤ ĒĢäņÜöĒĢśļŗż. ļśÉĒĢ£ ņŗ¼ņ£©ļÅÖ ņĪ░ņĀł ņ╣śļŻīļŖö ņŗ¼ļ░®ņäĖļÅÖņØ┤ ņØ╝ļČĆ ņ×¼ļ░£ĒĢśļŹöļØ╝ļÅä ņĀäļ░śņĀüņØĖ ļ╣łļÅäļéś ĻĖ░Ļ░ä ļō▒ņØ┤ Ļ░ÉņåīĒĢśņŚ¼ ņ”ØņāüņØ┤ ņĪ░ņĀłļÉśņŚłļŗżļ®┤ ņä▒Ļ│ĄņØ┤ļØ╝ ĒĢĀ ņłś ņ׳ļŗż. ĻĘĖļ”¼Ļ│Ā ņ╣śļŻīļź╝ ņŗ£ņ×æĒĢĀ ļĢī Ļ░£ļ│ä ĒÖśņ×Éļ¦łļŗż ņśłņāüļÉśļŖö ņØ┤ļōØņØä ņäżļ¬ģĒĢśļŖö Ļ▓āņØ┤ ĻĘ╝Ļ▒░ ņŚåļŖö ĻĖ░ļīĆļź╝ ļ░®ņ¦ĆĒĢśĻ│Ā ņéČņØś ņ¦łņØä ņĄ£ņĀüĒÖöĒĢśļŖöļŹ░ ļÅäņøĆņØ┤ ļÉ£ļŗż. ĻĘĖļ”¼Ļ│Ā ņŗ¼ļ░®ņäĖļÅÖĻ│╝ Ļ┤ĆļĀ©ĒĢśņŚ¼ ļÅÖļ░śļÉ£ ņ¦łĒÖśļōż(ļ╣äļ¦ī, Ļ│ĀĒśłņĢĢ, ņŗ¼ļČĆņĀä, ļŗ╣ļć©, ņłśļ®┤ļ¼┤ĒśĖĒØĪ)ņŚÉ ļīĆĒĢ£ ņ▓ĀņĀĆĒĢ£ Ļ┤Ćļ”¼Ļ░Ć ņäĀĒ¢ēļÉśņ¢┤ņĢ╝ ĒĢśļ®░[26,29,34,38,39], ĒØĪņŚ░, ņØīņŻ╝, ņÜ┤ļÅÖņŖĄĻ┤ĆĻ│╝ Ļ░ÖņØĆ ņāØĒÖ£ņŖĄĻ┤ĆņŚÉ ļīĆĒĢ£ ĻĄÉņĀĢļÅä ĒåĄĒĢ®ņĀüņ£╝ļĪ£ ņČöņĀü Ļ┤Ćņ░░ļÉśņ¢┤ņĢ╝ ĒĢ£ļŗż[4,6].
ņŗ¼ļ░®ņäĖļÅÖņŚÉ ļīĆĒĢ£ ĒåĄĒĢ®ņĀüņØĖ ņ╣śļŻīļź╝ ņ£äĒĢ┤ņä£ļŖö ĒÖśņ×ÉĻ░Ć ļ│æņŚÉ ļīĆĒĢ£ ĻĖ░ļ│ĖņĀüņØĖ ņ¦ĆņŗØņØä Ļ░Ćņ¦ĆĻ│Ā ņĀüĻĘ╣ņĀüņ£╝ļĪ£ ņ╣śļŻīņØś ņżæņŗ¼ņŚÉ ņä£ņĢ╝ ĒĢ£ļŗż. ņØ┤ Ļ│╝ņĀĢņŚÉņä£ ņØśņé¼ļōżņŚÉ ņØśĒĢ£ ņĀäļ¼ĖņĀüņØĖ ņ¦ĆņŗØņØ┤, ĒÖśņ×ÉņÖĆ ņØśņé¼ ņé¼ņØ┤ņØś ņØśņé¼ņåīĒåĄĻ│╝ ĻĄÉņ£ĪņØä ĒåĄĒĢśņŚ¼ ĒÖśņ×ÉņŚÉĻ▓ī ņøÉĒÖ£ĒĢśĻ▓ī ņĀäļŗ¼ļÉśņ¢┤ņĢ╝ ĒĢ£ļŗż. ĒÖśņ×Éļź╝ ņ▓śņØī ņĀæĒĢśĻ▓ī ļÉśļŖö 1ņ░© ņ¦äļŻīņØśņØś ņ¦äļŗ©ļČĆĒä░, ņ╣śļŻī ĻĘĖļ”¼Ļ│Ā ņ▓┤Ļ│äņĀüņØĖ ņČöņĀü Ļ┤Ćņ░░ņŚÉ ņØ┤ļź┤ĻĖ░Ļ╣īņ¦Ć ļŗ©Ļ│äņĀüņØ┤Ļ│Ā ĒåĄĒĢ®ņĀüņØĖ ņŗ¼ļ░®ņäĖļÅÖ Ļ┤Ćļ”¼ļŖö ņ¦łļ│æņØś ņ╣śļŻīņŚÉ ņ׳ņ¢┤ņä£ ļČĆņ×æņÜ®ņØä ņĄ£ņåīĒÖöĒĢśĻ│Ā, ļ│æņŚÉ ļīĆĒĢ£ ĒÖśņ×ÉļōżņØś ņØĖņ¦ĆļÅäļź╝ ļåÆņŚ¼ ņ╣śļŻī ņä▒Ļ│╝ļź╝ Ē¢źņāüņŗ£Ēé¼ Ļ▓āņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
REFERENCES
1. Kim D, Yang PS, Jang E, et al. Increasing trends in hospital care burden of atrial fibrillation in Korea, 2006 through 2015. Heart 2018 Apr 17 [Epub]. http://dx.doi.org/10.1136/heartjnl-2017-312930

2. Yoon M, Yang PS, Jang E, et al. Dynamic changes of CHA2DS2-VASc score and the risk of ischaemic stroke in asian patients with atrial fibrillation: a nationwide cohort study. Thromb Haemost 2018;118:1296ŌĆō1304.


3. Page K, Marwick TH, Lee R, et al. A systematic approach to chronic heart failure care: a consensus statement. Med J Aust 2014;201:146ŌĆō150.


4. Stock S, Pitcavage JM, Simic D, et al. Chronic care model strategies in the United States and Germany deliver patient-centered, high-quality diabetes care. Health Aff (Millwood) 2014;33:1540ŌĆō1548.


5. Lundstrom H, Siersma V, Nielsen AB, et al. The effectiveness of structured personal care of type 2 diabetes on recurrent outcomes: a 19 year follow-up of the study diabetes care in general practice (DCGP). Diabetologia 2014;57:1119ŌĆō1123.


6. Nieuwlaat R, Olsson SB, Lip GY, et al. Guideline-adherent antithrombotic treatment is associated with improved outcomes compared with undertreatment in high-risk patients with atrial fibrillation. The Euro Heart Survey on Atrial Fibrillation. Am Heart J 2007;153:1006ŌĆō1012.


7. Nu├▒o R, Coleman K, Bengoa R, Sauto R. Integrated care for chronic conditions: the contribution of the ICCC framework. Health Policy 2012;105:55ŌĆō64.


8. Hendriks JM, de Wit R, Crijns HJ, et al. Nurse-led care vs. usual care for patients with atrial fibrillation: results of a randomized trial of integrated chronic care vs. routine clinical care in ambulatory patients with atrial fibrillation. Eur Heart J 2012;33:2692ŌĆō2699.


9. Hendriks J, Tomini F, van Asselt T, Crijns H, Vrijhoef H. Cost-effectiveness of a specialized atrial fibrillation clinic vs. usual care in patients with atrial fibrillation. Europace 2013;15:1128ŌĆō1135.


10. Tran HN, Tafreshi J, Hernandez EA, Pai SM, Torres VI, Pai RG. A multidisciplinary atrial fibrillation clinic. Curr Cardiol Rev 2013;9:55ŌĆō62.



11. Conti A, Canuti E, Mariannini Y, et al. Clinical management of atrial fibrillation: early interventions, observation, and structured follow-up reduce hospitalizations. Am J Emerg Med 2012;30:1962ŌĆō1969.


12. Carter L, Gardner M, Magee K, et al. An integrated management approach to atrial fibrillation. J Am Heart Assoc 2016;5:e002950.



13. Bodenheimer T, Wagner EH, Grumbach K. Improving primary care for patients with chronic illness. JAMA 2002;288:1775ŌĆō1779.


14. Hibbard JH, Greene J. What the evidence shows about patient activation: better health outcomes and care experiences; fewer data on costs. Health Aff (Millwood) 2013;32:207ŌĆō214.


15. Aliot E, Breithardt G, Brugada J, et al. An international survey of physician and patient understanding, perception, and attitudes to atrial fibrillation and its contribution to cardiovascular disease morbidity and mortality. Europace 2010;12:626ŌĆō633.



16. Lip GY, Kamath S, Jafri M, Mohammed A, Bareford D. Ethnic differences in patient perceptions of atrial fibrillation and anticoagulation therapy: the West Birmingham Atrial Fibrillation Project. Stroke 2002;33:238ŌĆō242.


17. Lorig KR, Holman H. Self-management education: history, definition, outcomes, and mechanisms. Ann Behav Med 2003;26:1ŌĆō7.


18. Alonso-Coello P, Montori VM, Sol├Ā I, et al. Values and preferences in oral anticoagulation in patients with atrial fibrillation, physicians' and patients' perspectives: protocol for a two-phase study. BMC Health Serv Res 2008;8:221.



19. Peterson ED, Ho PM, Barton M, et al. ACC/AHA/AACVPR/AAFP/ANA concepts for clinician-patient shared accountability in performance measures: a report of the American College of Cardiology/American Heart Association task force on performance measures. Circulation 2014;130:1984ŌĆō1994.



20. Stewart S, Ball J, Horowitz JD, et al. Standard versus atrial fibrillation-specific management strategy (SAFETY) to reduce recurrent admission and prolong survival: pragmatic, multicentre, randomised controlled trial. Lancet 2015;385:775ŌĆō784.


21. Seaburg L, Hess EP, Coylewright M, Ting HH, McLeod CJ, Montori VM. Shared decision making in atrial fibrillation: where we are and where we should be going. Circulation 2014;129:704ŌĆō710.


22. Stiggelbout AM, Van der Weijden T, De Wit MP, et al. Shared decision making: really putting patients at the centre of healthcare. BMJ 2012;344:e256.


23. Elwyn G, Frosch D, Thomson R, et al. Shared decision making: a model for clinical practice. J Gen Intern Med 2012;27:1361ŌĆō1367.



24. Hendriks JM, de Wit R, Vrijhoef HJ, Tieleman RG, Crijns HJ. An integrated chronic care program for patients with atrial fibrillation: study protocol and methodology for an ongoing prospective randomised controlled trial. Int J Nurs Stud 2010;47:1310ŌĆō1316.


25. Lip GYH. The ABC pathway: an integrated approach to improve AF management. Nat Rev Cardiol 2017;14:627ŌĆō628.


26. Lee SS, Ae Kong K, Kim D, et al. Clinical implication of an impaired fasting glucose and prehypertension related to new onset atrial fibrillation in a healthy Asian population without underlying disease: a nationwide cohort study in Korea. Eur Heart J 2017;38:2599ŌĆō2607.


27. Baek YS, Yang PS, Kim TH, et al. Associations of abdominal obesity and new-onset atrial fibrillation in the general population. J Am Heart Assoc 2017;6:e004705.



28. Benjamin EJ, Levy D, Vaziri SM, D'Agostino RB, Belanger AJ, Wolf PA. Independent risk factors for atrial fibrillation in a population-based cohort. The framingham heart study. JAMA 1994;271:840ŌĆō844.


29. Wang TJ, Parise H, Levy D, et al. Obesity and the risk of new-onset atrial fibrillation. JAMA 2004;292:2471ŌĆō2477.


30. Gami AS, Hodge DO, Herges RM, et al. Obstructive sleep apnea, obesity, and the risk of incident atrial fibrillation. J Am Coll Cardiol 2007;49:565ŌĆō571.


31. Heeringa J, Kors JA, Hofman A, van Rooij FJ, Witteman JC. Cigarette smoking and risk of atrial fibrillation: the rotterdam study. Am Heart J 2008;156:1163ŌĆō1169.


32. Conen D, Tedrow UB, Cook NR, Moorthy MV, Buring JE, Albert CM. Alcohol consumption and risk of incident atrial fibrillation in women. JAMA 2008;300:2489ŌĆō2496.



33. Roh SY, Choi JI, Lee JY, et al. Catheter ablation of atrial fibrillation in patients with chronic lung disease. Circ Arrhythm Electrophysiol 2011;4:815ŌĆō822.


34. Kong KA, Park J, Hong SH, Hong YS, Sung YA, Lee H. Associations between body mass index and mortality or cardiovascular events in a general Korean population. PLoS One 2017;12:e0185024.



35. Manning WJ, Weintraub RM, Waksmonski CA, et al. Accuracy of transesophageal echocardiography for identifying left atrial thrombi. A prospective, intraoperative study. Ann Intern Med 1995;123:817ŌĆō822.


36. Hwang JJ, Chen JJ, Lin SC, et al. Diagnostic accuracy of transesophageal echocardiography for detecting left atrial thrombi in patients with rheumatic heart disease having undergone mitral valve operations. Am J Cardiol 1993;72:677ŌĆō681.


37. Lip G, Freedman B, De Caterina R, Potpara TS. Stroke prevention in atrial fibrillation: past, present and future. Comparing the guidelines and practical decision-making. Thromb Haemost 2017;117:1230ŌĆō1239.


38. Kim TH, Shim CY, Park JH, et al. Left ventricular diastolic dysfunction is associated with atrial remodeling and risk or presence of stroke in patients with paroxysmal atrial fibrillation. J Cardiol 2016;68:104ŌĆō109.


The basic concept of acute and chronic management of atrial fibrillation. Modified from [40].
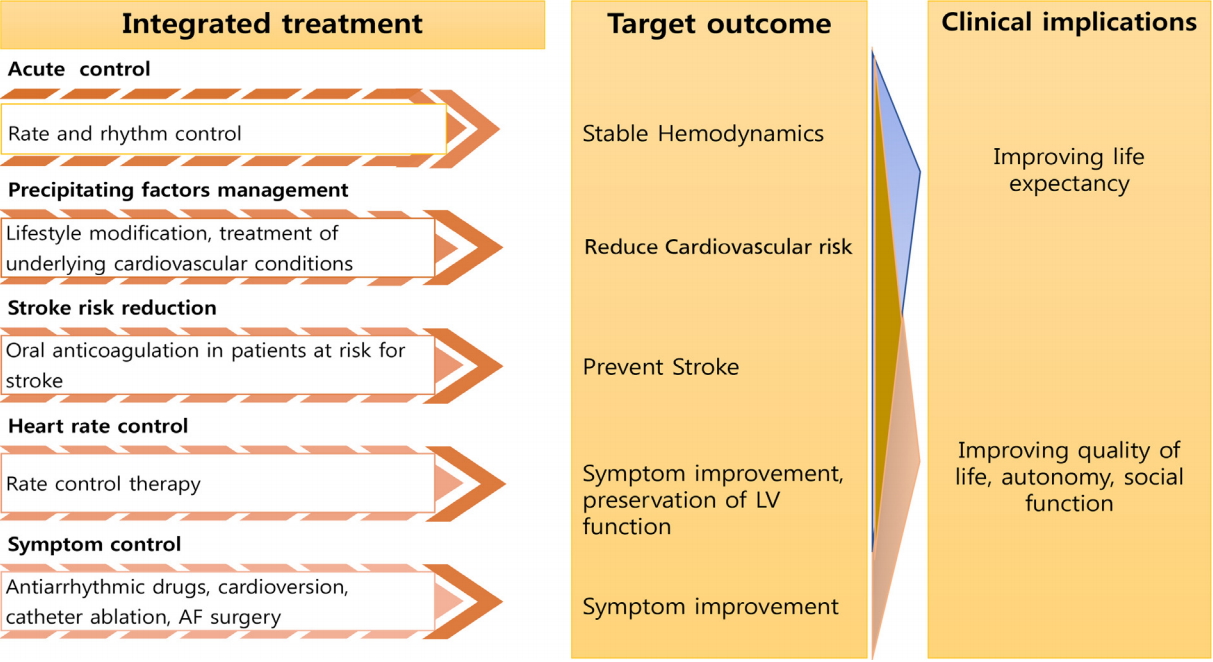
Figure┬Ā1.
Table┬Ā1.
Clinical conditions requiring urgent attention by a specialized atrial fibrillation service
Table┬Ā2.
Basic components of integrated atrial fibrillation management
Table┬Ā3.
Recommendations for diagnosis of atrial fibrillation
Table┬Ā4.
Goal-based follow-up of atrial fibrillation patients
-
METRICS

-
- 1 Crossref
- 0 Scopus
- 16,466 View
- 1,414 Download




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



