ņä£ ļĪĀ
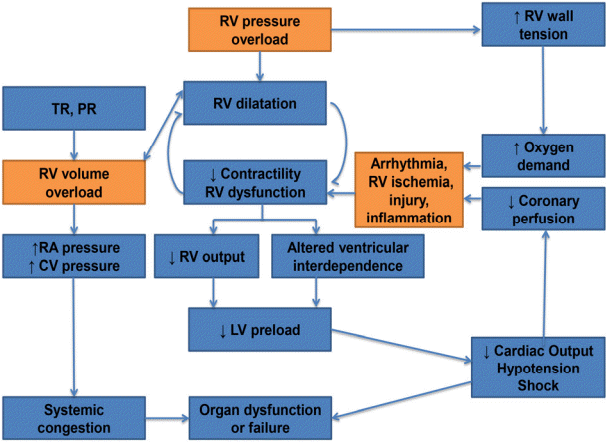
ņÜ░ņŗ¼ļČĆņĀäņØĆ ļ│Ąņ×ĪĒĢ£ ņ×äņāüņ”ØĒøäĻĄ░ņ£╝ļĪ£ņä£, ņÜ░ņŗ¼ņŗżņØ┤ ĒśłņĢĪņ£╝ļĪ£ ņ▒äņøīņ¦ĆĻ│Ā ĒśłņĢĪņØä ņÜ░ņŗ¼ņŗż ļ░¢ņ£╝ļĪ£ ļé┤ļ│┤ļé┤ļŖö ĻĖ░ļŖźņØä ņĀĆĒĢ┤ĒĢśļŖö ļŗżņ¢æĒĢ£ ĻĄ¼ņĪ░ņĀü, ĻĖ░ļŖźņĀü ņŗ¼ĒśłĻ┤Ć ņ¦łĒÖśļōżņŚÉ ņØśĒĢ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ļŖöļŹ░, ĒÅÉĻ│ĀĒśłņĢĢ, ņäĀņ▓£ņä▒ ņŗ¼ņן ņ¦łĒÖś, Ļ┤ĆņāüļÅÖļ¦ź ņ¦łĒÖś, ņóīņŗ¼ļČĆņĀä ļ░Å ĒīÉļ¦ē ņ¦łĒÖśņŚÉņä£ ļéśĒāĆļéĀ ņłś ņ׳ļŗż. ņÜ░ņŗ¼ļČĆņĀäņØś ņĀĢņØśļŖö ņĢłņĀĢņØä ņĘ©ĒĢĀ ļĢīļéś ņÜ┤ļÅÖĒĢĀ ļĢī ĒÅÉņł£ĒÖśĻ│äļĪ£ ņĄ£ņĀüĒÖöļÉ£ Ēśłļźśļź╝ ļé┤ļ│┤ļé┤ņ¦Ć ļ¬╗ĒĢśĻ│Ā ņĀĢļ¦źņĢĢņØś ņāüņŖ╣ņØ┤ ļÅÖļ░śļÉśĻ▒░ļéś ļÅÖļ░śļÉśņ¦Ć ņĢŖņØĆ ņāüĒā£ļź╝ ņØ╝ņ£╝ĒéżļŖö ņÜ░ņŗ¼ ņł£ĒÖśĻ│äņØś ĻĄ¼ņĪ░ņĀü, ĻĖ░ļŖźņĀü ļ│ĆĒÖöļĪ£ ņØĖĒĢ£ ņ×äņāüņ”ØĒøäĻĄ░ņØ┤ļŗż[1,2]. ņÜ░ņŗ¼ņŗżņØ┤ ņÜ░ņŗ¼ ņł£ĒÖśĻ│äņØś ļ¦żņÜ░ ņżæņÜöĒĢ£ ļČĆļČäņØ┤ņ¦Ćļ¦ī ņĀäņŗĀ ņĀĢļ¦źņŚÉņä£ ĒÅÉ ļ¬©ņäĖĒśłĻ┤ĆĻ╣īņ¦Ć ņł£ĒÖśĻ│äņØś ņ¢┤ļ¢ż ļČĆļČäņØ┤ļØ╝ļÅä ĻĖ░ļŖź ņןņĢĀļź╝ ņØ╝ņ£╝Ēéżļ®┤ ņÜ░ņŗ¼ļČĆņĀäņØś ņ”ØņāüņØ┤ ļéśĒāĆļéĀ ņłś ņ׳ļŗż. ņÜ░ņŗ¼ļČĆņĀäņØś ņŻ╝ņÜö ņ×äņāü ĒŖ╣ņ¦ĢļōżņØĆ 1) ņ▓┤ņĢĪ ņĀĆļźś, 2) Ļ░ÉņåīļÉ£ ņłśņČĢĻĖ░ ņśłļ╣äļĀź ļśÉļŖö ņĀüņØĆ ņŗ¼ņןļ░ĢņČ£ļ¤ē, 3) ņŗ¼ļ░® ļśÉļŖö ņŗ¼ņŗżņä▒ ļČĆņĀĢļ¦źņØĖļŹ░, ņ▓┤ņĢĪ ņĀĆļźśļŖö ļ¦Éņ┤ł ļČĆņóģ, ļ│Ąņłś ļ░Å ņĀäņŗĀ ļČĆņóģņØä ņØ╝ņ£╝Ēé¼ ņłś ņ׳Ļ│Ā, ņŗ¼ņןļ░ĢņČ£ļ¤ē Ļ░ÉņåīļŖö ņÜ┤ļÅÖ ļČłļé┤ņä▒Ļ│╝ Ēö╝ļĪ£ļź╝ ņ£Āļ░£ĒĢĀ ņłś ņ׳ļŗż. ņÜ░ņŗ¼ļČĆņĀäņØä ņØ╝ņ£╝ĒéżļŖö ņøÉņØĖņŚÉ ļö░ļØ╝ ļ│æĒā£ ņāØļ”¼ņØś ņ░©ņØ┤Ļ░Ć ņ׳ņ¦Ćļ¦ī Ļ░üĻ░üņØś ņ¦łĒÖśĻ│╝ ņŚ░Ļ┤ĆļÉśņ¢┤ ļŗżļŻ©Ļ▓ī ļÉĀ Ļ▓āņØ┤ļ»ĆļĪ£ ņŚ¼ĻĖ░ņä£ļŖö ņŻ╝ļĪ£ ņÜ░ņŗ¼ļČĆņĀäņØś ņ¢æņāüĻ│╝ ņ¦äļŗ©ņŚÉ ļīĆĒĢ┤ ļģ╝ĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ņĀĢņāü ņÜ░ņŗ¼ņŗż
ņĀĢņāü ņÜ░ņŗ¼ņŗżņØĆ ņ¢ćņØĆ ļ▓Įņ£╝ļĪ£ ļÉ£ ņ┤łņŖ╣ļŗ¼ ļ¬©ņ¢æņØś ĻĄ¼ņĪ░ņØ┤Ļ│Ā ņÜ░ņŗ¼ņŗż ņÖĖļ▓Į(free wall), ņŗ¼ņŗżņżæĻ▓® ļ░Å ņÜ░ņŗ¼ņŗż ņ£ĀņČ£ļĪ£ļĪ£ ĻĄ¼ņä▒ļÉśņ¢┤ ņ׳ļŗż. ņŗ¼ņŗżņżæĻ▓®ņØ┤ ņóīņŗ¼ņŗżĻ│╝ ņŗ¼ĻĘ╝ņä¼ņ£Āļź╝ Ļ│Ąņ£ĀĒĢśĻ│Ā ņ׳ņ¢┤ņä£ ņóīņŗ¼ņŗżņØ┤ ņÜ░ņŗ¼ņŗż ņłśņČĢ ĻĖ░ļŖźņØś 40%Ļ╣īņ¦Ć ļŗ┤ļŗ╣ĒĢśĻ▓ī ļÉ£ļŗż[2-4].
ņÖĖļ▓ĮņØś ĒÜĪņČĢ ņÜ┤ļÅÖņŚÉ ļ╣äĒĢ┤ ņŗ¼ņŗżņżæĻ▓®ņØĆ ĒÜ©Ļ│╝ņĀüņØĖ ņóģņČĢ ņłśņČĢĻ│╝ ļ╣äĒŗĆļ”╝ ņłśņČĢņØä ĒåĄĒĢ┤ ņĀäņ▓┤ ņÜ░ņŗ¼ņŗż ĻĖ░ļŖźņŚÉ Ļ░Ćņן ļ¦ÄņØ┤ ĻĖ░ņŚ¼ĒĢ£ļŗż[5].
ņÜ░ņŗ¼ļČĆņĀäņØś ņøÉņØĖĻ│╝ ļ│æĒā£ ņāØļ”¼
ņÜ░ņŗ¼ņŗżņØĆ ņĢĢļĀźņØ┤ļéś ņÜ®ņĀü Ļ│╝ļČĆĒĢś, ĒŚłĒśł, ņŗ¼ĻĘ╝ ņ¦łĒÖśņØ┤ļéś ņŗ¼ņןļ¦ēņŚÉ ņØśĒĢ£ ņĀ£ĒĢ£ ļō▒ņŚÉ ņśüĒ¢źņØä ļ░øĻ▓ī ļÉ£ļŗż. ņÜ░ņŗ¼ņŗżņØś ĻĖ░ļŖź ņןņĢĀļŖö ņŗ¼ĻĘ╝ņåÉņāüņØ┤ļéś ņŖżĒŖĖļĀłņŖżņŚÉ ņØśĒĢ┤ ņŗ£ņ×æļÉśĻ│Ā ņØ┤ļĀćļŗż ĒĢĀ ņāłļĪ£ņÜ┤ ņåÉņāüņØ┤ ņŚåņ¢┤ļÅä ņ¦äĒ¢ēĒĢĀ ņłś ņ׳ļŗż. ņÜ░ņŗ¼ļČĆņĀäņØś ņøÉņØĖņØ┤ ļ¦ÄĻ│Ā ļŗżņ¢æĒĢśņ¦Ćļ¦ī Ļ░Ćņן ĒØöĒĢ£ ņøÉņØĖņØĆ ņóīņŗ¼ļČĆņĀäņØ┤ļŗż(Table 1). ņóīņŗ¼ļČĆņĀäņØä ņØ╝ņ£╝ĒéżļŖö Ļ░ÖņØĆ ņÜöņØĖļōżņØ┤ ņÜ░ņŗ¼ņŗżņŚÉ ņśüĒ¢źņØä ņżä ņłś ņ׳ļŖöļŹ░, ņÜ░ņŗ¼ņŗż ņ×Éņ▓┤ņØś ĻĖ░ļŖź ņןņĢĀļź╝ ņØ╝ņ£╝Ēé¼ ņłś ņ׳Ļ│Ā, ņÜ░ņŗ¼ņŗżņØ┤ ĻĖ░ļŖźņØś ņāüļŗ╣ ļČĆļČäņØä ņóīņŗ¼ņŗżņŚÉ ņØśņĪ┤ĒĢśĻĖ░ ļĢīļ¼ĖņŚÉ ņÜ░ņŗ¼ņŗż ņłśņČĢļĀźņØ┤ ļŹöņÜ▒ Ļ░ÉņåīĒĢśĻ▓ī ļÉ£ļŗż.
ņÜ░ņŗ¼ņŗżņØĆ ņĀĢņāüņĀüņ£╝ļĪ£ ļé«ņØĆ ĒøäļČĆĒĢś, ņ”ē ņēĮĻ▓ī ĒÖĢņןļÉĀ ņłś ņ׳ļŖö ļÅÖļ¦źņł£ĒÖśņ£╝ļĪ£ ĒśłņĢĪņØä ļé┤ļ│┤ļéĖļŗż. ļö░ļØ╝ņä£ ĒøäļČĆĒĢśĻ░Ć ņ”ØĻ░ĆĒĢśļ®┤, ĒŖ╣Ē׳ ĻĖēņä▒ņ£╝ļĪ£ ņ”ØĻ░ĆĒĢśļ®┤, ņÜ░ņŗ¼ņŗż ĻĖ░ļŖźņØś ĒśäņĀĆĒĢ£ Ļ░ÉņåīĻ░Ć ņØ╝ņ¢┤ļéĀ ņłś ņ׳ļŗż(Fig. 1). ņāüņŖ╣ļÉ£ ņóīņĖĪ ņČ®ļ¦īņĢĢņØĆ ĒÅÉņł£ĒÖśĻ│äņØś ņĢĢļĀźņØä ņś¼ļ”┤ ļ┐Éļ¦ī ņĢäļŗłļØ╝ ĒśłĻ┤ĆĒāäņä▒ņØä ļé«ņČöņ¢┤ņä£ ņÜ░ņŗ¼ņŗż ĒøäļČĆĒĢśļź╝ ņ”ØĻ░Ćņŗ£Ēé©ļŗż[6]. ņŗ£Ļ░äņØ┤ ĒØÉļź┤ļ®┤ ņóīņŗ¼ļČĆņĀäņØĆ ĒÅÉļÅÖļ¦ź ĒśłĻ┤ĆņłśņČĢĻ│╝ ņ×¼ĒśĢņä▒ņØä ņ┤ēļ░£ĒĢ┤ņä£ ĒøäļČĆĒĢśļź╝ ļŹöņÜ▒ ņāüņŖ╣ņŗ£ĒéżĻ▓ī ļÉ£ļŗż.
ĒøäļČĆĒĢśĻ░Ć ļ¦īņä▒ņĀüņ£╝ļĪ£ ļśÉļŖö ņä£ņä£Ē׳ ņ¦äĒ¢ēĒĢśļ®┤ņä£ ņ”ØĻ░ĆĒĢśļŖö ļ¦īņä▒ņĀü ņĢĢļĀź Ļ│╝ļČĆĒĢś ņāüĒā£ņŚÉņä£ļŖö ņÜ░ņŗ¼ņŗżņØ┤ ļ╣äĻĄÉņĀü ņל ņĀüņØæĒĢśļŖöļŹ░, ņĢäņØ┤ņĀĀļ®®Ļ▒░ņ”ØĒøäĻĄ░Ļ│╝ ņäĀņ▓£ņä▒ ĒÅÉļÅÖļ¦źĒīÉ Ēśæņ░®ņ”ØņØ┤ ĻĘĖ ņśłņØ┤ļŗż. ņĢäņØ┤ņĀĀļ®®Ļ▒░ņ”ØĒøäĻĄ░ņØś Ļ▓ĮņÜ░ ņØ╝ņāØ ļÅÖņĢł ņóīņÜ░ ņŗ¼ņŗżļ▓ĮņØś ļæÉĻ╗śĻ░Ć Ļ░Öņ£╝ļ®┤ņä£ ņÜ░ņŗ¼ņŗżņØś ĒāäļĀźņØ┤ ņ£Āņ¦ĆļÉśĻ│Ā, ņÜ┤ļÅÖĒĢĀ ļĢīņ▓śļ¤╝ ņĀäņŗĀ ņĀĆĒĢŁņŚÉ ļīĆĒĢ£ ĒÅÉļÅÖļ¦ź ņĀĆĒĢŁņØś ņāüļīĆņĀü ļ╣äņ£©ņØ┤ ņ”ØĻ░ĆĒĢĀ ļĢī ņÜ░ņŗ¼ņŗżņŚÉņä£ ņĀäņŗĀ ņł£ĒÖśņ£╝ļĪ£ ņģśĒŖĖĻ░Ć ņØ┤ļŻ©ņ¢┤ņ¦Ćļ®┤ņä£ ņÜ░ņŗ¼ļČĆņĀäņØ┤ ļéśņżæņŚÉ ļéśĒāĆļé£ļŗż[7]. ņäĀņ▓£ņä▒ ĒÅÉļÅÖļ¦źĒīÉ Ēśæņ░®ņ”ØņØś Ļ▓ĮņÜ░ ņŗ¼ņŗż ļ╣äļīĆĻ░Ć ĒÅÉņćäņØś ņĀĢļÅäņŚÉ ļö░ļØ╝ ļŗżņ¢æĒĢśņ¦Ćļ¦ī ņÜ░ņŗ¼ņŗżņØĆ ļ╣äĻĄÉņĀü ņל ņĀüņØæĒĢśļŖöļŹ░, ņןĻĖ░Ļ░ä ņ╣śļŻīļ░øņ¦Ć ņĢŖņØĆ ņŗ¼ĒĢ£ ĒÅÉņćäļŖö ņÜ░ņŗ¼ļČĆņĀäĻ│╝ ņé╝ņ▓©ĒīÉ ņŚŁļźśņ”ØņØä ņ£Āļ░£ĒĢ£ļŗż[8].
ņØ╝ļ░śņĀüņ£╝ļĪ£ ņÜ░ņŗ¼ņŗżņØĆ ņĢĢļĀź Ļ│╝ļČĆĒĢśļ│┤ļŗżļŖö ņÜ®ņĀü Ļ│╝ļČĆĒĢśņŚÉ ļŹö ņל ņĀüņØæĒĢ£ļŗż. ņŗ¼ļ░®ņżæĻ▓®Ļ▓░ņåÉņ”ØĻ│╝ ņé╝ņ▓©ĒīÉ ņŚŁļźśņ”ØņŚÉņä£ ņÜ░ņŗ¼ņŗżņØĆ ņśżļ×½ļÅÖņĢł ņÜ░ņŗ¼ņŗż ņłśņČĢ ĻĖ░ļŖźņØś ņ£ĀņØśĒĢ£ Ļ░Éņåī ņŚåņØ┤ ņÜ®ņĀü Ļ│╝ļČĆĒĢśņŚÉ ņל Ļ▓¼ļöśļŗż[8]. ņØ┤ņÖĆ ļīĆņĪ░ņĀüņ£╝ļĪ£ ņä▒ņØĖņŚÉņä£ ņżæļō▒ļÅä ļé┤ņ¦Ć ņżæņ”ØņØś ņāłļĪ£ ņāØĻĖ┤ ĒÅÉĻ│ĀĒśłņĢĢņØĆ ņÜ░ņŗ¼ņŗż ĒÖĢņןĻ│╝ ņÜ░ņŗ¼ļČĆņĀäņØä ņØ╝ņ£╝Ēé©ļŗż. ņÜ░ņŗ¼ņŗżņØś ņĢĢļĀź Ļ│╝ļČĆĒĢśļŖö ļśÉĒĢ£ ņÜ░ņŗ¼ņŗż ĒŚłĒśłņØä ņØ╝ņ£╝ĒéżĻ│Ā ņÜ░ņŗ¼ņŗż ĻĖ░ļŖź ņןņĢĀļź╝ ņĢģĒÖöņŗ£Ēé¼ ņłś ņ׳ļŗż[9]. ļÅÖļ¼╝ ņŗżĒŚśĻ│╝ ņØĖĻ░ä ļīĆņāü ņŚ░ĻĄ¼ņŚÉņä£ Ļ┤Ćņ░░ļÉ£ Ļ▓āņ▓śļ¤╝ ņŗ¼ĻĘ╝ņØś Ļ▓░ĒĢ®ņĪ░ņ¦üņØś ļ░ĆļÅäĻ░Ć ņ”ØĻ░ĆĒĢśļŖö ļō▒ ņĪ░ņ¦üĒĢÖņĀü ļ│ĆĒÖöļÅä ņÜ░ņŗ¼ņŗż ņĢĢļĀź Ļ│╝ļČĆĒĢś ņāüĒā£ņŚÉņä£ ļŹöņÜ▒ ĒÖĢņŚ░ĒĢśļŗż[10,11]. ĒÅÉļÅÖļ¦ź ņāēņĀäņ”Ø Ļ░ÖņØĆ ĻĖēņä▒ ņĢĢļĀź Ļ│╝ļČĆĒĢś ņāüĒā£ņŚÉņä£ ĻĘĖ ņĀäņŚÉ ņĀĢņāüņØ┤ņŚłļŹś ņÜ░ņŗ¼ņŗżņØĆ ĻĖēņä▒ņ£╝ļĪ£ ņāüņŖ╣ļÉ£ ĒÅēĻĘĀ ĒÅÉļÅÖļ¦źņĢĢ 40 mmHg ņØ┤ņāüņØĖ ņāüĒā£ņŚÉ Ļ▓¼ļööņ¦Ć ļ¬╗ĒĢśĻ│Ā ņÜ░ņŗ¼ļČĆņĀäņØ┤ ņĪ░ĻĖ░ņŚÉ ļ░£ņāØĒĢ£ļŗż. ĻĘĖļ¤░ļŹ░ Ļ░ÖņØĆ ņĀĢļÅäņØś ĒÅÉļÅÖļ¦źņĢĢņŚÉņä£ļÅä ņé¼ļ×īņŚÉ ļö░ļØ╝ņä£ ņÜ░ņŗ¼ļČĆņĀäņØ┤ ļ░£ņāØĒĢśļŖö ņŗ£ĻĖ░Ļ░Ć ļŗżļźĖ Ļ▓āņØä ļ│┤ļ®┤ ņ£ĀņĀäņ×É ļ░£ĒśäņØ┤ļéś ņŗĀĻ▓ĮĒśĖļź┤ļ¬¼ ĒÖ£ņä▒ņØ┤ Ļ┤ĆņŚ¼ĒĢ£ļŗżļŖö Ļ▓āņØä ņāØĻ░üĒĢĀ ņłś ņ׳ļŗż[12]. ņÜ░ņŗ¼ņŗżņØ┤ ņĀüņØæĒĢśļŖö Ļ│╝ņĀĢņØĆ ļ│Ąņ×ĪĒĢśļ®░ ļ¦ÄņØĆ ņÜöņØĖļōżņŚÉ ņśüĒ¢źņØä ļ░øļŖöļŗż. Ļ░Ćņן ņżæņÜöĒĢ£ ņÜöņØĖņØĆ ņŗ¼ĻĘ╝ņåÉņāüņØ┤ļéś ņŖżĒŖĖļĀłņŖżņØś ĒśĢĒā£ņÖĆ ņŗ¼ĒĢ£ ņĀĢļÅä, ņ¦łĒÖśņØś ņŗ£Ļ░ä Ļ▓ĮĻ│╝, ņ¦łĒÖśņØ┤ ņŗ£ņ×æĒĢ£ ļĢī ļō▒ņØ┤ļŗż. ņØ┤ņÖĖņØś ņżæņÜöĒĢ£ ņÜöņØĖļōżņØĆ ņŗĀĻ▓ĮĒśĖļź┤ļ¬¼Ļ│ä ĒÖ£ņä▒ĒÖö, ņ£ĀņĀäņ×É ļ░£ĒśäņØś ļ│ĆĒÖö, ņŗ¼ņŗż ņ×¼ĒśĢņä▒ņØś ĒśĢĒā£ ļō▒ņØ┤ļŗż. ņØ┤ļōżņØ┤ ņāüĒśĖ ņ×æņÜ®ĒĢśņŚ¼ ņÜ░ņŗ¼ņŗż ĻĖ░ļŖź ņןņĢĀļź╝ ņØ╝ņ£╝Ēé©ļŗż. ļ¦ÄņØĆ ņŚ░ĻĄ¼ļōżņØ┤ ņÜ░ņŗ¼ļČĆņĀä ĒÖśņ×ÉņŚÉņä£ ņ×Éņ£©ņŗĀĻ▓ĮĻ│ä, ļĀłļŗī-ņĢżņ¦ĆņśżĒģÉņŗĀ-ņĢīļÅäņŖżĒģīļĪĀĻ│äĒåĄ, ļéśĒŖĖļź©ņØ┤ļć©ĒÄ®Ēŗ░ļō£, ņŚöļÅäĒģöļ”░Ļ│ä, ņé¼ņØ┤ĒåĀņ╣┤ņØĖņØś ņŚŁĒĢĀņØä ļģ╝ĒĢśņśĆļŗż.
ņÜ░ņŗ¼ļČĆņĀäņØś ļŗ©Ļ│äņÖĆ ņśłĒøä ņØĖņ×É
ņÜ░ņŗ¼ļČĆņĀäņØś ļ░£ņāØņØĆ ņóīņŗ¼ļČĆņĀäĻ│╝ Ļ░ÖņØ┤ ņĀÉņ¦äņĀüņ£╝ļĪ£ ņ¦äĒ¢ēĒĢ┤ņä£ ļ¼┤ņ”Øņāü ņÜ░ņŗ¼ņŗż ĻĖ░ļŖź ņןņĢĀņŚÉņä£ ņ”ØņāüņØ┤ ņ׳ļŖö ņÜ░ņŗ¼ļČĆņĀäņØä Ļ▒░ņ│É ļé£ņ╣śņä▒ ņÜ░ņŗ¼ļČĆņĀäņ£╝ļĪ£ ņ¦äĒ¢ēĒĢ£ļŗż. ĒÅÉļÅÖļ¦ź Ļ│ĀĒśłņĢĢĻ│╝ ņŚ░Ļ┤ĆļÉ£ ļé£ņ╣śņä▒ ņÜ░ņŗ¼ļČĆņĀäņØś ļ¦ÄņØĆ ĒÖśņ×ÉļōżņØ┤ ĒÅÉņØ┤ņŗØ ĒøäņŚÉ ņÜ░ņŗ¼ņŗż ĻĖ░ļŖźņØś ņ£ĀņØśĒĢ£ Ļ░£ņäĀņØä ļ│┤ņØ┤ļŖö Ļ▓āņØĆ ņÜ░ņŗ¼ņŗżņØś ĒÜīļ│Ą Ļ░ĆļŖźņä▒Ļ│╝ ĒØöĒ׳ ņé¼ņÜ®ļÉśļŖö ņÜ░ņŗ¼ņŗż ņłśņČĢ ĻĖ░ļŖź ņ¦ĆĒæ£ļōżņØś ļČĆĒĢś ņØśņĪ┤ņä▒ņØä ļéśĒāĆļéĖļŗż. ņÜ░ņŗ¼ļČĆņĀäņØś ņ¦äĒ¢ē ņĀĢļÅäļŖö ņøÉņØĖņØ┤ ļÉśļŖö ĻĖ░ņĀĆ ņ¦łĒÖśņŚÉ ļö░ļØ╝ ļŗżļźĖļŹ░, ņÜ░ņŗ¼ņŗż ņÜ®ņĀü Ļ│╝ļČĆĒĢś, ĒÅÉļÅÖļ¦źĒīÉ Ēśæņ░®ņ”Ø, ņĢäņØ┤ņĀĀļ®®Ļ▒░ņ”ØĒøäĻĄ░ņŚÉņä£ Ļ░Ćņן ņóŗņØĆ ņןĻĖ░ ņśłĒøäļź╝ ļéśĒāĆļéĖļŗż. ĒÅÉĻ│ĀĒśłņĢĢņØ┤ļéś ņäĀņ▓£ņä▒ ņŗ¼ņן ņ¦łĒÖśĻ│╝ ņŚ░Ļ┤ĆļÉ£ ņÜ░ņŗ¼ļČĆņĀä ĒÖśņ×ÉņŚÉņä£ Ļ░ÉņåīļÉ£ ņÜ┤ļÅÖļŖźļĀźņØĆ ņé¼ļ¦ØņØ┤ļéś ņ×ģņøÉņŚÉ ļīĆĒĢ£ Ļ░Ćņן ņżæņÜöĒĢ£ ņśłĒøä ņØĖņ×É ņżæ ĒĢśļéśņØ┤ļŗż. ļŗżļźĖ ņśłĒøä ņØĖņ×ÉļōżņØĆ ņÜ░ņŗ¼ņŗż ņłśņČĢ ĻĖ░ļŖź ņןņĢĀņØś ņĀĢļÅä, ņÜ░ņŗ¼ņŗż ņØ┤ņÖä ĻĖ░ļŖź ņןņĢĀ, ņŗĀĻ▓ĮĒśĖļź┤ļ¬¼Ļ│ä ĒÖ£ņä▒ņØś ņĀĢļÅä, ņŗ¼ļ░ĢļÅÖņłś ļ│ĆļÅÖļČĆņĀä, ļČĆņĀĢļ¦ź, ņóīņŗ¼ņŗż ņłśņČĢ ĻĖ░ļŖź ņןņĢĀ, Ēśłņ▓Ł ņÜöņé░Ļ│╝ ļ╣īļ”¼ļŻ©ļ╣ł ļō▒ņØ┤ļŗż.
ņÜ░ņŗ¼ļČĆņĀäņØś ņ×äņāü ņ¢æņāü
ņÜ░ņŗ¼ļČĆņĀäņØś ņ”Øņāüņ£╝ļĪ£ļŖö ĒĢśņ¦ĆļČĆņóģ, ļ│ĄļČĆ ĒīĮļ¦īĻ░É, ņåīĒÖö ņןņĢĀ, ņŗØņÜĢļČĆņ¦ä, ņśżņŗ¼, ņĀäņŗĀ ņćĀņĢĮĻ░É, Ēö╝ļĪ£Ļ░É, ņĀäņŗĀ ļČĆņóģ ļ░Å ĒśĖĒØĪĻ│żļ×Ć ļō▒ņØ┤ ļéśĒāĆļéĀ ņłś ņ׳ļŖöļŹ░, ņóīņŗ¼ļČĆņĀäņØś ņ”ØņāüĻ│╝ ĒĢ©Ļ╗ś ļéśĒāĆļéśĻĖ░ļÅä ĒĢ£ļŗż. ņØ┤ņÖĖņŚÉļÅä Ļ░äļ╣äļīĆ, ļ╣äņן ļ╣äļīĆ, ļ│Ąņłś ļō▒ ņÜ░ņŗ¼ļČĆņĀäņØś ņ×äņāü ņ¢æņāüņØĆ ĻĘ╝ļ│Ė ņøÉņØĖĻ│╝ ļÅÖļ░ś ņ¦łĒÖśņŚÉ ļö░ļØ╝ ļŗżņ¢æĒĢśĻ▓ī ļéśĒāĆļé£ļŗż(Table 2). ņäĀņ▓£ņä▒ ņŗ¼ņן ņ¦łĒÖśņŚÉ ņØśĒĢ£ ņÜ░ņŗ¼ļČĆņĀäņØś Ļ▓ĮņÜ░ ĒśĖĒØĪĻ│żļ×ĆņØ┤ Ļ░Ćņן ĒØöĒĢ£ ņ”ØņāüņØ┤ļ®░ ņé░ņåīņłśņÜöĻ░Ć ņ”ØĻ░ĆĒĢĀ ļĢī ņŗ¼ņןļ░ĢņČ£ļ¤ēņØś ņ”ØĻ░ĆĻ░Ć ļö░ļØ╝Ļ░Ćņ¦Ć ļ¬╗ĒĢśĻ│Ā ņé░ņåīĻ│ĄĻĖēņØ┤ ņČ®ļČäĒĢśņ¦Ć ļ¬╗ĒĢ┤ņä£ ņāØĻĖ┤ļŗż. ņÜ░ņŗ¼ļ░® ĒÖĢņןņŚÉ ļö░ļźĖ ļČĆņĀĢļ¦ź ļ░£ņāØņ£╝ļĪ£ ņŗ¼Ļ│äĒĢŁņ¦äĻ│╝ ļ╣łļ¦źņØä ļŖÉļéä ņłś ņ׳ņ£╝ļ®░, ņÜ░ņŗ¼ļČĆņĀäņ£╝ļĪ£ ņØĖĒĢ£ ņ▓Łņāēņ”Ø, Ļ│żļ┤ēņ¦Ć, ņŗżņŗĀ ļō▒ņØ┤ ļ░£ņāØĒĢĀ ņłś ņ׳ļŗż. Ļ▓ĮņĀĢļ¦źņØ┤ ĒÖĢņןļÉśĻ│Ā Ļ░äļ╣äļīĆ, ļ│Ąņłś, ļ¦Éļŗ©ļČĆņóģņØä ļ│┤ņØ╝ ņłś ņ׳ļŗż. ņŗ¼ņ×ĪņØīņØĆ ņé╝ņ▓©ĒīÉņŚŁļźśļĪ£ ĒØēĻ│© ņóīĒĢśņŚ░ņŚÉņä£ ņłśņČĢĻĖ░ ņŗ¼ņ×ĪņØīņØ┤ ļōżļ”¼ļ®░, ņĀ£2ņŗ¼ņØī ņżæ ĒÅÉņØīņØ┤ ņ”ØĻ░ĆĒĢśĻ│Ā, ņĀ£3, 4ņŗ¼ņØīņØ┤ ļōżļ”┤ ņłś ņ׳ļŗż[13].
ļīĆļČĆļČäņØś ņÜ░ņŗ¼ļČĆņĀäņØś ņ”ØņāüņØĆ ņĀäņŗĀņŚÉņä£ ļōżņ¢┤ņśżļŖö ņĀĢļ¦źĒśłņØ┤ ļīĆņĀĢļ¦źņŚÉ ņĀĢņ▓┤ļÉśņ¢┤ ņāØĻĖ░ļŖö ņ”ØņāüņØĖļŹ░, ņĀĢļ¦źņĢĢņØ┤ ņ”ØĻ░ĆĒĢśļ®┤ ļ░£ļ¬® ļśÉļŖö ņĀĢĻ░ĢņØ┤ ļČĆņ£äĻ░Ć ļČōļŖö ĒĢśņ¦Ć ļČĆņóģņØ┤ ņāØĻĖ░Ļ│Ā, Ļ░äņØ┤ļéś ļ╣äņןņØ┤ ņ╗żņĀĖ ļ│ĄļČĆ ĒīĮļ¦īĻ░ÉĻ│╝ ņåīĒÖöļČłļ¤ēņØä ĒśĖņåīĒĢśĻ▒░ļéś ņŗ¼ĒĢśļ®┤ ļ│ĄņłśĻ░Ć ņāØĻĖ░Ļ▓ī ļÉśĻ│Ā, Ļ░äĻĖ░ļŖź ņØ┤ņāüņ£╝ļĪ£ ĒÖ®ļŗ¼ņØ┤ ļéśĒāĆļéĀ ņłś ņ׳ļŗż. ņŗ¼ņןļ░ĢņČ£ļ¤ēņØ┤ Ļ░ÉņåīĒĢśļ®┤ ņŗ¼ĻĖ░ļŖź ņĀĆĒĢśņŚÉ ļö░ļźĖ ļ│┤ņāü ĻĖ░ņĀäņØ┤ ņ×æļÅÖĒĢśĻ▓ī ļÉśļŖöļŹ░, 1) ĻĄÉĻ░ÉņŗĀĻ▓ĮņØ┤ ĒÖ£ņä▒ĒÖöļÉśņ¢┤ ņŗ¼ņן ņłśņČĢļĀźĻ│╝ ļ¦źļ░Ģņłśļź╝ ņ”ØĻ░Ćņŗ£ĒéżĻ│Ā, ļ¦Éņ┤łĒśłĻ┤ĆņØ┤ ņłśņČĢĒĢśņŚ¼ ĒśłņĢĢņØä ņ£Āņ¦ĆĒĢśļĀżĻ│Ā ĒĢśĻ│Ā, 2) ņŗĀņןņ£╝ļĪ£ Ļ░ĆļŖö ĒśłņĢĪļ¤ēņØ┤ Ļ░ÉņåīĒĢśļ»ĆļĪ£ ņŗĀņןņŚÉņä£ ļ░░ņäżļÉśļŖö ņłśļČäļ¤ēņØä Ļ░Éņåīņŗ£ņ╝£ ĒśłņĢĪņØś ņ¢æņØä ņĀüņĀłĒĢśĻ▓ī ņ£Āņ¦ĆĒĢśļĀżļŖö ļ│┤ņāü ĻĖ░ņĀäņØ┤ ņ×æļÅÖļÉ£ļŗż. ļö░ļØ╝ņä£, ņØ┤ļ¤░ ļ│┤ņāü ĻĖ░ņĀäņŚÉ ņØśĒĢ┤ ļ╣łļ¦ź, ļ░£ĒĢ£ ļ░Å ņåīļ│Ćļ¤ēņØś Ļ░Éņåī ļō▒ņØ┤ ļéśĒāĆļéĀ ņłś ņ׳ļŗż.
ņÜ░ņŗ¼ļČĆņĀäņØś ņ¦äļŗ©
ņÜ░ņŗ¼ļČĆņĀäņØś ņ¦äļŗ©ņŚÉņä£ ļ│æļĀź ņ▓ŁņĘ©ņÖĆ ņŗĀņ▓┤ Ļ▓Ćņé¼ļŖö ņÜ░ņŗ¼ļČĆņĀäĻ│╝ ĻĘĖ ņøÉņØĖ ņ¦łĒÖś ļ░Å ļÅÖļ░ś ņ¦łĒÖśņØä ĒÅēĻ░ĆĒĢśĻĖ░ ņ£äĒĢ┤ ņżæņÜöĒĢśļŗż. ĒØēļČĆ ļ░®ņé¼ņäĀ ņ┤¼ņśüņØ┤ ĒĢäņÜöĒĢśĻ│Ā ļĢīļĢīļĪ£ ĒŖ╣ņ¦ĢņĀüņØĖ ļ│ĆĒÖöļź╝ ņ░ŠņØä ņłś ņ׳ļŗż. ļŗżļźĖ ĒÅÉņŗżņ¦łņä▒ ņ¦łĒÖśņØ┤ ņŚåļŖöņ¦Ć ņל ĒÅēĻ░ĆĒĢ┤ņĢ╝ ĒĢśĻ│Ā ņŗ¼ņןņ£żĻ│ĮņØś ņĀäņ▓┤ Ēś╣ņØĆ ņ¢┤ļŖÉ ĒĢ£ ļČĆļČäņØ┤ ņ╗żņĀĖ ņ׳ļŖöņ¦Ć ņŚ¼ļČĆĻ░Ć ņ¦äļŗ©ņ¦ĆĒæ£Ļ░Ć ļÉĀ ņłś ņ׳ļŗż. ņŗ¼ņĀäļÅä Ļ▓Ćņé¼ņŚÉņä£ ņÜ░ņŗ¼ļČĆņĀä ņ┤łĻĖ░ņŚÉļŖö ņÜ░ņĖĪĒÄĖņ£ä, ņÜ░ņŗ¼ļ░® ĒÖĢļīĆ(P pulmonale), ņÜ░ņŗ¼ņŗż ļ╣äĒøä, ņÜ░ņŗ¼ņŗż ĻĖ┤ņןĒśĢņØä ļ│┤ņØĖļŗż. ņÜ░ņŗ¼ņŗż ņĢĢļĀźņØ┤ ņĀäņŗĀ ņĢĢļĀź ņĀĢļÅäņØ┤Ļ▒░ļéś ņĢĮĻ░ä ļé«ņØä ņĀĢļÅäļĪ£ ļåÆņ£╝ļ®┤ ņŗ¼ņןņĢ× ņ£ĀļÅäņŚÉņä£ RĒīīĻ░Ć ņÜ░ņäĖĒĢśļ®┤ņä£ ļ░öļĪ£ ņäĀ TĒīīļź╝ ļ│┤ņØ┤ļ®░, ņĀäņŗĀ ņĢĢļĀźļ│┤ļŗż ļŹö ļåÆņØä Ļ▓ĮņÜ░ņŚÉļŖö ņÜ░ņĖĪ ĒØēļČĆ ņ£ĀļÅäņŚÉņä£ ĻĖ┤ņןĒśĢĒā£ļĪ£ ļéśĒāĆļéś TĒīī ņŚŁņ£äņÖĆ JĒīī ĒĢśĻ░Ģņ£╝ļĪ£ ļéśĒāĆļé£ļŗż. ņÜ░ņŗ¼ļČĆņĀäņŚÉ ĒŖ╣ņ¦ĢņĀüņØĖ ņāØĒÖöĒĢÖņĀü Ēæ£ņ¦Ćņ×ÉļŖö ņŚåņ¦Ćļ¦ī ļ¬ć Ļ░Ćņ¦Ć ļÅäņøĆņØ┤ ļÉśļŖö ņāØĒÖöĒĢÖņĀü Ēæ£ņ¦Ćņ×ÉļōżņØ┤ ņ׳ļŗż(Table 3). BĒśĢ ļéśĒŖĖļź©ņØ┤ļć©ĒÄ®Ēŗ░ļō£ņÖĆ ņŗ¼ņן ĒŖĖļĪ£ĒżļŗīņØś ļ│ĆĒÖöļŖö ĻĖēņä▒ ņÜ░ņŗ¼ļČĆņĀäņØ┤ ņāØĻĖ┤ ņøÉņØĖ ņ¦łĒÖśņŚÉ ļö░ļØ╝ ļŗ¼ļØ╝ņ¦äļŗż. ņØ┤ļ¤¼ĒĢ£ Ēæ£ņ¦Ćņ×ÉļŖö ņÜ░ņŗ¼ļČĆņĀäĻ│╝ ņŗ¼ĻĘ╝ņåÉņāüņØś ņŗĀņåŹĒĢ£ ņ¦äļŗ©ņŚÉ ļÅäņøĆņØ┤ ļÉ£ļŗż[14-17]. ņÜ░ņŗ¼ļČĆņĀäņØś ņ¦äļŗ©ņØä ņ£äĒĢ£ ņāłļĪ£ņÜ┤ ņāØĒÖöĒĢÖņĀü Ēæ£ņ¦Ćņ×ÉĻ░Ć ĒÅēĻ░ĆļÉśĻ│Ā ņ׳ļŗż[18-21].
ņÜ░ņŗ¼ņŗż ĻĖ░ļŖźņØś ņĀĢĒÖĢĒĢśĻ│Ā ĒżĻ┤äņĀüņØĖ ĒÅēĻ░ĆļŖö ņ¢┤ļĀĄļŗż. ņÜ░ņŗ¼ņŗżņØĆ ĻĖ░ļŖźņĀüņ£╝ļĪ£ ĒśĢņāüĒÖöĒĢśĻĖ░ ņ¢┤ļĀżņÜĖ ņłś ņ׳Ļ│Ā ņÜ░ņŗ¼ņŗżņØś ĒøäļČĆĒĢś ņØśņĪ┤ļÅäļŖö ņÜ░ņŗ¼ņŗżņØś Ļ│Āņ£Ā ĻĖ░ļŖźņØä ņלļ¬╗ ĒĢ┤ņäØĒĢśĻ▓ī ĒĢĀ ņłśļÅä ņ׳ļŗż. ļ╣äņ╣©ņŖĄņĀüņØĖ ļ░®ļ▓Ģņ£╝ļĪ£ ņŗ¼ņ┤łņØīĒīī Ļ▓Ćņé¼ņÖĆ ņ×ÉĻĖ░Ļ│Ąļ¬ģņśüņāü(magnetic resonance imaging, MRI)ņØ┤ Ļ░Ćņן ļ¦ÄņØ┤ ņō░ņØ┤ļŖö ļ░®ļ▓ĢņØ┤ļŗż[22].
ņŗ¼ņ┤łņØīĒīī Ļ▓Ćņé¼
ņŗ¼ņ┤łņØīĒīī Ļ▓Ćņé¼ļŖö ņÜ░ņŗ¼ņŗżņØś Ēü¼ĻĖ░, ĻĖ░ļŖź ļ░Å ļČĆĒĢś ņāüĒā£ļź╝ ĒÅēĻ░ĆĒĢśĻĖ░ ņ£äĒĢ┤ ņé¼ņÜ®ĒĢĀ ņłś ņ׳ļŖö ņ▓½ ļ▓łņ¦Ė Ļ▓Ćņé¼ņØ┤Ļ│Ā, ņ╣©ņāü ņŗ¼ņ┤łņØīĒīī Ļ▓Ćņé¼ļŖö ņŗ¼ņןņØś ĻĄ¼ņĪ░ņÖĆ ĻĖ░ļŖźņŚÉ ļīĆĒĢ£ ļ╣ĀļźĖ ņĀĢļ│┤ļź╝ ņŻ╝ļ®░ ņØæĻĖēņŗżņØ┤ļéś ņżæĒÖśņ×ÉņŗżņŚÉņä£ļÅä ņé¼ņÜ®ĒĢĀ ņłś ņ׳ļŗż. ņ”ēĻ░üņĀüņØĖ ņ╣śļŻīļź╝ ņÜöĒĢśļŖö ĻĖēņä▒ ņÜ░ņŗ¼ļČĆņĀäņØś ņÖĖņĀü ņøÉņØĖļōżņØä ļ░░ņĀ£ĒĢśĻ│Ā ĒĢśļīĆņĀĢļ¦źņØś ņ¦üĻ▓ĮņØä ņĖĪņĀĢĒĢśĻ│Ā ĒśĖĒØĪņŚÉ ļö░ļźĖ ļ│ĆĒÖöļź╝ ĒÅēĻ░ĆĒĢśĻĖ░ ņ£äĒĢ┤ ņé¼ņÜ®ļÉĀ ņłś ņ׳ļŗż. Ļ▓Įņé╝ņ▓©ĒīÉ ņĢĢļĀźņ░©ļź╝ ĻĄ¼ĒĢśņŚ¼ ĒÅÉļÅÖļ¦ź ņłśņČĢĻĖ░ņĢĢņØä Ļ│äņé░ĒĢśļŖö Ļ▓āņØĆ ņ╣©ņŖĄņĀüņØĖ ļ░®ļ▓ĢĻ│╝ ļ╣äĻĄÉĒĢĀ ļĢī ļ»┐ņØä ļ¦īĒĢ£ ļ░®ļ▓ĢņØ┤ļŗż. ņÜ░ņŗ¼ņŗż ĒÖĢņן, ĻĄ¼ĒśĢļÅä ļ░Å ņóīņŗ¼ņŗż ĒÖĢņןĻ│╝ ļ╣äĻĄÉĒĢ£ ņÜ░ņŗ¼ņŗż ĒÖĢņןņØś ņĀĢļÅäļź╝ ņĀĢĒÖĢĒĢśĻ▓ī ĒÅēĻ░ĆĒĢśĻĖ░ ņ£äĒĢ┤ņä£ļŖö ņÜ░ņŗ¼ņŗżņŚÉ ņ┤łņĀÉņØä ļ¦×ņČś ņŗ¼ņ▓©4ļ░®ļÅäņÖĆ ļŖæĻ│©ĒĢśļČĆņ░Į ļō▒ ņÜ░ņĖĪ ņŗ¼ņןņŚÉ ļīĆĒĢ£ ļ¬©ļōĀ Ļ░ĆļŖźĒĢ£ ņןļ®┤ņØä ĒÖ£ņÜ®ĒĢ┤ņĢ╝ ĒĢ£ļŗż. ņÜ░ņŗ¼ņŗż ĒÖĢņן, ņÜ░ņŗ¼ņŗż ļ╣äĒøä, ņé╝ņ▓©ĒīÉņŚŁļźśļź╝ ĒÅēĻ░ĆĒĢĀ ņłś ņ׳Ļ│Ā, ņ¢æ ņŗ¼ņŗżņØ┤ ļ│┤ņØ┤ļŖö ļŗ©ņČĢļ®┤ņŚÉņä£ ņŗ¼ņŗżņżæĻ▓®ņØś ļ¬©ņ¢æņØä ļ│┤ņĢä ņÜ░ņŗ¼ņŗż ņĢĢļĀźĻ│╝ ĒÅÉļÅÖļ¦ź Ēśæņ░®ņØ┤ ņŚåņØä Ļ▓ĮņÜ░ļŖö ĒÅÉļÅÖļ¦ź ņĢĢļĀźņØś ņĀĢļÅäļź╝ ņśłņĖĪĒĢĀ ņłś ņ׳ļŗż. ļ¦īņØ╝ ņóīņŗ¼ņŗżņØ┤ ņ¢┤ļŖÉ ņĀĢļÅä ļÅÖĻĘĖļ×Ć ļ¬©ņ¢æņØä Ļ░Ćņ¦ĆĻ│Ā ņ׳ļŗżļ®┤ ņÜ░ņŗ¼ņŗż ņĢĢļĀźņØĆ ņóīņŗ¼ņŗż ņĢĢļĀź ļśÉļŖö ņĀäņŗĀ ņłśņČĢĻĖ░ ĒśłņĢĢņØś 50% ņØ┤ĒĢśņØ┤Ļ│Ā, ņŗ¼ņŗżņżæĻ▓®ņØ┤ ĒÅēĒÅēĒĢ┤ņä£ Ļ▒░ņØś Dņ×É ļ¬©ņ¢æņØś ņóīņŗ¼ņŗż ĒśĢĒā£ļź╝ ņ¦Ćļŗłļ®┤ ņÜ░ņŗ¼ņŗż ņĢĢļĀźņØĆ ņóīņŗ¼ņŗż ņĢĢļĀź Ēś╣ņØĆ ņĀäņŗĀ ņĢĢļĀźņŚÉ ĻĘ╝ņé¼ĒĢśļ®░, ņŗ¼ņŗżņżæĻ▓®ņØ┤ ņóīņŗ¼ņŗż ņ¬Įņ£╝ļĪ£ ļ░ĆļĀż ņ׳ņ£╝ļ®┤ ņÜ░ņŗ¼ņŗż ņĢĢļĀźņØ┤ ņĀäņŗĀ ņĢĢļĀź ņØ┤ņāüņ£╝ļĪ£ ņāüņŖ╣Ē¢łļŗżļŖö Ļ▓āņØä ņČöņĖĪĒĢĀ ņłś ņ׳ļŗż. ĻĖ░ņłĀ ļ░£ļŗ¼ļĪ£ 3ņ░©ņøÉ ņŗ¼ņ┤łņØīĒīīĻĖ░ĻĖ░ļź╝ ņØ┤ņÜ®ĒĢ£ ņÜ░ņŗ¼ņŗż ņÜ®ņĀü ļ░Å ĻĖ░ļŖź ĒÅēĻ░ĆĻ░Ć Ēø©ņö¼ ņÜ®ņØ┤ĒĢ┤ņĪīļŗż.
ņÜ░ņŗ¼ņŗżņØś ņłśņČĢĻĖ░ ļ░Å ĒÖĢņןĻĖ░ ĻĖ░ļŖźņØĆ ņÜ░ņŗ¼ņŗż ņ£ĀņČ£ļĪ£, ņé╝ņ▓©ĒīÉ ņ£Āņ×ģļČĆņÖĆ ņĀĢļ¦źņŚÉņä£ņØś ņŚ¼ļ¤¼ ļÅäĒöīļ¤¼ ņ¦ĆĒæ£ņŚÉ ņØśĒĢ┤ Ļ░äņĀæņĀüņ£╝ļĪ£ ĒÅēĻ░ĆĒĢĀ ņłś ņ׳ļŗż. M ļ¬©ļō£ņÖĆ ņĪ░ņ¦üļÅäĒöīļ¤¼ ņśüņāüņØä ņØ┤ņÜ®ĒĢ┤ņä£ ņé╝ņ▓©ĒīÉļź£ņŚÉņä£ ņŗ¼ĻĘ╝ ņåŹļÅäņÖĆ ņŗ£Ļ░äņØä ņĖĪņĀĢĒĢśņŚ¼ ņÜ░ņŗ¼ņŗżņØś ĒÖĢņןĻĖ░ņÖĆ ņłśņČĢĻĖ░ņØś ņøĆņ¦üņ×äņØś ņ¦ĆĒæ£ļĪ£ņä£ ņé¼ņÜ®ĒĢśĻ│Ā ņ׳ļŗż. ņé╝ņ▓©ĒīÉņØś ņ£Āņ×ģ ĒśłļźśņåŹļÅäņÖĆļŖö ļŗ¼ļ”¼ ņé╝ņ▓©ĒīÉļź£ņØś ĒÖĢņןĻĖ░ ņåŹļÅäļŖö ņ╣©ņŖĄņĀüņ£╝ļĪ£ ņĖĪņĀĢļÉ£ ņÜ░ņŗ¼ņŗż ņĢĢļĀźĻ│╝ ņāüĻ┤ĆĻ┤ĆĻ│äĻ░Ć ņ׳ļŗż. ĻĖ░ĒĢśĒĢÖņĀü ĻĄ¼ņĪ░ ļ░Å Ļ│╝ļČĆĒĢśņÖĆļŖö ļ¼┤Ļ┤ĆĒĢśĻ▓ī ļÅäĒöīļ¤¼ļź╝ ņØ┤ņÜ®ĒĢ£ ņĀäņ▓┤ņĀüņØĖ ņŗ¼ĻĘ╝ ĻĖ░ļŖźņØä ņĀĢļ¤ēņĀüņ£╝ļĪ£ ņĖĪņĀĢĒĢĀ ņłś ņ׳ļŖö, ņ”ē ņŗ¼ĻĘ╝ ņłśĒ¢ē ņ¦ĆĒæ£(myocardial performance index) Ēś╣ņØĆ ņé╝ņ▓©ĒīÉļź£ņØś ļō▒ņÜ®ņĀü Ļ░ĆņåŹ(tricuspid annular isovolumic acceleration) ļō▒ņØĆ ņÜ░ņŗ¼ņŗż ĻĖ░ļŖź ĒÅēĻ░Ćļź╝ ņ£äĒĢśņŚ¼ ņ£ĀņÜ®ĒĢśļŗż. ņÜ░ņŗ¼ņŗż ņłśņČĢ ĻĖ░ļŖź ņØ┤ņāüņØ┤ ņ׳ņ£╝ļ®┤ ļō▒ņÜ®ņĀü ņłśņČĢĻĖ░ ņŗ£Ļ░äņØĆ ĻĖĖņ¢┤ņ¦ĆĻ│Ā, ņÜ░ņŗ¼ņŗż ļ░ĢņČ£ ņŗ£Ļ░äņØĆ ņ¦¦ņĢäņ¦äļŗż. ņÜ░ņŗ¼ņŗż ĒÖĢņן ĻĖ░ļŖź ņØ┤ņāüņ£╝ļĪ£ ļō▒ņÜ®ņĀü ĒÖĢņןĻĖ░ ņŗ£Ļ░äņØĆ ĻĖĖņ¢┤ņ¦äļŗż. ĻĘĖļ¤¼ļ»ĆļĪ£ ņĀäņ▓┤ņĀüņ£╝ļĪ£ ņÜ░ņŗ¼ņŗż ĻĖ░ļŖź ņØ┤ņāüņØ┤ ņ׳ņ£╝ļ®┤ ņŗ¼ĻĘ╝ ņłśĒ¢ē ņ¦ĆĒæ£Ļ░Ć ņ”ØĻ░ĆĒĢ£ļŗż. ņŗ¼ĻĘ╝ņØś ļ│ĆĒśĢ(strain)Ļ│╝ ļ│ĆĒśĢ ņåŹļÅä(strain rate)ņØä ņØ┤ņÜ®ĒĢ£ ņĪ░ņ¦üļÅäĒöīļ¤¼ ņśüņāüņØĆ ņŗ¼ĻĘ╝ ĻĖ░ļŖźņØś ņĀĢļ¤ēņĀü ļČäņäØņØä Ļ░ĆļŖźĒĢśĻ▓ī ĒĢśļ®░, ņŗ¼ĻĘ╝ļ▓ĮņŚÉņä£ ĻĄŁņåīņĀüņØĖ ņłśņČĢ ĻĖ░ļŖźņØä ĒÅēĻ░ĆĒĢśņŚ¼ ņÜ░ņŗ¼ņŗż ĻĖ░ļŖźņŚÉ Ļ┤ĆĒĢ£ ļ¦ÄņØĆ ņĀĢļ│┤ļź╝ ņżĆļŗż.
ņ┤łņØīĒīī ĻĖ░ļ▓ĢņØś ļ░£ņĀäņŚÉ ļö░ļØ╝ ņÜ░ņŗ¼ņŗż ņĀäņ▓┤ ļśÉļŖö ļČäņĀłņŚÉ ļīĆĒĢ£ ņ¦łņĀü ĒÅēĻ░ĆņŚÉņä£ ņ¢æņĀü ĒÅēĻ░ĆļĪ£ ļ░öļĆīĻ│Ā ņ׳ļŗż[23]. ļ»ĖĻĄŁ ņŗ¼ņ┤łņØīĒīīĒĢÖĒÜīņÖĆ ņ£Āļ¤Į ņŗ¼ĒśłĻ┤ĆņśüņāüĒĢÖĒÜīņØś ņĄ£ņŗĀ ĻČīĻ│ĀņĢłņØĆ ļŗżņØī ņ¦ĆĒæ£ļōż ņżæ ņĄ£ņåīĒĢ£ ĒĢśļéśļź╝ ĒĢśņŚ¼ņä£ ņĀäņ▓┤ņĀüņØĖ ņÜ░ņŗ¼ņŗż ĻĖ░ļŖźņØś ņ¢æņĀü ĒÅēĻ░Ćļź╝ ĒĢśļÅäļĪØ ĒĢśņśĆļŖöļŹ░[24], ņÜ░ņŗ¼ņŗż ļČäĒÜŹļ®┤ņĀü ļ│ĆĒÖö(right ventricular fractional area change, RVFAC); ņé╝ņ▓©ĒīÉļź£ ĒÅēļ®┤ ņłśņČĢņØ┤ļÅÖ(tricuspid annular plane systolic excursion, TAPSE); ņĪ░ņ¦üļÅäĒöīļ¤¼ ņśüņāüņØä ņØ┤ņÜ®ĒĢ£ ņé╝ņ▓©ĒīÉļź£ņØś ņłśņČĢĻĖ░ SŌĆÖ ņåŹļÅä, ļśÉļŖö ņÜ░ņŗ¼ņŗż ņŗ¼ĻĘ╝ ņłśĒ¢ē ņ¦ĆĒæ£ņØ┤ļŗż. TAPSEņÖĆ SŌĆÖ ņåŹļÅäņŚÉ ņČöĻ░ĆņĀüņ£╝ļĪ£ ņÜ░ņŗ¼ņŗż ņĀäņ▓┤ ļśÉļŖö ĻĄŁņåīņĀüņØĖ ņóģņČĢ ņłśņČĢņØä ļ│ĆĒśĢ ņŗ¼ņ┤łņØīĒīī Ļ▓Ćņé¼ļĪ£ ĒÅēĻ░ĆĒĢĀ ņłś ņ׳ļŗż. ņÜ░ņŗ¼ņŗż ļ░ĢņČ£ļźĀ(right ventricular ejection fraction, RVEF)ņØĆ ļČĆĒĢś ņāüĒā£ņŚÉ ļ¦żņÜ░ ņØśņĪ┤ņĀüņØ┤ņ¦Ćļ¦ī, Ļ░Ćņן ļ¦ÄņØ┤ ņé¼ņÜ®ļÉśļŖö ņÜ░ņŗ¼ņŗż ĻĖ░ļŖź ņ¦ĆĒæ£ņØ┤ļŗż. ņØ┤ļ®┤ņä▒ ņŗ¼ņ┤łņØīĒīī Ļ▓Ćņé¼ļĪ£ ĒÅēĻ░ĆĒĢ£ RVEFļŖö ĻČīĒĢśņ¦Ć ņĢŖņ£╝ļ®░ Ļ▓ĮĒŚśņØ┤ ļ¦ÄĻ│Ā ņĀüņĀłĒĢśĻ▓ī ņןļ╣äļź╝ Ļ░¢ņČś ņä╝Ēä░ņŚÉņä£ļŖö ņāüļŗ╣Ē׳ ņĀĢĒÖĢĒĢ£ 3ņ░©ņøÉ ņÜ░ņŗ¼ņŗż ņÜ®ņĀüĻ│╝ ļ░ĢņČ£ļźĀņØä ņĖĪņĀĢĒĢśĻ│Ā ņ׳ļŗż. Ļ░Ćņן ĒØöĒ׳ ņé¼ņÜ®ļÉśļŖö ņÜ░ņŗ¼ļČĆņĀäņØś ņŗ¼ņ┤łņØīĒīīņĀü ĒŖ╣ņ¦ĢļōżņØä Ēæ£ņŚÉ ĻĖ░ņłĀĒĢśņśĆļŗż(Table 4) [22,24,25].
ņÜ░ņŗ¼ņŗż ĻĖ░ļŖźņØś ļīĆļČĆļČäņØ┤ ņóģņČĢ ņłśņČĢņØä ĒåĄĒĢ┤ ņØ┤ļŻ©ņ¢┤ņ¦ĆĻĖ░ ļĢīļ¼ĖņŚÉ TAPSEĻ░Ć ņÜ░ņŗ¼ņŗż ĻĖ░ļŖź ĒÅēĻ░ĆņØś ļ¦żļĀźņĀüņØĖ Ēøäļ│┤ņ×ÉņØ┤ļŗż. TAPSEļŖö ĒÅÉļÅÖļ¦ź Ļ│ĀĒśłņĢĢĻ│╝ ņóīņŗ¼ļČĆņĀä ĒÖśņ×ÉļōżņØś ņŚ¼ļ¤¼ ņĮöĒśĖĒŖĖņŚÉņä£ ņ×äņāü Ļ▓░Ļ│╝ņÖĆ ņŚ░Ļ┤Ćņä▒ņØ┤ ņ׳ņØīņØä ļ│┤ņŚ¼ ņŻ╝ņŚłļŗż. ĻĘĖļ¤¼ļéś ļŗżļźĖ ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ļōżņØĆ TAPSEņØś ļ│ĆĒÖöĻ░Ć ņ¦łļ│æ Ļ▓ĮĻ│╝ņØś ļ»┐ņØä ļ¦īĒĢ£ Ēæ£ņŗ£ņ×ÉĻ░Ć ļÉśņ¦Ć ļ¬╗ĒĢśļ®░ ņäĀņ▓£ņä▒ ņŗ¼ņן ņ¦łĒÖśņØ┤ļéś ņŗ¼ņן ņłśņłĀ Ēøä ņĀäņ▓┤ ņÜ░ņŗ¼ņŗż ĻĖ░ļŖźņØä ļéśĒāĆļé┤ņ¦Ć ļ¬╗ĒĢ£ļŗżļŖö Ļ▓āņØä ņŗ£ņé¼ĒĢśņśĆļŗż. ņłśņłĀ ĒøäņŚÉ ņŗ¼ņŗżņżæĻ▓® ĻĖ░ļŖź ņĀĆĒĢśņÖĆ ņŗ¼ņןļ¦ē ņĀ£ņĢĮņØś ņåīņŗżļĪ£ ņØĖĒĢ┤ ņÜ░ņŗ¼ņŗżņØś ņóģņČĢ ņłśņČĢņØĆ ņĀĆĒĢśļÉśĻ│Ā ņÜ░ņŗ¼ņŗżņØĆ ņÖĖļ▓ĮņØś ĒÜĪņČĢ ņłśņČĢņŚÉ ļŹö ņØśņĪ┤ĒĢśĻ▓ī ļÉ£ļŗż. ņóģņČĢ ĻĖ░ļŖź Ļ░ÉņåīņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā, ĒŖ╣Ē׳ ĒøäļČĆĒĢśĻ░Ć ņ×æņØĆ Ļ▓ĮņÜ░ņŚÉ, RVFACņÖĆ RVEFļŖö ņ£Āņ¦ĆļÉĀ ņłś ņ׳ļŗż[26,27].
RVEFļŖö ĒÅēļ▓öĒĢ£ ņŗ¼ņ┤łņØīĒīī Ļ▓Ćņé¼ļĪ£ļŖö ĒĢ┤ņäØĒĢśĻĖ░ ņ¢┤ļĀĄņ¦Ćļ¦ī, RVFACņÖĆ TAPSEļŖö ĒÅÉĻ│ĀĒśłņĢĢ ĒÖśņ×ÉņØś ņĄ£ņŗĀ ņŚ░ĻĄ¼ņŚÉņä£ MRIļĪ£ ĻĄ¼ĒĢ£ RVEFņÖĆ ņóŗņØĆ ņāüĻ┤ĆĻ┤ĆĻ│äļź╝ ļ│┤ņŚ¼ ņŻ╝ņŚłļŗż[28]. ļ│ĆĒśĢ ņśüņāü(strain imaging)ņØĆ ņÜ░ņŗ¼ņŗż ĻĖ░ļŖź ĒÅēĻ░Ćļź╝ ņ£äĒĢ┤ņä£ ņé¼ņÜ®ņØ┤ ņ”ØĻ░ĆļÉśĻ│Ā ņ׳ļŗż. ļ│ĆĒśĢņØĆ ņÜ░ņŗ¼ņŗż ļČĆĒĢśņÖĆ ĻĖ░ļŖź ņןņĢĀņØś ļ│ĄĒĢ®ņĖĪņĀĢņØ┤ Ļ░ĆļŖźĒĢśĻ│Ā, ļ╣äņĀĢņāü ļ│ĆĒśĢ Ēī©Ēä┤ņØĆ ļ»ĖņäĖĒśłĻ┤Ć ĒŚłĒśłņØ┤ļéś ņÜ░ņŗ¼ņŗż ĒÖĢņןņŚÉ ņØśĒĢ£ ņŗ¼ĻĘ╝ Ēś╝ļ×Ć(myocardial disarray)ņ£╝ļĪ£ļČĆĒä░ ļ░£ņāØĒĢśĻ▓ī ļÉ£ļŗż. ņóīņŗ¼ņŗż ļ│┤ņĪ░ĻĖ░ĻĄ¼(left ventricular assist device) ņéĮņ×ģ ĒøäņŚÉ ņÜ░ņŗ¼ļČĆņĀäņØä ņśłņĖĪĒĢśĻĖ░ ņ£äĒĢ£ ņ£äĒŚśļÅä ĒÅēĻ░ĆļŖö ļ│┤ĒåĄ ņ×äņāü ņ¦ĆĒæ£ļōżņŚÉ ņ┤łņĀÉņØä ļ¦×ņČöņ¢┤ ņÖöņ¦Ćļ¦ī, ņĄ£ĻĘ╝ņŚÉļŖö ņŗ¼ņ┤łņØīĒīī Ļ▓Ćņé¼ļź╝ ņØ┤ņÜ®ĒĢ£ ļ│ĆĒśĢņØä ņĖĪņĀĢĒĢ┤ņä£ ĒÅēĻ░ĆĒĢśļĀżĻ│Ā ĒĢśĻ│Ā ņ׳ļŗż. ņÜ░ņŗ¼ņŗż ļ│ĆĒśĢ Ēī©Ēä┤ņØĆ ņ×äņāü ņ£äĒŚśļÅä ĒÅēĻ░ĆņŚÉ ņČöĻ░ĆņĀüņØĖ ļÅäņøĆņØä ņŻ╝ņŚłļŗż[29]. ņĢ×ņ£╝ļĪ£ļŖö ņÜ░ņŗ¼ļČĆņĀäņØś ņä▒Ē¢źņØ┤ ņ׳ļŖö ņ£äĒŚś ņØĖņ×Éļéś ņ¦łĒÖśņØ┤ ņ׳ļŖö ĒÖśņ×ÉņŚÉņä£ ņÜ░ņŗ¼ņŗż ļ│ĆĒśĢņØś ņØ╝ņāüņĀü ĒÅēĻ░ĆĻ░Ć ņŗ¼ņ┤łņØīĒīīņŗżņŚÉņä£ ļ░£ņĀäĒĢ┤ņĢ╝ ĒĢĀ ĒĢäņłśņĀüņØĖ ņłĀĻĖ░Ļ░Ć ļÉĀ Ļ▓āņØ┤ļŗż.
ņŗ¼ņן MRI
ņŗ¼ņן MRIļŖö ņÜ░ņŗ¼ņŗż ĻĖ░ļŖźņØś ļ╣äņ╣©ņŖĄņĀü ĒÅēĻ░ĆņØś ņĄ£ņĀüĒæ£ņżĆņØ┤ ļÉśņŚłĻ│Ā ņÜ░ņŗ¼ņŗż ņ¦łļ¤ē, ņÜ®ņĀü ļ░Å ļ░ĢņČ£ļźĀņØä ņĖĪņĀĢĒĢśļŖöļŹ░ Ļ░Ćņן ņĀĢĒÖĢĒĢ£ ļ░®ļ▓ĢņØ┤ļŗż. 3ņ░©ņøÉņ£╝ļĪ£ ņ×¼ņĪ░ĒĢ®ĒĢ£ ņŗ¼ņŗż ĻĄ¼ņĪ░ ļ░Å ņÜ®ņĀü ĒÅēĻ░ĆĻ░Ć Ļ░ĆļŖźĒĢśĻ│Ā, ņÜ░ņŗ¼ņŗż ĻĖ░ļŖź, ĒīÉļ¦ēņØś ĒÅÉņćäļČĆņĀäņØä ĒÅēĻ░ĆĒĢĀ ņłś ņ׳Ļ│Ā ņ×ÉĻĖ░Ļ│Ąļ¬ģ ĒśłĻ┤ĆņĪ░ņśüņłĀņØä Ļ░ĆļŖźĒĢśĻ▓ī ĒĢ£ļŗż. ĻĘĖļ¤░ļŹ░, ņł©ņØä ņ░ĖņĢäņĢ╝ ĒĢśĻ│Ā, ņŗ¼ņן ļ”¼ļō¼ņØ┤ ĻĘ£ņ╣ÖņĀüņØ┤ņ¢┤ņĢ╝ ĒĢśĻ│Ā, ĻĖłņåŹņ£╝ļĪ£ ļ¦īļōĀ ņןņ╣śļź╝ ņØ┤ņŗØĒĢ£ ĒÖśņ×ÉņŚÉĻ▓īļŖö ņé¼ņÜ®ĒĢĀ ņłś ņŚåĻ│Ā, ļ¦ÄņØĆ ļ╣äņÜ®ņØ┤ ļō£ļŖö ļŗ©ņĀÉņØ┤ ņ׳ļŗż. ĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ļŖö MRIļĪ£ ņĖĪņĀĢĒĢ£ RVEFņØś ļ│ĆĒÖöĻ░Ć ĒÅÉļÅÖļ¦ź Ļ│ĀĒśłņĢĢ ņ╣śļŻīļź╝ ļ░øļŖö ĒÖśņ×ÉļōżņØś ņ×äņāü Ļ▓░Ļ│╝ļź╝ Ļ░Ćņן ņל ņśłņĖĪĒĢśļŖö ļ│ĆņłśļØ╝Ļ│Ā ĒĢśņśĆļŗż[30].
ņŗ¼ņן ņ╗┤Ēō©Ēä░ļŗ©ņĖĄņ┤¼ņśü(computed tomography, CT)
ņŗ¼ņן CTļŖö ĻĖłņåŹņ£╝ļĪ£ ļ¦īļōĀ ņןņ╣śļź╝ ņØ┤ņŗØĒĢ£ ĒÖśņ×ÉņŚÉĻ▓ī ņé¼ņÜ® Ļ░ĆļŖźĒĢśļéś, ņŗ¼ņן ļ░ĢļÅÖņłśĻ░Ć ļé«ņĢäņĢ╝ ĒĢ£ļŗżļŖö ļŗ©ņĀÉņØ┤ ņ׳ļŗż. ĻĘĖļĀćņ¦Ćļ¦ī ļ╣äņ╣©ņŖĄņĀü Ļ▓Ćņé¼ļĪ£ ņēĮĻ│Ā ņŗĀņåŹĒĢśĻ▓ī ņ┤¼ņśüĒĢĀ ņłś ņ׳ņ£╝ļ®░, 3ņ░©ņøÉ ņśüņāüĒÖöĒĢśņŚ¼ ņÜ®ņĀü ņĖĪņĀĢ ļ░Å ĻĖ░ļŖź ĒÅēĻ░ĆĻ░Ć Ļ░ĆļŖźĒĢśļŗż.
ņ╣©ņŖĄņĀü ĒśłļźśņŚŁĒĢÖņĀü ĒÅēĻ░Ć
ņ╣©ņŖĄņĀü ĒśłņŚŁĒĢÖņĀü ĒÅēĻ░ĆļŖö ņäżļ¬ģļÉśņ¦Ć ņĢŖļŖö Ļ▓ĮņÜ░ļéś ņ╣śļŻīņŚÉ ņĀĆĒĢŁĒĢśļŖö ņÜ░ņŗ¼ļČĆņĀäņØś Ļ▓ĮņÜ░ ĻČīĻ│ĀļÉ£ļŗż. ņóīņÜ░ ņŗ¼ļ░®ņĢĢ, ņŗ¼ņןļ░ĢņČ£ļ¤ē, ĒÅÉĒśłĻ┤ĆņĀĆĒĢŁņŚÉ ļīĆĒĢ£ ņĀĢĒÖĢĒĢ£ ņĀĢļ│┤ļź╝ ņĀ£Ļ│ĄĒĢ£ļŗż. ņØ╝ļ░śņĀüņ£╝ļĪ£ ņ╣©ņŖĄņĀü ļ¬©ļŗłĒä░ļ¦üņØĆ Ļ░ĆļŖźĒĢ£ ņ¦¦ņØĆ ĻĖ░Ļ░ä ļÅÖņĢł ņé¼ņÜ®ĒĢ┤ņĢ╝ ĒĢśļŖöļŹ░, ņÜ░ņŗ¼ ļÅäĻ┤ĆņéĮņ×ģņŚÉ ņØśĒĢ┤ ņ¢╗ņØĆ ĒśłņŚŁĒĢÖņĀü ņ¦ĆĒæ£ļōżņØĆ ņÜ░ņŗ¼ ĻĖ░ļŖź ĒÅēĻ░ĆņŚÉ ļÅäņøĆņØ┤ ļÉ£ļŗż. ņāüņŖ╣ļÉ£ ņÜ░ņŗ¼ļ░®ņĢĢĻ│╝ ļé«ņØĆ ņŗ¼ņןļ░ĢņČ£ņ¦ĆņłśļŖö ĒÅÉļÅÖļ¦ź Ļ│ĀĒśłņĢĢ ņĮöĒśĖĒŖĖņŚÉņä£ ļŹö ļéśņü£ ņāØņĪ┤Ļ│╝ ņŚ░Ļ┤ĆņØ┤ ņ׳ņŚłļŗż[31]. ĒÅÉĒśłĻ┤ĆņĀĆĒĢŁņØś ņ”ØĻ░Ć(> 3 ņÜ░ļō£ ļŗ©ņ£ä)ļŖö ņóīņĖĪ ņŗ¼ņן ņ¦łĒÖśĻ│╝ ĒÅÉļÅÖļ¦ź Ļ│ĀĒśłņĢĢņŚÉņä£ ļČłļ¤ēĒĢ£ ņśłĒøäņÖĆ ņāüĻ┤ĆņØ┤ ņ׳ļŗż. ņØ╝ĒÜīļ░ĢņČ£ļ¤ēņØä ĒÅÉļ¦źņĢĢņ£╝ļĪ£ ļéśļłäņ¢┤ņä£(stroke volume/pulmonary pulse pressure) ĻĄ¼ĒĢ£ ĒÅÉĒśłĻ┤Ć ņł£ņØæļÅä(compliance)Ļ░Ć ņóīņŗ¼ļČĆņĀäĻ│╝ ĒÅÉļÅÖļ¦ź Ļ│ĀĒśłņĢĢņØś ņśłĒøä ņØĖņ×ÉļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[32,33]. ĻĘĖļ¤¼ļéś, ĒÅÉĒśłĻ┤Ć ņĀĆĒĢŁĻ│╝ ņł£ņØæļÅäļŖö ļ¬©ļæÉ ĒøäļČĆĒĢśņØś ņĖĪņĀĢņØ┤Ļ│Ā ņÜ░ņŗ¼ņŗż ĻĖ░ļŖźņØä ņ¦üņĀæ ļ░śņśüĒĢśņ¦ĆļŖö ņĢŖļŖöļŗż.
ņÜ░ņŗ¼ņŗż-ĒÅÉļÅÖļ¦ź Ļ▓░ĒĢ®(coupling)ņØś ņĖĪņĀĢ
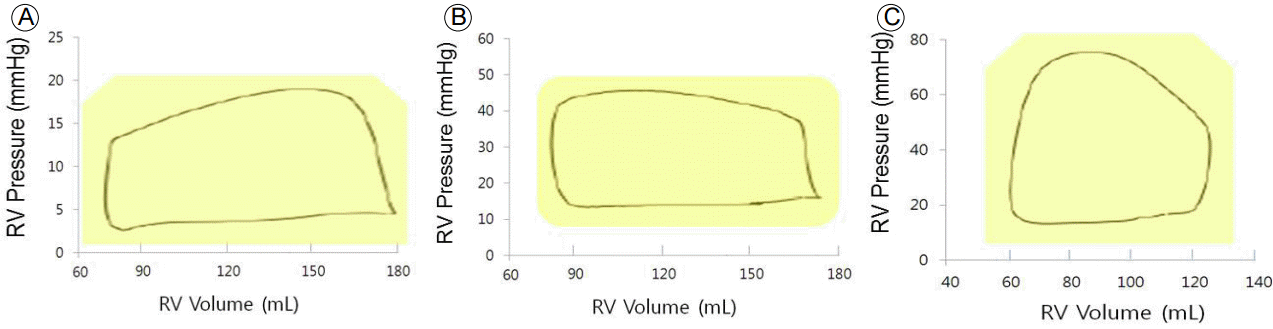
ņŗ¼ņŗż ĻĖ░ļŖźĻ│╝ ĒøäļČĆĒĢśņØś ĒÜ©Ļ│╝ļź╝ ĒÅēĻ░ĆĒĢśļŖö ņĄ£ņĀüĒæ£ņżĆņØĆ ņŗ¼ņŗż ņĢĢļĀźĻ│╝ ņÜ®ņĀüņØś Ļ┤ĆĻ│äļź╝ ĒåĄĒĢ┤ņä£ ņØ┤ļŻ©ņ¢┤ņ¦äļŗż. ņØ┤ļ¤¼ĒĢ£ ļČäņäØņØĆ ņóīņŗ¼ņŗżņŚÉņä£ ļ¦ÄņØ┤ ņØ┤ļŻ©ņ¢┤ņĪīņ¦Ćļ¦ī Ļ░ÖņØĆ ņøÉņ╣ÖņØ┤ ņÜ░ņŗ¼ņŗżņŚÉļÅä ĒĢ┤ļŗ╣ļÉ£ļŗż[34]. ļŗżņ¢æĒĢ£ ņĀäļČĆĒĢś ļśÉļŖö ĒøäļČĆĒĢśņŚÉ ņØśĒĢ┤ ņØ╝ļĀ©ņØś ņĢĢļĀź-ņÜ®ņĀü Ļ│Āļ”¼(pressure-volume loop)Ļ░Ć ņāØņä▒ļÉśĻ│Ā, Ļ░ü Ļ│Āļ”¼ņØś ņÜ®ņĀüņŚÉ ļīĆĒĢ£ ņĢĢļĀźņØś ņĄ£ļīĆ ļ╣äņ£©ņØ┤ Ļ▓░ņĀĢļÉ£ļŗż. ņĀĢņāü ņÜ░ņŗ¼ņŗż ņĢĢļĀź-ņÜ®ņĀü Ļ│Āļ”¼ļŖö, ĒśłĻ┤ĆĻ│äņØś ļé«ņØĆ ņĀĆĒĢŁņØä ļéśĒāĆļé┤ņä£, ļ░ĢņČ£ ĻĖ░Ļ░ä ļé┤ļé┤ ņĢĢļĀźņØ┤ Ļ░ÉņåīĒĢśļŖö ņé╝Ļ░üĒśĢ ļ¬©ņ¢æņØ┤ļŗż(Fig. 2A). ļö░ļØ╝ņä£ ņĢĢļĀźĻ│╝ ņÜ®ņĀüņØś ņĄ£ļīĆ ļ╣äņ£©ņØĆ ņłśņČĢĻĖ░ļ¦É ĻĘ╝ņ▓śņŚÉņä£ ļéśĒāĆļéśņ¦Ć ņĢŖĻ│Ā ņĢĢļĀź-ņÜ®ņĀü ĒÅēĻ░Ćļź╝ ņ¢┤ļĀĄĻ▓ī ĒĢ£ļŗż. ĻĘĖļ¤¼ļéś Ļ▓ĮļÅäņØś ĒÅÉĻ│ĀĒśłņĢĢņŚÉņä£ļŖö ņÜ░ņŗ¼ņŗżņØś ņĢĢļĀź-ņÜ®ņĀü Ļ│Āļ”¼ņØś ļ¬©ņ¢æņØ┤ ņóīņŗ¼ņŗżņ▓śļ¤╝ ļ│┤ļŗż ņ¦üĻ░üĒśĢ ļ¬©ņ¢æņ£╝ļĪ£ ļ│ĆĒĢśĻ▒░ļéś(Fig. 2B), ļŹö ņŗ¼ĒĢ£ ĒÅÉĻ│ĀĒśłņĢĢņŚÉņä£ļŖö ņé¼ļŗżļ”¼Ļ╝┤ ļ¬©ņ¢æņ£╝ļĪ£(Fig. 2C) ļ░öļĆīņ¢┤ņä£ ļ░ĢņČ£ ĻĖ░Ļ░ä ļé┤ļé┤ ņ¦ĆņåŹņĀüņ£╝ļĪ£ ņĢĢļĀźņØ┤ ņāüņŖ╣ĒĢśĻ▓ī ļÉ£ļŗż[35]. ļéśņżæņØś ļæÉ Ļ▓ĮņÜ░ņŚÉļŖö ņĢĢļĀźĻ│╝ ņÜ®ņĀüņØś ņĄ£ļīĆ ļ╣äņ£©ņØĆ ņóīņŗ¼ņŗżņ▓śļ¤╝ ņłśņČĢĻĖ░ļ¦É ĻĘ╝ņ▓śņŚÉņä£ ļéśĒāĆļéśņä£, ņłśņČĢĻĖ░ļ¦É ņĢĢļĀź-ņÜ®ņĀü Ļ┤ĆĻ│ä(end-systolic pressure-volume relationship)ļŖö Ļ░üĻ░üņØś ņĢĢļĀź-ņÜ®ņĀü Ļ│Āļ”¼ņØś ņłśņČĢĻĖ░ļ¦É ņĢĢļĀź(end-systolic pressure)ņĀÉņØä ņŚ░Ļ▓░ĒĢśņŚ¼ Ļ▓░ņĀĢļÉśļŖöļŹ░, ĻĘĖ ĻĖ░ņÜĖĻĖ░ļŖö ļ╣äĻĄÉņĀü ļČĆĒĢśņŚÉ ļÅģļ”ĮņĀüņØĖ ņłśņČĢļĀź ņĖĪņĀĢļ▓ĢņØĖ ņłśņČĢĻĖ░ļ¦É Ēāäņä▒ļÅä(endsystolic elastance)ņØ┤ļŗż. ĻĘĖņŚÉ ļ╣äĒĢ┤ TAPSE, RVFAC ļ░Å RVEFļŖö ļ¬©ļæÉ ļČĆĒĢśņŚÉ ņØśņĪ┤ņĀüņØ┤Ļ│Ā ņÜ░ņŗ¼ņŗż Ļ│Āņ£ĀņØś ņłśņČĢļĀźņØä ņ¦üņĀæņĀüņ£╝ļĪ£ ņĖĪņĀĢĒĢśņ¦Ć ņĢŖļŖöļŗż. ĻĘĖļ¤¼ļéś ņØ┤ļ¤¼ĒĢ£ ņ╣©ņŖĄņĀü ņĖĪņĀĢļ▓ĢņØĆ ĒŖ╣ņłś ņןļ╣äņÖĆ ņāüļŗ╣ĒĢ£ ņĀäļ¼ĖĻĖ░ņłĀņØ┤ ĒĢäņÜöĒĢ┤ņä£ ņØ╝ņāü ņ¦äļŗ©ņÜ®ņ£╝ļĪ£ļŖö ņŗżņÜ®ņĀüņØ┤ņ¦Ć ņĢŖļŗż.
Ļ▓░ ļĪĀ
ņÜ░ņŗ¼ļČĆņĀäņØĆ ņÜ░ņŗ¼ņŗż ņČ®ļ¦ī ņןņĢĀņÖĆ ļ░ĢņČ£ļ¤ē Ļ░ÉņåīļĪ£ ņØĖĒĢ┤ ņĀĢļ¦źĻ│äņØś ņÜĖĒśłņØ┤ ņāØĻĖ░ļŖö ņ×äņāüņ”ØĒøäĻĄ░ņØ┤ļŗż. ļö░ļØ╝ņä£ ņ▓┤ņĢĪ ņĀĆļźśņŚÉ ņØśĒĢ£ ļ¦Éņ┤ł ļČĆņóģ, ļ│Ąņłś ļ░Å ņĀäņŗĀ ļČĆņóģņØ┤ ļéśĒāĆļéĀ ņłś ņ׳Ļ│Ā Ļ░ÉņåīļÉ£ ņłśņČĢĻĖ░ ņśłļ╣äļĀź ļśÉļŖö ņĀüņØĆ ņŗ¼ņןļ░ĢņČ£ļ¤ēņ£╝ļĪ£ ņØĖĒĢ┤ ņÜ┤ļÅÖ ļČłļé┤ņä▒Ļ│╝ Ēö╝ļĪ£ļź╝ ņ£Āļ░£ĒĢĀ ņłś ņ׳ņ£╝ļ®░, ņÜ░ņŗ¼ļ░® ļśÉļŖö ņÜ░ņŗ¼ņŗżņØś ĒÖĢņןņ£╝ļĪ£ ņØĖĒĢ┤ ļČĆņĀĢļ¦źņØä ņ£Āļ░£ĒĢĀ ņłś ņ׳ļŗż. ņÜ░ņŗ¼ļČĆņĀäņØś ņ¦äļŗ©ņŚÉļŖö ļ│æļĀź ņ▓ŁņĘ©ņÖĆ ņŗĀņ▓┤ Ļ▓Ćņé¼Ļ░Ć ņżæņÜöĒĢśĻ│Ā ņĀĢļ¤ēņĀü ĒÅēĻ░Ćļź╝ ņ£äĒĢ┤ ļ╣äņ╣©ņŖĄņĀü ļ░®ļ▓ĢņØĖ ņŗ¼ņ┤łņØīĒīī Ļ▓Ćņé¼ņÖĆ ņŗ¼ņן MRI Ļ▓Ćņé¼ļź╝ ļ¦ÄņØ┤ ņé¼ņÜ®ĒĢśĻ│Ā ņ׳ņ£╝ļ®░, ņØ┤ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņÜ░ņŗ¼ņŗż ĻĄ¼ņĪ░, ņÜ®ņĀü, ņ¦łļ¤ē ļ░Å ņłśņČĢ ĻĖ░ļŖźņØä ĒÅēĻ░ĆĒĢ£ļŗż. ļśÉĒĢ£ ņøÉņØĖ ņ¦łĒÖś, ņĢģĒÖö ņÜöņØĖ, ņÜ░ņŗ¼ļČĆņĀäņØś ņŗ¼ĒĢ£ ņĀĢļÅä ļ░Å ņŗ¼ņן ĻĖ░ļŖźņØä ĒÅēĻ░ĆĒĢśļŖö Ļ▓āļÅä ņÜ░ņŗ¼ļČĆņĀäņØś ņ¦äļŗ©ņŚÉ ņżæņÜöĒĢśļŗż.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






