ņä£ ļĪĀ
ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢö(salivary duct carcinoma)ņØĆ ņĀäņ▓┤ ĒāĆņĢĪņäĀņĢöņØś 10% ļ»Ėļ¦īņØä ņ░©ņ¦ĆĒĢśļŖö ļō£ļ¼Ė ņóģņ¢æņØ┤ļŗż[1]. ņłśņłĀ Ļ░ĆļŖźĒĢ£ Ļ▓ĮņÜ░ ņłśņłĀņĀü ņĀłņĀ£, ņłśņłĀņØ┤ ņ¢┤ļĀżņÜ┤ ĻĄŁņåīņ¦äĒ¢ēņä▒ņØś Ļ▓ĮņÜ░ļŖö ļÅÖņŗ£ ĒÖöĒĢÖļ░®ņé¼ņäĀ ņ╣śļŻīĻ░Ć ĻČīĻ│ĀļÉ£ļŗż[2]. ĻĘĖļ¤¼ļéś ņØ┤ļ¤¼ĒĢ£ ņ╣śļŻīņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ņøÉĻ▓®ņĀäņØ┤ ļ░£ņāØņ£╝ļĪ£ ņśłĒøäļŖö ļČłļ¤ēĒĢśļŗż[1]. ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņØĆ ļŗżļźĖ ļæÉĻ▓ĮļČĆņĢöņŚÉņä£ ĒØöĒ׳ ļ░£Ļ▓¼ļÉśļŖö ĒÄĖĒÅēņäĖĒżņĢöņóģĻ│╝ļŖö ņĪ░ņ¦üĒĢÖņĀü, ņ×äņāüņĀüņ£╝ļĪ£ ļŗżļźĖ ĒŖ╣ņä▒ņØä Ļ░Ćņ¦ĆļŖöļŹ░ ĒśĢĒā£ĒĢÖņĀüņ£╝ļĪ£ ņ£Āļ░®ņØś ņ╣©ņŖĄņä▒ Ļ┤ĆņĢöņ▓śļ¤╝ Ļ┤Ć, Ļ│Ąļ¦ēņ▓┤ ĻĄ¼ņĪ░ ļ░Å ļæźņ¦ĆņäĖĒżļĪ£ ņØ┤ļŻ©ņ¢┤ņĀĖ ņ׳ņ£╝ļ®░ ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ļź╝ ļ░£ĒśäĒĢ£ļŗż[3]. ņŚÉņŖżĒŖĖļĪ£ņĀĀ ņłśņÜ®ņ▓┤ļéś ĒöäļĪ£Ļ▓īņŖżĒģīļĪĀ ņłśņÜ®ņ▓┤ļź╝ ņל ļ░£ĒśäĒĢśņ¦Ć ņĢŖļŖö ļ░śļ®┤ ļé©ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤(androgen receptor)ļŖö ĒØöĒĢśĻ▓ī ļ░£ĒśäĒĢśļ®░ ĒśĖļź┤ļ¬¼ ņ╣śļŻīņŚÉ ļ░śņØæĒĢśļŖö Ļ▓āņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ļŗż[4]. ņĀĆņ×ÉļōżņØĆ ņłśņłĀĻ│╝ ņłśņłĀ Ēøä ļÅÖņŗ£ ĒÖöĒĢÖļ░®ņé¼ņäĀ ņ╣śļŻī ļ░Å ņČöĻ░ĆņĀü ĒĢŁņĢöĒÖöĒĢÖ ņ╣śļŻī ņŗ£Ē¢ē Ēøä ņ×¼ļ░£ĒĢ£ ļé©ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ ņ¢æņä▒ ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņŚÉņä£ ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻī(androgen deprivation therapy)ņŚÉ ņóŗņØĆ ļ░śņØæņØä ļ│┤ņØĖ ņ”ØļĪĆļź╝ ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļŗż.
ņ”Ø ļĪĆ
ĒÖś ņ×É: 69ņäĖ ļé©ņ×É
ņŻ╝ ņåī: ņÜ░ņĖĪ Ļ▓ĮļČĆ ņóģļ¼╝
Ēśäļ│æļĀź: ļé┤ņøÉ 6Ļ░£ņøö ņĀäļČĆĒä░ ņÜ░ņĖĪ Ļ▓ĮļČĆņŚÉ ņóģļ¼╝ņØ┤ ņ┤ēņ¦ĆļÉśņŚłņ£╝ļ®░, ļé┤ņøÉ 1Ļ░£ņøö ņĀäļČĆĒä░ ņĀÉņ░© Ēü¼ĻĖ░Ļ░Ć ņ”ØĻ░ĆĒĢśņŚ¼ ļé┤ņøÉĒĢśņśĆļŗż.
Ļ│╝Ļ▒░ļĀź: ĒŖ╣ņØ┤ņé¼ĒĢŁņØĆ ņŚåņŚłļŗż.
ņØ┤ĒĢÖņĀü ņåīĻ▓¼: ļé┤ņøÉ ļŗ╣ņŗ£ ĒśłņĢĢ 100/60 mmHg, ļ¦źļ░Ģ 68ĒÜī/ļČä, ĒśĖĒØĪņłś 20ĒÜī/ļČä, ņ▓┤ņś© 36.7ŌäāņśĆļŗż. ĻĖēņä▒ ļ│æņāēņØä ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśņ£╝ļ®░ ņØśņŗØņØĆ ļ¬ģļŻīĒĢśņśĆĻ│Ā, ļæÉĻ▓ĮļČĆņ¦äņ░░ņŚÉņä£ ņÜ░ņĖĪ ņØ┤ĒĢśņäĀĻ│╝ ļÅÖņĖĪ ņćäĻ│©ĒĢśņŚÉ 6 cm Ēü¼ĻĖ░ņØś ļ¼┤ĒåĄņä▒, ņ£ĀņŚ░ĒĢ£ ņóģĻ┤┤Ļ░Ć ņ┤ēņ¦äļÉśņŚłļŗż. ĒØēļČĆ ņ¦äņ░░ņŚÉņä£ ņŗ¼ņØī ļ░Å ĒśĖĒØĪņØīņØś ņØ┤ņāüņåīĻ▓¼ņØĆ ņŚåņŚłĻ│Ā, ļ│ĄļČĆ ņ¦äņ░░ņŚÉņä£ ņĢĢĒåĄ, ņןĻĖ░ ļ╣äļīĆ ļ░Å ņóģļ¼╝ņØĆ ņ┤ēņ¦ĆļÉśņ¦Ć ņĢŖņĢśļŗż.
Ļ▓Ćņé¼ņŗż ņåīĻ▓¼: ĒŖ╣ņØ┤ņé¼ĒĢŁņØĆ ņŚåņŚłļŗż.
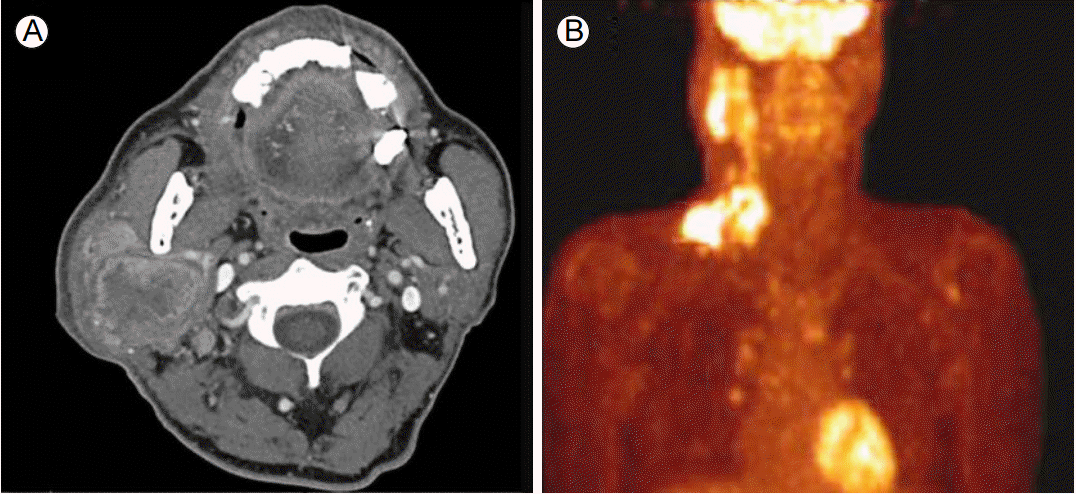
ļ░®ņé¼ņäĀ ņåīĻ▓¼: Ļ▓ĮļČĆ ņĀäņé░ĒÖöļŗ©ņĖĄņ┤¼ņśüņŚÉņä£ ļæÉĻ░£ņĀĆļź╝ ņ╣©ļ▓öĒĢśņ¦Ć ņĢŖļŖö 6 cm Ēü¼ĻĖ░ņØś ņØ┤ĒĢśņäĀ ņóģņ¢æĻ│╝ ņ¢æņĖĪ Ļ▓ĮļČĆņŚÉ ļŗżļ░£ņä▒ņØś ņóģļīĆļÉ£ ļ”╝ĒöäņĀłņØ┤ Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 1A).
ĒĢĄņØśĒĢÖĻ▓Ćņé¼ ņåīĻ▓¼: ņ¢æņĀäņ×Éļ░®ņČ£ļŗ©ņĖĄņ┤¼ņśü Ļ▓Ćņé¼(fludeoxyglucose-positron emission tomography/computed tomography)ņŚÉņä£ ņÜ░ņĖĪ ņØ┤ĒĢśņäĀĻ│╝ ļÅÖņĖĪ ņćäĻ│©ĒĢś ņśüņŚŁņŚÉ Ļ░ĢĒĢ£ 18F-fluro-deoxyglucose ņäŁņĘ©ņ£©ņØä ļ│┤ņØ┤ļŖö Ļ│╝ļīĆņé¼ ņóģĻ┤┤Ļ░Ć Ļ┤Ćņ░░ļÉśņŚłņ£╝ļ®░ ņøÉĻ▓®ņĀäņØ┤ļŖö Ļ┤Ćņ░░ļÉśņ¦Ć ņĢŖņĢśļŗż(Fig. 1B).
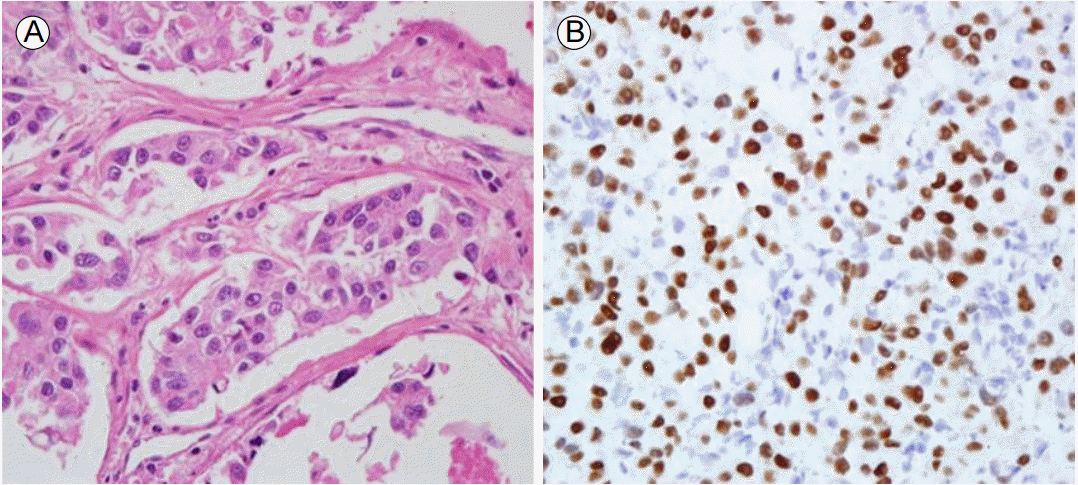
ļ│æļ”¼ ņåīĻ▓¼: ņÜ░ņĖĪ ņØ┤ĒĢśņäĀ ņóģĻ┤┤ņØś Ļ▓ĮĒö╝ņĀü ļ░öļŖś ņāØĻ▓ĆņØä ĒåĄĒĢ£ Ēśäļ»ĖĻ▓ĮņĀü ņĪ░ņ¦ü ņåīĻ▓¼ņŚÉņä£ļŖö Ļ┤ĆĻ│╝ ļæźņ¦Ćļź╝ ĒśĢņä▒ĒĢśļŖö ņ×ģļ░®ņäĖĒżņÖĆ ļŗżĻ░üņäĖĒżļōżņØ┤ Ļ┤Ćņ░░ļÉśļŖö ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņ£╝ļĪ£ ņ¦äļŗ©ļÉśņŚłļŗż(Fig. 2A). ņłśņłĀ Ēøä ņĪ░ņ¦ü ņåīĻ▓¼ņ£╝ļĪ£ ņóģņ¢æņØĆ ņŗĀĻ▓Į ņŻ╝ņ£ä ņ╣©ļ▓öĻ│╝ ĒśłĻ┤ĆĻ│╝ ļ”╝ĒöäĻ┤Ć ņ╣©ļ▓öņØä ļÅÖļ░śĒĢśņśĆĻ│Ā ļ░Ģļ”¼ļÉ£ 122Ļ░£ņØś ļ”╝ĒöäņĀł ņżæ 103Ļ░£ņŚÉņä£ ņĢöņäĖĒżĻ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż. ļśÉĒĢ£ ļ”╝ĒöäņĀłņØś ļīĆļČĆļČäņŚÉņä£ Ēö╝ļ¦ēņÖĖ ņ╣©ļ▓öņØä ļ│┤ņśĆĻ│Ā ņóģņ¢æĻ│╝ ļ”╝ĒöäņĀł ņĪ░ņ¦üņØś ļ®┤ņŚŁĒÖöĒĢÖņĀü ņŚ╝ņāēņŚÉņä£ļŖö ļé©ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ ņ¢æņä▒ļ░śņØæņØ┤ ĒÖĢņØĖļÉśņŚłļŗż(Fig. 2B).
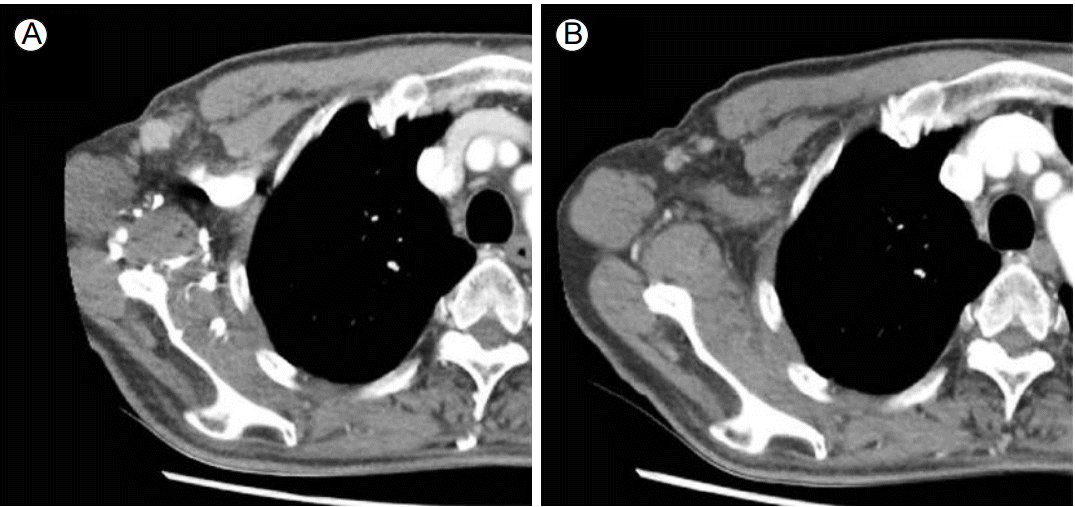
ņ╣śļŻī ļ░Å ņ×äņāüĻ▓ĮĻ│╝: ĒÖśņ×ÉļŖö ņ¢æņĖĪņä▒ Ļ▓ĮļČĆ ņ▓ŁņåīņłĀĻ│╝ ņØ┤ĒĢśņäĀ ņĀäņĀłņĀ£ņłĀņØä ļ░øņĢśļŗż. ņóģņ¢æ ņŻ╝ņ£ä ĒśłĻ┤ĆĻ│╝ ņŗĀĻ▓ĮņØä ņ╣©ļ▓öĒĢśņśĆņ£╝ļ®░ Ļ┤æļ▓öņ£äĒĢ£ ļ”╝ĒöäņĀłņĀäņØ┤Ļ░Ć ņ׳ņŚłņ£╝ļ»ĆļĪ£ ņłśņłĀ Ēøä ņ╣śļŻīļĪ£ ļÅÖņŗ£ ĒÖöĒĢÖļ░®ņé¼ņäĀ ņ╣śļŻī(cisplatin 35 mg/m2, ļ¦ż 1ņŻ╝ļ¦łļŗż, ņ┤Ø 66 Gy)ļź╝ ļ░øņĢśļŗż. ļśÉĒĢ£ ņČöĻ░ĆņĀüņ£╝ļĪ£ 2ņŻ╝ĻĖ░ņØś ĒĢŁņĢöĒÖöĒĢÖ ņ╣śļŻī(cisplatin 60 mg/m2, ļ¦ż 1ņŻ╝ļ¦łļŗż, 5-fluorouracil 750 mg/m2, ļ¦ż 4ņŻ╝ļ¦łļŗż)ļź╝ ļ░øņĢśļŗż. 2ļ▓łņ¦Ė ĒĢŁņĢöĒÖöĒĢÖ ņ╣śļŻī Ēøä ņŗ£Ē¢ēĒĢ£ Ļ▓ĮļČĆ ļŗ©ņĖĄĒÖöņ┤¼ņśüņŚÉņä£ļŖö ņłśņłĀļČĆņ£äņØś ņ×¼ļ░£ ņåīĻ▓¼ņØĆ ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśņ£╝ļéś ĒØēļČĆ ļŗ©ņĖĄĒÖöņ┤¼ņśüņāü ņØ┤ņĀäņŚÉ ļ│┤ņØ┤ņ¦Ć ņĢŖļŹś ļŗ©Ļ▓Į 1.5 cm Ēü¼ĻĖ░ņØś ļ”╝ĒöäņĀłļōżņØ┤ ņÜ░ņĖĪ ņĢĪņÖĆļČĆņŚÉ ņāłļĪŁĻ▓ī ļ░£Ļ▓¼ļÉśņŚłļŗż(Fig. 3A). ņ×¼ļ░£ ņŚ¼ļČĆļź╝ ĒÖĢņØĖĒĢśĻĖ░ ņ£äĒĢ┤ ņÜ░ņĖĪ ņĢĪņÖĆļČĆ ļ”╝ĒöäņĀłņŚÉ Ļ▓ĮĒö╝ņĀü ļ░öļŖś ņāØĻ▓ĆņØä ņŗ£Ē¢ēĒĢśņśĆĻ│Ā ļ│æļ”¼ Ļ▓░Ļ│╝ņāü ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņØä ĒÖĢņØĖĒĢĀ ņłś ņ׳ņŚłņ£╝ļ®░ ļ®┤ņŚŁņĪ░ņ¦üĒÖöĒĢÖ ņŚ╝ņāēņŚÉņä£ļÅä ļé©ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ņŚÉ ņ¢æņä▒ņØä ļ│┤ņśĆļŗż. ņłśņłĀĻ│╝ ļÅÖņŗ£ņŚÉ ĒÖöĒĢÖļ░®ņé¼ņäĀ ņ╣śļŻī ļ░Å ĒĢŁņĢö ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒ¢łņØīņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā ņ”ēņŗ£ ņ×¼ļ░£ĒĢśņśĆĻĖ░ ļĢīļ¼ĖņŚÉ ļ¦żņÜ░ Ļ│ĄĻ▓®ņĀüņØĖ ņóģņ¢æņ£╝ļĪ£ ņāØĻ░üļÉśņŚłļŗż. ņØ┤ņŚÉ bicalutamide (50 mgņØä 1ņØ╝ 1ĒÜī Ļ▓ĮĻĄ¼ Ēł¼ņŚ¼ļ░øņØī)ņÖĆ leuprolide (3.75 mgņØä 1ļŗ¼ 1ĒÜī ĻĘ╝ņ£Ī Ēł¼ņŚ¼ļ░øņØī)ļź╝ ĻĖ░ļ░śņ£╝ļĪ£ ĒĢ£ ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīļź╝ ņŗ£ņ×æĒĢśņśĆņ£╝ļ®░ ņ╣śļŻī 2Ļ░£ņøö Ēøä ĒØēļČĆ ļŗ©ņĖĄĒÖöņ┤¼ņśüņāü ņÜ░ņĖĪ ņĢĪņÖĆļČĆņØś ļ”╝ĒöäņĀłņØĆ Ēü¼ĻĖ░Ļ░Ć Ļ░ÉņåīĒĢśņśĆļŗż. ņ╣śļŻī 5Ļ░£ņøö ĒøäņŚÉļÅä ņÜ░ņĖĪ ņĢĪņÖĆļČĆ ļ”╝ĒöäņĀłņØĆ Ļ░ÉņåīļÉ£ ņ▒äļĪ£ ņ£Āņ¦ĆļÉśĻ│Ā ņ׳ņŚłļŗż(Fig. 3B). ņ╣śļŻī ļÅäņżæ ĒÖśņ×ÉļŖö ņŗ¼ĒśłĻ┤ĆĻ│ä ņ”Øņāü ļ░Å ĒśłĻ┤ĆņÜ┤ļÅÖņ”Øņāü ļō▒ņØś ļČĆņ×æņÜ®ņØä ĒśĖņåīĒĢśņ¦Ć ņĢŖņĢśņ£╝ļ®░ Ēśäņ×¼Ļ╣īņ¦Ć ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīļź╝ ņ£Āņ¦ĆĒĢśĻ│Ā ņ׳ļŗż.
Ļ│Ā ņ░░
ĒāĆņĢĪņäĀņĢöņØĆ ļæÉĻ▓ĮļČĆņĢöņØś 5% ļ»Ėļ¦īņØä ņ░©ņ¦ĆĒĢśļŖö ļō£ļ¼Ė ņóģņ¢æņ£╝ļĪ£ņä£ ņŚ¼ļ¤¼ ņĪ░ņ¦üĒĢÖņĀü ņĢäĒśĢņØä Ļ░Ćņ¦äļŗż[2]. ĒŖ╣Ē׳ ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņØĆ ĻĘĖ ņżæņŚÉņä£ļÅä ņĀäņ▓┤ ĒāĆņĢĪņäĀņĢöņØś 10% ļ»Ėļ¦īņØä ņ░©ņ¦ĆĒĢśļŖö ļō£ļ¼Ė ņĢäĒśĢņØ┤ļ®░ ņ¦äļŗ© ļŗ╣ņŗ£ 56-58%ņŚÉņä£ ļ”╝ĒöäņĀłņØä ņ╣©ļ▓öĒĢśļ®░ Ļ▓ĮļČĆ ļ”╝ĒöäņĀłņĀäņØ┤Ļ░Ć ļ░£Ļ▓¼ļÉ£ļŗż[2,5]. ņżæņĢÖņāØņĪ┤ĻĖ░Ļ░äņØĆ ņĢĮ 3ļģäņ£╝ļĪ£ ļŗżļźĖ ĒāĆņĢĪņäĀņĢöņŚÉ ļ╣äĒĢ┤ ņāØņĪ┤ņ£©ņØ┤ ļé«ņØĆ ļ¦żņÜ░ Ļ│ĄĻ▓®ņĀüņØĖ ņóģņ¢æņØ┤ļŗż[2,6]. ļīĆļČĆļČäņØś ĒÖśņ×ÉļōżņØĆ Ļ│ĀļĀ╣ņ£╝ļĪ£ ļé©ļģĆ ļ╣äņ£©ņØĆ 4:1ņØ┤ļ®░ ņØ┤ĒĢśņäĀņŚÉņä£ ĒśĖļ░£ĒĢśĻ│Ā ņĢĮ 30%ņŚÉņä£ ņĢłļ®┤ņŗĀĻ▓ĮņØä ņ╣©ļ▓öĒĢ£ļŗż[1]. ļŗżļźĖ ļæÉĻ▓ĮļČĆņĢöĻ│╝ ļ¦łņ░¼Ļ░Ćņ¦ĆļĪ£ ņłśņłĀ Ļ░ĆļŖźĒĢ£ Ļ▓ĮņÜ░ Ļ▓ĮļČĆ ņ▓ŁņåīņłĀņØä ĒżĒĢ©ĒĢ£ ņłśņłĀņĀü ņĀłņĀ£, ņłśņłĀņØ┤ ņ¢┤ļĀżņÜ┤ ĻĄŁņåīņ¦äĒ¢ēņä▒ņØś Ļ▓ĮņÜ░ ļÅÖņŗ£ ĒÖöĒĢÖļ░®ņé¼ņäĀ ņ╣śļŻīĻ░Ć ĻČīĻ│ĀļÉ£ļŗż[2]. ņłśņłĀ ņØ┤ĒøäņŚÉļÅä ņ×¼ļ░£ Ļ░ĆļŖźņä▒ņØ┤ ļåÆĻĖ░ ļĢīļ¼ĖņŚÉ ļ░®ņé¼ņäĀ ļŗ©ļÅģ ņ╣śļŻīļéś ļÅÖņŗ£ ĒÖöĒĢÖļ░®ņé¼ņäĀ ņ╣śļŻīļź╝ ņČöĻ░ĆĒĢśļŖö Ļ▓āņØ┤ ņāØņĪ┤ĻĖ░Ļ░ä ņŚ░ņןņŚÉ ļÅäņøĆņØ┤ ļÉ£ļŗż[7]. ņłśņłĀ Ēøä ļ│┤ņĪ░ ņ╣śļŻīļĪ£ņä£ ĒĢŁņĢöĒÖöĒĢÖ ņ╣śļŻīņØś ĒÜ©Ļ│╝ļŖö ļ¬ģĒÖĢĒĢśņ¦Ć ņĢŖņ£╝ļ®░, ņøÉĻ▓®ņĀäņØ┤Ļ░Ć ņ׳ļŖö Ļ▓ĮņÜ░ļØ╝ļÅä ĒĢŁņĢöĒÖöĒĢÖ ņ╣śļŻīņØś ļ░śņØæņØĆ ņóŗņ¦Ć ņĢŖņØĆ ĒÄĖņØ┤ļŗż. ņŻ╝ļĪ£ platinum, anthracycline, taxaneņØä ĻĖ░ļ░śņ£╝ļĪ£ ĒĢ£ ĒĢŁņĢöĒÖöĒĢÖ ņ╣śļŻīĻ░Ć ņŗ£Ē¢ēļÉśļéś ļīĆļČĆļČä ņåīĻĘ£ļ¬© ņŚ░ĻĄ¼ Ļ▓░Ļ│╝ņØ┤ļ®░ ņ╣śļŻīņØś ļ░śņØæĻĖ░Ļ░äņØĆ ļīĆļץ 6-9Ļ░£ņøö ņĀĢļÅäņŚÉ ļČłĻ│╝ĒĢśļŗż[8].
ņĄ£ĻĘ╝ ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņØ┤ ņäĖĒżņØś ĒśĢĒā£ļ┐Éļ¦ī ņĢäļŗłļØ╝ ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ ļ░Å human epidermal growth factor 2 protein (HER2) ļ░£ĒśäĻ│╝ Ļ░ÖņØĆ ņłśņÜ®ņ▓┤ ļ░£Ēśä ņ¢æņāüņŚÉņä£ ņ£Āļ░®ņĢöĻ│╝ņØś ņ£Āņé¼ņä▒ņØä ļ░£Ļ▓¼ĒĢ┤ņÖöļŗż. ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņŚÉņä£ HER2ņØś ļ░£ĒśäņØĆ 20-66% ņĀĢļÅäļĪ£ ļ│┤Ļ│ĀļÉ£ļŗż[7]. ņ£Āļ░®ņØś ņ╣©ņŖĄņä▒ Ļ┤ĆņĢöņ▓śļ¤╝ ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņŚÉņä£ļÅä HER2 Ļ│╝ļ░£ĒśäņØ┤ ļČłļ¤ēĒĢ£ ņśłĒøäņÖĆ Ļ┤ĆļĀ©ņØ┤ ņ׳ņØīņØ┤ ļ░ØĒśĆņĪīĻ│Ā HER2 ņłśņÜ®ņ▓┤ļź╝ ļ░®ĒĢ┤ĒĢśļŖö ļŗ©Ēü┤ļĪĀĒĢŁņ▓┤ņØĖ trastzumabņØ┤ HER2 ņ¢æņä▒ņØĖ ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņŚÉņä£ ĒĢśļéśņØś ņ╣śļŻī ļ░®ļ▓Ģņ£╝ļĪ£ ņĀ£ņŗ£ļÉśĻ│Ā ņ׳ļŗż[4,5]. ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņŚÉņä£ ļ░£ĒśäļÉśļŖö ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ļŖö ņŻ╝ļĪ£ ļé©ņä▒ ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ļĪ£ ļīĆļץ 40-90%ļĪ£ ĒØöĒĢśĻ▓ī ļ░£ĒśäĒĢśļéś ņŚÉņŖżĒŖĖļĪ£Ļ▓É ņłśņÜ®ņ▓┤ņÖĆ ĒöäļĪ£Ļ▓īņŖżĒģīļĪĀ ņłśņÜ®ņ▓┤ļŖö ļō£ļ¼╝Ļ▓ī ļ░£ĒśäļÉśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż[4]. ņŚ¼ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ ņ¢æņä▒ ņ£Āļ░®ņĢöņŚÉņä£ņØś ĒĢŁĒśĖļź┤ļ¬¼ ņ╣śļŻī ļ░Å ļé©ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ļź╝ Ļ░Ćņ¦ĆļŖö ņĀäļ”ĮņäĀņĢöņØś ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīļŖö ņØ┤ļ»Ė ĒÖ£ļ░£Ē׳ ņé¼ņÜ®ļÉśĻ│Ā ņ׳ļŖö ĒÜ©Ļ│╝ņĀüņØĖ ņ╣śļŻīļ▓Ģņ£╝ļĪ£ņä£ ņØ┤ļź╝ ĻĖ░ļ░śņ£╝ļĪ£ ĒĢśņŚ¼ ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤Ļ░Ć ņ¢æņä▒ņØĖ ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņØś ņāłļĪ£ņÜ┤ ņ╣śļŻī ļ░®ļ▓Ģņ£╝ļĪ£ņä£ ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīņŚÉ ļīĆĒĢ£ ņŗ£ļÅäļōżņØ┤ ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳ļŗż[3,9,10].
Locati ļō▒[9]ņØĆ ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīļź╝ ļ░øņØĆ ļé©ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ ņ¢æņä▒ ĒāĆņĢĪņäĀņĢö ĒÖśņ×ÉņŚÉ ļīĆĒĢ£ ĒøäĒ¢źņĀü ļČäņäØņØä ļ│┤Ļ│ĀĒĢśņśĆļŗż. ĻĘĖņżæ 8ļ¬ģņØś ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢö ĒÖśņ×ÉņØś ņ╣śļŻīļ░śņØæļźĀņØĆ 50%ņśĆļŗż[9]. 2011ļģä Jaspers ļō▒[10]ņØĆ ĒÅēĻĘĀ 12Ļ░£ņøöņØś ņżæņĢÖĻĖ░Ļ░ä ļÅÖņĢł ņČöņĀüĻ┤Ćņ░░ĒĢ£ ļé©ņä▒ĒśĖļź┤ļ¬¼ ņ¢æņä▒ņØĖ 10ļ¬ģņØś ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢö ĒÖśņ×É ņżæ ļČĆļČäĻ┤ĆĒĢ┤ļź╝ ļ│┤ņØĖ 2ļ¬ģņØś ĒÖśņ×Éļź╝ ļ│┤Ļ│ĀĒĢ©ņ£╝ļĪ£ņŹ© ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīņØś ĒÜ©Ļ│╝ļź╝ ļ│┤ņŚ¼ņŻ╝ņŚłĻ│Ā ĒåĄņ”Ø ņÖäĒÖöņŚÉļÅä ĒÜ©Ļ│╝Ļ░Ć ņ׳ņØīņØä ļ│┤Ļ│ĀĒĢśņŚ¼ ņÖäĒÖö ņ╣śļŻīļĪ£ņä£ņØś ņŚŁĒĢĀļÅä ņĀ£ņŗ£ĒĢśņśĆļŗż. ļśÉĒĢ£ Soper ļō▒[2]ņØĆ ļé©ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ ņ¢æņä▒ņØĖ ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢö ĒÖśņ×ÉņŚÉņä£ ļ░®ņé¼ņäĀ ņ╣śļŻīņÖĆ ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīļź╝ ļ│æĒĢ®ĒĢśņŚ¼ 2ļģä ņØ┤ņāü ņÖäņĀäĻ┤ĆĒĢ┤ļź╝ ļ│┤ņØ┤Ļ│Ā ņ׳ļŖö ĒÖśņ×Éļź╝ ļ│┤Ļ│ĀĒĢ£ ļ░öļÅä ņ׳ļŗż. ĻĘĖļ¤¼ļéś ļō£ļ¼╝Ļ▓ī ļ░£ņāØĒĢśļŖö ņĢöņØś ĒŖ╣ņä▒ņāü Ēśäņ×¼Ļ╣īņ¦Ć ļé©ņä▒ĒśĖļź┤ļ¬¼ ņ¢æņä▒ņØĖ ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņŚÉņä£ ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīņØś ĒÜ©ņÜ®ņä▒ņØä ņ”Øļ¬ģĒĢĀ ņłś ņ׳ļŖö ļīĆĻĘ£ļ¬© ņŚ░ĻĄ¼ļŖö ļ│┤Ļ│ĀļÉ£ ļ░öĻ░Ć ņŚåļŗż. ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņØ┤ ņäĖĒżļÅģņä▒ ĒĢŁņĢöĒÖöĒĢÖņÜöļ▓ĢņŚÉ ļ░śņØæņØ┤ ļ│äļĪ£ ņŚåļŖö ņĀÉĻ│╝ ļ│Ė ņ”ØļĪĆļź╝ ĒżĒĢ©ĒĢ£ ņŚ¼ļ¤¼ ņ”ØļĪĆļ│┤Ļ│Āļź╝ Ļ│ĀļĀżĒĢ£ļŗżļ®┤, ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņŚÉņä£ņØś ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīļŖö ņłśņłĀ Ēøä ļ│┤ņĪ░ņÜöļ▓ĢņØä ļ╣äļĪ»ĒĢ£ ņ×¼ļ░£, ņĀäņØ┤ņĢöņŚÉņä£ņØś Ļ│ĀņŗØņĀü ņÜöļ▓Ģ ļō▒ ļŗżņ¢æĒĢ£ ļ░®ļ®┤ņŚÉņä£ ĻĘĖ ņŚŁĒĢĀņØä ĒÖĢņØĖĒĢ┤ņĢ╝ ĒĢĀ ĒĢäņÜöĻ░Ć ņ׳Ļ▓Āļŗż. ļśÉĒĢ£ ļé©ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ ļ░£Ēśä ņŚ¼ļČĆĻ░Ć ņØ┤ļ¤¼ĒĢ£ ĒĢŁĒśĖļź┤ļ¬¼ ņ╣śļŻīņŚÉņØś ņśłņĖĪņØĖņ×ÉļĪ£ņä£ ņŚŁĒĢĀņØ┤ ņ׳ņØäņ¦ĆņŚÉ ļīĆĒĢ£ ņŚ░ĻĄ¼ļÅä ĒĢäņÜöĒĢśĻ▓Āļŗż.
ņĀĆņ×ÉļōżņØĆ ņłśņłĀĻ│╝ ņłśņłĀ Ēøä ņČöĻ░ĆņĀüņØĖ ņ╣śļŻīņŚÉļÅä ņ”ēņŗ£ ņ×¼ļ░£ĒĢ£ ļé©ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ ņ¢æņä▒ņØĖ ļ¦żņÜ░ Ļ│ĄĻ▓®ņĀüņØĖ ĻĄŁņåīņ¦äĒ¢ēņä▒ ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņŚÉņä£ ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņśĆņ£╝ļ®░ ņóŗņØĆ ļ░śņØæņØä ņ¢╗ņŚłļŗż. ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīļŖö ņØ┤ļ»Ė ņĀäļ”ĮņäĀņĢö ņ╣śļŻīņŚÉņä£ ĒÜ©Ļ│╝ņÖĆ ņĢłņĀĢņä▒ņØä ĒÖĢņØĖĒĢ£ ļ░ö ņ׳ļŖö ņ╣śļŻīļĪ£, ļ│Ė ņ”ØļĪĆņØś ĒÖśņ×ÉļÅä ĒŖ╣ļ│äĒĢ£ ļČĆņ×æņÜ®ņØä ļ│┤ņØ┤ņ¦Ć ņĢŖņĢśļŗż. ļ│Ė ņ”ØļĪĆļŖö ņČöņĀüĻ┤Ćņ░░ ĻĖ░Ļ░äņØ┤ ļŗżņåī ņ¦¦ņĢśļŹś ĒĢ£Ļ│äĻ░Ć ņ׳ņ¦Ćļ¦ī ĻĄŁļé┤ņŚÉņä£ļŖö ņĢäņ¦ü ļ│┤Ļ│ĀļÉ£ ņ”ØļĪĆĻ░Ć ņŚåņ¢┤ ĻĘĖ ņØśņØśĻ░Ć ņ׳ļŗżĻ│Ā ĒĢśĻ▓Āļŗż. Ļ▓░ļĪĀņĀüņ£╝ļĪ£ ņĀĆņ×ÉļōżņØĆ ļé©ņä▒ĒśĖļź┤ļ¬¼ ņłśņÜ®ņ▓┤ ņ¢æņä▒ņØĖ ĒāĆņĢĪņäĀĻ┤ĆņāüĒö╝ņĢöņŚÉņä£ ļé©ņä▒ĒśĖļź┤ļ¬¼ ļ░ĢĒāł ņ╣śļŻīĻ░Ć ĒĢśļéśņØś Ēæ£ņżĆņÜöļ▓ĢņØ┤ ļÉĀ ņłś ņ׳ļŖö Ļ░ĆļŖźņä▒ņØä ĒÖĢņØĖĒĢśņŚ¼ ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļŗż.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






