žĄú Ž°†
ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžĚÄ ŽßźÍłįžč†Ž∂Äž†Ąž¶ĚžĚė ÍįÄžě• ŪĚĒŪēú žõźžĚłžĚīŽ©į, žöįŽ¶¨ŽāėŽĚľžóźžĄúŽŹĄ žßÄžÜ枆ĀžúľŽ°ú ž¶ĚÍįÄž∂ĒžĄłžóź žěąŽč§. žēĆŽ∂ÄŽĮľŽá®ŽäĒ ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžĚė žßąŽ≥Ď ŪäĻžĚī ŪĎúžßĞ쟎°úžĄú žč†ž¶ĚžĚė žßĄŪĖȞ̥ žěė žėąžł°Ūē† ŽŅźŽßĆ žēĄŽčąŽĚľ žč¨ŪėąÍīÄÍ≥Ą Ūē©Ž≥Ďž¶Ě ŽįúžÉĚžĚė ŽŹÖŽ¶Ĺž†ĀžĚł žúĄŪóėžĚłžěźžĚīÍłįŽŹĄ ŪēėŽč§. ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžĚė žĻėŽ£Ć ŽįŹ žėąŽį©žúľŽ°úŽäĒ ŪėąŽčĻ ÍīÄŽ¶¨ ŽįŹ Ž†ąŽčĆ-žēąžßÄžė§ŪÖźžč†-žēĆŽŹĄžä§ŪÖĆŽ°†Í≥Ą žĖĶž†úž†úŽ•ľ žĚīžö©Ūēú Ūėąžēē ÍīÄŽ¶¨ÍįÄ ŪēĄžąėž†ĀžĚīŽč§. Í∑łŽü¨Žāė žĚīŽü¨Ūēú žĻėŽ£ĆžóźŽŹĄ Ž∂ąÍĶ¨ŪēėÍ≥† žĚľŽ∂Ğ󟞥úŽäĒ žßÄžÜ枆ĀžúľŽ°ú žßĄŪĖČŪēėžó¨ ŽßźÍłįžč†Ž∂Äž†Ąž¶ĚžúľŽ°ú žßĄŪĖČŪēėŽĮÄŽ°ú, žÉąŽ°úžöī Íłįž†ĄžĚė žēĹž†úŽ•ľ žā¨žö©Ūēėžó¨ žč†ž¶ĚžĚė žßĄŪĖȞ̥ žĖĶž†úŪēėŽ†§ŽäĒ žčúŽŹĄŽď§žĚī ŽßéžĚī žčúŪĖČŽźėÍ≥† žěąŽč§.
žßĄ Žč®
ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžĚÄ žēĆŽ∂ÄŽĮľŽá®žôÄ žč†ÍłįŽä•žě•žē†Ž°ú žßĄŽč®ŪēúŽč§. žēĆŽ∂ÄŽĮľŽá®ŽäĒ žēĆŽ∂ÄŽĮľ ŽįįžĄ§ŽüČžóź ŽĒįŽĚľ ŽĮłžĄłžēĆŽ∂ÄŽĮľŽá®žôÄ ÍĪįŽĆÄžēĆŽ∂ÄŽĮľŽá®Ž°ú ŽāėŽČúŽč§. ŽĮłžĄł žēĆŽ∂ÄŽĮľŽá®ŽäĒ žÜĆŽ≥Ä žēĆŽ∂ÄŽĮľ ŽįįžĄ§žĚī 20-200 ug/min (30-300 mg/day)žĚīÍĪįŽāė Ž¨īžěĎžúĄ žÜĆŽ≥ÄžĚė žēĆŽ∂ÄŽĮľ/ŪĀ¨Ž†ąžēĄŪčįŽčĆŽĻĄÍįÄ 30-300 ug/mgžĚīŽ©į, ÍĪįŽĆÄžēĆŽ∂ÄŽĮľŽá®ŽäĒ Í∑ł žĚīžÉĀžúľŽ°ú ž†ēžĚėŪēúŽč§(Table 1). žöīŽŹô, Íįźžóľ, Žįúžóī, žč¨Ž∂Äž†Ą, žč¨Ūēú Í≥†ŪėąŽčĻ ŽįŹ Í≥†Ūėąžēē, žěĄžč†, žöĒŽ°ú Íįźžóľ, ŪėąŽá®, žõĒÍ≤Ĺ ŽďĪžĚÄ žēĆŽ∂ÄŽĮľŽá® ŽįįžĄ§žĚĄ ž¶ĚÍįÄžčúžľú ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶Ě žßĄŽč®žĚĄ Ž∂Äž†ēŪôēŪēėÍ≤Ć Ūē† žąė žěąŽč§. ŽĒįŽĚľžĄú 3-6ÍįúžõĒ Žāīžóź 2ŪöĆ Í≤Äžā¨Ž•ľ ŽćĒ žčúŪĖČŪēėžó¨, žīĚ 3ŪöĆžĚė Í≤Äžā¨ ž§Ď 2ŪöĆ žĚīžÉĀžĚė žĚīžÉĀ žÜĆÍ≤¨žĚī Ž≥īžó¨žēľ žßĄŽč®Ūē† žąė žěąŽč§[1]. žč†ÍłįŽä•žĚė ž†ÄŪēėŽäĒ Ūėąž≤≠ ŪĀ¨Ž†ąžēĄŪčįŽčĆ žąėžĻėŽ•ľ žĚīžö©Ūēėžó¨ estimated glomerular filtration rate (eGFR)Ž°ú žł°ž†ēŪēėŽäĒŽćį, eGFRžóź ŽĒįŽĚľ žč†ÍłįŽä•žĚĄ 5Žč®Í≥ĄŽ°ú ÍĶ¨Ž∂ĄŪēúŽč§(Table 2).
ŽįĒžĚīžė§ŽßąžĽ§
ŪėĄžě¨ÍĻĆžßÄŽäĒ žēĆŽ∂ÄŽĮľŽá®ÍįÄ ÍįÄžě• žěė žēĆŽ†§žßĄ ŽįĒžĚīžė§ŽßąžĽ§žĚīžßÄŽßĆ, Í≥ĄžÜć ž¶ĚÍįÄŪēėŽäĒ ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžĚĄ Í≥†Ž†§Ūē† ŽēĆ žēĆŽ∂ÄŽĮľŽá® ŽįúžÉĚ žĚīž†ĄŽ∂ÄŪĄį ŽÜ掏ĄÍįÄ ž¶ĚÍįÄŪēėžó¨ žč†ž¶ĚžĚė žėąŪõĄŽ•ľ žėąžł°Ūē† žąė žěąŽäĒ ŽįĒžĚīžė§ŽßąžĽ§Ž•ľ Í∑úŽ™ÖŪēėŽäĒ Í≤ÉžĚī žč†ž¶Ě ŽįúžÉ̞̥ ÍįźžÜĆžčúŪā¨ žąė žěąŽäĒ ž§ĎžöĒŪēú Žį©Ž≤ēžĚīŽč§. Neutrophil gelatinase associated lipocalin, N-acetyl-beta-glucosaminidase, cystatin C, alpha 1-microglubulin, Ig G, M, type IV collagen, nephrin, angiotensinogen, liver-type fatty acid-binding protein ŽďĪžĚī 2Ūėē ŽčĻŽá®Ž≥Ϟ󟞥ú žč†ž¶ĚžĚė ž°įÍłį Ž≥ÄŪôĒžôÄ ÍīÄŽ†®žĚī žěąŽč§Í≥† žēĆŽ†§ž†ł žěąŽč§[2]. Í∑łŽü¨Žāė žĚīŽď§žĚÄ ŽĆÄÍįú žÜĆÍ∑úŽ™® žóįÍĶ¨Ž°úžĄú ž°įÍłį žč†ž¶ĚžĚė žä§ŪĀ¨Ž¶¨ŽčĚ ŽßąžĽ§Ž°úžĄúžĚė žú†žö©žĄĪžĚĄ ŪôēžĚłŪēėÍłį žúĄŪēú ŽĆÄÍ∑úŽ™® ž†ĄŪĖ•ž†ĀžĚł žóįÍĶ¨ÍįÄ ŪēĄžöĒŪēėŽč§.
žĻė Ž£Ć
ŪėąŽčĻž°įž†ą
Diabetes Control and Complications Trials (DCCT) žóįÍĶ¨žóźžĄúŽäĒ 1,441Ž™ÖžĚė ž†ú1Ūėē ŽčĻŽá®Ž≥Ď ŪôėžěźŽď§žóźÍ≤ĆžĄú HbA1cŽ•ľ 7.3 vs. 9.1%Ž°ú ž°įž†ąŪĖąžĚĄ ŽēĆ, 6.5ŽÖĄÍįĄžĚė ž∂Ēž†Ā ÍīÄžįįžóźžĄú ž†ĀÍ∑Ļž†ĀžĚł ŪėąŽčĻ ž°įž†ą ÍĶįžóźžĄú ŽĮłžĄł ŽįŹ ÍĪįŽĆÄžēĆŽ∂ÄŽĮľŽá® ŽįúžÉĚŽ•†žĚī ÍįĀÍįĀ 39%, 54%Ž°ú žú†žĚėŪēėÍ≤Ć ÍįźžÜĆŪēėžėÄŽč§[3]. ŽėźŪēú DCCT žĹĒŪėłŪ䳎•ľ 18ŽÖĄÍįĄ žóįžě•Ūēú Epidemiology of Diabetes Interventions and Complications žóįÍĶ¨žóźžĄúŽŹĄ žĚīŽü¨Ūēú Í≤įÍ≥ľÍįÄ žßÄžÜ掟ėžóąŽč§[4]. ž†ú2Ūėē ŽčĻŽá®Ž≥Ď ŪôėžěźŽď§žĚĄ ŽĆÄžÉĀžúľŽ°ú Ūēú UK Prospective Diabetes Study (UKPDS) žóįÍĶ¨žóźžĄúŽäĒ ž†ĀÍ∑Ļž†Ā žĻėŽ£ĆÍĶįÍ≥ľ Í≥†žčĚž†Ā žĻėŽ£ĆÍĶįžĚė 10ŽÖĄÍįĄžĚė ž∂Ēž†ĀÍīÄžįį ŽŹôžēą ŽįúžÉĚŪēú HbA1c 11% žį®žĚīÍįÄ ŽĮłžĄłžēĆŽ∂ÄŽĮľŽá® ŽįúžÉĚ 33% ÍįźžÜĆžôÄ žóįÍīÄžĚī žěąžóąŽč§[5]. žĚīŽäĒ Action in Diabetes and Vascular disease žóįÍĶ¨žóźžĄúŽŹĄ ÍįôžēĄžĄú, 11,140Ž™ÖžĚė ž†ú2Ūėē ŽčĻŽá®Ž≥Ď ŪôėžěźŽď§žóźžĄú ž†ĀÍ∑Ļž†Ā žĻėŽ£ĆÍĶįžóźžĄú ŽĮłžĄł ŽįŹ ÍĪįŽĆÄžēĆŽ∂ÄŽĮľŽá®ÍįÄ ÍįĀÍįĀ 9%, 30% ÍįźžÜĆŪēėžėÄŽč§[6]. žĚīŽü¨Ūēú Í≤įÍ≥ľŽď§žóź Í∑ľÍĪįŪēėžó¨ ŽĮłÍĶ≠ ŽčĻŽá®Ž≥Ď ŪēôŪöƞ󟞥úŽäĒ ŽčĻŽá®Ž≥Ď ŪôėžěźžĚė ŪėąŽčĻ ž°įž†ąžĚĄ HbA1c 7% ŽĮłŽßĆ, žöįŽ¶¨ŽāėŽĚľŽäĒ 6.5% ŽĮłŽßĆžúľŽ°ú ŪēėŽŹĄŽ°Ě Í∂ĆÍ≥†ŪēėÍ≥† žěąŽč§.
Ūėąžēēž°įž†ą
Ūėąžēēž°įž†ąžĚĄ žěė Ūē†žąėŽ°Ě ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžĚė žßĄŪĖČžĚī Žä¶žĖīžßĄŽč§ŽäĒ Í≤ÉžĚÄ žěė žēĆŽ†§ž†ł žěąŽč§. UKPDSžóź ŽĒįŽ•īŽ©ī ŪėąžēēžĚī 10 mmHg ÍįźžÜĆŪē† ŽēĆ ŽčĻŽá®Ž≥Ď Ūē©Ž≥Ďž¶ĚÍ≥ľ žā¨ŽßĚžĚī ÍįĀÍįĀ 12%, 15% ÍįźžÜĆŪēėŽäĒ Í≤ÉžúľŽ°ú žēĆŽ†§ž°ĆŽč§[7]. Ž†ąŽčĆ-žēąžßÄžė§ŪÖźžč†Í≥Ą(renin angiotensin aldosterone system, RAS) žĖĶž†úž†úŽäĒ Žč§Ž•ł ŪėąžēēžēĹŽ≥īŽč§ žč†ž¶Ě žĻėŽ£ĆžóźžĄú žöįžõĒŪēúŽćį, žĚīŽäĒ žąėž∂ú žā¨ÍĶ¨ž≤ī žĄłŽŹôŽß•(efferent arteriole)žĚĄ žĚīžôĄžčúžľú žā¨ÍĶ¨ž≤īŽāīžēēžĚĄ ž§ĄžĚīÍ≥† Žč®ŽįĪŽá®Ž•ľ ÍįźžÜĆžčúŪā§Íłį ŽēĆŽ¨łžĚīŽč§. Micro-Albuminuria Reduction with Valsartan žóįÍĶ¨žóź ŽĒįŽ•īŽ©ī Žč§Ž•ł ŪėąžēēžēĹž†úžôÄ ŽĻĄžä∑ŪēėÍ≤Ć ŪėąžēēžĚĄ ž°įž†ąŪēėžó¨ŽŹĄ valsartanžĚī amlodipinežóź ŽĻĄŪēī ŽĮłžĄłžēĆŽ∂ÄŽĮľŽá® ÍįźžÜĆŪö®Í≥ľÍįÄ ŽćĒ ŽõįžĖīŽā¨Žč§(56 vs. 92%) [8]. 698Ž™ÖžĚė Í≥†ŪėąžēēžĚī žóÜŽäĒ ŽĮłžĄłŽč®ŽįĪŽá®Ž•ľ ÍįĞߥ 1Ūėē ŽčĻŽá®Ž≥Ď ŪôėžěźžóźžĄú angiotensin converting enzyme inhibitor (ACEI)ŽäĒ ÍĪįŽĆÄžēĆŽ∂ÄŽĮľŽá®Ž°úžĚė žßĄŪĖȞ̥ 60% žĖĶž†úŪēėžėÄžúľŽ©į, ž†ēžÉĀžúľŽ°ú ŪöĆŽ≥ĶžĚī 3Žįį ŽćĒ ŽßéžēėŽč§[9]. žĚīŪõĄ ACEIžĚė žĚīŽü¨Ūēú Ūö®Í≥ľÍįÄ 2Ūėē ŽčĻŽá®Ž≥Ď ŪôėžěźžóźžĄúŽŹĄ ŪôēžĚłŽźėžóąŽč§[10]. žēąžßÄžė§ŪÖźžč† žąėžö©ž≤ī žĖĶž†úž†ú(angiotensin II receptor blocker, ARB)Ž•ľ žā¨žö©Ūēú žó¨Žü¨ žóįÍĶ¨žóźžĄúŽŹĄ ACEI žóįÍĶ¨ Í≤įÍ≥ľžôÄ žú†žā¨Ūēėžó¨ žēĆŽ∂ÄŽĮľŽá®žĚė žßĄŪĖČ, žč†ÍłįŽä• žēÖŪôĒ ŽįŹ žč†Ž∂Äž†Ąž¶ĚžúľŽ°úžĚė žßĄŪĖȞ̥ žú†žĚėŪēėÍ≤Ć žĖĶž†úŪēėžėÄŽč§[11-13].
RAS žĖĶž†úž†úŽď§ ÍįĄžĚė Ž≥ĎŪē© žĻėŽ£Ć
ACEIžôÄ ARB Ž≥ĎŪē©
ACEIŽāė ARB žā¨žö©žóźŽŹĄ Ž∂ąÍĶ¨ŪēėÍ≥† žč†ž¶ĚžĚė žĚľŽ∂ÄŽäĒ Í≥ĄžÜć žßĄŪĖČŪēėŽäĒŽćį, žĚīŽ•ľ žÉĀžáĄŪēėÍłį žúĄŪēī RAS žĖĶž†úž†ú ÍįĄžĚė Ž≥ĎŪē©žöĒŽ≤ēžĚī žčúŽŹĄŽźėžóąŽč§. ÍįÄžě• ŽĆÄŪĎúž†ĀžúľŽ°úŽäĒ ACEIžôÄ ARB Ž≥ĎŪē©žĚīŽč§. Candesartan and Lisinopril Micro-albuminuria žóįÍĶ¨žóźžĄúŽäĒ candesartanÍ≥ľ lisinopril Ž≥ĎŪē© 12ž£ľžóź ÍįĀÍįĀžĚė žĻėŽ£ĆŽ≥īŽč§ŽŹĄ žú†žĚėŪēėÍ≤Ć ŽĮłžĄłžēĆŽ∂ÄŽĮľŽá® ŽįúžÉ̞̥ ÍįźžÜĆžčúžľįŽč§[14]. Í∑łŽü¨Žāė žĚīŽäĒ ž†ĀžĚÄ žąėžĚė ŪôėžěźŽ°ú žßßÍ≤Ć ÍīÄžįįŪēú žóįÍĶ¨žėÄÍ≥†, Ongoing Telmisartan Along and in Combination with Ramipril Global Endpoint Trial žóįÍĶ¨žóźžĄúŽäĒ 5,620Ž™ÖžĚė žč¨ŪėąÍīÄÍ≥Ą Ūē©Ž≥Ďž¶ĚžĚī ŽÜíÍ≥†, žēĆŽ∂ÄŽĮľŽá®ŽäĒ žč¨ŪēėžßÄ žēäžĚÄ ŪôėžěźŽ•ľ ŽĆÄžÉĀžúľŽ°ú(37.5% ŽčĻŽá®) ramipril, telmisartan Žč®ŽŹÖ ŽėźŽäĒ Ž≥ĎŪē©žúľŽ°ú žĻėŽ£ĆŪĖąžĚĄ ŽēĆ Ūą¨žĄĚ, ŪĀ¨Ž†ąžēĄŪčįŽčĆ 2Žįį žĚīžÉĀ žÉĀžäĻ ŽįŹ žā¨ŽßĚžĚė Ž≥ĶŪē© outcomežĚī Ž≥ĎŪē©ÍĶįžóźžĄú žú†žĚėŪēėÍ≤Ć ŽÜížēėŽč§(hazards ratio 1.09; 95% confidence interval 1.01-1.18, p < 0.037)[15]. žĚīŽäĒ Ž≥ĎŪē©ÍĶįžóźžĄú ŪėąžēēžĚī 2-3 mmHg ŽćĒ ÍįźžÜĆŪēėžó¨ ͳȞĄĪ žč†Ž∂Äž†ĄžĚī ŽćĒ ŽßéžēėŽćė Í≤ɞ󟞥ú ÍłįžĚłŪēúŽč§. žĚīŪõĄ Veterans Affairs Nephropathy in Diabetes žóįÍĶ¨žóźžĄú 1,448Ž™ÖžĚė 2Ūėē ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžóźžĄú losartanÍ≥ľ lisinopril Ž≥ĎŪē©ÍĶįžóźžĄú renal outcomežĚī ŽćĒ žĘčžēĄžßÄžßÄ žēäÍ≥† Í≥†žĻľŽ•®Ūėąž¶Ě, ͳȞĄĪžč†Ž∂Äž†ĄžĚī ŽćĒ ŽßéžĚī žÉĚÍĻÄžĚī Žč§žčú ŪôēžĚłŽźėžĖī[16], ACEIžôÄ ARBžĚė Ž≥ĎŪē©žöĒŽ≤ēžĚÄ ŽćĒ žĚīžÉĀ Í∂ĆÍ≥†ŽźėžßÄ žēäÍ≥† žěąŽč§.
ACEI/ARBžôÄ Ž†ąŽčĆ žĖĶž†úž†ú ŽėźŽäĒ žēĆŽŹĄžä§ŪÖĆŽ°† žĖĶž†úž†úžĚė Ž≥ĎŪē©
Ž†ąŽčĆ žĖĶž†úž†úÍįÄ RAS žĖĶž†úž†ú žā¨žö©žúľŽ°ú Ž≥īžÉĀž†ĀžúľŽ°ú ž¶ĚÍįÄŽźú Ž†ąŽčĆ ŪôúžĄĪŽŹĄŽ•ľ ÍįźžÜĆžčúžľú ŽŹĄžõÄžĚī Žź† Í≤ÉžĚīŽěÄ ÍįÄžĄ§Ūēėžóź žčúŪĖČŽźú Aliskiren in the Evaluation of Proteinuria in Diabetes žóįÍĶ¨ŽäĒ losartan žĶúŽĆÄ žö©ŽüČžóź Ž†ąŽčĆ žĖĶž†úž†úžĚł aliskirenžĚĄ ž∂ĒÍįÄŪēú žóįÍĶ¨žĚīŽč§. 592Ž™ÖžĚė Í≥†ŪėąžēēžĚī žěąŽäĒ žč†ž¶ĚŪôėžěźžóźžĄú aliskirenžĚÄ ŪėąžēēÍ≥ľ Ž¨īÍīÄŪēėÍ≤Ć žÜĆŽ≥ÄžēĆŽ∂ÄŽĮľ ŽįįžĄ§ŽüȞ̥ 20% ÍįźžÜĆžčúžľįŽč§[17]. Í∑łŽü¨Žāė Aliskiren Trial in Type 2 Diabetes Using Cardio-Renal Endpoints žóįÍĶ¨žóźžĄúŽäĒ renal outcome Ūėłž†Ą žóÜžĚī Í≥†žĻľŽ•®Ūėąž¶ĚžĚī ž¶ĚÍįÄŪēėžó¨ ž°įÍłį žĘÖŽ£ĆŽźėžóąŽč§[18]. ŽėźŪēú žēĆŽŹĄžä§ŪÖĆŽ°† žĖĶž†úž†úžôÄ RAS žĖĶž†úž†úžĚė Ž≥ĎŪē© žĻėŽ£ĆŽŹĄ žčúŪĖČŽźėžóąžúľŽ©į, Ž©ĒŪÉÄŽ∂ĄžĄĚžóźžĄú Žč®ŽŹÖ žĻėŽ£ĆŽ≥īŽč§ Žč®ŽįĪŽá® ÍįźžÜĆ Ūö®Í≥ľŽ•ľ Ž≥īžėÄŽč§[19]. Í∑łŽü¨Žāė Í≥†žĻľžäėŪėąž¶ĚžĚī ž¶ĚÍįÄŪēėŽ©į, ŽĆÄÍ∑úŽ™® žóįÍĶ¨žóźžĄú žč†ž¶ĚžĚė žßĄŪĖČžĚī Ūėłž†ĄŽźėŽäĒ Í≤įÍ≥ľŽ•ľ Ž≥ł žóįÍĶ¨ŽäĒ žēĄžßĀ žóÜŽč§. žĚīŽü¨Ūēú Í≤įÍ≥ľŽď§žĚĄ ŽįĒŪÉēžúľŽ°ú RAS žĖĶž†úž†úŽď§ ÍįĄžĚė Ž≥ĎŪē©žĚÄ Í∂ĆÍ≥†ŽźėžßÄ žēäŽäĒŽč§.
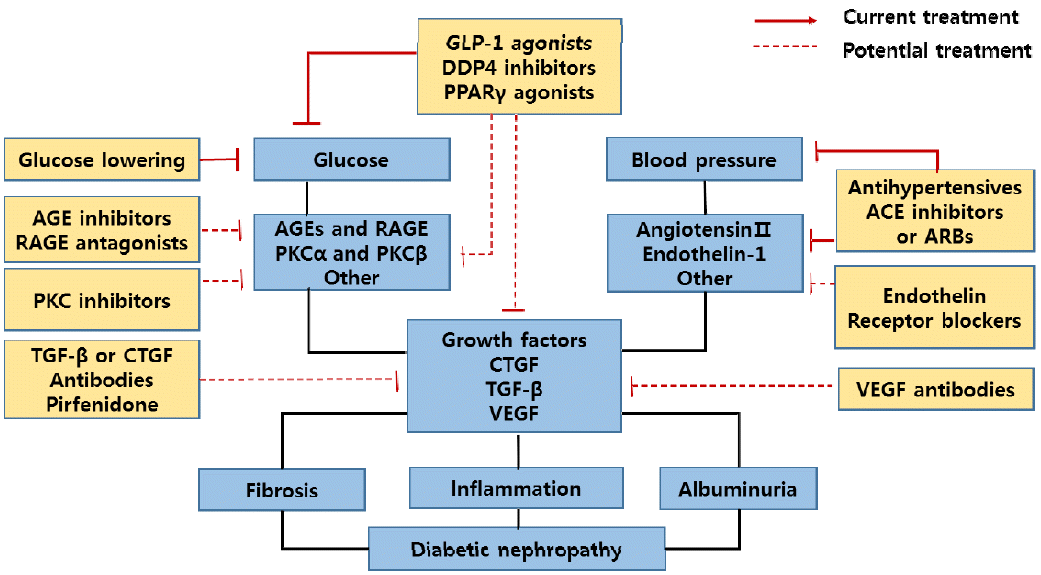
žÉąŽ°úžöī žĻėŽ£Ćž†úŽď§(Fig. 1)
ŽčĻŽá®Ž≥Ď žĻėŽ£Ćž†ú
žĶúÍ∑ľ ŽßéžĚī žā¨žö©ŽźėÍ≥† žěąŽäĒ dipeptidyl peptidase-4 žĖĶž†úž†úŽāė glucagon-like peptide 1 agonistŽäĒ žč†žě•žĚė ŽāėŪ䳎•® ŽįįžĄ§žĚĄ ž¶ĚÍįÄžčúŪāīžúľŽ°úžć® žč†žā¨ÍĶ¨ž≤ī žó¨Í≥ľžú®žĚĄ ÍįźžÜĆžčúŪā®Žč§. 6ÍįúžõĒžĚė sitagliptin [20], 12ž£ľžĚė alogliptin žĻėŽ£ĆÍįÄ Žč®ŽįĪŽá®Ž•ľ ÍįźžÜĆžčúžľįžúľŽāė[21] žĚīŽü¨Ūēú Ūö®Í≥ľÍįÄ ŪėąŽčĻ ÍįēŪēėŪö®Í≥ľžóź ÍłįžĚłŪēėŽäĒžßÄ, žč†žě•žóź ŽĮłžĻėŽäĒ žßĀž†Ďž†ĀžĚł žėĀŪĖ•žĚłžßÄŽäĒ ÍĶ¨Ž≥ĄŪēėÍłį žĖīŽ†ĶŽč§. 4ÍįúžĚė 3žÉĀ žóįÍĶ¨žĚė pooled analysisžóźžĄú RAS žĖĶž†úž†úŽ•ľ Ūą¨žó¨ ŽįõÍ≥† žěąŽäĒ 217Ž™ÖžĚė ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶Ě ŪôėžěźžóźžĄú žēĆŽ∂ÄŽĮľŽá® ÍįźžÜĆÍįÄ HbA1cžôÄ Ž¨īÍīÄŪēėÍ≤Ć ÍīÄžįįŽźėžĖī žč†žě• ŪäĻžĚīž†ĀžĚł Ūö®Í≥ľŽ•ľ žßÄŽčź ÍįÄŽä•žĄĪžĚĄ žčúžā¨ŪēúŽč§[22].
Sodium-glucose co-transporter 2 žĖĶž†úž†úŽäĒ žč†žě• Í∑ľžúĄžĄłŽá®ÍīĞ󟞥ú ŽāėŪ䳎•® žě¨ŪĚ°žąėŽ•ľ žĖĶž†úŪēėžó¨ žõźžúĄžĄłŽá®ÍīÄžĚė ŽāėŪ䳎•® ŽÜ掏ĄŽ•ľ ŽÜížěĄžúľŽ°úžć® žąėžěÖ žā¨ÍĶ¨ž≤ī žÜĆŽŹôŽß•(afferent arteriole)žĚĄ žąėž∂ēŪēėÍ≤Ć ŽßƎ吏Ėī GFRžĚĄ ž†ēžÉĀŪôĒžčúŪā®Žč§. ŽėźŪēú in vitro žóįÍĶ¨žóźžĄú Í≥†ŪėąŽčĻžóź žĚėŪēú žóľž¶Ě ŽįŹ žĄ¨žú†ŪôĒ ŽįėžĚĎŽŹĄ žĖĶž†úŪē† žąė žěąžóąŽč§[23]. žěĄžÉĀ žóįÍĶ¨žĚė žĚľžį® Ž≥ÄžąėŽäĒ žēĄŽčąžßÄŽßĆ post hoc Ž∂ĄžĄĚžóź žĚėŪēėŽ©ī canagliflozin [24], empagliflozin [25] žĻėŽ£ĆÍĶįžóźžĄú ŽĆÄž°įÍĶį ŽĆÄŽĻĄ GFRžĚÄ žēĹÍįĄ ÍįźžÜĆŪēėžßÄŽßĆ Í≥ĄžÜć žā¨žö© žčú Ūėłž†ĄŽźėŽäĒ žĖĎžÉĀžĚĄ Ž≥īžĚīŽ©į, žēĆŽ∂ÄŽĮľŽá®ŽäĒ žßÄžÜ枆ĀžúľŽ°ú ÍįźžÜĆŪēėŽäĒ Í≤įÍ≥ľŽ•ľ Ž≥īžėÄŽč§. žĚīŽäĒ žč†ž¶Ě žīąÍłįžóź žā¨ÍĶ¨ž≤ī žó¨Í≥ľžú® ž¶ĚÍįÄŽ•ľ ÍĶźž†ēŪē®žúľŽ°úžć® žč†žě• Ž≥īŪėł Ūö®Í≥ľŽ•ľ žěÖž¶ĚŪēú Í≤ÉžĚīŽĚľ ŪēėÍ≤†Žč§.
Bardoxolone methyl
ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžĚė ž£ľŽźú Íłįž†ĄžĚÄ žāįŪôĒž†Ā žä§Ū䳎†ąžä§žôÄ žóľž¶ĚŽįėžĚĎžúľŽ°úžĄú, Ūē≠žāįŪôĒ, Ūē≠žóľž¶Ě ž†úž†úžĚł bardoxolone methylžĚÄ žÉąŽ°úžöī žč†ž¶Ě žĻėŽ£Ćž†úŽ°úžĄú ŽßéžĚÄ ÍłįŽĆÄŽ•ľ ŽįõžēėŽč§. Bardoxolone methylžĚÄ žīąÍłį žóįÍĶ¨žóźžĄúŽäĒ GFRžĚĄ ž¶ĚÍįÄžčúžľįžúľŽāė[26], ŪõĄžÜć žóįÍĶ¨žóźžĄú GFR 15-30 mL/min/1.73 m2žĚė 2,185Ž™ÖžĚė 2Ūėē ŽčĻŽá®Ž≥Ď ŪôėžěźŽ•ľ ŽĆÄžÉĀžúľŽ°ú Ūēú žóįÍĶ¨ŽäĒ ž°įÍłį žĘÖŽ£ĆŽźėžóąŽč§. GFRžĚÄ ž¶ĚÍįÄŪēīŽŹĄ ŽßĆžĄĪ žč†Ž∂Äž†ĄžĚīŽāė žč¨ŪėąÍīÄÍ≥Ą žā¨ŽßĚ ÍįźžÜĆ Ūö®Í≥ľÍįÄ žóÜÍ≥† žč¨ŪėąÍīÄÍ≥Ą žßąŪôė ŽįúžÉĚžĚī žú†žĚėŪēėÍ≤Ć ž¶ĚÍįÄŽźėžóąÍłį ŽēĆŽ¨łžĚīŽč§[27]. Bardoxolone methylžĚī žôú žč¨ŪėąÍīÄÍ≥Ą žßąŪôėžĚĄ ž¶ĚÍįÄžčúŪā§ŽäĒžßÄ Ūôēžč§ŪēėžßÄ žēäžúľŽāė ž≤īžē°ŽüČ ž¶ĚÍįÄ, Í≥†Ūėąžēē, žč¨Ž∂Äž†Ą ž¶ĚÍįÄÍįÄ žõźžĚłžúľŽ°ú žÉĚÍįĀŽźúŽč§.
Pirfenidone
ŽßĆžĄĪžč†Ž∂Äž†ĄžúľŽ°úžĚė žßĄŪĖČžĚÄ ŽßźÍłį Ž≥ÄŪôĒžĚł ŽĄ§ŪĒĄŽ°† ŪĆĆÍīīžôÄ žĄ¨žú†ŪôĒÍįÄ ŪäĻžßēž†ĀžĚīŽč§. PirfenidonežĚÄ Ūē≠žĄ¨žú†ŪôĒ ž†úž†úŽ°úžĄú žÉĚž•źŽ™®ŽćłžóźžĄú žĘčžĚÄ Ūö®Í≥ľŽ•ľ Ž≥īžėÄŽč§. žĚłž≤ī ŽĆÄžÉĀ ŪĆƞ̾ŽüŅ žóįÍĶ¨žóźžĄú GFRžĚĄ ž¶ĚÍįÄžčúžľįžúľŽāė ŪÜĶÍ≥ĄŪēôž†ĀžĚł žú†žĚėžĄĪžĚÄ žóÜžóąžúľŽ©į, 40%žóź Žč¨ŪēėŽäĒ ŽÜížĚÄ ž§ĎŽŹĄ ŪÉąŽĚĹŽ•†žĚĄ Ž≥īžó¨[28], žēĄžßĀ žč†ŽĘįžĄĪ žěąŽäĒ Í≤įÍ≥ľŽ•ľ žĖĽžßÄ Ž™ĽŪēėÍ≥† žěąŽč§.
Vitamin D žąėžö©ž≤ī ŪôúžĄĪŪôĒ ž†úž†ú
Vitamin D žąėžö©ž≤ī ŪôúžĄĪŪôĒ ž†úž†úŽäĒ Ūē≠žóľž¶Ě, Ūē≠Žč®ŽįĪ žěĎžö©žĚĄ žßÄŽčĆŽč§. Selective Vitamin D Receptor Activation with Paricalcitol for Reduction of Albuminuria in Patients with Type 2 Diabetes žóįÍĶ¨žóźžĄúŽäĒ 2 ug/džĚė paricalcitolžĚī Í≥†žĻľžäėŪėąž¶ĚžĚė Ž∂ÄžěĎžö© žóÜžĚī žēĆŽ∂ÄŽĮľŽá®Ž•ľ žßÄžÜ枆ĀžúľŽ°ú ÍįźžÜĆžčúŪā§ŽäĒ Í≤ÉžĚī ŪôēžĚłŽźėžóąŽč§[29]. žĚī žóįÍĶ¨Ž•ľ Ū܆ŽĆÄŽ°ú Vitamin D žąėžö©ž≤ī ŪôúžĄĪŪôĒ ž†úž†úÍįÄ ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžĚė žßĄŪĖȞ̥ žĖĶž†úŪēėŽäĒžßÄžóź ŽĆÄŪēú ŪõĄžÜć žóįÍĶ¨ÍįÄ ŪēĄžöĒŪēėŽč§.
žĄ†ŪÉĚž†Ā endothelin žąėžö©ž≤ī žĖĶž†úž†ú
žč†žě• Žāī endothelin žąėžö©ž≤ī ŪôúžĄĪŪôĒŽäĒ mesangial cell ž¶ĚžčĚ, žóľž¶Ě, žĄ¨žú†ŪôĒŽ•ľ žīȞߥŪēėŽ©į, žó¨Žü¨ žóįÍĶ¨žóźžĄú endothelin žąėžö©ž≤ī A žĖĶž†úŽäĒ žč§Ūóėž†ĀžĚł ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžĚĄ Ūėłž†ĄžčúžľįžúľŽ©į, avosentan 12ž£ľ žā¨žö©Ūēú žěĄžÉĀ žóįÍĶ¨žóźžĄú žēĆŽ∂ÄŽĮľŽá®ÍįÄ ÍįźžÜĆŽźėžóąŽč§[30]. žĚīŽü¨Ūēú Í≤įÍ≥ľŽäĒ ŪõĄžÜć žóįÍĶ¨žóźžĄúŽŹĄ ŪôēžĚłŽźėžóąŽč§[31]. žĚīŽäĒ 1,392Ž™ÖžĚė RAS žĖĶž†úž†úŽ•ľ žā¨žö©ŪēėŽćė ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶Ě ŪôėžěźžóźžĄú avosentan (25 or 50 mg) ŽėźŽäĒ žúĄžēŞ̥ ž∂ĒÍįÄŪēú žóįÍĶ¨žĚīŽč§. ŽĻĄŽ°Ě avosentanžĚī Žč®ŽįĪŽá®ŽäĒ ž§ĄžėÄžßÄŽßĆ 4ÍįúžõĒ ŽßĆžóź ž°įÍłį žĘÖŽ£ĆŽźėžóąŽäĒŽćį, žĚīŽäĒ ž≤īžē° ž†ÄŽ•ė, žč¨Ž∂Äž†ĄÍ≥ľ ÍįôžĚÄ žč¨ŪėąÍīÄÍ≥Ą žßąŪôė ŽįúžÉĚžĚī žú†žĚėŪēėÍ≤Ć ž¶ĚÍįÄŪĖąÍłį ŽēĆŽ¨łžĚīŽč§. žĚīŽü¨Ūēú Ž∂ÄžěĎžö©žĚÄ endothelin žąėžö©ž≤ī B žĖĶž†úžóź žĚėŪēėŽĮÄŽ°ú, ŪėĄžě¨ endothelin žąėžö©ž≤ī A žĄ†ŪÉĚžĄĪžĚī ŽćĒ ŪĀį atrasentanžĚĄ žā¨žö©Ūēú ŽĆÄÍ∑úŽ™® žěĄžÉĀžóįÍĶ¨ÍįÄ žßĄŪĖČ ž§ĎžĚīŽč§.
Í≤į Ž°†
ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶ĚžĚÄ žēĆŽ∂ÄŽĮľŽá®ŽĚľŽäĒ Ūôēžč§Ūēú žßąŽ≥Ď ŽßąžĽ§ÍįÄ ž°īžě¨ŪēėÍ≥† žč†ž¶Ě Íłįž†ĄžĚė ž£ľŽźú Ž≥Ϟ̳žĚł RAS žĖĶž†úž†úŽ•ľ žā¨žö©Ūē®žóźŽŹĄ Ž∂ąÍĶ¨ŪēėÍ≥† žĚľŽ∂Ğ󟞥úŽäĒ žßÄžÜ枆ĀžúľŽ°ú žßĄŪĖČŪēėžó¨ ŽßĆžĄĪ žč†Ž∂Äž†Ąž¶ĚžúľŽ°ú žßĄŪĖČŪēėžó¨, ŽčĻŽá®Ž≥Ďžóź žĚėŪēú ŽßĆžĄĪ žč†Ž∂Äž†Ąž¶ĚžĚÄ ŽāėŽā†žĚī ž¶ĚÍįÄ žĚľŽ°úžóź žěąŽč§. žĚīŽü¨Ūēú ÍīÄž†źžóźžĄú Ž≥ľ ŽēĆ, ŽčĻŽá®Ž≥ĎžĄĪ žč†ž¶Ě ŪôėžěźžóźžĄú ŪėąŽčĻ, Ūėąžēē, Í≥†žßÄŪėąž¶ĚžĚė žēĹŽ¨ľž†Ā žĻėŽ£ĆŽŅźŽßĆ žēĄŽčąŽĚľ ŪĚ°žóį, ž≤īž§ĎÍįźžÜĆ, žöīŽŹô ŽďĪÍ≥ľ ÍįôžĚÄ žÉĚŪôúžäĶÍīÄ ÍĶźž†ēžĚĄ žě•ÍłįÍįĄ žčúŪĖČŪēėžó¨ žč†ž¶ĚžĚĄ žúĄžčúŪēú ŽĮłžĄłŪėąÍīÄŪē©Ž≥Ďž¶ĚžĚĄ 60%, žā¨ŽßĚžĚīŽāė žč¨ŪėąÍīÄÍ≥Ą žßąŪôė ŽįúžÉ̞̥ 50% ÍįźžÜĆžčúŪā® Steno-2 Í≤įÍ≥ľ[32]Ž•ľ žě¨ž°įŽ™ÖŪē† ŪēĄžöĒÍįÄ žěąŽč§. ž¶Č ŪėĄžě¨ÍĻĆžßÄŽäĒ ŽčĻŽá®Ž≥ĎžĚė ž†ĄŽįėž†Ā žĻėŽ£ĆžóźžĄú žöĒÍĶ¨ŽźėŽäĒ Í≤ÉÍ≥ľ ÍįôžĚī Žč§žĖĎŪēú žúĄŪóėžĚłžěźŽď§žĚĄ Ž™®ŽĎź ÍīÄŽ¶¨ŪēėŽäĒ Í≤ÉžĚī žč†ž¶ĚžĚė žėąŪõĄŽ•ľ Ūėłž†ĄžčúŪā§ŽäĒ ÍįÄžě• žĘčžĚÄ Žį©Ž≤ēžĚīŽč§. Í∑łŽü¨Žāė ŪēúŪéłžúľŽ°úŽäĒ žč†ž¶ĚžĚė Ž≥ĎŪÉúžÉĚŽ¶¨žóź Í∑ľÍĪįŪēú žč†žēĹ ÍįúŽįú ŽįŹ ŽćĒ ŽāėžēĄÍįÄ žč†žě• žě¨žÉĚ žĻėŽ£Ć, ž¶Č ž§ĄÍłįžĄłŪŹ¨žôÄ ÍįôžĚÄ Žč§Ž•ł žł°Ž©īžĚė žĻėŽ£Ćž†ú ÍįúŽįúžóźŽŹĄ Ūěėžć®žēľ Ūē† Í≤ÉžĚīŽč§.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






