서 론
혈관육종은 혈관 내피세포에서 기원하는 드문 악성 종양으로, 모든 연부조직 육종의 1-2% 정도를 차지하며 주로 남성에게서 많이 발견된다[1]. 호발 부위는 주로 두피와 얼굴 피부지만, 드물게 소장에서도 발견된다. 현재까지 소장에서 발생한 혈관육종은 국내에는 1예가 보고되었으며 국외에는 48예가 보고되었다[2,3]. 소장에 발생한 원발성 혈관육종은 매우 드물며, 신속하고 정확한 진단 및 샘암종, 림프종, 악성 흑색종과 감별이 어렵다[4]. 진단을 위해서는 조직검사와 면역조직화학염색이 필요하고, 수술적 절제와 항암치료에도 반응이 좋지 않아 예후도 불량하다. 혈관육종의 전이는 림프 및 혈액을 통해 이루어지며 85%의 환자에서 림프절, 간, 폐, 뼈에 발생한다[5].
이에 저자들은 객혈, 호흡곤란을 주소로 내원하여 폐전이, 뼈전이를 동반한 십이지장 혈관육종으로 진단된 1예를 경험하여 소장을 침범한 혈관육종의 국내외 문헌고찰과 함께 보고한다.
증 례
환 자: 65세 남자
주 소: 호흡곤란, 객혈
현병력: 내원 2개월 전부터 소량의 객혈이 지속되었으며, 내원 2일 전부터 객혈의 양과 횟수가 증가하고 호흡곤란이 동반되어 본원 응급실을 방문하였다.
과거력: 10년 전 직장암을 진단받고 수술, 항암화학치료 그리고 방사선치료를 받았다. 9년 전 고혈압과 뇌졸중을, 7년 전에는 심근경색을 진단받아 관상동맥에 스텐트를 삽입하고 약물치료 중이었다. 2개월 전 흉통과 객혈로 본원 방문하여 허혈성 심부전 진단받고 약물치료를 시행하였고, 객혈에 대한 검사로 흉부 전산화단층촬영(computed tomography, CT) 및 기관지내시경을 시행하였으나 특이 소견이 없어 추적관찰하기로 하였다. 당시에 동반된 소구성 저색소성 빈혈에 대해 대장내시경을 시행하였지만 하부위장관 출혈의 소견은 보이지 않았고, 2개월 전 외부병원에서 시행한 상부위장관 내시경에서 상부위장관 출혈의 소견이 없었기 때문에 본원에서는 상부위장관 내시경은 시행하지 않았다.
가족력: 특이사항 없었다.
사회력: 특이사항 없었다.
이학적 소견: 응급실 내원 당시 혈압 100/60 mmHg, 맥박 78회/분, 호흡수 20회/분, 체온은 정상이었고, 의식은 명료하였다. 만성 병색에 전신 무력감이 있어 보였으며, 결막은 창백하였고 공막 황달 소견은 보이지 않았다. 청진에서 심잡음은 들리지 않았으며 심박동은 규칙적이었으나, 양측 폐야에서 경도의 악설음이 청진되었다.
검사실 소견: 혈액검사에서 백혈구 7,790/mm3, 혈색소 8.7 g/dL, 혈소판 192,000/mm3이었고, 평균적혈구 용적 75 fL, 적혈구 평균 혈색소 농도 30 g/dL이었다. 혈청 생화학검사에서 ALP 226 IU/L (104-338 IU/L), AST 12 IU/L, ALT 19 IU/L, 총 단백 5.6 g/dL, 알부민 3.1 g/dL, 총 빌리루빈 0.6 mg/dL이었고 HBsAg 음성, anti-HBs 양성, anti-HCV 음성이었다.
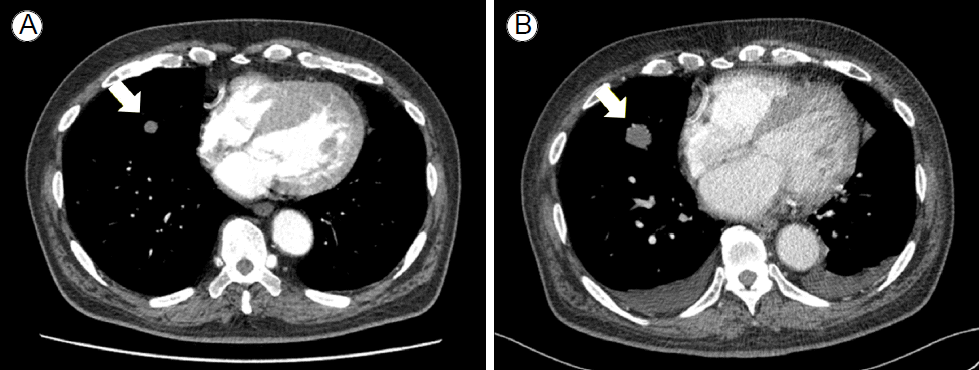
방사선 소견: 응급실에서 촬영한 단순 흉부방사선 사진은 정상이었으나, 흉부 전산화단층촬영에서는 양폐야에 간유리 음영을 동반한 여러 개의 다양한 크기의 결절들이 관찰되어(Fig. 1) 전산화단층촬영 유도하에 경피적 폐침생검을 시행하였다.
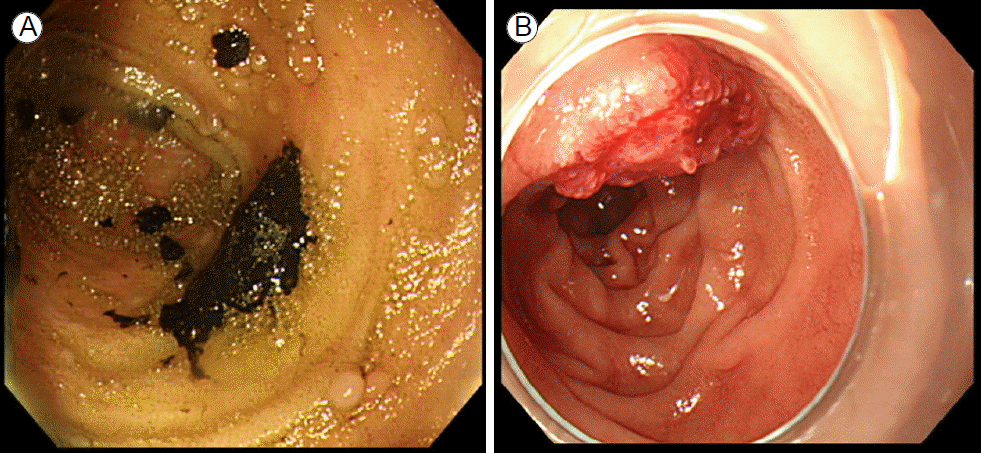
2차 내시경 소견: 입원 중 빈혈이 지속되어 대장내시경을 재시행하였고 말단 회장에 응고된 혈액이 관찰되어 상부위장관 내시경을 시행하였다. 십이지장 제3부까지 삽입하여 자세히 살펴본 결과, 십이지장 제2부의 원위 방향에 자발 출혈을 동반한 2 × 2 cm 크기의 종괴가 관찰되어 생검을 시행하였다(Fig. 2).
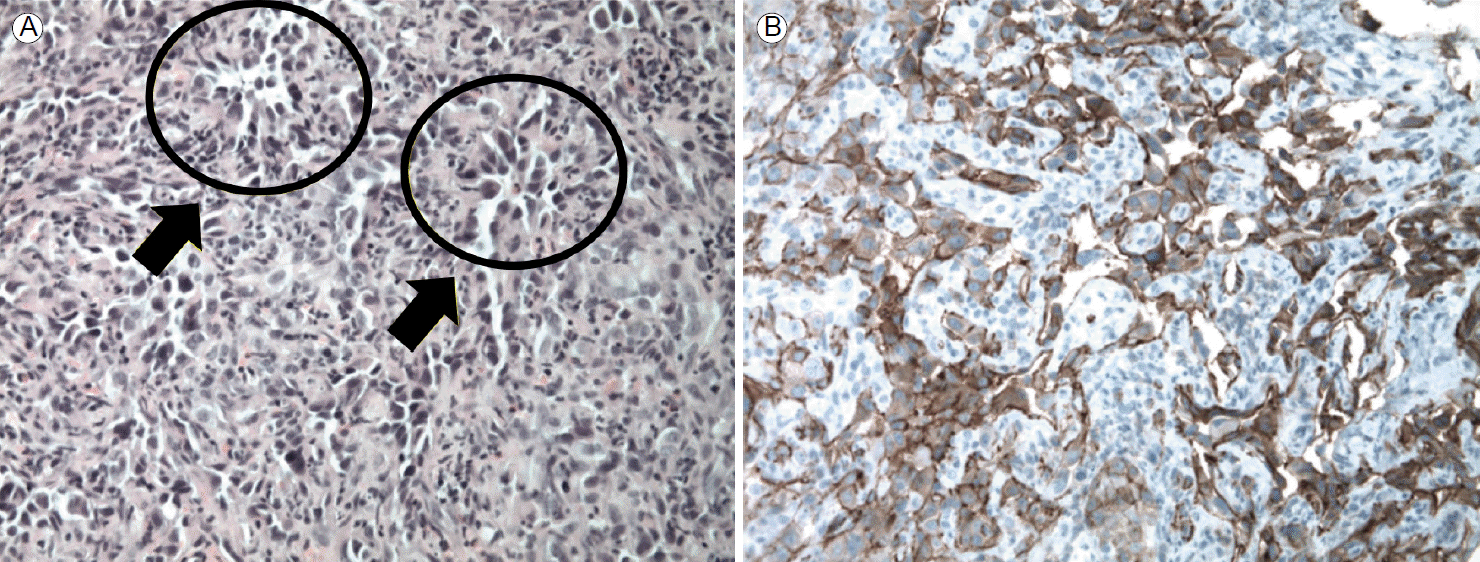
병리소견: 내시경적 생검을 통한 현미경적 조직소견에서는 과염색성의 핵과 호산구성 세포질로 이루어진 불룩하고 방추형의 다각형의 세포들로 둘러싸인 혈관들이 문합하는 소견이 관찰되었다(Fig. 3). 이들 종양세포는 vimentin, CD31에 대한 면역조직화학염색에서 양성 소견을 보였으나(Fig. 3). cytokeratin 7, cytokeratin 20, TTF-1에는 음성 소견을 보였다. 전산화단층촬영 유도하 경피적 폐침 생검에서는 크고 과염색성의 세포들이 불규칙한 모양 및 크기로 혈관들은 문합하는 소견이 관찰되었으며, 이는 혈관육종의 폐침범 소견에 합당하였다.
핵의학 검사소견: 타 장기 침범 여부를 확인하기 위해 시행한 양성자 방출 단층촬영 검사(fludeoxyglucose [FDG]-positron emission tomography/CT)에서는 십이지장에 최대 표준화 섭취값(standard uptake value) 8.6으로 증가된 18F-FDG 섭취율이 관찰되었고, 폐결절의 18F-FDG 섭취율은 SUV 5.3, 골반뼈와 오른쪽 근위 대퇴골에서 SUV 7.3, 6.2로 관찰되어 폐와 뼈침범이 확인되었다(Fig. 4).
경과: 환자의 만성 출혈에 대한 고식적 수술과 전신 항암화학치료를 계획하였으나, 환자는 허혈성 심질환 등의 다른 건강상의 이유로 치료방법을 결정하지 못하여 자의로 퇴원하였다. 그러나 1개월 후에 발열, 기침, 호흡곤란이 발생하여 다시 본원 응급실로 내원하였고, 추적 흉부 전산화단층촬영에서 폐 결절들의 크기 및 개수가 증가하였으며, 부폐렴성 흉수도 관찰되어 혈관육종의 경과가 급격히 진행함을 알 수 있었다(Fig. 1).
고 찰
혈관육종은 혈관 또는 림프관의 내피세포에서 기원하는 악성종양으로 연부조직 육종의 1-2% 정도를 차지하며, 주로 피부와 피하조직에 발생하고, 간, 비장, 심장과 같은 내부 장기에도 발생하기도 한다[1]. 소장에 발생하는 혈관육종은 드물게 보고되며 위장관 출혈, 복통, 장폐쇄, 복부팽만, 빈혈, 체중 감소 등의 증상으로 나타난다[6]. 이번 증례에서는 위장관 출혈의 원인으로 생각되는 2 × 2 cm 크기의 십이지장 단일 종괴와 전이로 생각되는 다발성의 작은 종괴가 폐와 뼈에서 발견되었다. 혈관육종의 호발부위를 살펴보면 9.5%가 몸통에, 3.6%가 뼈에서 발견되며, 폐에서 원발하는 경우는 더욱 드물다. 그리고 혈관육종은 진단 시에 이미 전이가 되어 있는 경우가 많으며, 주된 전이 부위는 폐, 간, 뼈, 림프절, 피부이다[5]. 이러한 역학적 특성을 바탕으로 다발성 폐전이 및 뼈전이를 동반한 십이지장에 발생한 원발성 혈관육종으로 진단할 수 있었다.
이번 증례처럼 혈관육종이 폐로 전이되는 경우 객혈, 기흉, 혈흉 등의 호흡기 증상을 일으킬 수도 있다. 혈관육종의 발생원인은 분명하지 않지만, 만성적인 림프부종, 이전에 수술적 치료 또는 방사선치료를 받은 병력, Vinyl chloride, Thorium dioxide, Arsenic과 같은 물질을 오랫동안 취급한 사람에서 혈관육종이 발생할 수 있다. 또 장기간 이물질 잔류, 유전적 요인 또한 혈관육종의 발생과 관련이 있다[7,8].
국내 1예, 국외 48예의 소장에 발생한 혈관육종에 대한 문헌들을 고찰해 보면 임상양상을 확인할 수 있었던 30명의 환자 중에서 16명이 위장관출혈 또는 빈혈이 주증상이었으며, 9명이 복통, 5명이 장폐쇄를 주증상으로 호소하였다. 치료 방법을 확인할 수 있었던 29명의 모든 환자들이 수술적 치료를 받았고, 그 중 7명에서 항암화학치료를 추가로 하였다. 30명 중에서 8명이 자궁경부암, 자궁암, 호지킨병, 골연골증의 치료로 하복부 또는 골반부위에 방사선치료를 받은 병력이 있었다[2,3].
2007년 Virtanen 등[9]이 보고한 방사선치료 이후에 발생한 몸통의 혈관육종에 대한 코호트연구를 검토해 보면, 몸통에 혈관육종이 발생한 모든 환자가 여성이었으며 모두 유방암 또는 여성생식기암의 치료로 방사선치료를 받았었다. 이 연구에서는 방사선치료와 혈관육종의 발생에 대해 명확한 연관성은 제시하지 못하였지만, 항암화학치료와 방사선치료를 병합할 시에 혈관육종의 발생 위험도가 증가하는 것으로 나타났다. 1948년 Cahan 등[10]은 방사선 치료 후 발생한 육종의 4가지 진단적 기준을 제시하였는데, 발생 부위의 방사선 조사의 과거력, 5년 이상의 잠복기, 방사선 조사 부위에서 기인한 악성 종양을 조직학적으로 증명, 방사선 조사 부위에 새로 발생한 종양은 과거에 방사선 치료를 받은 종양과 다른 조직소견을 가질 것이었다. 이번 증례는 남성 환자였고 10년 전 직장암으로 하복부에 항암화학치료 및 방사선치료를 받은 병력이 있었으나 혈관육종이 하복부에 원발하지 않아 Cahan 등[10]의 진단 기준에는 부합하지 않고, 유방암 또는 여성생식기암이 아닌 직장암의 치료 후에 혈관육종이 발생한 증례는 아직 보고되지 않았으므로 직장암에 대한 항암화학치료 및 방사선치료를 받은 병력과 십이지장 혈관육종 발생과의 연관성에 대해서는 추후 연구가 필요할 것으로 생각한다.
혈관육종은 과염색성의 핵과 호산구성 세포질로 이루어진 불룩하고 방추형의 다각형의 세포들로 둘러싸인 혈관들이 문합하는 조직소견이 관찰된다. 상피세포양 형태를 보일 경우 전이암종, 림프종, 악성 흑색종과 감별이 어렵기 때문에 정확한 진단을 위해서는 면역조직화학 검사가 필요하다[6]. 가장 특징적인 염색소견은 CD31, CD34, 제8인자와 같은 혈관 내피세포 표지자에 양성소견을 보이는 것으로 이번 증례에는 vimentin, CD31에 양성소견을 보여 혈관특성을 보이는 악성 중배엽 종양인 혈관육종으로 진단되었다.
혈관육종의 일반적인 치료는 광범위절제술 및 수술 후 방사선요법으로 알려져 있지만, 혈관육종의 공격적인 증식과 전이로 인해 수술적 완전절제는 대부분이 불가능하다. 최근 수술적 절제와 항암화학치료를 병합하는 방법이 주로 사용되지만 치료의 효과는 불분명하다[4].
일반적으로 혈관육종의 예후는 매우 불량하며 진단 후 단기간 내에 환자를 사망에 이르게 하는 공격적인 임상경과를 보이기 때문에 대부분 2년 이상 생존하지 못하며, 평균 생존기간은 2개월에서 6개월 정도이다. 또한, 몇몇의 연구에서 혈관육종의 침범 장기에 따라 예후가 다른 것으로 알려져 있다. 본 증례에서처럼 소장에 발생한 혈관육종의 예후는 타장기에 비해 불량하며, 대부분의 환자가 진단 후 수개월 내에 사망하거나, 수술 이후 사망한다. 나이, 종양의 크기, 후복강의 원발병소, 유사분열의 정도 등이 불량한 예후와 관련된 인자들이다[5].




 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






