ى„œ ë،
ى•Œë ˆë¥´ê¸° 비ى—¼ى€ 비강 ë‚´ ى—¼ى¦ë°کى‘ىœ¼ë،œ ى½§ë¬¼, ى½”막يک, ى¬ى±„기, ى½”ê°€ë ¤ى›€ 등ىک ى¦ىƒپى´ ë°œىƒي•کëٹ” ى§ˆي™کى´ë‹¤. ى›گى¸ى—گ ë”°ë¼ ى½”ى گ막ى—گى„œ ى¼ى–´ë‚کëٹ” IgE 매개ى„± ى—¼ى¦ ë°کى‘ى—گ ىکي•œ ى•Œë ˆë¥´ê¸° 비ى—¼ê³¼ ى´ى™€ ê´€ë ¨ى´ ى—†ëٹ” 비ى•Œë ˆë¥´ê¸° 비ى—¼ىœ¼ë،œ 구분ëگœë‹¤. ى•Œë ˆë¥´ê¸° 비ى—¼ىک ىœ ë³‘ë¥ ى€ ى „ى²´ ى¸êµ¬ىک ى•½ 10-25%ى—گ 달ي•کë©° ىµœê·¼ ى•Œë ˆë¥´ê¸° ى§ˆي™کى´ 급ى¦ي•کë©´ى„œ ى¦ê°€ى¶”ى„¸ë¥¼ ë³´ى´ê³ ىˆë‹¤. ى´ëں¬ي•œ 높ى€ ىœ ë³‘ë¥ ë،œ ى¸ي•کى—¬ 비ى—¼ى—گ 따른 ى‚¶ىک ى§ˆ ى €ي•کى™€ ىک료비 ى§€ى¶œى´ ى•ىœ¼ë،œ ى‚¬يڑŒê²½ى œى پى¸ 문ى œê°€ ëگ ىˆک ىˆë‹¤. ëکگي•œ ى²œى‹ ي™کىگىک ى•½ 60-80%ê°€ ى•Œë ˆë¥´ê¸° 비ى—¼ى´ ىˆىœ¼ë©°[1,2] ى•Œë ˆë¥´ê¸° 비ى—¼ ي™کىگىک ى•½ 20-40% ê°€ëں‰ى´ ى²œى‹ى„ ëڈ™ë°کي•کê³ ىˆë‹¤[3]. ë”°ë¼ى„œ 비ى—¼ ي™کىگى—گى„œ ى²œى‹ىک ëڈ™ë°ک ى—¬ë¶€ë¥¼ ي™•ى¸ي•کê³ ى پى ˆي•œ ى¹ک료를 ي•کëٹ” 것ى´ 매ىڑ° ى¤‘ىڑ”ي•ک다.
ي™کê²½ى،°ى ˆ
ى—¬ëں¬ ê°€ى§€ ي،ى… ى•Œë ˆë¥´ê²گ ى¤‘ى—گى„œëڈ„ ى§‘먼ى§€ى§„드기가 ى•Œë ˆë¥´ê¸° 비ى—¼ى—گى„œ ê°€ى¥ ى¤‘ىڑ”ي•œ ي•ى›گىœ¼ë،œ ى•Œë ¤ى ¸ ىˆë‹¤[4]. ê·¸ëں¬ë‚ک 대부분 비ى—¼ ي™کىگ를 대ىƒپىœ¼ë،œ ي•œ ى—°êµ¬ى—گى„œëٹ” ى§‘먼ى§€ى§„드기 ى•Œë ˆë¥´ê²گ يڑŒي”¼ë§Œىœ¼ë،œ ى„ىƒپى پى¸ يک¸ى „ى„ ىœ ë°œي• ى •ëڈ„ë،œ ىک미 ىˆëٹ” ى•Œë ˆë¥´ê²گ ىˆکى¹کê°گى†Œë¥¼ ë³´ى´ى§€ ى•ٹê³ ىˆىœ¼ë©°[5] 비ى—¼ى¦ىƒپى„ يک¸ى „ى‹œي‚¤ى§€ ى•ٹê³ ىˆë‹¤[6]. ê·¸ëں¬ë‚ک ى—¬ëں¬ 비ى—¼ى¹ک료ى§€ى¹¨ى—گى„œëٹ” ى•Œë ˆë¥´ê²گىک يڑŒي”¼ë¥¼ 권ى¥ي•کê³ ىˆë‹¤[7,8].
ى²œى‹ىک ê²½ىڑ°ى—گى„œëڈ„ ى§ˆë³‘ى،°ى ˆ ë°ڈ ى•½ë¬¼ ى‚¬ىڑ©ëں‰ى„ ê°گى†Œى‹œي‚¤ê¸° ىœ„ي•´ ى•Œë ˆë¥´ê²گ يڑŒي”¼ ë°ڈ ي™کê²½ى،°ى ˆى„ 권ى¥ي•کê³ ىˆë‹¤. ê·¸ëں¬ë‚ک ى²œى‹ىک ê²½ىڑ°ëٹ” ي™کê²½ى،°ى ˆى„ ي†µي•´ ى•Œë ˆë¥´ê²گ ىˆکى¹ک를 ê°گى†Œى‹œى¼œ يٹ¹يˆ ى†Œى•„ى—گى„œëٹ” ى„ىƒپى پ يک¸ى „ى„ 기대ي• ىˆک ىˆë‹¤[5,9].
ى•½ë¬¼ى¹ک료
비ى—¼ ى¹ک료ى—گ ى‚¬ىڑ©ëگکëٹ” ى•½ى œëٹ” 대부분 경구ىڑ© يک¹ى€ 비강 ë‚´ë،œ يˆ¬ى—¬ي•œë‹¤. 비강 ë‚´ يˆ¬ى—¬ë°©ى‹ى€ ى•½ى œê°€ 비강 ë‚´ى—گ ى§پى ‘ ى „달ëگکى–´ 높ى€ ë†چëڈ„를 ىœ ى§€ي• ىˆک ىˆê³ ى „ى‹ 부ى‘ىڑ©ى„ ىµœى†Œي™”ي•œë‹¤ëٹ” ى¥ى گى´ ىˆë‹¤. 대부분ىک ى•Œë ˆë¥´ê¸° 비ى—¼ ي™کىگ들ى€ ى•Œë ˆë¥´ê¸°ê²°ë§‰ى—¼ يک¹ى€ ى²œى‹ى„ ëڈ™ë°کي•کëٹ” ê²½ىڑ°ê°€ ë§ژىœ¼ë¯€ë،œ ى´ë¥¼ ê³ ë ¤ي•کى—¬ ى•½ى œë¥¼ ى„ يƒي•کëڈ„ë، ي•œë‹¤(Table 1).
ي•يˆىٹ¤يƒ€ë¯¼ى œ
ي•يˆىٹ¤يƒ€ë¯¼ى œëٹ” H1ىˆکىڑ©ى²´ 길ي•ى œë،œ, ي‘œى پى„¸يڈ¬ىک يˆىٹ¤يƒ€ë¯¼ ىˆکىڑ©ى²´ى—گ ê²½ىںپى پىœ¼ë،œ ى‘ىڑ©ي•کى—¬ يˆىٹ¤يƒ€ë¯¼ىک ê²°ي•©ى„ 막ëٹ” ى—ي• ى„ ي•œë‹¤. 비ى—¼ى—گى„œىک ي•يˆىٹ¤يƒ€ë¯¼ى œëٹ” ى½§ë¬¼, ى¬ى±„기, ى½”ê°€ë ¤ى›€ى—گ يڑ¨ê³¼ى پى´ë‹¤.
1ى„¸ëŒ€ ي•يˆىٹ¤يƒ€ë¯¼ى œ
1ى„¸ëŒ€ ي•يˆىٹ¤يƒ€ë¯¼ى œëٹ” ى¤‘ى¶”ى‹ 경계ىک H1ىˆکىڑ©ى²´ى—گ ى‘ىڑ©ي•کى—¬ ى،¸ë¦¼, ى–´ى§€ëں¬ى›€, ë¬´ë ¥ê°گ 등 부ى‘ىڑ©ى´ ë‚کيƒ€ë‚ ىˆک ىˆë‹¤. 변비, ى„¤ى‚¬, ë©”ىٹ¤ê؛¼ى›€, 구ي† 등ىک ى†Œي™”ى¥ى• ê°€ ë°œىƒي• ىˆک ىˆىœ¼ë©° ي•ى½œë¦°, ي•ë¬´ىٹ¤ى¹´ë¦°ى„± يڑ¨ê³¼ى—گ ë”°ë¼ ë‹¤ى–‘ي•œ ى •ëڈ„ىک ى گ막건ى،°, ى‹œë ¥يگë ¤ى§گ, 변비, 배뇨곤ë€, 빈맥, 발기부ى „ 등ى´ ë‚کيƒ€ë‚ ىˆک ىˆë‹¤. ê·¸ëں¬ë¯€ë،œ 1ى„¸ëŒ€ ي•يˆىٹ¤يƒ€ë¯¼ى œë¥¼ 당뇨병, 녹내ى¥, ى „립ى„ 비대, ى‹¬ى¥ ى§ˆي™کى´ ىˆëٹ” ي™کىگى—گ게 ى²کë°©ي•کëٹ” 것ى€ ى£¼ىک를 ىڑ”ي•œë‹¤. ي•يˆىٹ¤يƒ€ë¯¼ى œëٹ” ى¤‘ى¶”ى‹ ê²½ ى–µى œى œى¸ ى•Œى½”ىک¬, barbiturates, 기يƒ€ ى§„ى •ى œى™€ىک 병ىڑ© ى‹œ ى£¼ىک를 ىڑ”ي•کê³ MAO ى–µى œى œى¸ iproniazid, phenelzine를 يˆ¬ى—¬ي•کëٹ” ي™کىگى—گى„œëٹ” 금기ى´ë‹¤.
2ى„¸ëŒ€ ي•يˆىٹ¤يƒ€ë¯¼ى œ
2ى„¸ëŒ€ ي•يˆىٹ¤يƒ€ë¯¼ى œëٹ” blood brain barrier (BBB)를 ى‰½ê²Œ ي†µê³¼ي•کى§€ ى•ٹى•„ ى¤‘ى¶”ى‹ 경계ىک H1 ىˆکىڑ©ى²´ى—گ 대ي•œ ê²°ي•©ë ¥ى´ ى•½ي•کى—¬ 1ى„¸ëŒ€ ي•يˆىٹ¤يƒ€ë¯¼ى œى—گ 비ي•کى—¬ ى§„ى •ى‘ىڑ©ى´ ى پى€ يژ¸ى´ë‹¤. ي•کى§€ë§Œ fexofenadineى„ ى œى™¸ي•œ ëھ¨ë“ ى•½ë¬¼ى—گى„œ BBB를 ي†µê³¼ي• ىˆکëٹ” ىˆىœ¼ë¯€ë،œ ي™کىگى—گ ë”°ë¼ى„œ ى§„ى •ى‘ىڑ©ى„ ë³´ى´ê¸°ëڈ„ ي•کë©° cetirizineىک ê²½ىڑ° 11-14% ي™کىگى—گى„œ ى§„ى •ى‘ىڑ©ى„ ë³´ى´ëٹ” 것ىœ¼ë،œ ى•Œë ¤ى ¸ ىˆë‹¤. ي•ى½œë¦°ى„± يڑ¨ê³¼ê°€ ى پىœ¼ë¯€ë،œ 당뇨병, 녹내ى¥, ى „립ى„ 비대, ى‹¬ى¥ ى§ˆي™کى´ ىˆëٹ” ي™کىگى—گى„œëڈ„ 비êµگى پ ى•ˆى „ي•ک게 ى‚¬ىڑ©ي• ىˆک ىˆë‹¤. ë”°ë¼ى„œ 2ى„¸ëŒ€ ي•يˆىٹ¤يƒ€ë¯¼ى œë¥¼ 1ى„¸ëŒ€ ي•يˆىٹ¤يƒ€ë¯¼ى œë³´ë‹¤ 먼ى € ى‚¬ىڑ©ي• 것ى„ 권ى¥ي•کê³ ىˆë‹¤[10].
비강ىڑ© ي•يˆىٹ¤يƒ€ë¯¼ى œ
비강ىڑ© ي•يˆىٹ¤يƒ€ë¯¼ى œëٹ” 경구ىڑ© ي•يˆىٹ¤يƒ€ë¯¼ى œى™€ 달리 ى½”막يکى—گëڈ„ يڑ¨ê³¼ê°€ ىˆë‹¤. ي”ي•œ 부ى‘ىڑ©ىœ¼ë،œ ى“´ë§›ى´ ë‚کê³ (19.7%) ى²´ë‚´ë،œëڈ„ ي،ىˆکëگکى–´ ى§„ى •ى‘ىڑ©(11.5%)ى„ ë‚کيƒ€ë‚¼ ىˆک ىˆë‹¤.
ى¹ک료ى§€ى¹¨ى—گى„œëٹ” 계ى ˆى„± ى•Œë ˆë¥´ê¸° 비ى—¼ ي™کىگى—گى„œ 경구ىڑ© 2ى„¸ëŒ€ ي•يˆىٹ¤يƒ€ë¯¼ى œë¥¼ 비강 ë‚´ ي•يˆىٹ¤يƒ€ë¯¼ى œë³´ë‹¤ ى¶”ى²œي•œë‹¤[10].
비강ىڑ© ىٹ¤ي…Œë،œى´ë“œى œ
비강 ë‚´ ىٹ¤ي…Œë،œى´ë“œى œ ى‚¬ىڑ©ى€ ى „ى‹ 부ى‘ىڑ©ىک ë°œىƒ ê°€ëٹ¥ى„±ى„ ىµœى†Œي™”ي•کë©´ى„œ 비강 ى گ막ىک ى•½ë¬¼ë†چëڈ„를 높게 ىœ ى§€ي• ىˆک ىˆëٹ” 방법ى´ë‹¤. ى´ëٹ” ى•Œë ˆë¥´ê¸° 비ى—¼ ى¦ىƒپë؟گ만 ى•„ë‹ˆë¼ ى•ˆêµ¬ ى¦ىƒپëڈ„ ê°™ى´ يک¸ى „ى‹œي‚¬ ىˆک ىˆë‹¤[11]. ى½”막يک ى¦ىƒپى„ يک¸ى „ى‹œي‚¤ëٹ”ëچ° 비강 ë‚´ ىٹ¤ي…Œë،œى´ë“œى œى œê°€ ى¼ى°¨ ى•½ى œë،œى„œ 다른 ى•½ى œë³´ë‹¤ يڑ¨ê³¼ى پى´ë‹¤. 비강 ë‚´ ىٹ¤ي…Œë،œى´ë“œى œëٹ” 부ى‘ىڑ©ى´ ىƒپ대ى پىœ¼ë،œ ى پê³ ى¥ê¸°ى پىœ¼ë،œ ى‚¬ىڑ©ي•کëچ”ë¼ëڈ„ 비강ى گ막ىک ىœ„ى¶•ى„ ىœ ë°œي•کى§€ ى•ٹىœ¼ë©° 경구 ىٹ¤ي…Œë،œى´ë“œى œë¥¼ ى‚¬ىڑ©ي• ë•Œ ê³ ë ¤ي•´ى•¼ي•کëٹ” 부ى‘ىڑ©ى´ ê±°ىک ى—†ى–´ ى•ˆى „ي•ک게 ى‚¬ىڑ©ي• ىˆک ىˆë‹¤. ى†Œى•„ى—گى„œ ى‚¬ىڑ©ي•کëٹ” ي،ى…ىڑ© ىٹ¤ي…Œë،œى´ë“œê°€ ىµœى¢…ى پىœ¼ë،œ ى„±ى¥ى§€ى—°ى„ ى¼ىœ¼ي‚¨ë‹¤ëٹ” ë³´ê³ ê°€ ىµœê·¼ى—گ ىˆى—ˆë‹¤[12]. ê·¸ëں¬ë‚ک 비강 ë‚´ ىٹ¤ي…Œë،œى´ë“œى—گى„œëٹ” 1ë…„ê°„ 단기 ى—°êµ¬ى´ى§€ë§Œ ى„±ى¥ى§€ى—°ى´ ى—†ى—ˆë‹¤ëٹ” ى—°êµ¬ 결과가 ىˆى—ˆë‹¤[13].
ë”°ë¼ى„œ ى¹ک료ى§€ى¹¨ى—گى„œëٹ” ى„±ى¸ ى•Œë ˆë¥´ê¸° 비ى—¼ىک ى¹ک료ى œë،œ 비강 ë‚´ ىٹ¤ي…Œë،œى´ë“œë¥¼ ê°•ë ¥يˆ ى¶”ى²œي•کë©° 경구 ë¥کى½”يٹ¸ë¦¬ى—”ى–µى œى œë³´ë‹¤ 권ى¥ي•œë‹¤[10].
ë¥کى½”يٹ¸ë¦¬ى—”ى–µى œى œ
ë¥کى½”يٹ¸ë¦¬ى—”ى–µى œى œëٹ” ى•Œë ˆë¥´ê¸° 비ى—¼ ë°ڈ 결막ى—¼ ى¦ىƒپ ê°œى„ ى—گ يڑ¨ê³¼ê°€ ىˆë‹¤. ë¥کى½”يٹ¸ë¦¬ى—”ى–µى œى œى™€ ي•يˆىٹ¤يƒ€ë¯¼ى œىک 병ي•©ىڑ”법과 ë¥کى½”يٹ¸ë¦¬ى—”ى–µى œى œ 단ى¼ىڑ”법ى—گ 비ي•´ ى¶”ê°€ى پى¸ ى´ë“ى´ 별ë،œ ى—†ى–´ 계ى ˆى„± ى•Œë ˆë¥´ê¸° 비ى—¼ ي™کىگى—گى„œëٹ” ي•يˆىٹ¤يƒ€ë¯¼ى œ 단ëڈ…ىڑ”법ى´ ى¼ى°¨ى پىœ¼ë،œ 권ى¥ëگœë‹¤.
ëکگي•œ ى•Œë ˆë¥´ê¸° 비ى—¼ê³¼ ى²œى‹ى´ ëڈ™ى‹œى—گ ىˆëٹ” ي™کىگى—گى„œ ë¥کى½”يٹ¸ë¦¬ى—”ى–µى œى œë¥¼ ى‚¬ىڑ©ي•کë©´ ى½” ى¦ىƒپë؟گ만 ى•„ë‹ˆë¼ ê¸°ê´€ى§€ ى¦ىƒپى„ يک¸ى „ى‹œي‚¨ë‹¤. ى¼ë¶€ ê°€ى´ë“œë¼ى¸ى—گى„œëٹ” 비ى—¼ى´ ëڈ™ë°کëگœ ê²½ي•œ ى²œى‹ ي™کىگى—گى„œ ى¼ى°¨ ى•½ى œë،œ ë¥کى½”يٹ¸ë¦¬ى—”ى–µى œى œ 단ëڈ…ى‚¬ىڑ©ى„ 권ىœ ي•ک기ëڈ„ ي•œë‹¤[14]. ê·¸ëں¬ë‚ک 2010ë…„ ê°œى •ëگœ ARIA ى§€ى¹¨ى—گى„œëٹ” ى²œى‹ ى¹ک료 ëھ©ى پىک 단ى¼ى œى œë،œëٹ” ي،ى…ىٹ¤ي…Œë،œى´ë“œى œê°€ 경구ىڑ© ë¥کى½”يٹ¸ë¦¬ى—”ى œë³´ë‹¤ ىڑ°ى›”ي•کë‹¤ê³ ê¶Œê³ ي•کê³ ىˆë‹¤[10].
يکˆê´€ىˆکى¶•ى œ
ى•Œë ˆë¥´ê¸° يک¹ى€ 비ى•Œë ˆë¥´ê¸° 비ى—¼ى—گى„œ ى½”막يکىک ى¹ک료를 ىœ„ي•´ى„œ 단기간 비강 ë‚´ يکˆê´€ىˆکى¶•ى œë¥¼ ى‚¬ىڑ©ي•کëٹ” 것ى€ يڑ¨ê³¼ى پى´ë‹¤. ê·¸ëں¬ë‚ک ى½”ê°€ë ¤ى›€ى´ë‚ک, ى¬ى±„기, ى½§ë¬¼ى—گëٹ” يڑ¨ê³¼ê°€ ى—†ë‹¤. 비강 ë‚´ يکˆê´€ىˆکى¶•ى œë¥¼ ى¥ê¸°ê°„(10ى¼ ى´ىƒپ) ى‚¬ىڑ©ي• ê²½ىڑ°ى—گëٹ” ë°کëڈ™ى„± 비강ى گ막 부ى¢…ى„ ى¼ىœ¼ي‚¬ ىˆک ىˆë‹¤(rhinitis mediamentosa, drug-induced rhinitis, rebound rhinitis) [15].
경구ىڑ© يکˆê´€ىˆکى¶•ى œë،œëٹ” ephedrine, phenylephrine, phenylpropanolamine 등ى´ ىˆىœ¼ë©° يٹ¹يˆ pseudoephedrineى´ 경구 يکˆê´€ىˆکى¶•ى œë،œ ê°€ى¥ ë§ژى´ ى“°ى´ê³ ىˆë‹¤. ى „ى‹ ى پى¸ 부ى‘ىڑ©ى€ 드물ى§€ ى•ٹىœ¼ë©° 불ى•ˆ, ى–´ى§€ëں¬ى›€, ë‘گي†µ, ى†گ떨림, 불면, ى‹¬ê³„ي•ى§„, ê³ يکˆى•• 등ى´ ىˆë‹¤. 녹내ى¥ى´ë‚ک ê°‘ىƒپى„ ي•ى§„ى¦ى´ ىˆëٹ” ي™کىگ, ى „립ى„ 비대ى¦ىœ¼ë،œ ى†Œë³€ى €ë¥کê°€ ىˆëٹ” ê³ ë ¹ ي™کىگى—گى„œëٹ” ى£¼ىکي•کى—¬ى•¼ ي•œë‹¤.
경구ىڑ© يکˆê´€ىˆکى¶•ى œى™€ ي•يˆىٹ¤يƒ€ë¯¼ى œ ë³µي•©ى œى œëٹ” ë§ژى´ ى‚¬ىڑ©ëگکê³ ىˆىœ¼ë©° يٹ¹يˆ pseudoephedrineى´ ي•يˆىٹ¤يƒ€ë¯¼ê³¼ ë³µي•©ى œى œë،œ ي”يˆ ى‚¬ىڑ©ëگکê³ ىˆë‹¤. ى´ëٹ” ى¬ى±„기, ى½§ë¬¼ ى™¸ى—گëڈ„ ى½”막يکى„ يک¸ى „ى‹œي‚¬ ىˆک ىˆë‹¤. ëکگي•œ ibuprofenê³¼ pseudoephedrine, chlorpheniramine ë³µي•©ى‚¬ىڑ©ى´ ى•Œë ˆë¥´ê¸° 비ى—¼ىک ى¦ىƒپê°œى„ ى—گ 부가ى پى¸ يڑ¨ê³¼ê°€ ىˆىŒى´ ë³´ê³ ëگکى—ˆë‹¤[16].
ë©´ى—ىڑ”법
ى•Œë ˆë¥´ê¸° ë©´ى—ىڑ”법ى€ ى•Œë ˆë¥´ê¸° ي™کىگى—گ게 ى›گى¸ ى•Œë ˆë¥´ê²گى„ ى گى§„ى پىœ¼ë،œ يˆ¬ى—¬ي•کى—¬ ى•Œë ˆë¥´ê²گى—گ 대ي•œ ë‚´ى„±ى„ ىœ ë°œي•کى—¬ ى§ˆي™کىک 경과를 변경ى‹œي‚¤ëٹ” 방법ى´ë‹¤. ى•Œë ˆë¥´ê¸° 비ى—¼ ي™کىگى—گى„œ ë©´ى—ىڑ”법ى€ 3ë…„ ى´ىƒپ ى¶©ë¶„ي•œ 기간 ëڈ™ى•ˆ ى¹ک료ي•کë©´ ى¤‘단 ي›„ى—گëڈ„ ى¹ک료يڑ¨ê³¼ê°€ ى§€ى†چëگکë©°[17] ي–¥ي›„ ى²œى‹ىœ¼ë،œ ى§„ي–‰ëگکëٹ” ىœ„ي—کى„ ى¤„ى—¬ ى£¼ê³ [18] ىƒˆë،œىڑ´ ى•Œë ˆë¥´ê²گى—گ ê°گى‘ëگکëٹ” 것ى„ ىکˆë°©ي• ىˆک ىˆë‹¤[19].
ى•Œë ˆë¥´ê¸° 비ى—¼ى—گ ى‚¬ىڑ©ëگکëٹ” ë©´ى—ىڑ”법ى€ يˆ¬ى—¬ê²½ë،œى—گ ë”°ë¼ ي”¼ي•کë©´ى—ىڑ”법과 ى„¤ي•کë©´ى—ىڑ”법ىœ¼ë،œ ë‚ک뉜다.
ë©´ى—ىڑ”법 대ىƒپ ي™کىگ ى„ ى •
ë©´ى—ىڑ”법ى€ ى›گى¸ ى•Œë ˆë¥´ê²گى—گ ىکي•œ IgE ë°کى‘ê³¼ ى„ىƒپى¦ىƒپê³¼ىک ى—°ê´€ى„±ى´ ي™•ى‹¤ي•œ ي™کىگ를 대ىƒپىœ¼ë،œ ي•œë‹¤[20]. ى›گى¸ ى•Œë ˆë¥´ê²گى€ ي”¼ë¶€ë‹¨ىگى‹œي—ک ëکگëٹ” يکˆى² ë‚´ يٹ¹ى´ IgE ي•ى²´ ى¸،ى •ىœ¼ë،œ يŒگ단ي•کë‚ک ى‹¤ى œ ى¦ىƒپê³¼ىک ى—°ê´€ى„±ى´ ى—†ëٹ” ê²½ىڑ°ëڈ„ ë§ژىœ¼ë¯€ë،œ ى„ىƒپى پ يŒگ단ى´ ى¤‘ىڑ”ي•ک다.
ë©´ى—ىڑ”법ىک ى ˆëŒ€ى پ 금기ى¦ىœ¼ë،œëٹ” â‘ ى‹¬ي•œ ى „ى‹ ë©´ى— ى§ˆي™کى´ë‚ک ى•…ى„±ى¢…ى–‘ى„ ى•“ê³ ىˆëٹ” ê²½ىڑ°, â‘، 부ى‘ىڑ© ë°œىƒ ى‹œ ى‘급ى²کى¹کë،œ ى‚¬ىڑ©ëگکëٹ” ى—گي”¼ë„¤ي”„린ى„ ى‚¬ىڑ©ي• ىˆک ى—†ëٹ” ي™کىگ, ىکˆë¥¼ 들ى–´ ê´€ىƒپëڈ™ë§¥ ى§ˆي™کى´ë‚ک ى‹¬ي•œ ê³ يکˆى••ىœ¼ë،œ ë² يƒ€ى°¨ë‹¨ى œë¥¼ 매ى¼ ë³µىڑ©ي•´ى•¼ ي•کëٹ” ê²½ىڑ°, â‘¢ ي™کىگىک ىˆœى‘ëڈ„ê°€ ë‚کىپœ ê²½ىڑ°ى´ë‹¤. ىƒپ대ى پ 금기ى¦ىœ¼ë،œëٹ” â‘ 5ى„¸ 미만ىک ىکپىœ ى•„ ي™کىگ, â‘، ى¤‘ى¦ ى²œى‹ي™کىگ, â‘¢ ى„ى‹ ى¤‘ى—گ ë©´ى—ىڑ”법ى„ ى‹œى‘ي•کëٹ” 것 등ى´ ىˆë‹¤[20].
ë©´ى—ىڑ”법 대ىƒپ ى•Œë ˆë¥´ê²گ ى„ ى •
ىµœê·¼ê¹Œى§€ ى´ى¤‘맹검 대ى،°ى—°êµ¬ë¥¼ ي†µي•کى—¬ ë©´ى—ىڑ”법ىک يڑ¨ëٹ¥ى´ ëھ…ي™•ي•ک게 ى…ى¦ëگœ ى•Œë ˆë¥´ê²گىœ¼ë،œëٹ” 꽃가루(ى”ë””, ëڈ¼ى§€ي’€ë¥ک, ىگى‘ë‚ک무, ى‘¥, ê°œىژê°ˆë‚ک무)ى™€ ى§‘먼ى§€ى§„드기, ë°”ي€´, 곤ى¶©ëڈ…, ê·¸ë¦¬ê³ ê³°يŒ،ى´(Alternaria, Cladosporium)ى—گى„œ ىœ ىکي•œ يڑ¨ê³¼ê°€ ى…ى¦ëگکى—ˆىœ¼ë©°, ëڈ™ë¬¼ ى•Œë ˆë¥´ê²گىک ê²½ىڑ°ى—گëٹ” ê³ ى–‘ى´ ي„¸, ê°œ 비듬ى´ ىˆë‹¤. ë”°ë¼ى„œ ى•Œë ˆë¥´ê¸° ي”¼ë¶€ë‹¨ىگى‹œي—ک ë°ڈ يکˆى² يٹ¹ى´ IgE ê²€ى‚¬ ê²°ê³¼ى™€ ي•¨ê»ک ë³‘ë ¥ىƒپ ي™کىگى—گ게 ى„ىƒپى پىœ¼ë،œ ىک미를 ê°€ى§€ëٹ” ي•œ ى¢…ë¥ک يک¹ى€ ê°€ëٹ¥ي•œ ى†Œىˆکىک ى•Œë ˆë¥´ê²گىœ¼ë،œ ë©´ى—ىڑ”법ى„ ى‹¤ى‹œي•کëٹ” 것ى´ ë°”ëŒى§پي•ک다. ëکگي•œ ى—¬ëں¬ ى¢…ë¥کىک 꽃가루ى—گ ëڈ™ى‹œى—گ ê°گى‘ëگœ ê²½ىڑ°ëٹ” ي•ى›گê°„ىک êµگى°¨ ي•ى›گى„±ى„ ê³ ë ¤ي•کى—¬ ي•ى›گى„ ى„ يƒي•کëڈ„ë، ي•œë‹¤.
ىڑ°ë¦¬ë‚کë¼ى—گى„œ ى¤‘ىڑ”ي•œ ى•Œë ˆë¥´ê²گ
ىڑ°ë¦¬ë‚کë¼ ي™کê²½ى—گى„œ ى¤‘ىڑ”ي•œ ي،ى… ى•Œë ˆë¥´ê²گىœ¼ë،œëٹ” ى§‘먼ى§€ى§„드기(D. farinae, D. pteronyssinus), ى،ى´ˆ 꽃가루, ىˆکëھ© 꽃가루, ى”ë”” 꽃가루 등ى´ ىˆىœ¼ë©°[21] ë©´ى—ىڑ”법ى—گ يڈ¬ي•¨ي• ىˆک ىˆë‹¤[22-24].
ى§‘먼ى§€ى§„드기ëٹ” êµë‚´ ى—°êµ¬ى—گى„œ ê°€ى¥ ë§ژى´ ë©´ى—ىڑ”법ىک يڑ¨ê³¼ê°€ ë³´ê³ ëگœ ى•Œë ˆë¥´ê²گى´ë©° 다ىŒىœ¼ë،œëٹ” 꽃가루 ى•Œë ˆë¥´ê²گى´ ىˆë‹¤. êµë‚´ى—گى„œëٹ” 계ى ˆى—گ ë”°ë¼ 3-5ى›”ى—گ ىˆکëھ©ë¥ک(ى°¸ë‚ک무, ىک¤ë¦¬ë‚ک무, ىگى‘ë‚ک무), 5-9ى›” ى”ë””ë¥ک, 8-10ى›” ى،ى´ˆë¥ک(ى‘¥, ëڈ¼ى§€ي’€) 꽃가루가 ى£¼ë،œ ê´€ى°°ëگœë‹¤[25]. ëکگي•œ ىµœê·¼ ى• ى™„ëڈ™ë¬¼ى—گ ىکي•œ ى•Œë ˆë¥´ê¸° ى§ˆي™کى´ يپ° 문ى œë،œ 대ë‘گëگکê³ ىˆى–´ يڑŒي”¼ê°€ ى–´ë ¤ىڑ¸ ê²½ىڑ° ëڈ™ë¬¼ ى•Œë ˆë¥´ê²گëڈ„ ë©´ى—ىڑ”법ى—گ يڈ¬ي•¨ى‹œي‚¤ëٹ” 것ى´ ى¢‹ê² 다. ë”°ë¼ى„œ ىڑ°ë¦¬ë‚کë¼ى—گى„œëٹ” ى§‘먼ى§€ى§„드기, 꽃가루 ë°ڈ ëڈ™ë¬¼ ى•Œë ˆë¥´ê²گ 등ى´ ë©´ى—ىڑ”법ى„ ى‹œي–‰ي•کëٹ” ى¤‘ىڑ”ي•œ ى•Œë ˆë¥´ê²گى´ ëگکê² ë‹¤[26].
ى„¤ي•کë©´ى—ىڑ”법
ىµœى پىڑ©ëں‰(ê³ ىڑ©ëں‰)ىک ى„¤ي•کë©´ى—ىڑ”법ى€ ى„±ى¸ê³¼ ى†Œى•„ىک ى•Œë ˆë¥´ê¸° 비ى—¼ى—گ يڑ¨ê³¼ى پى´ë‹¤[27-31]. ى„¤ي•کë©´ى—ىڑ”법ى€ يک€ ë°‘ى—گ ى•Œë ˆë¥´ê²گ ى¶”ى¶œى•،ى„ 1-2분 ëڈ™ى•ˆ ë¨¸ê¸ˆê³ ىˆë‹¤ê°€ ى‚¼ي‚¤ëٹ” 방법ى´ ى¼ë°کى پى´ë©° ى´ˆê¸°ى—گ ى•Œë ˆë¥´ê²گىک ىڑ©ëں‰ى„ ىک¬ë¦¬ëٹ” ى¦ëں‰ë‹¨ê³„를 ê±°ى³گ ى پى ˆي•œ ىœ ى§€ىڑ©ëں‰ىœ¼ë،œ ىœ ى§€ي•œë‹¤.
ى„¤ي•کë©´ى—ىڑ”법ى€ ê³ ىڑ©ëں‰ى´ëچ”ë¼ëڈ„ ى•ˆى „ي•کë©° ى¤‘대ي•œ 부ى‘ىڑ©ى´ ى پ다[32-34]. ëکگي•œ ى„¤ي•کë©´ى—ىڑ”법ى€ ي™کىگê°€ ىٹ¤ىٹ¤ë،œ ى§‘ى—گى„œ يˆ¬ى—¬ي•ک므ë،œ, ى²کë°©ي•کëٹ” ىکى‚¬ëٹ” 부ى‘ىڑ© ë°œىƒ ى‹œ 대ى²ک방법ى´ë‚ک يˆ¬ى—¬ë¥¼ ëھ»ي–ˆى„ ë•Œىک ىڑ©ëں‰ى،°ى • 등ى—گ 대ي•œ ي™کىگêµگىœ،ى„ 미리 ى‹œي–‰ي•کى—¬ى•¼ ي•œë‹¤.
ي• IgE ى¹ک료
ي• IgE (recombinant, humanized, monoclonal anti-IgE; Omalizumab) ي•ى²´ëٹ” ىœ 리 IgEى™€ ë³µي•©ى²´ë¥¼ 만들ى–´ 비만ى„¸يڈ¬ ë°ڈ يک¸ى—¼ê¸°êµ¬ى™€ IgE ىک ê²°ي•©ى„ ë°©ي•´ي•کê³ ىœ 리 IgE를 ë‚®ى¶”ëٹ” ى‘ىڑ©ى„ ي•œë‹¤[35]. omalizumabى€ يکˆى² ë‚´ ىœ 리 IgE ىˆکى¹ک를 ë‚®ى¶”ى–´ ى£¼ ى¦ىƒپى„ ى¤„ى—¬ى£¼ê³ ى‚¶ىک ى§ˆى„ ي–¥ىƒپى‹œي‚¨ë‹¤[36]. يٹ¹يˆ ى²œى‹ê³¼ 비ى—¼ى´ ëڈ™ى‹œى—گ ىˆëٹ” ي™کىگى—گى„œ omalizumabى„ ى‚¬ىڑ©ي•کë©´ ى½”ى¦ىƒپ ë°ڈ 기관ى§€ ى¦ىƒپى„ ëھ¨ë‘گ ê°œى„ ى‹œي‚¤ë©° ى²œى‹ى•…ي™”를 ىکˆë°©ي• ىˆک ىˆë‹¤[37]. ê·¸ëں¬ë‚ک ىڑ°ë¦¬ë‚کë¼ى—گى„œëٹ” ى¤‘ى¦ ى²œى‹ ي™کىگى—گى„œë§Œ omalizumab ى¹ک료가 ى¸ى •ëگکê³ ىˆىœ¼ë©° ى•Œë ˆë¥´ê¸° 비ى—¼ىک ى¹ک료ë،œëٹ” 권ى¥ëگکى§€ ى•ٹëٹ”다. ي•کى§€ë§Œ ى²œى‹ê³¼ 비ى—¼ى´ ëھ¨ë‘گ ىˆê³ ëھ…ë°±ي•œ IgE ê´€ë ¨ى„±ى´ ىˆىœ¼ë©° ى پى ˆي•œ ى²œى‹ ى¹ک료ى—گëڈ„ ى،°ى ˆى´ ىک ëگکى§€ ى•ٹëٹ” ê²½ىڑ°ى—گëٹ” ى²œى‹ىک ى¹ک료 ëھ©ى پىœ¼ë،œ Omalizumabى¹ک료를 ê³ ë ¤ي• ىˆک ىˆىœ¼ë©°[10] 부가ى پى¸ 비ى—¼ ى¦ىƒپ ê°œى„ ى—گëڈ„ يڑ¨ê³¼ë¥¼ 기대ي• ىˆک ىˆê² 다.
ىˆکىˆ ى پ ى¹ک료
ىˆکىˆ ى€ ى•Œë ˆë¥´ê¸° ى§ˆي™ک ىگى²´ë¥¼ ى¹ک료ي•کëٹ” ëچ°ëٹ” ëڈ„ى›€ى´ ëگکى§€ ى•ٹىœ¼ë‚ک 비갑개비ي›„, ى—°ê³¨ يک¹ى€ 뼈ى—گ ىکي•œ ىƒپ기ëڈ„يڈگى‡„ 등ى„ ى¹ک료ي•کëٹ”ëچ° ىˆکىˆ ى´ ëڈ„ى›€ى´ ëگک기ëڈ„ ي•œë‹¤(Table 2).
ى¹ک료ى§€ى¹¨
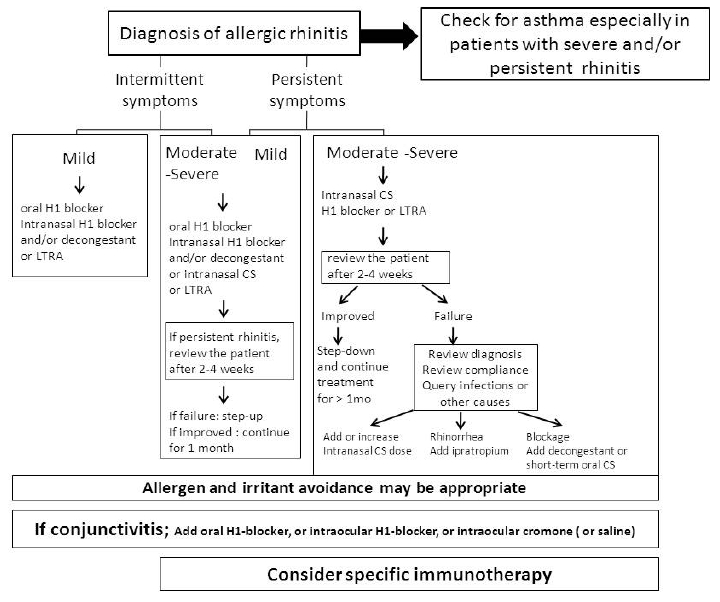
비ى—¼ ى¹ک료ى§€ى¹¨ى¸ ARIA (Allergic Rhinitis and its Impact on Asthma)ى—گى„œëٹ” ى¹ک료방ى¹¨ى„ 다ىŒê³¼ ê°™ى´ ى œى‹œي•کê³ ىˆë‹¤(Fig. 1).
ê²° ë،
ى•Œë ˆë¥´ê¸° 비ى—¼ى€ ى›گى¸ ى•Œë ˆë¥´ê²گى„ ê·œëھ…ي•کى—¬ ي™کê²½ى،°ى ˆى„ ي†µي•کى—¬ يڑŒي”¼ي•کê³ ى•½ë¬¼ى¹ک료를 ي†µي•´ ىƒپ기ëڈ„ى—¼ى¦ى„ ى™„ي™”ى‹œى¼œ ى¹ک료ي•کëٹ” ë‚´ê³¼ى پ ى§ˆي™کى´ë‹¤. ى•Œë ˆë¥´ê¸° 비ى—¼ ي™کىگى—گى„œ ى²œى‹ى„ ëڈ™ë°کي•کê³ ىˆëٹ” ê²½ىڑ°ê°€ ë§ژىœ¼ë¯€ë،œ ى²œى‹ى—¬ë¶€ë¥¼ ي™•ى¸ي•کëٹ” 것ى´ ى¹ک료ى—گ ى¤‘ىڑ”ي•کë©° ى پى ˆي•œ ى•½ë¬¼ى¹ک료 ë°ڈ ë©´ى—ى¹ک료 등ى„ ي†µي•کى—¬ ى¦ىƒپê°œى„ ë°ڈ ى•½ë¬¼ ى‚¬ىڑ©ëں‰ى„ ê°گى†Œى‹œى¼œ ى‚¶ىک ى§ˆى„ ê°œى„ ى‹œي‚¬ ىˆک ىˆë‹¤.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






