서 론
종양괴사인자 억제제는 자가면역질환 특히 류마티스 관절염(Rheumatoid arthritis, RA)과 강직성 척추염에서 폭넓게 쓰이며 대표적인 부작용은 결핵 및 기회감염의 증가이다[1]. 미만성 폐포 출혈은 감염 없이 폐의 소혈관에서 폐포 내로 출혈을 일으켜 호흡곤란 및 저산소증을 일으키고 양폐야에서 광범위한 침윤을 일으켜 사망률을 높이는 주의를 요하는 합병증이다[2]. 이를 일으키는 주요 원인으로는 면역학적 원인 이외에 약물에 의한 직접 독성 등의 원인이 있으나 아직까지 adalimumab에 의한 미만성 폐포 출혈의 보고는 없다. 저자들은 RA 치료로 종양괴사인자 억제제 중 하나인 adalimumab 투여 중 미만성 폐포 출혈이 생긴 증례를 경험하였기에 문헌고찰과 함께 증례 보고하는 바이다.
증 례
환 자: 69세 여자
주 소: 호흡곤란
현병력: 내원 3년 전 RA 진단받고 메토트렉세이트(Methotrexate, MTX), 하이드록시클로로퀸, 레플루노마이드, 비스테로이드성 항염제 그리고 저용량 부신피질 호르몬 등의 약물 치료를 하였다. 내원 1년 전 간기능 이상으로 MTX, 레플루노마이드를 중단하였다. 이후 발생한 RA 질병 활성도 증가로 타크로리무스 2 mg을 추가하였다. 내원 8개월 전 또 다시 양측 손목을 포함한 수지관절의 동통 및 부종이 심해지고 ESR, C-반응단백이 상승하여 Disease Activity Score-28 (DAS-28)이 7.3으로 상승하였다. 경구용 부신피질 호르몬 증량 및 관절강 내 주사로 증상을 조절하다 MTX와 함께 adalimumab을 피하주사로 투여하였다. 투여 3개월 후 DAS-28은 3.1로 낮은 질병 활성도를 유지하면서 증상이 호전되었다. 투여 9개월인 내원 3일 전부터 갑작스런 호흡곤란이 발생하여 입원하였다.
과거력: 내원 6년 전 관상동맥 조영술로 확인된 좌회선 동맥(left circumflex artery)의 둔한경계가지(obtusal margninal branch)에 의미 있는 협착으로 아스피린 100 mg 복용 중이며, 내원 4년 전 당뇨를 진단받고 경구용 혈당강하제(메포민 500 mg, 글리메피라이드 3 mg) 복용 중이다. 간염, 폐결핵의 기왕력은 없다.
가족력: 특이소견 없음.
진찰 소견: 내원 시 활력징후는 혈압 120/80 mmHg, 맥박 124회/분, 호흡수 24회/분, 체온 37.7℃였다. 신체 검사에서 신장은 152 cm, 몸무게는 50 kg이었다. 급성 병색을 보였으나 의식은 명료하였고 흉부 청진상, 양폐야에서 악설음이 청진되었으나 천명음 및 비정상적은 심음은 들리지 않았다. 대관절과 수지관절의 부종이나 압통 소견은 관찰되지 않았으며 양측 손목의 변형이 있으나 압통은 없었다. 그 외 경부림프절 및 갑상선 비대 등의 소견은 보이지 않았고 복부진찰에서 간이나 비장의 비대 소견 보이지 않았다.
검사실 소견: 말초혈액검사에서 백혈구 11,360/mm3 (호중구 93.2%, 림프구 3.3%, 단핵구 1.8%, 호산구 0.6%, 호염구 0.1%), 혈색소 10.2 g/dL, 혈소판 433,000/mm3였다. 동맥혈가 스분석은 pH 7.48, PCO2 25.1 mmHg, PO2 61 mmHg, HCO3 18.9 mmol/L, SaO2 81%로 저산소증을 보였다. 생화학 검사에서 AST/ALT 47/19 U/L, 총 단백 5.88 g/dL, 알부민 3.24 g/dL, 혈액요소질소 11.6 mg/dL, 크레아티닌 0.94 mg/dL으로 정상이었고, 요화학 검사상 혈뇨나 단백뇨는 없었다. 갑상선기능은 정상이었다. 적혈구 침강속도는 120 mmHr, C-반응성 단백은 10.8 mg/dL로 상승되었다. 면역학적 검사에서 류마티스인자 648 IU/mL, 항 CCP 항체 100 U/mL 이상, 항핵항체는 speckled pattern으로 양성(1:40), 이중나선 DNA 항체와 항중성구세포질 항체는 음성이었고 항, 사구체 기저막 항체(anti GBM Ab)는 음성이었다.
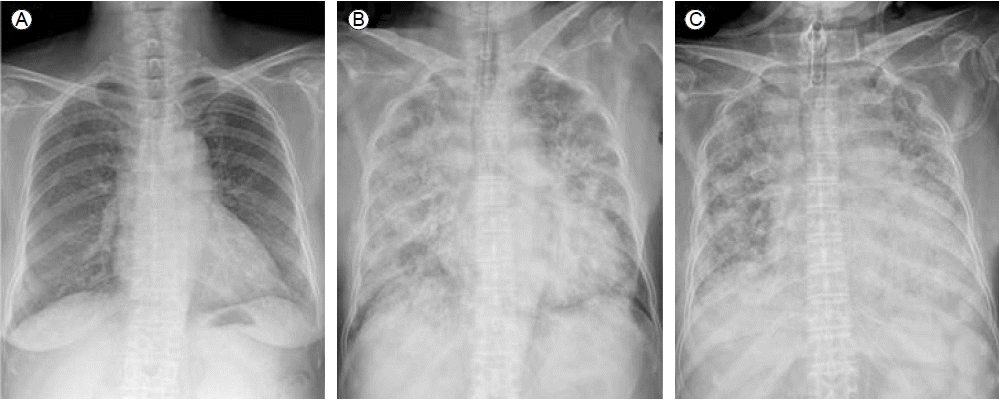
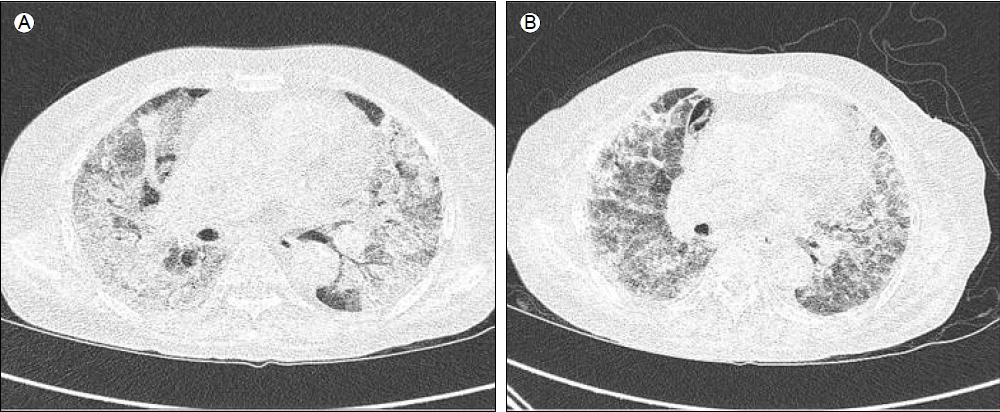
방사선 소견: 흉부 X-선 사진에서 양 폐야 대부분에 미만성 폐침윤(pneumonic infiltration) 소견이 관찰되고(Fig. 1B) 고해상도 흉부 전산화 단층촬영(HRCT)에서 양폐야 대부분을 차지하고 있는 미만성 간유리 음영과 소엽사이막 비후가 보였다(Fig. 2A). 흉막 삼출, 심낭 삼출액의 동반이나 종격동 내에 의미 있게 커져있는 림프절들은 없었다.
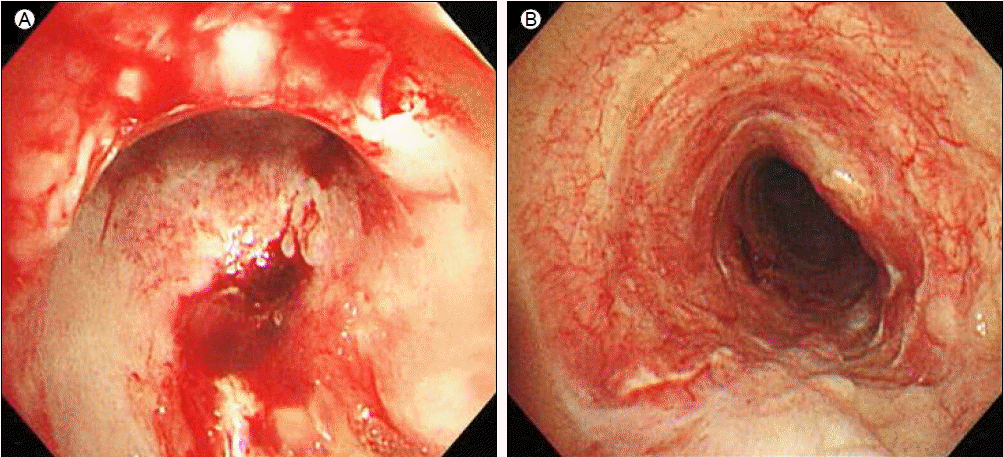
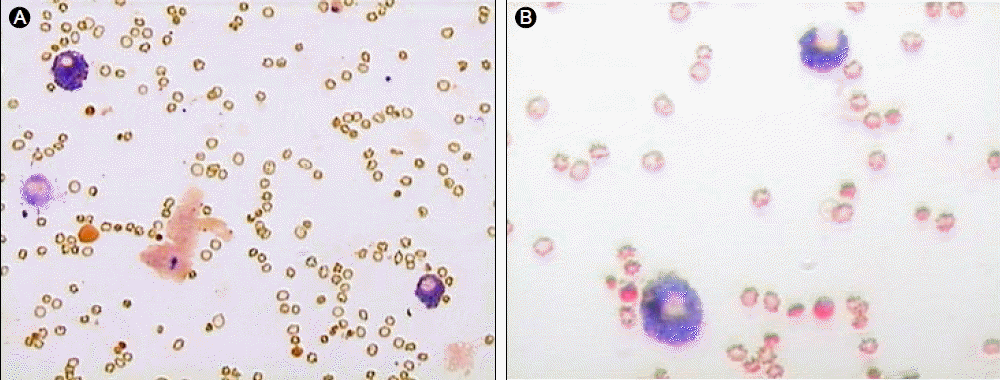
치료 및 경과: 입원 후 호흡곤란이 악화되고 산소를 mask 10 L로 공급하여도 산소포화도가 유지되지 않아 기관 내 삽관을 시행하고 면역저하 상태의 폐렴에 준하여 Ceftazidime, Levofloxacin의 항생제를 투여하였다. 입원 2일째, 오래된 혈액빛(old blood clot) 양상의 가래가 지속적으로 흡인되어 기관지 내시경을 시행하였다. 왼쪽 및 오른쪽 주기관지 점막은 정상으로 관찰되었으나 기관지 말단 부위에서 폐포 출혈이 의심되는 적색변성부위가 확인되었고 폐포 세척 시 핏빛 소견이 보였다(Fig. 3). 폐포 세척액 배양 검사에서 세균이나 진균은 보이지 않았다. 기관지 폐포 세척액에서 헤모시데린 풍부한 대식세포(hemosiderin-laden macrophage)가 관찰되어(Fig. 4) 미만성 페포 출혈(diffuse alveolar hemorrhage, DAH) 진단 하에 전신적 스테로이드 투여(프레드니솔 125 mg)를 시작하였다. 또한 면역글로불린(Intravenous Immunoglobulin, IVIG)을 DAH에 준하여 20 g/day의 용량으로 5일간 투여하였다. 이후 산소 포화도가 상승하고 호흡 곤란이 호전되어 입원 13일째 기계 환기 및 삽관을 제거하였다. 추적관찰 시 시행한 흉부 X-선 사진과 HRCT에서도 미만성 폐침윤의 호전 소견을 보였다(Fig. 1C, 2B). 그러나 입원 18일째 다시 호흡곤란을 호소하고 양 폐야의 폐침윤이 악화되었다. 기관 삽관을 하고 기관지 내시경 등의 검사에서 DAH의 재발이 확인되어 프레드니솔 40 mg과 IVIG를 동반 투여하였고, 시행한 가래 검사상 MRSA 동정되어 Vancomycin 투여하였다. 입원 38일째 기관지 절개술을 시행하였고, Imipenem을 추가로 사용하던 중 산소 포화도 떨어지면서 BUN/Cr 상승, 소변 배출이 시간당 10cc 이하, 가래 검사상 MRSA 지속적으로 동정되어 항생제를 Linezolid로 변경하고 지속적 신대체요법(CRRT)을 시행하였다. 가래 검사상 Acinetobacter baumanii 동정되어 Colistin 투여하였으나 기계 호흡에서 일 호흡 용적(tidal volume)이 100 mL 미만으로 떨어지고 동맥혈 가스분석상 호흡성 산증 보이는 패혈증으로 사망하였다.
고 찰
DAH는 폐포모세혈관막의 손상으로 폐모세혈관 및 폐정맥으로부터 폐포 내 출혈을 일으킨다[2]. 임상증상은 호흡곤란, 저산소증, 객혈, 혈색소의 감소, 그리고 미만성 폐침윤을 특징으로 하며 세 가지 조직학적 타입 즉 폐모세혈관염으로 알려진 소혈관염, 경증 폐출혈(bland pulmonary hemorrhage), 그 외에 약, 응고질환, 감염 등으로 인한 미만성 폐포손상으로 분류될 수 있다[2]. 원인에 따라 크게 면역성과 비면역성으로 나눌 수 있다[3]. 면역학적 원인은 혈관염, 결체조직질환, 특히 전신홍반 루프스, 항사구체기저막신염 등이 있으며 비면역성 원인은 심장질환, 응고장애, 감염, 약독성 및 특발성을 들 수 있겠다. 원인이 무엇이든지 간에 DAH는 즉각적인 판단과 빠른 치료를 요하는 응급질환이다. 주 치료는 보존적 치료와 동시에 고농도 스테로이드 정주와 면역 억제제(특히 사이클로포스파마이드, IVIG)를 사용한다.
DAH와 관련된 혈관염의 예로는 전신성 혈관염 중 전신 홍반 루프스, RA 등 자가면역질환에 이차적으로 합병된 혈관염, 그 외 항호중구세포질항체연관 혈관염(anti-neutrophil cytoplasmic antibody (ANCA)-associated vasculitis, AAV) 중 베게너육아종증, 현미경적 다발성 혈관염(Microscopic polyangitis), 알레르기성 혈관염(Churg strauss syndrome)과 같은 소혈관염이 있다. 이는 종종 급속 진행성 사구체신염(Rapidly progressive glomerulonephritis)과 미만성 폐포 출혈을 합친 폐신장증후군(pulmonary renal syndrome)으로 총칭되기도 했다[4]. 드물지만 헤노흐-쇤라인 자반증(Henoch-Schoenlein purpura), 베체트병, 이식 후 거부 반응에서도 발생할 수 있으며 후천성면역결핍증후군, 골수이식 후 특발성 폐헤모시데린침착증(pulmonary hemosiderosis), 승모판협착증(Mitral stenosis)가 있는 환자에서도 복합적인 기전으로 동반 가능하다[2,3].
이 외 약물에 의해서도 상기 질환이 유발될 수 있는데 제시되는 기전으로는 면역관련 과민 반응(hypersensitivity reaction), 직접독성(direcrt toxicity), 응고장애(coagulation defect)가 있다[5]. 첫 번째 면역관련 기전으로 DAH를 유발하는 대표적인 약제는 프로필티오우라실(prophythoiouracil), 다이페닐히단토인(diphenylhydantoin), 전트란스형레티노익엑시드(all-transretinoicacid), 페니실린(penicillin), 항암제, 설파살라진(sulfasalazine), 하이드라라진(hydralazine), 항류코트리엔제(leukotriene antagonist), 미토마이신(mitomycin)이 있다. 두 번째 직접독성 기전에 의한 약제로는 아미오다론(amiodarone), 니트로푸란토인(nitrofurantoin) 이 외에 항암제, 골수이식, 코카인이 있다. 마지막으로 약물에 의한 손상 기전으로는 혈액응고결핍과 관련하여 발생하는 DAH이다. 종류는 혈전용해제, 항응고제, 혈소판 응집억제제, 약제 기인성 혈소판 감소증, 덱스트란 70이 있다.
종양괴사인제 억제제는 RA, 강직성 척추염, 건선 등의 자가면역질환의 치료에 폭넓게 쓰이며 관련된 흔한 부작용으로 피부부작용, 전신홍반성루프스양반응(systemic lupus erythematous-like reactions), 혈관염 및 감염성 또는 비감염성 폐질환 등이 있다. 종양괴사인자 억제제에 의한 DAH는 매우 드물며 관련된 보고로는 크론병 치료로 infliximab 투여 중인 35세 여성에서 발생한 경우가 있다[6]. Infliximab이 DAH에 기여하는 병리기전이 확실하게 밝혀진 상태는 아니나 직접 독성이 가장 합당한 기전으로 여겨지고 있다. Infliximab과 관련된 다른 사례로는 강직성 척추염으로 infliximab 투여 중에 발생한 DAH이다. 당시 환자는 aspirin, 항혈소판제재를 복용하고 있었지만 이 약제와 DAH 발생과의 인과관계가 없어 infliximab과 관련하여 발생한 DAH로 보고되었다[7]. 또 다른 사례는 RA, 건선의 치료로 투여 중인 etanrcept에 의 해 발생한 DAH와 급성 호흡부전 증후군이다[8]. 이 증례는 etanecept와 관련하여 처음으로 보고된 DAH였고 관련된 감염으로 급성 폐손상 증후군으로까지 발병된 증례였다. 이 외에 비생물학적 항류마티스 약제(disease modifying antirheumatic drugs, DMARDs)인 Leflunomide에 의한 DAH도 있다. 이 약제로 인한 폐 손상은 흔히 다음과 같은 네 가지 소견 즉 미만성 폐포 손상, 급성호산구성폐렴, 과민반응, 기질성 폐렴으로 나뉘는데 leflunomide로 인한 혈관염은 아마도 면역복합체의 염증 반응에 의한 것으로 여겨진다[9].
Adalimumab은 종양궤사인자에 대한 인간화 단클론항체로 약제 사용과 관련한 인지질항제증후군(antiphospholipid syndrome) 및 심각한 획득성 혈우병 A (acquired haemophilia A) 그리고 헤노흐-쇤라인 자반증과 같은 혈관염의 증례 보고는 있었으나[10] 본 증례와 같은 DAH는 국내 보고 및 외국 보고 또한 없었다. 본 증례의 경우 RA 자체에 의한 DAH로 보기엔 이미 내원 5개월 이상 질병의 활성도가 잘 유지되고 있었고 다른 유발 가능한 약제인 레플루노마이드는 이미 1년 전 중단한 상태였다. 또한 관상동맥 질환으로 복용중인 아스피린의 경우 저용량인 100 mg이어서 배제가 가능하였다. 종양괴사인자 억제제의 RA 치료효과는 언급할 필요도 없이 우수하다. 그러나 임상에서 사용 시 나타날 수 있는 심각한 부작용을 고려하고 써야 하며 특히 고령, 기저 폐질환 및 혈액 응고 결핍을 일으킬 수 있는 약제를 복용하고 있는 경우는 DAH 또한 염두에 두어야겠다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






