 |
 |
| Korean J Med > Volume 80(6); 2011 > Article |
|
요약
목적:
일반적으로 약물방출스텐트(DES, drug-eluting stent)가 시술 이후 추적검사에서 합병증 발생률이 낮은 것으로 알려져 있어 일반 금속스텐트(BMS, bare metal stent)보다 주로 시술에 이용되고 있다. 본 연구에서는 관상동맥의 혈관직경에 따라서 DES와 BMS 사이에서의 후기 합병증 차이를 밝히고자 하였으며 특히 동맥직경이 3.5 mm 이상인 혈관을 대상으로 연구를 시행하였다.
방법:
2000년 9월에서 2008년 6월까지 경피적 관상동맥 중재술을 시술 받은 환자 중 DES를 시술 받은 134예(59.9 ± 10.6세, 남자 90명, 68.7%)와 BMS를 시술한 115예(60.3 ± 8.9세, 남자 82명, 71.3%)를 대상으로, 시술 후 12개월 동안 임상경과와 주요 심혈관계사고, 즉 심장사, 심근경색, 재관류를 위한 관상동맥우회술 등을 비교하였다.
결과:
혈관병변의 길이는 DES와 BMS 사이에 차이가 없었고(19.7 ± 9.1 mm vs. 18.6 ± 4.5 mm, p = 0.248), 길이도 DES의 경우에 더 긴 경향을 보였으나, 통계적으로 유의한 차이는 없었다(22.6 ± 5.2 mm vs. 21.9 ± 4.5 mm, p = 0.207). 시술 12개월 후의 추적검사에서 주요심혈관사고는 BMS군과 DES군에서 통계적인 차이가 없었다(BMS 13명, 11.3% vs. DES 12명 9.0%, p = 0.486). 이중 항혈소판제(dual antiplatelet therapy) 투여기간은 DES 시술군에서 BMS 시술군보다 길었다(240 ± 2.7일 vs. 348 ± 1.7일, p = 0.042).
Abstract
Background/Aims:
Drug-eluting stents (DES) are superior to bare metal stents (BMS) in reducing restenosis rates across a wide range of patients and lesion subsets.This study compared the clinical outcomes of DES versus BMS in patients with large coronary arteries (≥ 3.5 mm).
Methods:
The study compared 134 patients (59.9 ± 10.6 years, 90 men, 44 women) who underwent single vessel angioplasty with DESimplantation in large vessels with 115 patients (60.3 ± 8.9 years, 82 men, 33 women) who received BMS. The clinical outcomes at 12 months were compared between groups. The study end points were major adverse cardiac events (MACE), including cardiac death, nonfatal myocardial infarction, and the need for target vessel and target lesion revascularization.
Results:
The baseline clinical coronary angiography and procedural characteristics were similar in both groups. The duration of dual antiplatelet therapy was longer in the DES group than in the BMS group (240 ± 2.7 vs. 348 ± 1.7 days, p = 0.042). During the 12-month clinical follow-up, MACE were observed in 13 patients (11.3%) with BMS and 12 patients (9.0%) with DES (p = 0.486).
큰 관상동맥은 혈류를 공급하는 심근영역이 넓으며 전체 심혈관중재술의 대상혈관 중 1/3을 차지한다[1,2]. 과거의 연구결과들은 일반 금속스텐트 시술 시에 시술의 대상이 되는 혈관의 직경에 따라서 재협착률이 어떻게 차이를 보이는가를 밝히는 데 주로 초점을 두었다[3]. 큰 관상동맥은 작은 혈관에 비하여 혈관내피 과형성을 제어하는 데 다소 유리하여 혈관이 클수록 낮은 재협착률 및 재시술률을 보였다[3,4]. 최근의 연구들은 약물방출스텐트(DES, drug eluting stent)와 기존의 일반 금속스텐트(BMS, bare metal stent)와의 임상결과를 주로 비교하였다[4-13]. DES는 재협착률을 상당히 줄였으며 시술 후의 주요심혈관사고를 감소시키는 것이 대규모 연구에서 밝혀졌다[4,5]. 그러나 DES와 BMS를 각각 관상동맥의 크기에 따라 임상효과를 밝히려는 시도는 많지 않았다. 큰 관상동맥의 시술에서는 DES가 BMS보다 꼭 유리하다는 연구결과는 아직까지는 거의 없는 상태이다.
본 연구에서는 3.5 mm 이상의 큰 관상동맥에서 BMS와 DES를 시술 받은 각각의 환자를 대상으로 주요심혈관사고(MACE, major adverse cardiac events)의 차이 및 재협착에 의한 재시술률 차이를 밝히고자 하였다.
2000년 9월에서 2008년 6월까지 본원에서 경피적 관상동맥 중재술을 시술 받은 환자 중 관상동맥 직경이 3.5 mm 이상인 큰 혈관을 시술 받은 환자 중 혈관 직경 50% 이상의 협착이 관찰되면서 협심증 증상을 갖거나 해당 혈관의 혈액공급을 받는 심장부위의 허혈 소견이 관찰되는 모든 환자를 대상으로 하였다. 환자 중 심인성 쇼크, 다른 기관에 암이 있는 경우, 관상동맥이식술을 시행한 경우는 대상에서 제외하였다.
연구의 대상이 되는 환자군은 총 249명이었으며, 이 중 BMS는 115명(60.3 ± 8.9세, 남자 82명, 71.3%)이며 DES는 134명(59.9 ± 10.6세, 남자 90명, 68.7%)이었다. 환자의 임상결과에 영향을 미칠 수 있는 성별, 연령, 과거력, 관련 질환, 심혈관 질환에 따른 분류가 이루어졌으며 두 군 사이에 임상적인 차이는 없었다(Table 1).
혈관 시술은 관상동맥조영술상 관상동맥 직경의 50% 이상 협착이 있는 병변에 풍선확장술을 먼저 시행하였고, 이후에 표준절차에 따라서 스텐트가 삽입되었다. 심혈관 중재술에 대한 평가는 시술자 이외에 2명의 전문가에 의해서 이루어졌다.
DES와 BMS가 시행된 시술 혈관에 대한 비교에서 혈관의 위치 및 시술 혈관의 수에서 유의한 차이는 없었다(Table 2). 그러나 시술 시 병변의 길이는 BMS에 비해서 DES가 길게 측정되었다(BMS 18.6 ± 4.5 mm vs. DES 19.7 ± 9.1 mm; p = 0.248). 또한 시술 스텐트의 길이 또한 DES가 길었으며(BMS 21.9 ± 4.5 mm vs. DES 22.6 ± 5.2 mm; p = 0.207) 삽입 스텐트 수 / 환자의 비율도 DES가 크게 측정되었다(BMS 1.29 ± 0.18 vs. DES 1.35 ± 0.60, p = 0.401).
그러나 병변의 길이, 스텐트의 길이, 환자당 스텐트 개수 등은 차이가 없었다.
심혈관 중재술 이후 aspirin과 clopidogrel을 투여하였으며, BMS와 DES 두 그룹 간 aspirin 투여기간에 유의한 차이는 없었으나, clopidogrel 투여기간에 있어서는 유의한 차이를 보였다(BMS 240 ± 2.7일 vs. DES 348 ± 1.7일, p = 0.042, Table 3).
이와 같이 BMS군에서 clopidogrel의 복용기간이 상대적으로 짧은 것은 ACC/AHA 가이드라인에 의하여 clopidogrel를 사용하였으며 BMS군에서 소화성궤양출혈, 비출혈, 발치, 외과적 수술 등으로 clopidogrel를 DES보다 빨리 중단하였기 때문이다(BMS 10명, 8.7% vs. DES 9명, 6.7%, p = 0.038, Table 4).
12개월 후 추적검사에서 두 군 사이의 심혈관 사망률, 치명적이지 않은 심근경색증, 목표병변 재시술, 목표혈관 재시술과 주요심혈관사고 모두 DES가 BMS보다 더 좋은 경향을 보였으나, 통계학적으로 유의한 차이는 없었다(BMS 13명, 11.3% vs. DES 12명 9.0%, p = 0.486). Kaplan-Meier 법을 이용한 1년 생존분석결과 두 군 간의 유의한 차이는 없었다(Fig. 1).
DES는 BMS에 비하여 시술 후 재협착률이 낮아서 일반적으로 BMS보다 시술 후 임상결과가 우수한 것으로 알려져 있다. 그러나 시술 대상이 되는 관상동맥이 큰 경우에는 다른 임상결과가 나올 수 있을 것이라는 가정이 있었고, 그것을 바탕으로 이미 앞서 연구들이 진행되었으나 그 숫자가 많지 않았으며 환자규모, 연구방식에 있어서 한계를 지니고 있었다.
큰 관상동맥에 대한 스텐트중재술 이후 임상결과 차이를 밝힌 기존의 연구들은 대체로 DES가 BMS에 비하여 임상 효과 면에서 의미 있는 차이가 없다는 결과가 많았다[1,2,14, 27,31]. 그러나 상당수의 연구들은 대상 환자수가 충분하지 않거나 단일기관에 의하여 진행된 경우가 많았다. 비교적 최근에 발표된 연구에서는 연구 규모 및 과정에서 과거의 연구들에 비하여 비교적 신뢰할 것으로 평가할 수 있으나 시술 1년 후 시점에서의 임상결과 비교가 명확하지 않았다[31].
본 연구는 시술 1년이 되는 시점에서의 임상결과를 확인하기 위함이며 BMS, DES 두 군 사이에서의 MACE의 차이를 분석하면서 MACE에 영향을 미칠 수 있는 baseline characteristics에 연관성도 밝히고자 하였다. 본원에서 스텐트시술을 받은 두 환자군에서 clopidogrel 복용기간의 의미 있는 차이를 보였으며 이 점이 stent thrombosis과 관련된 합병증을 증가시킬 가능성에 대해서도 확인할 수 있었다.
본 연구는 3.5 mm 이상의 큰 관상동맥에서 스텐트 시술 시 DES와 BMS의 임상효과를 비교하였으며 12개월 후 추적검사를 시행하였을 때 두 군 사이의 임상효과에는 차이가 없는 것으로 판명되었다. 각각의 항목으로 세분하였을 때에도 심혈관 사망률, 치명적이지 않은 심근경색증, 목표병변재시술, 목표혈관재시술 등에 대해서는 DES가 BMS보다 더 좋은 경향을 보였으나 통계학적으로 유의한 차이는 없었다(Table 5).
현재 중재시술 분야는 지속적인 발전을 거듭하고 있다. 이를 가능하게 한 가장 핵심적인 것은 스텐트의 개발이었다[14]. 스텐트 시술은 과거 풍선확장술의 심각한 합병증이었던 급성 혹은 아급성 혈관폐색을 현격히 감소시켰으며 장기 재협착률도 현저히 감소시켰다. 아울러 스텐트시술의 기술적인 발달과 각종 약물의 개발로 중재시술의 적응증도 점차 확대되어 관상동맥구 병변(ostial lesion), 관상동맥분지 병변(bifurcation lesion), 주관상동맥 병변(left main lesion) 및 다혈관 병변(multivessel disease) 등에도 관상동맥 중재술이 가능하게 되었다[15-18]. 이러한 스텐트 자체에 대한 개발 노력과 함께 약물을 통하여 스텐트 시술의 가장 큰 난제인 재협착을 줄이기 위한 노력도 함께 진행되었다[19].
DES는 이러한 배경하에 재협착 감소 약물의 효과를 극대화하면서도 인체에 미치는 약제 부작용을 최소화하자는 취지로 개발되었다[20]. 최근의 관심의 초점은 재협착이며 DES의 가장 큰 목적도 재협착을 감소시키는 데 있다. 재협착은 한마디로 관상동맥 내막이 풍선확장술로 손상을 받게 되어 일어나는 치유과정이 원하지 않게 과도하게 일어난 결과로 요약할 수 있다. 풍선확장술로 혈관 내막이 손상을 받고 중막이 확장하게 되면 정상적인 재생과정으로 염증반응이 일어나게 되며, 육아조직이 증식되고, 혈관이 재형성된다. 풍선확장술 후 재협착의 과정은 초기탄성반동(early elastic recoil), 신생내막 증식(neointimal hyperplasia)과 후 기혈관재형성(late vessel remodeling)으로 구분할 수 있다[21]. 이중 관상동맥 스텐트 시술 후에는 신생내막증식이 가장 중요한 재협착의 기전으로 알려져 있다. 신내막과형성은 스텐트 시술 후 주로 6개월 내에 발생하며 프로테오글라이칸 기질 내에 평활근 세포(smooth muscle cell)가 과도하게 증식하여 혈관을 재협착을 발생시키는 과정이다[22,23].
이러한 문제를 완벽하게 해결한 스텐트는 개발 중이므로 현재로서는 항혈소판제의 투약으로 스텐트 혈전을 예방하고 치료하고 있는 실정이다[24]. 따라서 aspirin과 clopidogrel을 장기간 유지해야 하며 이로 인한 불필요한 합병증(출혈, 혈소판 감소증)은 동반하게 된다. 최근에는 이 중 항혈소판제 약물복용이 DES를 삽입 받은 환자에서 적정 투약 기간이 얼마나 필요한가에 대한 많은 임상 연구들이 발표되고 있으며 적정 투약 기간에 대한 여러 가지 의견도 제시되고 있다[25-30].
2007년 Journal of Interventional Cardiology에서 Tania, Guido 등의 저자들은 급성 심근경색증 환자들을 대상으로 한 DES와 BMS삽입술 이후의 임상효과를 비교한 대규모 메타분석에서 두 군 간의 목표병변 재협착 발생률(DES 6.2% vs. BMS 7.4%; p = 0.231)에 차이가 없다고 보고하였다[26]. 따라서 DES와 BMS의 선택에 새로운 기준이 필요할 것으로 판단되었다. 과거에 많은 연구에서 DES가 BMS보다 전반적으로 임상적인 효과가 있는 것으로 밝혀졌지만 시술 대상이 되는 관상동맥의 크기별로 분류하여 그 임상결과를 비교하는 연구는 잘 알려지지 않았다.
저자들은 대상 혈관의 크기가 클수록 재협착 발생률의 차이가 없을 것이라는 가정하에 비교적 큰 사이즈(직경 3.5 mm 이상)의 관상동맥 혈관에 BMS와 DES가 삽입된 환자군 각각에서 중재술 이후 임상결과의 차이를 분석하였다. DES와 BMS군 간의 기본특성의 차이는 없었으며 약물치료에서 clopidogrel의 사용기간이 BMS군에서 유의하게 적었다. 일 년 후의 임상결과는 사망률, 치명적이지 않은 심근경색증, 목표혈관 재시술, 목표병변재시술 등의 MACE를 비교하였으며, 두 군 사이에 통계적으로 유의한 차이는 없었다.
저자들의 결과로 보면 크기가 큰 관상동맥 질환에는 DES나 BMS에서 유의한 차이가 없으며 오히려 약물투여기간만이 DES에서 더 길어지므로 특정한 환자군에서는 BMS로 시술하는 것이 유리할 수 있다. 특히 장기간의 약물복용이 어려운 환자나 출혈위험이 있는 환자, 수술적 치료를 앞둔 환자에서 관상동맥 협착이 발생한 경우에서는 3.5 mm 이상의 병변일 경우 BMS를 먼저 고려해 볼 수 있을 것이다. 그러나 심혈관계 고위험군 환자(당뇨병 등)나 광범위한 관상동맥병변, 기존의 시술부위의 재협착, 혈관의 만성적인 완전폐색(chronic total occlusion)과 같이 재협착 발생률이 높은 경우는 DES가 여전히 우세할 것이다.
본 연구는 단일기관에서 진행되었으며 대상 환자의 숫자가 적다는 한계가 있다(BMS 115명, DES 134명). 또한 연구의 대상은 2000년 이후 스텐트 삽입술을 시행 받은 환자이며 초기에는 BMS에 의한 시술만 이루어졌고 DES는 본원에 도입된 2004년부터 가능하였다.
2004년 이후에는 주로 DES에 의한 시술만 이루어졌으므로 BMS와 DES가 주로 시행된 시기는 차이가 있었다. 시술의 시기적인 차이로 인하여 연구결과에 영향을 미칠 수 있는 변수의 발생가능성은 본 연구가 후향적으로 이루어진 데서 온 제한점으로 판단된다.
따라서 대규모 전향적 연구를 시행하여 장기간의 추적관찰을 통한 DES와 BMS의 두 군 간의 임상 결과를 관찰하는 것이 필요하며 결과에 따라서는 향후 새로운 스텐트 삽입술의 지침을 제시할 수 있을 것으로 보인다.
REFERENCES
1. Steinberg DH, Mishra S, Javaid A, et al. Comparison of effectiveness of bare metal stents versus drug-eluting stents in large (> or = 3.5 mm) coronary arteries. Am J Cardiol 2007;99:599–602.


2. Quizhpe AR, Feres F, de Ribamar Costa J Jr, et al. Drug-eluting stents vs bare metal stents for the treatment of large coronary vessels. Am Heart J 2007;154:373–378.


3. Joen DJ, Hong GR, Bae JH, et al. Immediate and follow-up results after long stent implantaton in diffuse long coronary lesions. Korean J Med 2000;58:48–57.
4. James SK, Stenestrand U, Lindbäck J, et al. Long-term safety and efficacy of drug-eluting versus bare-metal stents in Sweden. N Engl J Med 2009;360:1933–1945.


5. Kishore JH, Ricardo C, Pichard L. Clinical outcomes following drug-eluting versus bare metal stent implantation for lesion subsets excluded from pivotal clinical trials: finding from the GHOST Study (Guthrie Health System Off-Label StenT Study). J Interv Cardiol 2008;21:315–324.

6. Koutouzis M, Nikolidakis S, Arealis G, Kyriakides ZS. Very late in-stent restenosis in a bare metal stent. Cardiology 2007;107:360–361.


7. Malenka DJ, Kaplan AV, Lucas FL, Sharp SM, Skinner JS. Outcomes Following Coronary Stenting in the era of bare-metal vs. the era of drug-eluting stents. JAMA 2008;299:2868–2876.



8. Strozzi M, Anić D. Comparison of stent graft, sirolimus stent, and bare metal stent implanted in patients with acute coronary syndrome: clinical and angiographic follow-up. Croat Med J 2007;48:348–352.


9. Khattab AA, Otto A, Hochadel M, Toelg R, Geist V, Richardt G. Drug-eluting stents versus bare metal stents following rotational atherectomy for heavily calcified coronary lesions: late angiographic and clinical follow-up results. J Interv Cardiol 2007;20:100–106.


10. Jensen J, Lagerqvist B, Aasa M, Särev T, Nilsson T, Tornvall P. Clinical and angiographic follow-up after coronary drug-eluting and bare metal stent implantation: do drug-eluting stents hold the promise? J Intern Med 2006;260:118–124.


11. Steinberg DH, Waksman R. Drug-eluting stent thrombosis vs bare metal stent restenosis: finding the lesser of two evils. Am Heart Hosp J 2007;5:151–154.


12. Spaulding C, Daemen J, Boersma E, Cutlip DE, Serruys PW. A pooled analysis of data comparing sirolimus-eluting stents with bare-metal stents. N Engl J Med 2007;356:989–997.


13. Fuchs AT, Kuehnl A, Pelisek J, et al. Meta-analysis shows similar risk of thrombosis after drug-eluting stent, bare-metal stent, or angioplasty. Endothelium 2008;15:93–100.


14. Lee SH, Jeong MH, Hong YJ, et al. A long stent is the only predictive factor for coronary stent restenosis. Korean J Med 2001;60:529–536.
15. Barlis P, Kaplan S, Dimopoulos K, Ferrante G, Di Mario C. Comparison of bare-metal and sirolimus-or paclitaxel-eluting stents for aorto-ostial coronary disease. Cardiology 2008;111:270–276.


16. Stone GW, Ellis SG, Cannon L, et al. Comparison of a polymer-based paclitaxel-eluting stent with a bare metal stent in patients with complex coronary artery disease: a randomized controlled trial. JAMA 2005;294:1215–1223.


17. Tanigawa J, Sutaria N, Goktekin O, Di Mario C. Treatment of unprotected left main coronary artery stenosis in the drug-eluting stent era. J Interv Cardiol 2005;18:455–465.


18. Tanzilli G, Pelliccia F, Pasceri V, et al. Randomized study on provisional stenting with sirolimus-eluting stent vs. bare metal stent for the treatment of true coronary bifurcations: the PROSUMER (PROvisional with sirolimus-eluting vs. bare metal stents in truE bifuRcations) study. Int J Cardiol 2011;146:240–241.


19. Beohar N, Davidson CJ, Kip KE, et al. Outcomes and complications associated with off-label and untested use of drug-eluting stents. JAMA 2007;297:1992–2000.


20. Ma X, Oyamada S, Gao F, et al. Paclitaxel/sirolimus combination coated drug-eluting stent: in vitro and in vivo drug release studies. J Pharm Biomed Anal 2011;54:807–811.



21. Zimarino M, Renda G, De Caterina R. Optimal duration of antiplatelet therapy in recipients of coronary drug-eluting stents. Drugs 2005;65:725–732.


22. Moohebati M, Falsoleiman H, Dehghani M, et al. Serum inflammatory and immune marker response after bare-metal or drug-eluting stent implantation following percutaneous coronary intervention. Angiology 2011;62:184–190.


23. Alt E, Haehnel I, Beilharz C, et al. Inhibition of neointimaformation after experimental coronary artery stenting: a new biodegradable stent coating releasing hirudin and the prostacyclin analogue iloprost. Circulation 2000;101:1453–1458.


24. Ho PM, Peterson ED, Wang L, et al. Incidence of death and acute myocardial infarction associated with stopping clopidogrel after acute coronary syndrome. JAMA 2008;299:532–539.


25. Mauri L, Hsieh WH, Massaro JM, Ho KK, D'Agostino R, Cutlip DE. Stent thrombosis in randomized clinical trials of drug-eluting stents. N Engl J Med 2007;356:1020–1029.


26. Chechi T, Vittori G, Biondi Zoccai GG, et al. Single-center randomized evaluation of paclitaxel-eluting versus conventional stent in acute myocardial infarction (SELECTION). J Interv Cardiol 2007;20:282–291.


27. De Felice F, Fiorilli R, Parma A, et al. Comparison of one-year cardiac events with drug-eluting versus bare metal stent implantation in rescue coronary angioplasty. Am J Cardiol 2011;107:210–214.


28. Seo YU, Koh YY, Kang MJ, Chang KS, Hong SP. Predictors of side branch occlusions just after coronary stenting. Korean J Med 2004;67:153–160.
29. Lee SW, Lee SW, Hong MK, et al. Bail-out stenting for left main coronary artery dissection during catheter-based procedure: acute and long-term results. Korean J Med 2004;66:571–575.


Kaplan-Meier curves during the 12-month clinical follow-up. The graph shows that the rate of major adverse cardiac events (myocardial infarction, target lesion revascularization, target vessel revascularization, and death) is not different according to the type of stent (p = 0.166).
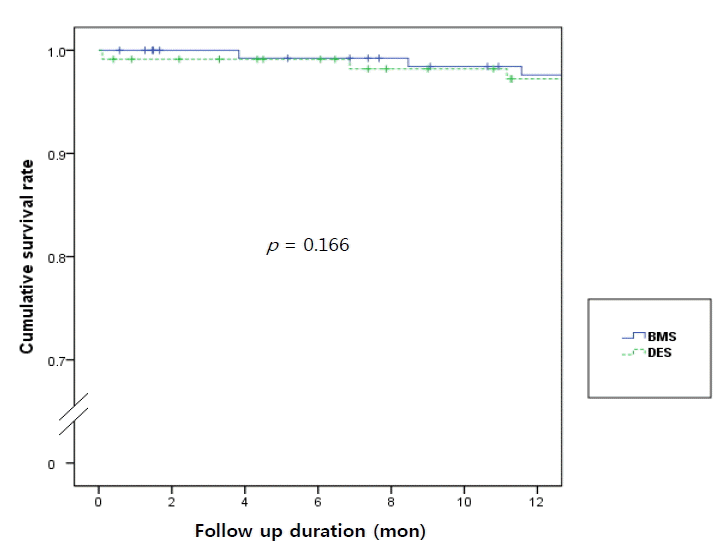
Figure 1.
Table 1.
Baseline clinical characteristics
Table 2.
Coronary angiographic findings and procedural characteristics
Table 3.
Duration of medical treatment for coronary intervention during the 1-year clinical follow-up
Table 4.
Factors forcing the stoppage of antiplatelet agents during the post-intervention period
Table 5.
Clinical outcomes during the 1-year clinical follow-up
- TOOLS
-
 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link XML Download
XML Download Full text via DOI
Full text via DOI-
 Download Citation
Download Citation
 Print
Print-
Share :








