 |
 |
| Korean J Med > Volume 93(6); 2018 > Article |
|
Abstract
A small number of viable tuberculosis bacilli can reside in an individual with latent tuberculosis infection (LTBI) without obvious clinical symptoms or abnormal chest radiographs. Diagnosis and treatment of LTBI are important for tuberculosis (TB) control in public and private healthcare facilities, particularly in high-risk populations. The updated 2017 Korean guidelines for TB recommend that tuberculin skin tests, interferon-gamma release assays, or a combination of them can be used for the diagnosis of LTBI, depending on the age and immune status of the patient as well as their TB contact history. For diagnosis of LTBI, exclusion of active TB is essential, and the possibility of healed TB in those without a history of treatment for TB but at risk of its development must be considered. The treatment options for LTBI include isoniazid, rifampicin, isoniazid/rifampicin, and isoniazid/rifapentine. The benefits and risks of these agents based on the age of the patient and their hepatotoxicity must be considered when selecting the appropriate drug. Standardized diagnosis and treatment of LTBI based on the updated 2017 guidelines will contribute to the control of TB in Korea as well as to further revisions of the guidelines.
Ļ▓░ĒĢĄĻĘĀņŚÉ Ļ░ÉņŚ╝ņØ┤ ļÉśļ®┤ Ļ░ÉņŚ╝ņ×ÉņØś 90%ļŖö Ļ░ÉņŚ╝ņŚÉļÅä ļČłĻĄ¼ĒĢśĻ│Ā Ļ▓░ĒĢĄņØ┤ ļ░£ļ│æĒĢśņ¦Ć ņĢŖņ£╝ļ®░, ņĢĮ 5% ņĀĢļÅäļŖö Ļ░ÉņŚ╝ Ēøä 1-2ļģä ļé┤ņŚÉ Ļ▓░ĒĢĄņØ┤ ļ░£ļ│æĒĢĀ ĒÖĢļźĀņØ┤ ļåÆĻ│Ā, ļéśļ©Ėņ¦Ć 5%ļŖö ņØ┤Ēøä ĒÅēņāØņØś ņ¢┤ļŖÉ ņł£Ļ░äņŚÉ Ļ▓░ĒĢĄņØ┤ ļ░£ļ│æĒĢśĻ▓ī ļÉ£ļŗż. ņ×Āļ│ĄĻ▓░ĒĢĄ Ļ░ÉņŚ╝(latent tuberculosis infection, LTBI)ņØ┤ļ×Ć Ļ▓░ĒĢĄĻĘĀņŚÉ Ļ░ÉņŚ╝ņØ┤ ļÉśņŚłņ£╝ļéś ņÖĖļČĆļĪ£ ļéśĒāĆļéśļŖö ņ”ØņāüņØ┤ ņŚåĻ│Ā, ļ░®ņé¼ņäĀĒĢÖņĀü Ļ▓Ćņé¼ļéś ļ»ĖņāØļ¼╝ĒĢÖņĀüņØĖ ņ”ØĻ▒░Ļ░Ć ņŚåļŖö ņĀĢņāüņØĖ Ļ▓ĮņÜ░ļź╝ ļ¦ÉĒĢ£ļŗż[1]. ņÜ░ļ”¼ļéśļØ╝ņØś Ļ▓ĮņÜ░ļŖö ņŚ░Ļ░ä Ļ▓░ĒĢĄ ĒÖśņ×É ļ░£ļ│æļźĀņØ┤ 2010ļģä Ļ▓ĮņÜ░ 97ļ¬ģ/10ļ¦ī ļ¬ģņŚÉņä£ 2017ļģä Ļ▓ĮņÜ░ 70ļ¬ģ/10ļ¦ī ļ¬ģņ£╝ļĪ£ ņĀÉņ░© Ļ░Éņåī ņČöņäĖļź╝ ļ│┤ņØ┤Ļ│Ā ņ׳ņ¢┤, ņäĖĻ│äņŚÉņä£ ņżæĻ░ä ņĀĢļÅä(intermediate)ņŚÉ ņåŹĒĢ£ļŗż[2,3]. 2016ļģäņŚÉ ļ»ĖĻĄŁĻ│╝ ņśüĻĄŁņØś LTBI ņ¦äļŻī ņ¦Ćņ╣©ņØ┤ Ļ░£ņĀĢļÉśņŚłļŗż[4,5]. ĻĄŁļé┤ņØś Ļ▓ĮņÜ░ Ļ▓░ĒĢĄ Ēć┤ņ╣ś ļ░®ļ▓ĢņŚÉ ņ׳ņ¢┤ņä£ļŖö Ļ│╝Ļ▒░ņŚÉ ņżæļÅäņĀü ņĀäļץņØä ņĘ©ĒĢśĻ│Ā ņ׳ņŚłņ£╝ļéś, Ļ▓░ĒĢĄņØś ņ¦æļŗ© ļ░£ļ│æņØś ņ×”ņØĆ ļ│┤Ļ│Ā ĻĘĖļ”¼Ļ│Ā ļģĖļĀ╣ĒÖö ļ░Å ņØśĒĢÖņØś ļ░£ņĀäņŚÉ ļö░ļźĖ ļ®┤ņŚŁ ņĀĆĒĢś ĒÖśņ×ÉļōżņØś ņ”ØĻ░Ć ņČöņäĖļĪ£ ņØĖĒĢśņŚ¼ ņ×Āļ│ĄĻ▓░ĒĢĄ ĒÖśņ×ÉņŚÉ ļīĆĒĢ£ ņ╣śļŻī ņ¦Ćņ╣©ņØ┤ 2011ļģä ĻĄŁļé┤ Ļ▓░ĒĢĄ ņ¦äļŻī ņ¦Ćņ╣©ļČĆĒä░ Ļ░ĢĒÖöļÉśņŚłĻ│Ā[6], 2014ļģäĻ│╝ 2017ļģäņŚÉ ĻĖ░ņĪ┤ ņ¦äļŻī ņ¦Ćņ╣©ņØ┤ Ļ░£ņĀĢļÉśņŚłļŗż[7]. Ēśäņ×¼ ĻĄŁļé┤ņŚÉņä£ļŖö LTBIņØś ņ¦äļŗ©ņŚÉ ņ╣śļŻīņŚÉ ļīĆĒĢ£ ņØśļŻīņĀü ņé¼ĒÜīņĀü ĒĢ®ņØśĻ░Ć ņ”ØĻ░ĆĒĢśĻ│Ā ņ׳ļŖö Ļ░ĆņÜ┤ļŹ░, ļ│Ė ĻĖĆņŚÉņä£ļŖö ĻĄŁļé┤ņØś 2017 Ļ▓░ĒĢĄ ņ¦äļŻī ņ¦Ćņ╣©ņØś LTBI Ļ┤ĆļĀ© ļé┤ņÜ® ņżæ ņŻ╝ņÜö ņé¼ĒĢŁ ļ░Å Ļ░£ņĀĢ ņé¼ĒĢŁ ņżæņŗ¼ņ£╝ļĪ£ ņé┤ĒÄ┤ļ│┤Ļ│Āņ×É ĒĢ£ļŗż.
Ēł¼ļ▓Āļź┤ņ┐©ļ”░ Ļ▓Ćņé¼(tuberculin skin test, TST)ļź╝ ĒåĄĒĢśņŚ¼ ĒÖĢņØĖļÉ£ ĻĄŁļé┤ Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ļźĀņØĆ 1985ļģäĻ│╝ 1995ļģäļÅäņØś Ļ▓ĮņÜ░ 20-24ņäĖņŚÉņä£ Ļ░üĻ░ü 74.5%ņÖĆ 59.3%ņØś ņ¢æņä▒ļźĀņØä ļ│┤ņśĆĻ│Ā[8], 2000ļģäļÅä ņżæļ░śņØś 15-20ņäĖ Ļ│Āļō▒ĒĢÖņāØĻ│╝ ņĀŖņØĆ ĻĄ░ņØĖņŚÉņä£ļŖö 20-30%ņØś TST ņ¢æņä▒ļźĀņØä ļ│┤ņśĆņ£╝ļéś[9,10], BCG ņČöĻ░Ć ņĀæņóģņØä ļ░øņ¦Ć ņĢŖņØĆ ļīĆņāüņ×ÉĻ░Ć ļīĆļŗżņłśņØĖ 2000ļģäļÅä Ēøäļ░ś ļ░Å 2010ļģäļÅä ņ┤łļ░śņŚÉņä£ņØś 20ļīĆļź╝ ņĀäĒøäĒĢ£ ņŚ░ļĀ╣ļīĆņØś TST ņ¢æņä▒ļźĀņØĆ 14-16%ļĪ£ Ļ░ÉņåīĒĢśņśĆļŗż[11].
LTBI Ļ▓Ćņé¼ļŖö Ļ▓░ĒĢĄĻĘĀņŚÉ Ļ░ÉņŚ╝ņØ┤ ļÉśņŚłņ£╝ļéś ļ░£ļ│æĒĢśņ¦Ć ņĢŖņØĆ ņāüĒā£ņŚÉņä£ ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄņ£╝ļĪ£ ņ¦äĒ¢ēĒĢĀ ņ£äĒŚśņØ┤ ļåÆņØĆ Ļ░£ņØĖ ļ░Å ņ¦æļŗ©ņØä ļīĆņāüņ£╝ļĪ£ ĒĢśļŖö targeted TST ņøÉņ╣ÖņØä ņżĆņÜ®ĒĢśĻ│Ā[12], Ļ│╝Ļ▒░ LTBI ņ╣śļŻīņ×É ļśÉļŖö ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄņØä ņ╣śļŻīĒĢ£ ļīĆņāüņ×ÉņØś ņāłļĪ£ņÜ┤ Ļ░ÉņŚ╝ņØ┤ ņØśņŗ¼ļÉśļŖö Ļ▓ĮņÜ░ļŖö ĒĢ┤ļŗ╣ ļīĆņāüņ×ÉņØś Ļ▓░ĒĢĄ ļ░£ļ│æ ņ£äĒŚśļÅäļź╝ Ļ│ĀļĀżĒĢśņŚ¼ LTBI ņ╣śļŻī ņŚ¼ļČĆļź╝ Ļ▓░ņĀĢĒĢ£ļŗż.
ĻĄŁļé┤ņØś LTBI ņ¦äļŗ©ņŚÉļŖö RT-23 2Tļź╝ ņé¼ņÜ®ĒĢ£ TST Ļ▓Ćņé¼ņÖĆ interferon-gamma release assay (IGRA) Ļ▓Ćņé¼Ļ░Ć ņé¼ņÜ®ļÉśļ®░, IGRA Ļ▓Ćņé¼ņØś ņóģļźśņŚÉļŖö QuantiFERONŌōć-TB Gold In Tube (QFT-IT; Qiagen, Hilden, Germany), ņŚ¼ĻĖ░ņŚÉ ĒĢŁņøÉ TB2Ļ░Ć ņČöĻ░ĆļÉ£ QFT-Plus (Qiagen, Hilden, Germany) ĻĘĖļ”¼Ļ│Ā T-SPOT.TB (TSPOT; Oxford Immunotec, Abingdon, UK) Ļ▓Ćņé¼ ļō▒ņØ┤ ņ׳ļŗż. ņØ┤ Ļ▓Ćņé¼ļōżņØĆ ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄĻ│╝ LTBIļź╝ ĻĄ¼ļČäĒĢśņ¦Ć ļ¬╗ĒĢśļ®░, ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄņØä ļ░░ņĀ£ĒĢśļŖö Ļ│╝ņĀĢņØ┤ ĒĢäņÜöĒĢśļŗż. TST Ļ▓Ćņé¼ņŚÉ Ļ┤ĆĒĢ£ 2017ļģäņØś Ļ░£ņĀĢ ņ¦Ćņ╣©ņŚÉņä£ļŖö TSTļź╝ ĻĖ░ļ│Ė Ļ▓Ćņé¼ļĪ£ ņé¼ņÜ®ĒĢĀ ļĢī BCG ņĀæņóģļĀźņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░ TST ņ£äņ¢æņä▒ņØä ļ░░ņĀ£ĒĢśĻĖ░ ņ£äĒĢśņŚ¼ IGRAļź╝ ņČöĻ░ĆļĪ£ ņŗ£Ē¢ēĒĢśļ®░, BCG ņĀæņóģļĀźņØ┤ ņŚåļŖö Ļ▓ĮņÜ░ TST ļŗ©ļÅģņ£╝ļĪ£ LTBIļź╝ ņ¦äļŗ©ĒĢĀ ņłś ņ׳ļŗż. ļŗ©, BCG ņĀæņóģĒĢ£ Ļ▓ĮņÜ░ļØ╝ļÅä TST 15 mm ņØ┤ņāüņØĖ Ļ▓ĮņÜ░ļŖö IGRA Ļ▓Ćņé¼ ņŚåņØ┤ LTBI ņ¢æņä▒ņ£╝ļĪ£ ņ¦äļŗ©ĒĢĀ ņłś ņ׳ļŗż. Ļ│╝Ļ▒░ TST Ļ▓Ćņé¼ņŚÉņä£ ņØīņä▒ņØ┤ ĒÖĢņØĖļÉ£ Ļ▓ĮņÜ░ņŚÉļŖö TST ļŗ©ļÅģņ£╝ļĪ£ LTBIļź╝ ņ¦äļŗ©ĒĢ£ļŗż. IGRA Ļ▓Ćņé¼ņØś Ļ▓ĮņÜ░ļŖö TSTņŚÉņä£ņÖĆ ļ¦łņ░¼Ļ░Ćņ¦ĆļĪ£ ņ¢æņä▒ņØś Ļ▓░Ļ│╝Ļ░Ć ļéśņśżļ®┤ ņØ┤Ēøä ļ░śļ│Ą Ļ▓Ćņé¼ļź╝ ļŗżņŗ£ ĒĢśņ¦Ć ņĢŖļÅäļĪØ ĻČīĻ│ĀĒĢ£ļŗż.
ņĀĢņāü ļ®┤ņŚŁņØĖņŚÉņä£ļŖö TSTĻ░Ć LTBI ņ¦äļŗ©ņØś ņ£ĀņØ╝ĒĢ£ Ļ▓Ćņé¼ļĪ£ ņŚ¼Ļ▓©ņĪīņ£╝ļéś, IGRA ļŗ©ļÅģ Ēś╣ņØĆ TST/IGRA 2ļŗ©Ļ│ä Ļ▓Ćņé¼(two-step strategy)ņŚÉļÅä ņé¼ņÜ® Ļ░ĆļŖźĒĢśļŗż. ļ»ĖĻĄŁņØĆ IGRA ļśÉļŖö TSTļź╝ ņé¼ņÜ®ĒĢĀ ņłś ņ׳ļŗżĻ│Ā ĻČīĻ│ĀĒĢśļÉś, ņĄ£ĻĘ╝ ņ¦Ćņ╣©ņŚÉņä£ļŖö IGRAļź╝ ņÜ░ņäĀ ĻČīĻ│ĀĒĢśĻ│Ā ņ׳Ļ│Ā[4], ņśüĻĄŁņØĆ TSTļź╝ ĻĖ░ļ│Ėņ£╝ļĪ£ ĒĢśļÉś ņāüĒÖ®ņŚÉ ļö░ļØ╝ IGRA ļŗ©ļÅģ ļśÉļŖö ņČöĻ░Ć Ļ▓Ćņé¼ļź╝ ĒĢśļÅäļĪØ ĻČīĻ│ĀĒĢśĻ│Ā ņ׳ļŗż[5]. TST/IGRA 2ļŗ©Ļ│ä Ļ▓Ćņé¼ļŖö BCG ņĀæņóģņØ┤ļéś ļ╣äĻ▓░ĒĢĄ ĒĢŁņé░ĻĘĀ Ļ░ÉņŚ╝ņŚÉ ņØśĒĢ£ TST ņ£äņ¢æņä▒ņØś Ļ░ĆļŖźņä▒ņØ┤ ņ”ØĻ░ĆĒĢśļ»ĆļĪ£ ĒŖ╣ņØ┤ļÅäĻ░Ć ļåÆņØĆ IGRAļź╝ ņČöĻ░Ć ņŗ£Ē¢ēĒĢśļŖö ļ░®ļ▓ĢņØ┤ļŗż. ņ¦äļŗ©ņĀü ņĀæĻĘ╝ ņĢīĻ│Āļ”¼ņ”śņØĆ ĻĘĖļ”╝ 1Ļ│╝ Ļ░Öļŗż.
ļ®┤ņŚŁ ņĀĆĒĢśņ×ÉņŚÉņä£ļŖö IGRA ļŗ©ļÅģ Ēś╣ņØĆ TSTņÖĆ IGRA Ļ▓Ćņé¼ ļ│æĒĢ®ļ▓ĢņØä ņé¼ņÜ®ĒĢĀ ņłś ņ׳ņ£╝ļ®░ TST ļŗ©ļÅģņ£╝ļĪ£ LTBI ņØīņä▒ņ£╝ļĪ£ ņ¦äļŗ©ĒĢśļŖö Ļ▓āņØĆ ĻČīĻ│ĀĒĢśņ¦Ć ņĢŖļŖöļŗż. ļæÉ Ļ▓Ćņé¼ļź╝ ļ│æĒĢ® ņé¼ņÜ®ņŗ£ ļæÉ Ļ▓Ćņé¼ ņżæ ĒĢśļéśļØ╝ļÅä ņ¢æņä▒ņØ╝ ļĢī Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ņ£╝ļĪ£ ĒīÉņĀĢĒĢ£ļŗż. ņĀĢņāü ļ®┤ņŚŁņØĖņŚÉņä£ļŖö TST ņ¢æņä▒ņ×ÉņŚÉņä£ IGRAļź╝ ņŗ£Ē¢ēĒĢśļŖö 2ļŗ©Ļ│ä ļ▓ĢņØä ņŗ£Ē¢ē Ļ░ĆļŖźĒĢśļéś, ļ®┤ņŚŁ ņĀĆĒĢśņ×ÉņŚÉņä£ļŖö ņĀüņÜ®ļÉśņ¦Ć ņĢŖļŖöļŗż[13]. LTBIĻ▓Ćņé¼Ļ░Ć ņØīņä▒ņØ┤ļŹöļØ╝ļÅä Ļ│╝Ļ▒░ Ļ▓░ĒĢĄ ņ╣śļŻīļĀź ņŚåņØ┤ ņ×ÉņŚ░ ņ╣śņ£ĀļÉ£ Ļ▓░ĒĢĄ ļ│æļ│ĆņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░ļŖö LTBIļĪ£ Ļ░äņŻ╝ĒĢ£ļŗż. ĒĢ£ĒÄĖ ļ®┤ņŚŁ ņĀĆĒĢśņ×ÉņŚÉņä£ IGRA Ļ▓░Ļ│╝Ļ░Ć ĒīÉļÅģ ļČłļŖź(indeterminate result)ņØĖ Ļ▓ĮņÜ░ ļ░śļ│Ą Ļ▓Ćņé¼ņŗ£ ļŗżņŗ£ ĒīÉļÅģ ļČłļŖźņØĖ Ļ▓ĮņÜ░Ļ░Ć ĒØöĒĢśļ»ĆļĪ£, IGRA ļŗ©ļÅģĻ▓Ćņé¼ņŚÉņä£ ĒīÉļÅģ ļČłļŖźņ£╝ļĪ£ ļéśņśżļŖö Ļ▓ĮņÜ░ļŖö TST Ļ▓░Ļ│╝ņŚÉ ļö░ļØ╝ņä£ LTBI ņŚ¼ļČĆļź╝ ņ¦äļŗ©ĒĢ£ļŗż[14]. ņ¦äļŗ©ņĀü ņĀæĻĘ╝ ņĢīĻ│Āļ”¼ņ”śņØĆ ĻĘĖļ”╝ 2ņÖĆ Ļ░Öļŗż.
ņŚ░ņåŹņĀüņØĖ Ēł¼ļ▓Āļź┤ņ┐©ļ”░ Ļ▓Ćņé¼(serial TST)ļØ╝ ĒĢśļ®┤ ņĀæņ┤ēņ×É Ļ▓Ćņ¦äņØś LTBI Ļ▓Ćņé¼ņŚÉņä£ window period ĻĖ░Ļ░ä(ņĀäņŚ╝ņä▒ Ļ▓░ĒĢĄ ĒÖśņ×ÉņÖĆ ļ¦łņ¦Ćļ¦ēņ£╝ļĪ£ ņĀæņ┤ēĒĢ£ņ¦Ć 8ņŻ╝Ļ░Ć ņ¦Ćļéśņ¦Ć ņĢŖņØĆ ĻĖ░Ļ░ä)ņØś TST ņ£äņØīņä▒ ļ░śņØæņØä Ļ│ĀļĀżĒĢśņŚ¼ ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄ ĒÖśņ×É ņĀæņ┤ē Ēøä 8ņŻ╝ ĒøäņŚÉ TSTļź╝ ļŗżņŗ£ ņŗ£Ē¢ēĒĢśļŖö serial TSTņÖĆ ņØśļŻīņØĖ ņĀĢĻĖ░Ļ▓Ćņ¦ä ļō▒ņØś LTBI Ļ▓Ćņé¼ņŚÉņä£ ņ”ØĒÅŁ ĒÜ©Ļ│╝(Ļ▓░ĒĢĄĻĘĀņŚÉ Ļ░ÉņŚ╝ļÉ£ ņ¦Ć ņśżļ×£ ņŗ£Ļ░äņØ┤ Ļ▓ĮĻ│╝ĒĢ£ ņé¼ļ×īņŚÉņä£ ņ▓śņØī TST Ļ▓Ćņé¼ļĪ£ ņØĖĒĢ┤ņä£ ĻĖ░ņ¢Ą ļ®┤ņŚŁ ļ░śņØæņ£╝ļĪ£ 1-4ņŻ╝ Ēøä ļæÉ ļ▓łņ¦Ė TST Ļ▓Ćņé¼ņŚÉņä£ņĢ╝ ļŖ”Ļ▓ī ļ░śņØæņØ┤ ļéśĒāĆļéśļŖö Ļ▓ā)ļź╝ Ļ│ĀļĀżĒĢśņŚ¼ ļæÉ ļ▓łņ¦Ė TSTļź╝ 1-4ņŻ╝ ĒøäņŚÉ ņŗ£Ē¢ēĒĢśļÉś ņĀĢĻĖ░ņĀü ņČöĻ░Ć Ļ▓Ćņé¼ļź╝ ņ£äĒĢ£ ĻĖ░ņĀĆ Ļ▓Ćņé¼ļĪ£ ņŗ£Ē¢ēĒĢśļŖö two-step TST Ļ▓Ćņé¼Ļ░Ć ņ׳ļŗż.
Ļ▓░ĒĢĄ ļ░£ļ│æ ņ£äĒŚśĻĄ░(Ļ│Ā┬Ęņżæļō▒ļÅä ņ£äĒŚśĻĄ░, Table 1)ņØĖ Ļ▓ĮņÜ░ ĒśĖĒØĪĻĖ░ Ļ▓░ĒĢĄ ĒÖśņ×ÉņÖĆņØś ņĀæņ┤ēņ×É Ļ▓Ćņ¦äņŚÉņä£ serial TSTļź╝ ņŗ£Ē¢ēĒĢ£ļŗż. ņ▓½ ļ▓łņ¦Ė TST Ļ▓░Ļ│╝Ļ░Ć 5 mm ļ»Ėļ¦īņØĖ Ļ▓ĮņÜ░ ļæÉ ļ▓łņ¦Ė TST Ļ▓░Ļ│╝Ļ░Ć 10 mm ņØ┤ņāüņØ┤ļ®┤ ņ¢æņĀäļÉ£ Ļ▓āņ£╝ļĪ£ ĒīÉņĀĢĒĢśļ®░, ņ▓½ ļ▓łņ¦Ė TST Ļ▓░Ļ│╝Ļ░Ć 5-9 mmņØĖ Ļ▓ĮņÜ░ļŖö ļæÉ ļ▓łņ¦Ė TST Ļ▓░Ļ│╝Ļ░Ć 6 mm ņØ┤ņāü ņ”ØĻ░ĆĒĢśņśĆņØä ļĢī ņ¢æņĀäņ£╝ļĪ£ ĒīÉņĀĢĒĢ£ļŗż. ĒĢ£ĒÄĖ Ļ▓░ĒĢĄĻĘĀņØä ļŗżļŻ©ļŖö Ļ▓Ćņé¼ņŗż ļśÉļŖö Ļ▓░ĒĢĄ ĒÖśņ×ÉņÖĆ ņĀæņ┤ēņØ┤ ļ¦ÄņØĆ ĒÖśĻ▓ĮņŚÉņä£ ņØ╝ĒĢśļŖö ņé¼ļ×īļōżņŚÉ ļīĆĒĢ┤ņä£ ņĄ£ĻĘ╝ Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ ņŚ¼ļČĆļź╝ ĒÖĢņØĖĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ņØ╝ņĀĢ ĻĖ░Ļ░äļ¦łļŗż ņĀĢĻĖ░ņĀüņØĖ TSTļź╝ ņŗ£Ē¢ēĒĢśļŖö two-step TST Ļ▓ĮņÜ░ņØś ĻĖ░ņżĆļÅä ļ¦łņ░¼Ļ░Ćņ¦ĆņØ┤ļŗż. ĻĘĖļ¤¼ļéś ņĀæņ┤ēņ×É Ļ▓Ćņ¦äņØś Ļ▓ĮņÜ░, ņĀæņ┤ēĒĢ£ Ļ░ÉņŚ╝ņøÉņØ┤ ņĀäņŚ╝ļĀźņØ┤ ļåÆņØĆ Ļ▓ĮņÜ░, ņĀæņ┤ēņ×ÉĻ░Ć Ļ░ÉņŚ╝ņøÉĻ│╝ ĻĖ┤ļ░Ć Ēś╣ņØĆ ņןĻĖ░Ļ░ä ņĀæņ┤ēĒĢ£ Ļ▓ĮņÜ░, ņĀæņ┤ēņ×ÉĻ░Ć 5ņäĖ ļ»Ėļ¦īņØ┤Ļ▒░ļéś ļ®┤ņŚŁ ņĀĆĒĢśņ×ÉņØĖ Ļ▓ĮņÜ░ ļō▒ņŚÉņä£ļŖö ņØ┤ņĀä Ļ▓░Ļ│╝ļ│┤ļŗż 6 mm ņØ┤ņāü ņ”ØĻ░ĆĒĢśļ®┤ ņ¢æņĀäļÉ£ Ļ▓āņ£╝ļĪ£ ņĘ©ĻĖēĒĢĀ ņłś ņ׳ļŗż(ņśł, 3 mm ŌåÆ 9 mm).
5ņäĖ ļ»Ėļ¦īņŚÉņä£ LTBI Ļ▓Ćņé¼ļ▓Ģņ£╝ļĪ£ IGRA ņé¼ņÜ®ņØä ĻĖłĒĢśĻ│Ā ņ׳ņ£╝ļ®░, 5-18ņäĖņØś Ļ▓ĮņÜ░ļÅä TST Ļ▓░Ļ│╝Ļ░Ć ņ£äņ¢æņä▒ņØ╝ Ļ░ĆļŖźņä▒ņØ┤ ļåÆņØĆ Ļ▓ĮņÜ░(BCGļź╝ 1ņäĖ ņØ┤Ēøä ņĀæņóģļ░øņĢśĻ▒░ļéś 2ĒÜī ņØ┤ņāü ņĀæņóģļ░øņØĆ Ļ▓ĮņÜ░ ļō▒)ļź╝ ņĀ£ņÖĖĒĢśĻ│ĀļŖö IGRA ļŗ©ļÅģ ņé¼ņÜ®ņØä ĻČīĒĢśĻ│Ā ņ׳ņ¦Ć ņĢŖļŗż.
LTBI Ļ▓Ćņé¼ļź╝ ĒĢśļŖö Ļ▓āņØĆ LTBI ņ╣śļŻīļź╝ ĒĢśĻĖ░ ņ£äĒĢ©ņØ┤ļŗż. LTBI Ļ▓Ćņé¼ ļīĆņāüņ×ÉļŖö Ēü¼Ļ▓ī ŌĆ£ņĀäņŚ╝ņä▒ Ļ▓░ĒĢĄ ĒÖśņ×ÉņÖĆ ņĀæņ┤ēĒĢ£ ņĀæņ┤ēņ×É Ļ▓Ćņ¦ä ļīĆņāüņ×ÉŌĆØĻ░Ć ņĢäļŗī Ļ▓ĮņÜ░ņÖĆ ŌĆ£ņĀæņ┤ēņ×É Ļ▓Ćņ¦ä ļīĆņāüņ×ÉŌĆØņØĖ Ļ▓ĮņÜ░ļĪ£ ļéśļłłļŗż.
Ļ▓░ĒĢĄ ļ░£ļ│æ Ļ│Āņ£äĒŚśĻĄ░Ļ│╝ Ļ▓░ĒĢĄļ░£ļ│æ ņżæļō▒ļÅä ņ£äĒŚśĻĄ░ņ£╝ļĪ£ ļČäļźśļź╝ ĒĢĀ ņłś ņ׳ņ£╝ļ®░[15], Ļ▓░ĒĢĄ ļ░£ļ│æ Ļ│Āņ£äĒŚśĻĄ░ņŚÉņä£ļŖö LTBIļĪ£ ĒīÉļ¬ģļÉ£ Ļ▓ĮņÜ░ņŚÉ LTBI ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśļ®░, Ļ▓░ĒĢĄ ļ░£ļ│æ ņżæļō▒ļÅä ņ£äĒŚśĻĄ░ņŚÉņä£ļŖö LTBIļĪ£ ĒīÉļ¬ģļÉ£ Ļ▓ĮņÜ░ņŚÉ LTBI ņ╣śļŻīļź╝ Ļ│ĀļĀżĒĢĀ ņłś ņ׳ļŗż. 2017 Ļ░£ņĀĢĒīÉ ņ¦Ćņ╣©ņŚÉņä£ļŖö ĻĖ░ņĪ┤ņØś ņżæļō▒ļÅä ļ▓öņ£äņŚÉņä£[16] ĒØēļČĆ XņäĀņāü Ļ│╝Ļ▒░ Ļ▓░ĒĢĄ ņ╣śļŻīļĀź ņŚåņØ┤ ņ×ÉņŚ░ ņ╣śņ£ĀļÉ£ Ļ▓░ĒĢĄ ļ│æļ│ĆņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░Ļ░Ć Ļ│Āņ£äĒŚśĻĄ░ņ£╝ļĪ£ ļ│ĆĻ▓ĮļÉśņŚłĻ│Ā, ĒØēļČĆ XņäĀ ļ░Å CTņāü ņ╣śņ£ĀļÉ£ Ļ▓░ĒĢĄ ņØśņŗ¼ ņåīĻ▓¼ņØ┤ Ļ┤Ćņ░░ļÉĀ ļĢī Ļ│╝Ļ▒░ņØś ņĀüņĀłĒĢ£ Ļ▓░ĒĢĄ ņ╣śļŻīļĀźņØä ļ░śļō£ņŗ£ ĒÖĢņØĖĒĢśĻ│Ā, Ļ│╝Ļ▒░ ĒØēļČĆ XņäĀĻ│╝ ļ╣äĻĄÉĒĢśĻ│Ā ņäĖĻĘĀĒĢÖņĀü Ļ▓Ćņé¼ ļ░Å Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ ļō▒ņØä ĒåĄĒĢ£ ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄņØä ļ░░ņĀ£ĒĢśļŖö Ļ│╝ņĀĢņØ┤ ĒĢäņÜöĒĢśļŗż. Ļ▓░ĒĢĄ ļ░£ļ│æ Ļ│Āņ£äĒŚśĻĄ░ņŚÉņä£ Ļ│╝Ļ▒░ Ļ▓░ĒĢĄ ņ╣śļŻīļĀź ņŚåņØ┤ ņ×ÉņŚ░ ņ╣śņ£ĀļÉ£ Ļ▓░ĒĢĄ ļ│æļ│ĆņØ┤ ņĪ┤ņ×¼ĒĢśļŖö Ļ▓ĮņÜ░ LTBI Ļ▓Ćņé¼ Ļ▓░Ļ│╝ņÖĆ ļ¼┤Ļ┤ĆĒĢśĻ▓ī LTBIļĪ£ ņ¦äļŗ©ĒĢśļ®░, Ļ▓░ĒĢĄ ļ░£ļ│æ ņżæļō▒ļÅä ņ£äĒŚśĻĄ░ Ēś╣ņØĆ ņ£äĒŚśņØĖņ×ÉĻ░Ć ņŚåļŖö ņĀĢņāüņØĖņŚÉņä£ ņ×ÉņŚ░ ņ╣śņ£ĀļÉ£ Ļ▓░ĒĢĄ ļ│æļ│ĆņØś ĒØēļČĆ XņäĀ ņåīĻ▓¼ņØä ļ│┤ņØ╝ Ļ▓ĮņÜ░ Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ņĢ╝ ĒĢśļ®░, ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░ LTBIļĪ£ ņ¦äļŗ©ĒĢśĻ│Ā ņ╣śļŻīĒĢ£ļŗż. ļŗ©, ņżæļō▒ļÅä ņ£äĒŚśĻĄ░ņŚÉņä£ļŖö Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ Ļ▓Ćņé¼ ņØīņä▒ņØ┤ļØ╝ļÅä LTBI ņ╣śļŻīļź╝ Ļ│ĀļĀżĒĢĀ ņłś ņ׳ļŗż. ĒĢ£ĒÄĖ ņ£äĒŚśĻĄ░ņØś ļČäļźśņŚÉ ņ׳ņ¢┤ņä£ļŖö ŌĆ£ļ¦īņä▒ņŗĀļČĆņĀäŌĆØņØä ŌĆ£Ēł¼ņäØ ņżæņØĖ ļ¦īņä▒ņŗĀļČĆņĀäŌĆØņ£╝ļĪ£ ņÜ®ņ¢┤Ļ░Ć ļ│ĆĻ▓ĮļÉśņŚłļŗż[7].
ņĀæņ┤ēņ×É Ļ▓Ćņ¦äņŗ£ LTBI Ļ▓Ćņé¼ļŖö ņ£äņŚÉņä£ ļČäļźśĒĢ£ Ļ▓░ĒĢĄ ļ░£ļ│æņØś ņ£äĒŚśĻĄ░ņØ┤ ņĢäļŗī Ļ▓ĮņÜ░ņŚÉ ņāüĒĢ£ ņŚ░ļĀ╣ ņĀ£ĒĢ£ņØ┤ 35ņäĖņŚÉņä£ 65ņäĖ ņØ┤ĒĢśļĪ£ ņāüĒ¢ź ņĪ░ņĀĢļÉśņŚłņ£╝ļ®░ ņØ┤ļŖö ņŚ░ļĀ╣ ņ”ØĻ░ĆņŚÉ ļö░ļźĖ LTBI ņ╣śļŻīņØś ļ╣äņÜ® ļīĆļ╣ä ĒÜ©Ļ│╝ļź╝ 65ņäĖļĪ£ ņĀ£ņŗ£ĒĢ£ 2016ļģä ņśüĻĄŁņØś National Institute for Health and Clinical Excellence (NICE) ņ¦Ćņ╣©ņØś ļé┤ņÜ®ņØä ņłśņÜ®ĒĢ£ Ļ▓░Ļ│╝ņØ┤ļ®░[5], Ļ░äļÅģņä▒ņØ┤ ņĀüņØĆ rifapentineņØä ņé¼ņÜ®ĒĢśņŚ¼ isoniazid, rifapentineņØś 3Ļ░£ņøö Ļ░äĒŚÉ ņÜöļ▓Ģ(3H1P1, ņŻ╝ 1ĒÜīņö® ņ┤Ø 12ĒÜī ļ│ĄņÜ®)ņØä ņé¼ņÜ®ĒĢśļŖö Ļ▓ĮņÜ░ļŖö ņāüĒĢ£ ņŚ░ļĀ╣ ņĀ£ĒĢ£ ņŚåņØ┤ ņé¼ņÜ®Ļ░ĆļŖźĒĢ£ Ļ▓āņ£╝ļĪ£ ļ│ĆĻ▓ĮļÉśņŚłļŖöļŹ░, ņØ┤ļŖö ĻĄŁļé┤ņØś ļåÆņØĆ Ļ▓░ĒĢĄ ņ£Āļ│æļźĀņØä Ļ░Éņåīņŗ£ĒéżĻĖ░ ņ£äĒĢ£ ņĀĢņ▒ģņĀüņØĖ ļīĆņĢłņØ┤ļŗż. ņ£äņŚÉņä£ ļČäļźśĒĢ£ Ļ▓░ĒĢĄ ļ░£ļ│æ Ļ│Āņ£äĒŚśĻ│╝ ņżæļō▒ļÅä ņ£äĒŚśĻĄ░ņŚÉ ņåŹĒĢśļŖö ļīĆņāüņ×ÉņØś Ļ▓ĮņÜ░ ņĀäņŚ╝ņä▒ Ļ▓░ĒĢĄ ĒÖśņ×ÉņÖĆ ņĀæņ┤ēĒĢ£ Ļ▓ĮņÜ░ ņĀæņ┤ēņ×É Ļ▓Ćņ¦äņØä ņŗ£Ē¢ēĒĢśņŚ¼ LTBI Ļ░ÉņŚ╝ņØ┤ ĒīÉļ¬ģļÉśļ®┤ LTBI ņ╣śļŻīļź╝ Ļ│ĀļĀżĒĢśļŖö Ļ▓āņØ┤ ņĢäļŗłļØ╝ ļ░śļō£ņŗ£ ņŗ£Ē¢ēĒĢ┤ņĢ╝ ĒĢ£ļŗż.
ņ▓śņØī TST ņØīņä▒ņØĖ Ļ▓ĮņÜ░ļŖö ņ£äņŚÉņä£ ļČäļźśĒĢ£ Ļ▓░ĒĢĄ ļ░£ļ│æ ņżæļō▒ļÅä ņ£äĒŚśĻĄ░Ļ│╝ Ļ│Āņ£äĒŚśĻĄ░ņØä ļīĆņāüņ£╝ļĪ£ ņČöĻ░Ć Ļ▓Ćņé¼ TST (serial TST)ļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ ņŚ¼ļČĆļź╝ ņ×¼ĒīÉņĀĢĒĢśĻ▓ī ļÉ£ļŗż. ņÖ£ļāÉĒĢśļ®┤ ĒśĖĒØĪĻĖ░ļź╝ ĒåĄĒĢśņŚ¼ Ļ▓░ĒĢĄĻĘĀņØ┤ ņ╣©ļ▓öĒĢśļ®┤ 2-8ņŻ╝ņŚÉ Ļ▒Ėņ│Éņä£ Ļ▓░ĒĢĄĻĘĀņŚÉ ļīĆĒĢ£ ņäĖĒżļ¦żĻ░£ņä▒ ļ®┤ņŚŁ ļ░śņØæņØ┤ ĒśĢņä▒ļÉśļŖöļŹ░, ņĀäņŚ╝ņä▒ Ļ▓░ĒĢĄ ĒÖśņ×ÉņÖĆ ņĀæņ┤ēĒĢśņŚ¼ Ļ▓░ĒĢĄĻĘĀņŚÉ Ļ░ÉņŚ╝ļÉśļŹöļØ╝ļÅä 8ņŻ╝Ļ╣īņ¦ĆļŖö Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ Ļ▓Ćņé¼ņŚÉņä£ ņ£äņØīņä▒ņØä ļ│┤ņØ╝ ņłś ņ׳ĻĖ░ ļĢīļ¼ĖņØ┤ļ®░(window period), ņØ┤ Ļ▓ĮņÜ░ņŚÉļŖö Ļ▓░ĒĢĄ ĒÖśņ×ÉņÖĆ ļ¦łņ¦Ćļ¦ē ņĀæņ┤ē Ēøä 8ņŻ╝ ĒøäņŚÉ ņČöĻ░Ć TST Ļ▓Ćņé¼ļź╝ ļŗżņŗ£ ņŗ£Ē¢ēĒĢ┤ņä£(serial TST) Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ ņŚ¼ļČĆļź╝ ņ×¼ĒīÉņĀĢĒĢśĻ▓ī ļÉ£ļŗż[17]. Ļ▓░ĒĢĄ ļ░£ļ│æ Ļ│Āņ£äĒŚśĻĄ░ņØĖ ŌĆ£2ņäĖ(24Ļ░£ņøö) ļ»Ėļ¦ī[5], ņןĻĖ░ņØ┤ņŗØņ£╝ļĪ£ ņØĖĒĢśņŚ¼ ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ļź╝ ļ│ĄņÜ® ņżæņØĖ ņ×É, tumor necrosis factor (TNF) ņé¼ņÜ®ņ×ÉŌĆØ ļō▒ņØś Ļ▓ĮņÜ░ļŖö ņØ┤ window period ĻĖ░Ļ░äņØś TST Ļ▓░Ļ│╝Ļ░Ć ņØīņä▒ņØĖ Ļ▓ĮņÜ░ņŚÉļÅä ņØ╝ļŗ© LTBI ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśĻ│Ā, ņĀäņŚ╝ņä▒ Ļ▓░ĒĢĄ ĒÖśņ×ÉņÖĆ ļ¦łņ¦Ćļ¦ēņ£╝ļĪ£ ņĀæņ┤ēĒĢ£ņ¦Ć 8ņŻ╝Ļ░Ć ņ¦Ćļé£ ĒøäņŚÉ Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ Ļ▓Ćņé¼ļź╝ ļŗżņŗ£ ņŗ£Ē¢ēĒĢ┤ņä£ ņØ┤ļĢīļÅä ņØīņä▒ņØ┤ļ®┤ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢśĻ│Ā ņ¢æņä▒ņØ┤ļ®┤ ņĄ£ĻĘ╝ Ļ░ÉņŚ╝ņ£╝ļĪ£ ņ¦äļŗ©ĒĢśĻ│Ā LTBI ņ╣śļŻīļź╝ ņ£Āņ¦ĆĒĢśļ®░, HIV Ļ░ÉņŚ╝ņØĖ Ļ▓ĮņÜ░ņŚÉļŖö Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ Ļ▓Ćņé¼ņŚÉņä£ ņØīņä▒ņØ┤ļØ╝ļÅä ņ×Āļ│ĄĻ▓░ĒĢĄ ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢ£ļŗż. Ļ▓░ĒĢĄ ļ░£ļ│æ ņżæļō▒ļÅä ņ£äĒŚśĻĄ░ņØĖ ŌĆ£2ņäĖļČĆĒä░ 18ņäĖ ņØ┤ĒĢśņØś ņåīņĢäņ▓Łņåīļģä, ĻĘ£ĒÅÉņ”Ø, ņןĻĖ░Ļ░ä ņŖżĒģīļĪ£ņØ┤ļō£ļź╝ ņé¼ņÜ® ņżæņØ┤Ļ▒░ļéś ņé¼ņÜ® ņśłņĀĢņ×É, Ēł¼ņäØ ņżæņØĖ ļ¦īņä▒ņŗĀļČĆņĀä, ļŗ╣ļć©ļ│æ, ļæÉĻ▓ĮļČĆņĢö ļ░Å ĒśłņĢĪņĢö, ņ£äņĀłņĀ£ņłĀ Ēś╣ņØĆ Ļ│ĄĒÜīņן ņÜ░ĒÜīņłĀ ņŗ£Ē¢ē Ēś╣ņØĆ ņŗ£Ē¢ē ņśłņĀĢņ×ÉŌĆØ ļō▒ņØś Ļ▓ĮņÜ░ļŖö ņĀäņŚ╝ņä▒ Ļ▓░ĒĢĄ ĒÖśņ×ÉņÖĆ ļ¦łņ¦Ćļ¦ēņ£╝ļĪ£ ņĀæņ┤ēĒĢ£ņ¦Ć 8ņŻ╝Ļ░Ć Ļ▓ĮĻ│╝ĒĢśņ¦Ć ņĢŖņØĆ ņāüĒÖ®(window period)ņŚÉņä£ TSTĻ░Ć ņØīņä▒ņØĖ Ļ▓ĮņÜ░ LTBI ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢśņ¦Ć ņĢŖĻ│Ā Ļ┤Ćņ░░ĒĢśļŗżĻ░Ć ļ¦łņ¦Ćļ¦ēņ£╝ļĪ£ ņĀæņ┤ēĒĢ£ņ¦Ć 8ņŻ╝(window period)Ļ░Ć ņ¦Ćļé£ ĒøäņŚÉ Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ Ļ▓Ćņé¼ļź╝ ļŗżņŗ£ ņŗ£Ē¢ēĒĢ┤ņä£ ņØ┤ļĢīļÅä ņØīņä▒ņØ┤ļ®┤ Ļ▓ĮĻ│╝ Ļ┤Ćņ░░ĒĢśĻ│Ā ņ¢æņä▒ņØ┤ļ®┤ ņĄ£ĻĘ╝ Ļ░ÉņŚ╝ņ£╝ļĪ£ ņ¦äļŗ©ĒĢśĻ│Ā LTBI ņ╣śļŻīļź╝ ņŗ£ņ×æĒĢ£ļŗż[17].
LTBIņØś ņ╣śļŻīļŖö ļŗżņØīĻ│╝ Ļ░ÖĻ│Ā, ņĄ£ĻĘ╝ ņĀäņŚ╝ņä▒ Ļ▓░ĒĢĄ ĒÖśņ×ÉņØś ņĀæņ┤ēņ×ÉņØś Ļ▓ĮņÜ░ ņĢĮņĀ£ ņäĀĒāØņŗ£ ņĀäņŚ╝ņøÉ(index case)ņØś ņĢĮņĀ£ Ļ░Éņłśņä▒ Ļ▓░Ļ│╝ļź╝ ņ░ĖĻ│ĀĒĢ£ļŗż.
Isoniazid (5 mg/kg/ņØ╝, ņĄ£ļīĆ 300 mg/ņØ╝) 9Ļ░£ņøö ņÜöļ▓Ģ(9H)ņØä ĻČīĻ│ĀĒĢśļéś 6H ņ╣śļŻīļÅä ļ╣äņÜ®-ĒÜ©Ļ│╝ ļ®┤ņŚÉņä£ļÅä ņÜ░ņłśĒĢśļ»ĆļĪ£ Ļ│ĀļĀżĒĢĀ ņłś ņ׳ļŗż.
ļ”¼Ēī£ĒĢĆ ļŗ©ļÅģ ņÜöļ▓Ģ: rifampin 4Ļ░£ņøö ņÜöļ▓Ģ(4R)ņØĆ ņ╣śļŻī ņÖäļŻīņ£©ņØ┤ ņÜ░ņłśĒĢśļ®░[18], ņØ┤ņåīļŗłņĢäņ¦Ćļō£ ļé┤ņä▒ Ļ▓░ĒĢĄ ņĀæņ┤ēņ×ÉņØś ņ╣śļŻīņĀ£ļĪ£ Ļ│ĀļĀżĒĢ┤ ļ│╝ ņłś ņ׳ļŗż.
ņØ┤ņåīļŗłņĢäņ¦Ćļō£/ļ”¼Ēī£ĒĢĆ ļ│æĒĢ® ņÜöļ▓Ģ: 3Ļ░£ņøö ņØ┤ņåīļŗłņĢäņ¦Ćļō£/ļ”¼Ēī£ĒĢĆ ļ│æĒĢ® ņÜöļ▓Ģ(3HR)ņØĆ ņśüĻĄŁņŚÉņä£ ĻČīĻ│ĀĒĢśĻ│Ā ņ׳ņ£╝ļ®░, ņĢĮļ¼╝ ļ│ĄņÜ® ĻĖ░Ļ░äņØ┤ ņ¦¦ņ£╝ļ»ĆļĪ£ ņł£ņØæļÅä ļ®┤ņŚÉņä£ ņÜ░ņłśĒĢśĻ│Ā, ņ╣śļŻī ĒÜ©Ļ│╝ ļ®┤ņŚÉņä£ļÅä 9Hļ│┤ļŗż ņÜ░ņłśĒĢśļŗżĻ│Ā ļ│┤Ļ│ĀļÉ£ ļ░ö ņ׳ļŗż[19].
ņØ┤ņåīļŗłņĢäņ¦Ćļō£/ļ”¼ĒīīĒÄ£Ēŗ┤ 12ĒÜī Ļ░äĒŚÉņĀü ņÜöļ▓Ģ: isoniazid, rifapentine 3Ļ░£ņøö Ļ░äĒŚÉ ņÜöļ▓Ģ(3H1P1)ņØĆ ņŻ╝ 1ĒÜī, ņ┤Ø 12ĒÜī ļ│ĄņÜ®ļ▓Ģņ£╝ļĪ£ ņāłļĪ£ņÜ┤ ņ╣śļŻīļ▓Ģņ£╝ļĪ£ ĻČīĻ│ĀļÉśņŚłņ£╝ļ®░, ņ▓┤ņżæ 50 kg ņØ┤ņāüņØś Ļ▓ĮņÜ░ ņØ┤ņåīļŗłņĢäņ¦Ćļō£ļŖö 900 mg/ņØ╝, ļ”¼ĒīīĒÄ£Ēŗ┤ņØĆ 900 mg/ņØ╝ņØ┤ļéś[20] ĻĄŁļé┤ņŚÉņä£ļŖö ņĢäņ¦ü Ļ▓ĮĒŚśņØ┤ ļ¦Äņ¦Ć ņĢŖļŗż.
ņĀæņ┤ēņ×É ņĪ░ņé¼ņāü LTBI ņ¢æņä▒ņØ┤Ļ│Ā Ļ░äļÅģņä▒ņØś ņ£äĒŚśņØĖņ×ÉĻ░Ć ņŚåļŖö Ļ▓ĮņÜ░ 9H/4R/3HRņØĆ 65ņäĖ ņØ┤ĒĢśņŚÉņä£ ņ╣śļŻī Ļ░ĆļŖźĒĢśļ®░, 3H1P1ņØĆ ļéśņØ┤ ņāüĒĢ£ ņŚåņØ┤ ņé¼ņÜ® Ļ░ĆļŖźĒĢśļŗż. Ļ░äļÅģņä▒ņØś ņ£äĒŚśņØĖņ×ÉĻ░Ć ņ׳ļŖö Ļ▓ĮņÜ░ 9H/4R/3HRņØĆ 35ņäĖ ņØ┤ĒĢś, 3H1P1ņØĆ 65ņäĖ ņØ┤ĒĢśņŚÉņä£ ņ╣śļŻīĻ░ĆļŖźĒĢśļéś, ĒØēļČĆ XņäĀ ņØ┤ņāü ņåīĻ▓¼ņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░ 3H1P1ņØĆ ļéśņØ┤ ņĀ£ĒĢ£ ņŚåņØ┤ ņé¼ņÜ® Ļ░ĆļŖźĒĢśļŗż. 35ņäĖ ņ┤łĻ│╝, 65ņäĖ ņØ┤ĒĢśņŚÉņä£ Ļ░äļÅģņä▒ ņ£äĒŚśņØĖņ×ÉĻ░Ć ņ׳ļŖö Ļ▓ĮņÜ░ 9H/3HR/4RņØś ņé¼ņÜ®ņØĆ ņ£äĒŚśĻ│╝ ņØ┤ļōØņØä Ļ│ĀļĀżĒĢśņŚ¼ ņé¼ņÜ®ĒĢśņŚ¼ņĢ╝ ĒĢ£ļŗż.
LTBI ņ╣śļŻī ņĀä ĻĖ░ņĀĆ Ļ▓Ćņé¼ļĪ£ complete blood count, aspartate aminotransferase/alanine aminotransferase, bilirubin Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśļ®░, ņ╣śļŻī ņŗ£ņ×æ ņŗ£ņĀÉ ļ░Å ļ¦żļŗ¼ ļ│æļĀź ņ▓ŁņĘ© ļ░Å ņ¦äņ░░ņØä ĒĢ┤ņĢ╝ ĒĢśļ®░, ĻĖ░ņĀĆ Ļ░äĻĖ░ļŖź Ļ▓Ćņé¼ņŚÉņä£ ņØ┤ņāüņØ┤ ņ׳Ļ▒░ļéś ņ£äĒŚśņØĖņ×ÉĻ░Ć ņ׳ļŖö Ļ▓ĮņÜ░ņŚÉļŖö ļ¦żļŗ¼ Ļ░äĻĖ░ļŖź Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢ£ļŗż. LTBI ņ╣śļŻīņØś Ļ▓░Ļ│╝ļź╝ ĒÖĢņØĖĒĢśĻĖ░ ņ£äĒĢ£ Ļ▓Ćņé¼ ļ░®ļ▓ĢņØĆ ņŚåļŗż.
9H ņÜöļ▓ĢņØ┤ ĻČīņןļÉśļ®░, ņŚäļ¦łĻ░Ć ņØ┤ņåīļŗłņĢäņ¦Ćļō£ ņ╣śļŻī ņżæņØ┤ļ®░ ļ¬©ņ£Āņłśņ£Āļź╝ ļ░øĻ│Ā ņ׳ļŖö ņśüņĢäņŚÉĻ▓īļŖö Ēö╝ļ”¼ļÅģņŗĀņØä ļ│┤ņČ®ĒĢ┤ ņżĆļŗż. ĒĢ£ĒÄĖ 4R ņ╣śļŻīļÅä Ļ░ĆļŖźĒĢśļéś ņČöĻ░Ć ņŚ░ĻĄ¼Ļ░Ć ĒĢäņÜöĒĢśļŗż.
ņØ╝ļ░śņĀüņ£╝ļĪ£ ņ╣śļŻīļź╝ ĻČīņןĒĢśņ¦Ć ņĢŖņ£╝ļ®░, 2ļģäĻ░ä ņČöņĀü Ļ┤Ćņ░░ Ļ░Éņŗ£ĒĢ£ļŗż.
LTBIņØś ņ¦äļŗ©ņØĆ ļ®┤ņŚŁ ņĀĆĒĢśņ×ÉņŚÉņä£ņØś LTBI ņ¦äļŗ© ĻĖ░ņżĆņØä ļö░ļźĖļŗż. IGRA ļŗ©ļÅģ Ēś╣ņØĆ ļæÉ Ļ▓Ćņé¼ ļ│æĒĢ®ļ▓ĢņØä ņé¼ņÜ®ĒĢĀ ņłś ņ׳ņ£╝ļ®░, TST ļŗ©ļÅģņ£╝ļĪ£ LTBI ņØīņä▒ņ£╝ļĪ£ ņ¦äļŗ©ĒĢśļŖö Ļ▓āņØĆ ĻČīĻ│ĀĒĢśņ¦Ć ņĢŖļŖöļŗż. ļæÉ Ļ▓Ćņé¼ ļ│æĒĢ® ņé¼ņÜ®ņŗ£ ļæÉ Ļ▓Ćņé¼ ņżæ ĒĢśļéśļØ╝ļÅä ņ¢æņä▒ņØ╝ ļĢī Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ņ£╝ļĪ£ ĒīÉņĀĢĒĢ£ļŗż. TST ņ¢æņä▒ ĻĖ░ņżĆņØĆ Ļ▓ĮĻ▓░ņØś Ēü¼ĻĖ░ 10 mm ņØ┤ņāüņØ┤ļŗż.
ĻĖ░ņĀĆ Ļ▓Ćņé¼ļĪ£ ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄņØ┤ ņ¦äļŗ©ļÉśļ®┤ Ļ▓░ĒĢĄ ņ╣śļŻīļź╝ ņŗ£ņ×æĒĢ£ļŗż. ņØ┤ Ļ▓ĮņÜ░ TNFĻĖĖĒĢŁņĀ£ ņ╣śļŻīļŖö Ļ▓░ĒĢĄ ņ╣śļŻī ņóģļŻī Ēøä ņŗ£ņ×æĒĢśļŖö Ļ▓āņØä ĻČīĻ│ĀĒĢśļéś, ĒĢŁĻ▓░ĒĢĄ ņ╣śļŻī ļ░śņØæņØ┤ ņ¢æĒśĖĒĢśĻ│Ā, ņżæņ”Ø Ļ▓░ĒĢĄņØ┤ ņĢäļŗłļ®░ ņĢĮņĀ£ Ļ░Éņłśņä▒ Ļ▓░ĒĢĄņØĖ Ļ▓ĮņÜ░ 2Ļ░£ņøö ņ¦æņżæ ņ╣śļŻīĻĖ░ ņØ┤Ēøä TNFĻĖĖĒĢŁņĀ£ ņŗ£ņ×æņØä Ļ│ĀļĀżĒĢĀ ņłś ņ׳ļŗż. ĻĖ░ņĀĆ Ļ▓Ćņé¼ļĪ£ LTBIĻ░Ć ņ¦äļŗ©ļÉśļ®┤ LTBI ņ╣śļŻīļź╝ ņŗ£Ē¢ēĒĢ£ļŗż. ņ╣śļŻī ņŗ£ņ×æ 3ņŻ╝ ĒøäļČĆĒä░ TNFĻĖĖĒĢŁņĀ£ ņ╣śļŻī ņŗ£ņ×æņØä ĻČīĻ│ĀĒĢ┤ ļ│╝ ņłś ņ׳ņ£╝ļ®░, ņŗ£ĻĖēĒĢ£ Ļ▓ĮņÜ░ņŚÉ LTBI ņ╣śļŻī ņŗ£ņ×æĻ│╝ ļÅÖņŗ£ņŚÉ ņŗ£ņ×æĒĢśļŖö Ļ▓āņØä Ļ│ĀļĀżĒĢĀ ņłś ņ׳ņ£╝ļéś ĻĘ╝Ļ▒░ļŖö ļČĆņĪ▒ĒĢśļŗż.
TNFĻĖĖĒĢŁņĀ£ ņ╣śļŻī ņżæ Ļ▓░ĒĢĄ Ļ▓Ćņé¼ņŚÉ ļīĆĒĢ┤ņä£ļŖö ņĀĢĻĖ░ņĀüņØĖ ĒØēļČĆ XņäĀ Ļ▓Ćņé¼ļ│┤ļŗżļŖö Ļ▓░ĒĢĄ ņØśņŗ¼ ņ”Øņāü ļ░£ņāØņŗ£ ņŗĀņåŹĒ׳ Ļ▓Ćņé¼ĒĢśļŖö ļ░®ļ▓ĢņØ┤ ļŹö ņäĀĒśĖļÉśļ®░, TNFĻĖĖĒĢŁņĀ£ ņé¼ņÜ® ņżæ ļ░£ņāØĒĢ£ Ļ▓░ĒĢĄņØĆ ĒÅÉņÖĖĻ▓░ĒĢĄ, ļ╣äĻ▓░ĒĢĄ ĒĢŁņāüĻĘĀ ņ¦łĒÖś, ņżæņ”Ø Ļ▓░ĒĢĄņØś ļ░£ņāØ ļ╣łļÅäĻ░Ć ļåÆņ£╝ļ»ĆļĪ£ ņØ┤ņŚÉ ļīĆĒĢ£ ņŻ╝ņØśĻ░Ć ĒĢäņÜöĒĢśļŗż.
ņןĻĖ░ ņØ┤ņŗØņ£╝ļĪ£ ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ļź╝ ļ│ĄņÜ® ņżæņØ┤Ļ▒░ļéś ļ│ĄņÜ® ņśłņĀĢņ×ÉļŖö ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄ ļ░Å LTBIņŚÉ ļīĆĒĢ£ Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ņĢ╝ ĒĢśļ®░, LTBI ņ¦äļŗ©ņØĆ ļ®┤ņŚŁ ņĀĆĒĢśņ×ÉņŚÉņä£ LTBI ņ¦äļŗ© ĻĖ░ņżĆņØä ļö░ļźĖļŗż. IGRA Ļ▓Ćņé¼ņŗ£ ĒīÉļÅģ ļČłļŖź(indeterminate result)ņØä ņżäņØ┤ĻĖ░ ņ£äĒĢ┤ņä£ļŖö Ļ░ĆļŖźĒĢ£ ĒĢ£ ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ ļ│ĄņÜ® ņĀäņŚÉ LTBI Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśļŖö Ļ▓āņØä ĻČīĻ│ĀĒĢ£ļŗż. TSTļéś IGRA Ļ▓░Ļ│╝ņÖĆ ļ¼┤Ļ┤ĆĒĢśĻ▓ī Ļ│╝Ļ▒░ Ļ▓░ĒĢĄņ╣śļŻīļĀź ņŚåņØ┤ ņ×ÉņŚ░ ņ╣śņ£ĀļÉ£ Ļ▓░ĒĢĄ ļ│æļ│ĆņØ┤ ņĪ┤ņ×¼ĒĢśļŖö Ļ▓ĮņÜ░ņŚÉļŖö, ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄņØ┤ ļ░░ņĀ£ļÉśļ®┤ TSTņÖĆ IGRA Ļ▓░Ļ│╝ņÖĆ ļ¼┤Ļ┤ĆĒĢśĻ▓ī LTBIļĪ£ Ļ░äņŻ╝ĒĢ£ļŗż. ĻĄŁļé┤ņŚÉņä£ 312ļ¬ģņØś ņŗĀņן ņØ┤ņŗØ ĒÖśņ×Éļź╝ ļīĆņāüņ£╝ļĪ£ TSTņÖĆ T-SPOT.TB Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ LTBIļź╝ ņ¦äļŗ©ĒĢśĻ│Ā ņ╣śļŻīĒĢ£ ņŚ░ĻĄ¼ņŚÉņä£ļŖö TST ņØīņä▒ņØĖ ĒÖśņ×ÉļōżņŚÉņä£ T-SPOT.TB Ļ▓Ćņé¼ ņŗ£Ē¢ēņØ┤ ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄ ļ░£ļ│æņØä ņśłņĖĪĒĢśļŖöļŹ░ ņ£ĀņÜ®ĒĢ©ņØä ļ│┤ņŚ¼ņŻ╝ņŚłļŗż[21]. ĻĄŁļé┤ņŚÉņä£ ņŗĀņן ņØ┤ņŗØ ņĀä ĒÖśņ×ÉļōżņŚÉņä£ TSTņÖĆ IGRA Ļ▓░Ļ│╝ņØś ņØ╝ņ╣śļÅä(QFT-IT, T-SPOT.TB)Ļ░Ć ļåÆņ¦Ć ņĢŖņØīņØä Ļ│ĀļĀżĒĢĀ ļĢī[22,23], ņØ┤ņŗØ ņśłņĀĢņ×É ļśÉļŖö ņØ┤ņŗØ ĒÖśņ×ÉņŚÉņä£ļŖö TSTņÖĆ IGRA ļæÉ Ļ░Ćņ¦Ć ņżæ ņ¢┤ļŖÉ ĒĢ£ Ļ▓Ćņé¼ļØ╝ļÅä ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░ļŖö Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ ņ¢æņä▒ņ£╝ļĪ£ ĒÅēĻ░ĆĒĢśĻ│Ā ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄņØ┤ ļ░░ņĀ£ļÉśļ®┤ LTBIļĪ£ ņ¦äļŗ©ĒĢ£ļŗż. LTBI ņ╣śļŻīļŖö ņØ┤ņåīļŗłņĢäņ¦Ćļō£ 9Ļ░£ņøö ņÜöļ▓Ģ(9H)ņØä ĻČīĻ│ĀĒĢśļéś, ņØ┤ņŗØ ņĀä ļ®┤ņŚŁņ¢ĄņĀ£ņĀ£ļź╝ ņé¼ņÜ®ĒĢśĻĖ░ ņĀäņŚÉ ņ╣śļŻī ņÖäļŻīĒĢĀ Ļ▓ĮņÜ░ ļ”¼Ēī£ĒĢĆ 4Ļ░£ņøö ņÜöļ▓Ģ(4R) ļ░Å ņØ┤ņåīļŗłņĢäņ¦Ćļō£/ļ”¼Ēī£ĒĢĆ 3Ļ░£ņøö ņÜöļ▓Ģ(3HR)ļÅä ņäĀĒāØņĀüņ£╝ļĪ£ Ļ│ĀļĀżĒĢĀ ņłś ņ׳ļŗż. ņØ┤ņåīļŗłņĢäņ¦Ćļō£ ņ╣śļŻīņŗ£ Ēö╝ļ”¼ļÅģņŗĀ(25-50 mg/ņØ╝)ņØä Ļ░ÖņØ┤ ļ│ĄņÜ®ĒĢ£ļŗż.
ņØśļŻīĻĖ░Ļ┤Ć ņóģņé¼ņ×ÉļŖö ņ¦üņŚģņĀüņØĖ ļģĖņČ£ ņ£äĒŚśņ£╝ļĪ£ ņØĖĒĢ┤ņä£ Ļ▓░ĒĢĄ ļ░£ļ│æņØś ņāüļīĆ ņ£äĒŚśļÅäĻ░Ć ņØ╝ļ░śņØĖņŚÉ ļ╣äĒĢ┤ņä£ ļåÆņĢäņä£[24,25], ņ¦üņןļé┤ Ļ│ĀņÜ® ņĀäĒøäņŚÉ ļ░£ņāØĒĢśļŖö LTBIļź╝ ņ¦äļŗ©ĒĢśĻ│Ā ņ╣śļŻīĒĢśļŖö Ļ▓āņØ┤ ņäĀņ¦äĻĄŁņØś ņČöņäĖņØ┤ļŗż[5]. Ļ▓░ĒĢĄ ĒÖśņ×Éļź╝ ņ¦üņĀæ ņ¦äļŻīĒĢśĻ▒░ļéś Ļ░äĒśĖĒĢśļŖö ļČĆņä£ņØś ņ¦üņøÉ ļ░Å Ļ▓░ĒĢĄ Ļ░ÉņŚ╝ņŚÉ ļģĖņČ£ļÉĀ ņ£äĒŚśņØ┤ ļåÆņØĆ Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśļŖö ņ¦üņøÉļōżņŚÉ ļīĆĒĢ£ ļČäļźśļź╝ ņ¦łļ│æĻ┤Ćļ”¼ļ│ĖļČĆņŚÉņä£ ņŗ£Ē¢ēĒĢ£ļ░ö ņ׳ņ£╝ļ®░(Table 3), ņØ┤ļź╝ ĻĖ░ļ│Ėņ£╝ļĪ£ ĒĢśņŚ¼ ĻĖ░ņżĆ 1ĻĄ░(Ļ▓░ĒĢĄ ĒÖśņ×Éļź╝ Ļ▓Ćņ¦ä, ņ╣śļŻī, ņ¦äļŗ©ĒĢśļŖö ņØśļŻīņØĖ ļ░Å ņØśļŻīĻĖ░ņé¼ ļō▒) ļ░Å 2ĻĄ░(ņŗĀņāØņĢä, ļ®┤ņŚŁ ņĀĆĒĢśņ×É ļō▒ ļ®┤ņŚŁņØ┤ ņĢĮĒĢśņŚ¼ Ļ▓░ĒĢĄ ļ░£ļ│æņŗ£ ņżæņ”Ø Ļ▓░ĒĢĄ ņ£äĒŚśņØ┤ ļåÆņØĆ ĒÖśņ×ÉņÖĆ ņĀæņ┤ēĒĢśļŖö ņóģņé¼ņ×É)ņŚÉ ĒĢ┤ļŗ╣ĒĢśļŖö ņØśļŻīĻĖ░Ļ┤Ć ņóģņé¼ņ×ÉņØś Ļ▓ĮņÜ░ņŚÉļŖö ņŻ╝ĻĖ░ņĀüņØĖ LTBI Ļ▓Ćņé¼ļź╝ ņŗ£Ē¢ēĒĢśņŚ¼ņĢ╝ ĒĢ£ļŗż. ņŻ╝ĻĖ░ņĀüņØĖ LTBI Ļ▓Ćņé¼ļĪ£ļŖö TSTĻ░Ć ĻČīĻ│ĀļÉśļéś, ĻĘ╝Ļ▒░ļŖö ļČĆņĪ▒ĒĢśņ¦Ćļ¦ī IGRAļź╝ ņŗ£Ē¢ēĒĢĀ ņłś ņ׳ļŗż. ņØśļŻīĻĖ░Ļ┤Ć Ļ▓░ĒĢĄ Ļ┤Ćļ”¼ņŚÉ ļö░ļźĖ ņØśļŻīĻĖ░Ļ┤Ć ņóģņé¼ņ×ÉņØś LTBI ņ╣śļŻī ļīĆņāüņ×ÉļŖö 1) ņŻ╝ĻĖ░ņĀü TST ļśÉļŖö IGRA Ļ▓Ćņé¼ņŚÉņä£ ņ¢æņĀäņØ┤ ĒÖĢņØĖļÉ£ Ļ▓ĮņÜ░, 2) 1, 2ĻĄ░ ņØśļŻīĻĖ░Ļ┤Ć ņóģņé¼ņ×ÉņØ┤ļ®┤ņä£ LTBI ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░, 3) ĒØēļČĆ XņäĀņāü Ļ▓░ĒĢĄ Ļ│╝Ļ▒░ ņ╣śļŻīļĀź ņŚåņØ┤ ņ×ÉņŚ░ ņ╣śņ£ĀļÉ£ ļ│æļ│ĆņØ┤ ņ׳ņ£╝ļ®┤ņä£ LTBI Ļ▓Ćņé¼ ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░ņØ┤ļŗż.
ļŗ©ņ▓┤ ņāØĒÖ£ ņĀäņŚÉ Ļ░ÉņŚ╝ņ×Éļź╝ ņ░ŠĻĖ░ ņ£äĒĢ£ ņ¦æļŗ©ņĀü ņäĀļ│ä Ļ▓Ćņé¼ļĪ£ LTBI Ļ▓Ćņé¼ļŖö ĒÜ©ņÜ®ņä▒ņØ┤ ļåÆņ¦Ć ņĢŖņ£╝ļéś, ļŗżļ¦ī ņØśļŻīĻĖ░Ļ┤Ć, ņé░Ēøä ņĪ░ļ”¼ņøÉ, ĒĢÖĻĄÉ, ņ£Āņ╣śņøÉ, ņ¢┤ļ”░ņØ┤ņ¦æ, ņĢäļÅÖļ│Ąņ¦Ćņŗ£ņäż ļō▒ ĒŖ╣ņĀĢ ņ¦æļŗ©ņŗ£ņäż ļé┤ņŚÉņä£ Ļ▓░ĒĢĄ ļ░£ļ│æ ņé¼ļĪĆĻ░Ć ļ¦ÄņØ┤ ļ│┤Ļ│ĀļÉśĻ│Ā ņ׳Ļ│Ā, ņØ┤ļŖö ņ¦æļŗ© ļé┤ņŚÉņä£ ņĀäĒīī ņ£äĒŚś ļō▒ ņé¼ĒÜīņĀü ĒīīĻĖēĒÜ©Ļ│╝Ļ░Ć Ēü¼ĻĖ░ ļĢīļ¼ĖņŚÉ, ĻĄŁĻ░ĆņŚÉņä£ļŖö 2016ļģäĻ│╝ 2017ļģäņŚÉ Ļ▓░ĒĢĄ ņśłļ░®ļ▓ĢņØä Ļ░£ņĀĢĒĢśņŚ¼ ņé░Ēøä ņĪ░ļ”¼ņøÉ, ņ┤ł┬Ęņżæ┬ĘĻ│Āļō▒ĒĢÖĻĄÉ, ņ£Āņ╣śņøÉ, ņ¢┤ļ”░ņØ┤ņ¦æ, ņĢäļÅÖļ│Ąņ¦Ćņŗ£ņäż ļō▒ņŚÉ ĻĘ╝ļ¼┤ĒĢśļŖö ņóģņé¼ņ×É ļ░Å ĻĄÉņ¦üņøÉņŚÉ ļīĆĒĢ£ ņ×Āļ│ĄĻ▓░ĒĢĄ Ļ▓Ćņ¦äņØä ņØśļ¼┤ĒÖöĒĢśņśĆļŗż[26].
2017 ņ¦Ćņ╣©ņŚÉņä£ ņØ┤ņĀä ņ¦Ćņ╣©Ļ│╝ ļ╣äĻĄÉĒĢśņŚ¼ ļ│ĆĒÖöļÉ£ ņĀÉņØä ņóģĒĢ®ĒĢ┤ ļ│Ėļŗżļ®┤ ļŗżņØīĻ│╝ Ļ░Öļŗż. LTBI ņ¦äļŗ©ņŚÉ ņ׳ņ¢┤ņä£, TST Ļ▓░Ļ│╝Ļ░Ć 10 mm ņØ┤ņāü 15 mm ļ»Ėļ¦īņØĖ Ļ▓ĮņÜ░ BCG ņĀæņóģļĀźņØ┤ ņ׳ļŖö Ļ▓ĮņÜ░ IGRAļź╝ ņČöĻ░ĆļĪ£ ņŗ£Ē¢ēĒĢśĻ│Ā, BCG ņĀæņóģņØś Ļ▓ĮņÜ░ļØ╝ļÅä TSTĻ░Ć 15 mm ņØ┤ņāüņØĖ Ļ▓ĮņÜ░ļŖö ļŗ©ļÅģņ£╝ļĪ£ LTBI ņ¢æņä▒ ņ¦äļŗ©ņØ┤ Ļ░ĆļŖźĒĢśļÅäļĪØ ĒĢśņśĆļŗż. ĒØēļČĆ XņäĀņŚÉņä£ Ļ│╝Ļ▒░ Ļ▓░ĒĢĄ ņ╣śļŻīļĀź ņŚåņØ┤ ņ×ÉņŚ░ ņ╣śņ£ĀļÉ£ Ļ▓░ĒĢĄ ļ│æļ│ĆņØ┤ ņĪ┤ņ×¼ĒĢśļŖö Ļ▓ĮņÜ░, ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄņØä ļ░░ņĀ£ĒĢ£ ļÆż Ļ│Āņ£äĒŚśĻĄ░ņØś Ļ▓ĮņÜ░ļŖö LTBI Ļ▓Ćņé¼ Ļ▓░Ļ│╝ņÖĆ ļ¼┤Ļ┤ĆĒĢśĻ▓ī LTBI ņ╣śļŻīļź╝ ņŗ£ņ×æĒĢśĻ│Ā, ĻĘĖ ņÖĖņØś Ļ▓ĮņÜ░ļŖö LTBI Ļ▓Ćņé¼ Ēøä ņ¢æņä▒ņØĖ Ļ▓ĮņÜ░ņŚÉ ņ╣śļŻīļź╝ ĒĢśļÅäļĪØ ĻČīĻ│ĀĒĢśĻ│Ā ņ׳ļŗż. Ļ▓░ĒĢĄ ņĀæņ┤ēņ×É Ļ▓Ćņ¦ä ļīĆņāüņ×ÉņØś ņŚ░ļĀ╣ ņĀ£ĒĢ£ņØ┤ 35ņäĖņŚÉņä£ 65ņäĖļĪ£ ņāüĒ¢ź ņĪ░ņĀĢļÉśņŚłĻ│Ā, Ļ│Āņ£äĒŚśĻĄ░ņØä ņĀ£ņÖĖĒĢ£ ņ╣śļŻī ļīĆņāüņ×ÉņØś Ļ▓ĮņÜ░ 9H/4R/3HRņØä Ļ░äļÅģņä▒ ņ£äĒŚśņØĖņ×ÉĻ░Ć ņŚåļŖö Ļ▓ĮņÜ░ 65ņäĖ ņØ┤ĒĢśņŚÉņä£ ņé¼ņÜ®ĒĢĀ ņłś ņ׳ņ£╝ļéś Ļ░äļÅģņä▒ ņ£äĒŚśņØĖņ×ÉĻ░Ć ņ׳ļŖö Ļ▓ĮņÜ░ļŖö 35ņäĖ ņØ┤ĒĢśņŚÉņä£ ĻČīĻ│ĀĒĢśĻ│Ā ņ׳ņ£╝ļ®░, 3H1P1ļŖö ņŚ░ļĀ╣ ņĀ£ĒĢ£ ņŚåņØ┤ ņé¼ņÜ® Ļ░ĆļŖźĒĢśļéś Ļ░äļÅģņä▒ ņ£äĒŚśņØĖņ×ÉĻ░Ć ņ׳ļŖö Ļ▓ĮņÜ░ 65ņäĖ ņØ┤ĒĢśļĪ£ ņĀ£ĒĢ£ņØä ļæÉņŚłļŗż. ĒĢ£ĒÄĖ ņØśļŻīĻĖ░Ļ┤Ć ņóģņé¼ņ×ÉļōżņŚÉ ļīĆĒĢ┤ņä£ļŖö ņØśļŻīĻĖ░Ļ┤Ć ņóģņé¼ņ×ÉļōżņØä 4ĻĄ░ņ£╝ļĪ£ ļČäļźśĒĢśņŚ¼, 1ĻĄ░Ļ│╝ 2ĻĄ░ņØś Ļ▓ĮņÜ░ LTBI ņ¢æņä▒ņ×ÉļōżņØś Ļ▓ĮņÜ░ļŖö ņ╣śļŻīļź╝ ĻČīĻ│ĀĒĢśĻ│Ā ņ׳ļŗż.
ņĄ£ĻĘ╝Ļ╣īņ¦Ć ĻĄŁļé┤ Ļ▓░ĒĢĄ ņĀĢņ▒ģņØĆ recent infectionņ£╝ļĪ£ ņØĖĒĢ┤ņä£ ļ░£ņāØĒĢ£ ņ×Āļ│ĄĻ▓░ĒĢĄ Ļ░ÉņŚ╝ņ×Éļź╝ ņżäņØ┤ļŖöļŹ░ ņŻ╝ļĀźņØä ĒĢśņŚ¼ ņ¢┤ļŖÉ ņĀĢļÅäņØś ņä▒Ļ│╝ļź╝ ļ│┤ņĢśņ£╝ļéś, ņĢ×ņ£╝ļĪ£ļŖö remote infectionņŚÉ ņØśĒĢ┤ņä£ ņāØĻĖ┤ ļģĖņØĖ LTBI ĒÖśņ×ÉĻ░Ć ĒÖ£ļÅÖņä▒ Ļ▓░ĒĢĄņ£╝ļĪ£ ņ¦äĒ¢ēĒĢśļŖö Ļ▓āņØä ļ¦ēĻĖ░ ņ£äĒĢ£ ļīĆņ▒ģņØ┤ ņżæņÜöĒĢśļŗż. ņŚ░ļĀ╣ņØ┤ ļåÆņØĆ ļīĆņāüņ×Éļōż Ļ▓ĮņÜ░ļŖö LTBI ņ╣śļŻīļĪ£ ņØĖĒĢ£ ļČĆņ×æņÜ®ņØä ņĄ£ņåīĒÖöĒĢśļ®┤ņä£ ņĀäņŚ╝ņä▒ Ļ▓░ĒĢĄ ĒÖśņ×ÉņØś ļ░£ņāØņØä ņ¢ĄņĀ£ĒĢśļŖö Ļ▓āņØ┤ ņżæņÜöĒĢ£ Ļ┤ĆĻ▒┤ņØĖļŹ░, ņØ┤ļź╝ ņ£äĒĢ┤ņä£ļŖö ļ╣äņÜ® ļīĆļ╣ä ĒÜ©Ļ│╝ļź╝ Ļ│ĀļĀżĒĢ£ ĻĄŁļé┤ņØś ĻĘ╝Ļ▒░ ĻĖ░ļ░śņØś ņĀĢņ▒ģņØ┤ ņĀ£ņŗ£ļÉśņ¢┤ņĢ╝ ĒĢĀ Ļ▓āņØ┤ļŗż. ĒĢ£ĒÄĖ, ĻĄŁļé┤ ĒÖśņ×ÉņŚÉ ļ╣äĒĢ┤ņä£ ļ»Ėļ╣äĒĢ£ ņł½ņ×ÉņØ┤ļéś ņĄ£ĻĘ╝ ņ”ØĻ░Ć ņČöņäĖņŚÉ ņ׳ļŖö ņÖĖĻĄŁņØĖ Ļ▓░ĒĢĄ ņ£Āņ×ģņØä ņ¢ĄņĀ£ĒĢśĻĖ░ ņ£äĒĢ£ ņ×Āļ│ĄĻ▓░ĒĢĄņĀĢņ▒ģ Ļ░£ļ░£ļÅä ĒĢäņÜöĒĢ£ ņŗ£ņĀÉņ£╝ļĪ£ ņāØĻ░üļÉ£ļŗż.
REFERENCES
2. WHO. Global tuberculosis control. Geneva: World Health Organization, 2011.
3. WHO. Global tuberculosis report 2017. Geneva: World Health Organization, 2018.
4. Lewinsohn DM, Leonard MK, LoBue PA, et al. Official American Thoracic Society/Infectious Diseases Society of America/Centers for Disease Control and Prevention Clinical Practice Guidelines: diagnosis of tuberculosis in adults and children. Clin Infect Dis 2017;64:e1ŌĆōe33.


5. National Institute for Health and Clinical Excellence (NICE). Clinical guideline 33. Tuberculosis. Clinical diagnosis and management of Tuberculosis, and Measures for its Prevention and Control [Internet]. London (UK): NICE, c2016. [cited 2018 Oct 1] Available from: http://www.nice.org.uk/ guidance/ng33
6. Joint Committee for the Revision of Korean Guidelines for Tuberculosis & Korea Centers for Disease Control and Prevention. Korean Guidelines for Tuberculosis [Internet]. Seoul (KR): Korea Centers for Disease Control and Prevention, c2011. [cited 2018 Oct 1]. Available from: http://tbzero.cdc.go.kr/tbzero/main.do
7. Joint Committee for the Revision of Korean Guidelines for Tuberculosis & Korea Centers for Disease Control and Prevention. Korean Guidelines for Tuberculosis [Internet]. Seoul (KR): Korea Centers for Disease Control and Prevention, c2017. [cited 2018 Oct 1]. Available from: http://www.lungkorea.org/bbs/?code=guide
8. Hong YP, Kim SJ, Lew WJ, Lee EK, Han YC. The seventh nationwide tuberculosis prevalence survey in Korea, 1995. Int J Tuberc Lung Dis 1998;2:27ŌĆō36.

9. Choi CM, Kang CI, Kim DH, et al. The role of TST in the diagnosis of latent tuberculosis infection among military personnel in South Korea. Int J Tuberc Lung Dis 2006;10:1342ŌĆō1346.

10. Lee JY, Choi HJ, Park IN, et al. Comparison of two commercial interferon-gamma assays for diagnosing Mycobacterium tuberculosis infection. Eur Respir J 2006;28:24ŌĆō30.


11. Lee SW, Oh SY, Lee JB, Choi CM, Kim HJ. Tuberculin skin test distribution following a change in BCG vaccination policy. PLoS One 2014;9:e86419.



12. Targeted tuberculin testing and treatment of latent tuberculosis infection. This official statement of the American thoracic society was adopted by the ATS board of directors, July 1999. This is a joint statement of the American thoracic society (ATS) and the centers for disease control and prevention (CDC). This statement was endorsed by the council of the infectious diseases society of America. (IDSA), September 1999, and the sections of this statement. Am J Respir Crit Care Med 2000;161(4 Pt 2):S221ŌĆōS247.


13. Solovic I, Sester M, Gomez-Reino JJ, et al. The risk of tuberculosis related to tumour necrosis factor antagonist therapies: a TBNET consensus statement. Eur Respir J 2010;36:1185ŌĆō1206.


14. Metcalfe JZ, Cattamanchi A, McCulloch CE, Lew JD, Ha NP, Graviss EA. Test variability of the QuantiFERON-TB gold in-tube assay in clinical practice. Am J Respir Crit Care Med 2013;187:206ŌĆō211.



15. Pulblic Health Agency of Canada. Canadian tuberculosis standard. 7th Ed. Vancouver: Centre for Disease Control, 2014.
16. Mazurek GH, Jereb J, Vernon A, et al. Updated guidelines for using interferon gamma release assays to detect mycobacterium tuberculosis infection - United States, 2010. MMWR Recomm Rep 2010;59(RR-5):1ŌĆō25.
17. National Tuberculosis Controllers Association; Centers for Disease Control and Prevention (CDC). Guidelines for the investigation of contacts of persons with infectious tuberculosis. Recommendations from the national tuberculosis controllers association and CDC. MMWR Recomm Rep 2005;54(RR-15):1ŌĆō47.
18. Menzies D, Adjobimey M, Ruslami R, et al. Four months of rifampin or nine months of isoniazid for latent tuberculosis in adults. N Engl J Med 2018;379:440ŌĆō453.


19. Spyridis NP, Spyridis PG, Gelesme A, et al. The effectiveness of a 9-month regimen of isoniazid alone versus 3- and 4-month regimens of isoniazid plus rifampin for treatment of latent tuberculosis infection in children: results of an 11-year randomized study. Clin Infect Dis 2007;45:715ŌĆō722.


20. Sterling TR, Villarino ME, Borisov AS, et al. Three months of rifapentine and isoniazid for latent tuberculosis infection. N Engl J Med 2011;365:2155ŌĆō2166.


21. Kim SH, Lee SO, Park JB, et al. A prospective longitudinal study evaluating the usefulness of a T-cell-based assay for latent tuberculosis infection in kidney transplant recipients. Am J Transplant 2011;11:1927ŌĆō1935.


22. Kim SY, Jung GS, Kim SK, et al. Comparison of the tuberculin skin test and interferon-╬│ release assay for the diagnosis of latent tuberculosis infection before kidney transplantation. Infection 2013;41:103ŌĆō110.


23. Kim SH, Lee SO, Park IA, et al. Diagnostic usefulness of a T cell-based assay for latent tuberculosis infection in kidney transplant candidates before transplantation. Transpl Infect Dis 2010;12:113ŌĆō119.


24. Jo KW, Hong Y, Park JS, et al. Prevalence of latent tuberculosis infection among health care workers in South Korea: a multicenter study. Tuberc Respir Dis (Seoul) 2013;75:18ŌĆō24.



25. Kim SJ, Lee SH, Kim IS, Kim HJ, Kim SK, Rieder HL. Risk of occupational tuberculosis in national tuberculosis programme laboratories in Korea. Int J Tuberc Lung Dis 2007;11:138ŌĆō142.

26. Korea Centers for Disease Control and Prevention. 2018 manual of national tuberculosis control [Internet]. Osong (KR): Korea Centers for Disease Control and Prevention, c2018. [cited 2018 Oct 1]. Available from: http://tbzero.cdc.go.kr/tbzero/main.do
LTBI diagnosis in immune-competent subjects; TST alone (A), TST/IGRA two step test (B), or IGRA test alone (C) [7]. TB, tuberculosis; Hx, history; P.Ex, physical examination; CXR, chest radiographs; BCG, bacillus calmette guerin; LTBI, latent tuberculosis infection.
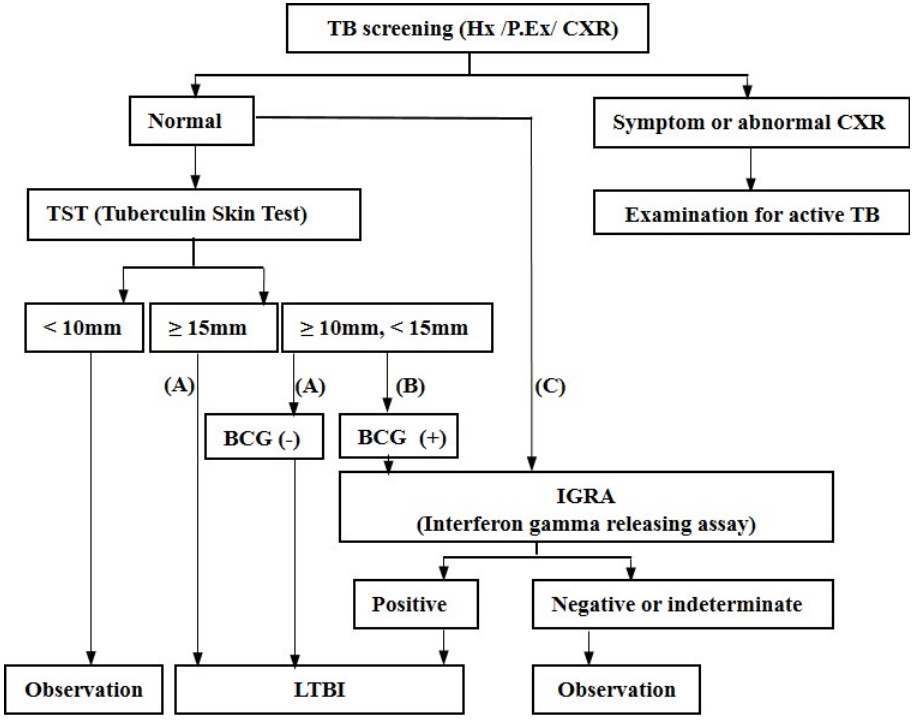
Figure┬Ā1.
Latent tuberculosis infection (LTBI) diagnosis in immune-compromised subjects. TST-negative result alone cannot exclude LTBI, but TST-positive result alone can indicate LTBI (A). IGRA positive result alone can indicate LTBI (B) [7]. TB, tuberculosis; Hx, history; P.Ex, physical examination; CXR, chest radiographs.

Figure┬Ā2.
Table┬Ā1.
Summary for indications of LTBI treatment (non-contacts to an infectious TB patient) [7]
Table┬Ā2.
Summary for indications of LTBI treatment (contacts to an infectious TB patient) [7]
Table┬Ā3.
Categories of health care workers by Korean Centers for Disease Control and Prevention [7]
-
METRICS

-
- 1 Crossref
- 0 Scopus
- 27,671 View
- 1,744 Download



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



