 |
 |
| Korean J Med > Volume 98(6); 2023 > Article |
|
Abstract
Korea has one of the highest rates of end-stage kidney disease (ESKD) worldwide and nearly half of all new cases are attributed to diabetes. Diabetes represents a critical aspect of chronic kidney disease (CKD)-related mortality that entails substantial treatment costs. Given the profound impact of ESKD, it is imperative to initiate robust initiatives to formulate and implement effective preventive and therapeutic strategies. These strategies should target the prevention of CKD development in individuals with diabetes and decelerate the progression of diabetic kidney disease. Recognizing this challenge, the Korean Society of Nephrology (KSN) has introduced the kidney health plan 2033, a comprehensive endeavor designed to alleviate the burdens associated with CKD and ESKD in Korea. As part of this initiative, KSN has undertaken the development of the KSN 2023 practical recommendations for the management of diabetic kidney disease. The hope is that implementation of this guideline will delay the onset of kidney-related complications in diabetic patients throughout the country.
만성콩팥병(chronic kidney disease)은 전 세계적으로 심각한 공중보건 문제를 일으키는 대표적인 비전염 질환(noncommunicable disease) 중 하나이다[1]. 지난 수십여 년간 만성콩팥병 환자 수는 지속적으로 증가하고 있다[2,3]. 1990년 이래 만성콩팥병 유병률은 29.3%나 상승하여 2017년 기준 전 세계 인구 중 9.1%가 만성콩팥병을 앓고 있다[1,4]. 만성콩팥병의 심각성은 질병 그 자체뿐 아니라 다른 질병의 이환이나 사망에 끼치는 영향으로도 판단할 수 있는데, 다른 전통적인 심혈관 위험인자들과는 별개로 심혈관 질환의 강력하고 독립적인 위험인자로 잘 알려져 있다[1,4]. 그동안 만성콩팥병 그리고 콩팥병의 원인 질환인 당뇨병 및 고혈압 등에 대한 조기 진단 및 치료 기술의 발전에 따라 신대체요법(renal replacement therapy)을 필요로 하는 말기콩팥병(end-stage kidney disease)으로의 진행이 이전보다는 억제되는 경향이 있기는 하지만 만성콩팥병과 말기콩팥병으로 지출되는 의료 비용은 1960년대 이후 지속적으로 증가하고 있다[1,5]. 우리나라 2021 건강보험통계연보에 따르면 만성콩팥병으로 진료받은 환자 수는 2021년 기준 약 28만 명으로 고혈압 701만 명, 당뇨병 356만 명, 심장 질환 178만 명, 대뇌혈관 질환 111만 명, 간 질환 199만 명, 관절염 500만 명에 비해 훨씬 적지만 만성콩팥병으로 지출된 진료비는 약 2.4조 원으로 연간 1인당 진료비로는 심장 질환, 대뇌혈관 질환은 물론 악성 신생물 진료비보다도 훨씬 높다(Fig. 1) [6].
만성콩팥병이 증가하게 된 이유는 고혈압, 당뇨병 및 비만 등 콩팥병 위험인자들을 가진 유병 인구의 증가로 인한 것이다[2,3]. 콩팥병 위험 질환들 중 고혈압의 경우 혈압 조절이 지속적으로 향상되어 왔기에[7], 현 시점에 있어 만성콩팥병의 가장 중요한 위험인자는 당뇨병이다. 2017년 기준 당뇨병에 기인한 만성콩팥병 환자는 전체 만성콩팥병 환자의 30.7%를 차지하고 있다[1,2]. 미국의 경우 당뇨병 환자 중 24.5% 그리고 심지어 당뇨병전단계(prediabetes) 환자 중 14.3%가 이미 만성콩팥병 3-4단계라는 보고도 있다[3]. 우리나라의 경우 당뇨병 환자들 중 추정사구체여과율(estimated glomerular filtration rate)이 60 mL/min/1.73 m2 미만인 환자가 8.6% 그리고 알부민뇨가 동반된 환자가 26.7%라는 보고가 있다[8]. 대한신장학회 등록위원회의 2022년 신대체요법 현황 보고서에 따르면[9] 우리나라의 말기콩팥병 발병률은 2020년 이후 다소 주춤하는 경향이 있으나 유병률은 지속적으로 증가하고 있으며, 당뇨병은 이러한 말기콩팥병의 원인 질환 중 수십여 년째 부동의 1위를 차지하고 있다(Fig. 2). 미국 United States Renal Data System 자료에 따르면 2010년과 2020년 사이 우리나라의 당뇨병에 의한 말기콩팥병의 평균 연간 발생률의 증가는 인구 백만 명당 9.7명으로, 조사된 나라들 중 1위였다[10]. 특히 2010년과 비교하여 2020년에 전체 말기콩팥병 발생률 백분율은 96.2% 증가하여 당뇨병에 의한 말기콩팥병 발생률 백분율의 증가인 84.6%와 높은 연관성을 보였는데[10], 이는 우리나라의 경우 당뇨병이 말기콩팥병 환자 발생 증가를 주도했음을 의미한다. 따라서 당뇨병에 의한 만성콩팥병에서 말기콩팥병으로의 진행을 억제하여야만 전체 말기콩팥병 환자 수의 증가를 억제할 수 있을 것으로 생각된다. 이에 대한신장학회에서는 kidney health plan 2033을 통하여 2033년까지 당뇨병에 의한 말기콩팥병 환자의 비율을 10% 감소시키는 것을 목표로 하였고, 그 실천 방안 중 하나로 당뇨병콩팥병 진료지침(Korean Society of Nephrology 2023 practical recommendations for the management of diabetic kidney disease)을 개발하게 되었다[11].
이번 우리나라 당뇨병콩팥병 진료지침 발간 이전에 Kidney Disease: Improving Global Outcomes (KDIGO)에서는 2020년에 KDIGO clinical practice guideline for diabetes management in chronic kidney disease를 발표한 바 있는데[12], 유례없이 2년만에 개정하여 새롭게 발간하였다[13]. 이는 최근 짧은 기간 동안 새로운 치료법과 관련하여 많은 연구 결과들이 소개되면서 진료지침에 빨리 반영할 필요성이 있었기 때문이었다[13]. 2022년 개정판에서는 sodium-glucose cotransporter-2 (SGLT2) 억제제와 비스테로이드무기질부신피질호르몬수용체길항제(nonsteroidal mineralocorticoid receptor antagonist)가 부각되었는데 특히 SGLT2억제제는 단순한 혈당강하치료제가 아닌 만성콩팥병이 동반된 환자에서의 포괄 치료제 개념으로 격상되었으며 비스테로이드무기질부신피질호르몬수용체길항제도 포괄 치료 전략에 새롭게 포함되었다는 것이 특징이다[12,13]. 사실 KDIGO 임상진료지침의 대상은 정확히는 만성콩팥병 환자에서의 당뇨병 치료인데, 이는 당뇨병이 동반된 환자에서 발생한 만성콩팥병의 원인이 반드시 당뇨병이 아닐 수 있다는 점에 기인한다[13]. 기존의 ‘당뇨병신장병증(diabetic nephropathy)’이라는 용어는 오랜 기간 사용해 오고 있지만 이 용어가 임상 진단 용어인지 아니면 콩팥생검을 통한 병리 진단 용어인지에 대해서 지금까지도 국제적으로 일치된 정의가 확립되어 있지 않아 사용하지 않는 것이 추천된다[12,13]. 한편 ‘당뇨병콩팥병(diabetic kidney disease)’이라는 용어는 만성콩팥병이 당뇨병에 의하여 발생하였다는 의미가 함축되어 있는 용어이므로 이 용어 역시 사용에 있어 제한적일 수 있지만, 설령 당뇨병이 콩팥병의 일차적인 원인 질환이 아니라고 하더라도 동반된 당뇨병이 임상 경과 중 어떤 식으로든 콩팥에 영향을 줄 것이라는 점을 고려한다면 ‘당뇨병콩팥병’이라는 용어의 사용이 불합리한 것은 아니다[11]. 대한신장학회 당뇨병콩팥병 진료지침에서는 ‘당뇨병콩팥병’이라는 용어를 사용함으로써 당뇨병의 대표적인 합병증이 콩팥병이라는 인식 개선과 함께 당뇨병 환자에서의 콩팥병 증상과 징후를 조기에 진단하고 치료가 되어야 한다는 점을 강조하고자 하였다. 또한 대한의사협회 의학용어 6판(https://term.kma.org/)을 기준으로 하여 지침에 사용되는 용어들을 모두 우리말로 표기하려고 노력하였다.
KDIGO 2022 만성콩팥병에서의 당뇨병 임상진료지침의 경우 크게 5장(chapter)으로 구성되어 있어서 포괄 치료, 혈당 감시 및 목표, 생활습관 중재, 혈당강하 치료 및 환자 관리 접근법에 대하여 13개의 권장문(recommendation)과 52개의 실천 요령(practice point)을 제시하고 있다[13,14]. 어떻게 보면 KDIGO 임상진료지침은 만성콩팥병이 동반된 당뇨병 치료와 관련하여 생활습관 교정, 자가 관리 및 최우선 치료제 등의 내용으로만 한정되어 있는데[13] 이 임상진료지침에 포함되지 않은 만성콩팥병의 일반 평가 및 관리, 지질, 혈압 등에 대한 지침은 따로 개발되어 있기 때문이다[15-17]. 반면 대한신장학회 당뇨병콩팥병 진료지침은 총 9장에 총 99개의 권고문을 제시하고 있다. 이는 우리나라 당뇨병콩팥병과 말기콩팥병의 현황부터 시작해서 당뇨병콩팥병의 진단, 신장 전문의 협진 시기, 당뇨병콩팥병에서의 혈당감시 및 조절 목표, 비약물 치료, 약물 치료, 포괄 치료, 합병증 관리, 투석 요법 그리고 소아청소년 당뇨병콩팥병의 진단과 치료까지 당뇨병콩팥병 관리와 관련한 모든 내용을 포함하고자 하였다(Table 1) [11].
당뇨병이 동반된 만성콩팥병 환자에서 당화혈색소 목표를 어떻게 할 것인가에 대한 논의는 오래 전부터 지속되고 있다. 이전에 수행된 체계적 문헌연구 결과에 따르면 당화혈색소 목표를 7.0% 미만으로 하였을 때 비치명적 심근경색의 발병률과 중등도 알부민뇨의 발병 및 진행을 감소시켰지만 근거의 수준은 높지 않았고, 당화혈색소 목표를 6.5% 이하로 하였을 때 중등도 알부민뇨 및 말기콩팥병의 발병률이 감소하는 경향이 있었다[18]. 한편 사망률 면에서는 당화혈색소 목표를 6.0% 이하로 하였을 때와 이보다 높은 당화혈색소 목표를 비교한 두 개의 연구 결과를 보면 당화혈색소 목표를 더 낮게 하더라도 사망률 증가가 일정하지 않아 보였지만, 심혈관 위험이 높은 2형당뇨병 환자를 대상으로 한 action to control cardiovascular risk in diabetes (ACCORD) 연구에서는 낮은 당화혈색소 목표에 배정된 참가자들에서 사망률이 더 높았다[19,20]. 따라서 혈당 조절이 너무 불량하거나 반대로 너무 엄격하게 혈당을 조절하는 경우에서 사망 위험이 증가할 가능성이 있지만[21] 당화혈색소를 어느 정도 낮게 유지하는 것이 콩팥병 진행을 억제하는 데 있어 유리하므로[22] 사망의 위험은 낮추면서 동시에 콩팥병 진행의 위험을 최소화하기 위해서는 환자 개인별 특성에 따라 적합한 당화혈색소 목표를 설정하는 것이 중요하겠다. 따라서 당뇨병콩팥병 진료지침에서는 투석 전 당뇨병콩팥병 환자에서는 당화혈색소 목표를 7% 미만으로 하되 환자 특성에 맞추어 개별화하도록 하였다[11].
당뇨병이 동반된 만성콩팥병 환자에서의 SGLT2억제제의 콩팥 및 심혈관 이득은 이미 잘 알려져 있다. 특히 만성콩팥병 환자들을 대상으로 한 dapagliflozin and prevention of adverse outcomes in chronic kidney disease (DAPA-CKD) 연구, effect of sotagliflozin on cardiovascular and renal events in patients with type 2 diabetes and moderate renal impairment who are at cardiovascular risk (SCORED) 연구 그리고 study of heart and kidney protection with empagliflozin (EMPA-KIDNEY) 연구의 결과에 따라 추정사구체여과율 20 mL/min/1.73 m2 이상이라면 SGLT2 억제제를 사용할 수 있는 근거가 제시되었다[23-25]. 더욱이 현재까지 수행된 SGLT2억제제 임상시험 13개를 메타분석한 결과를 보면 SGLT2억제제의 사용은 콩팥병 진행 위험을 37% 낮추었으며 급성 콩팥손상의 위험과 심혈관 사망이나 심부전으로 인한 입원 위험을 각각 23%씩 낮출 수 있었는데, 이러한 효과는 당뇨병 유무와는 상관이 없었다[26]. 또한 EMPA-KIDNEY 연구 결과 및 dapagliflozin effect on cardiovascular events–thrombolysis in myocardial infarction 58 (DECLARE-TIMI 58) 연구의 사후분석 결과를 보면, SGLT2억제제의 콩팥 보호 효과는 알부민뇨 여부와도 무관하고 심지어는 KDIGO 분류상 콩팥병 진행 위험이 낮은 환자들에서도 확인되고 있다[25,27]. 따라서 당뇨병콩팥병 진료지침에서는 알부민뇨 유무와 무관하게 추정사구체여과율이 20 mL/min/1.73 m2 이상이라면 SGLT2억제제를 사용하도록 권고하였다. 또한 SGLT2억제제 사용 후 초기에 추정사구체여과율이 감소할 수 있는데, 30% 이상 감소하는 경우는 드물다고 보고되었다[28,29]. 만약 SGLT2억제제 사용 후 추정사구체여과율이 사용 전과 비교하여 30%를 초과하여 감소한다면 환자가 저혈량 상태인지 아니면 다른 신독성약물의 사용이나 급성 콩팥손상 등의 다른 원인이 있는지에 대한 평가가 필요하다[11,17]. 즉 SGLT2억제제를 투여한 후 사구체여과율의 변동이 클 때에는 SGLT2억제제를 중단하기보다는 다른 원인에 의한 콩팥의 기능 변화를 살펴보는 것이 우선이라는 것이다. 그만큼 뛰어난 콩팥 및 심혈관 보호 효과로 인하여 향후 SGLT2억제제는 당뇨병 유무에 무관하게 거의 모든 만성콩팥병 환자들에게 적용되어야 할 필수 약제로 자리 잡을 것으로 예상되고 있다[30].
당뇨병이 동반된 만성콩팥병 환자에서의 목표 혈압은 여전히 논란이 많다. 당뇨병콩팥병 진료지침에서는 고혈압이 동반된 당뇨병콩팥병 환자에서 표준화된 진료실혈압 측정을 기준으로 하여 수축기혈압을 120 mmHg 미만이 되도록 권고하고 있다[11]. 이 권고는 2021년 KDIGO 만성콩팥병에서의 혈압 조절을 위한 임상진료지침을 수용한 것으로, KDIGO 임상진료 지침은 systolic blood pressure intervention trial (SPRINT) 연구 결과에 많이 의존하였다[31,32]. SPRINT 연구는 연구 대상자 약 28%가 추정사구체여과율 20-60 mL/min/1.73 m2의 만성콩팥병 환자로서 비교적 많은 만성콩팥병 환자를 포함하였다[31,32]. 비록 당뇨병 및 단백뇨 1 g/day 이상인 환자는 제외되었지만 연구 대상자의 약 42%는 당뇨병전단계였고[32], 사후비교분석에서 당뇨병전단계 여부와 상관없이 집중 혈압 조절의 이득이 확인되었다[33]. 또한 최근 메타분석 결과에 따르면 당뇨병 환자들에서도 집중 혈압 조절이 표준 혈압 조절에 비하여 뇌졸중이나 심부전 위험 측면에서 유리하다는 것이 관찰되었다[34]. 그러나 진행된 당뇨병콩팥병 환자에서의 혈압 목표에 대한 근거는 아직 많지 않으므로 당뇨병콩팥병 환자에서의의 보편적인 목표 혈압은 수축기혈압 기준으로 120 mmHg 미만으로 하되 환자 개개인의 특성을 고려할 필요는 있겠다[11].
혈압이 정상인 당뇨병콩팥병 환자에서의 레닌-안지오텐신계억제제의 사용
고혈압이 동반되지 않은 당뇨병콩팥병 환자에서도 레닌-안지오텐신계억제제(renin-angiotensin system inhibitor)가 효과가 있을지에 대한 근거는 많지 않다. 그러나 reduction of endpoints in NIDDM with the angiotensin II antagonist losartan (RENNAL) 연구 및 investigation on type 2 diabetic nephropathy (INNOVATION) 연구에 참여한 대상자들 일부가 정상 혈압이었다는 점을 감안하면[35,36], 고혈압이 동반되지 않는 환자들에서도 레닌-안지오텐신계억제제 사용이 이로울 것으로 보인다[12,13]. 특히 알부민뇨 혹은 단백뇨의 수준이 증가함에 따라 콩팥병 진행의 위험이 커진다는 점을 생각해보면 고혈압이 없더라도 알부민뇨 혹은 단백뇨가 동반된 당뇨병콩팥병 환자에서는 환자가 감내할 수 있는 범위 내에서 레닌-안지오텐신계억제제를 사용하는 것이 타당할 것이다. 또한 당뇨병콩팥병 진료지침은 다른 지침에 비해 혈압 조절 목표를 낮게 제시하고 있으므로 이 혈압 목표를 달성하기 위해서는 보다 많은 당뇨병콩팥병 환자들이 레닌-안지오텐신계억제제를 처방받을 가능성이 높을 것이다.
기존의 스테로이드무기부신피질호르몬수용체길항제(steroidal mineralocorticoid receptor antagonist)는 소규모 연구에서 항단백뇨 효과를 보여주기는 하였으나 궁극적으로 콩팥병 진행을 지연시킬 수 있는지에 대해서는 명확한 근거가 없었다[14]. 새로이 출시된 비스테로이드무기질부신피질호르몬수용체길항제인 피네레논(finerenone)은 finerenone in reducing kidney failure and disease progression in diabetic kidney disease (FIDELIO-DKD)와 finerenone in reducing cardiovascular mortality and morbidity in diabetic kidney disease (FIGARO-DKD) 연구를 통하여 콩팥 및 심혈관 이득을 입증하였다[37,38]. FIDELIO-DKD 연구와 FIGARO-DKD 연구의 통합 분석 결과 역시 피네레논은 심혈관 복합 변수에 대한 위험뿐 아니라 콩팥 복합 변수 및 신대체요법에 대한 위험을 유의하게 낮추었다[39]. 비록 피네레논을 사용하게 되면 고칼륨혈증 발생이 다소 증가하지만 고칼륨혈증으로 인하여 피네레논을 영구적으로 중단하는 경우는 전반적으로 많지 않았으며 피네레논을 투여받기 전에 혈청포타슘이 정상이었던 대상자들에서 고칼륨혈증으로 인한 사망은 유의하지 않았다[39]. 이러한 근거에 따라 2022년 KDIGO 만성콩팥병에서의 당뇨병 임상진료지침과 마찬가지로 2023년 당뇨병콩팥병 진료지침은 추정사구체여과율 25 mL/min/1.73 m2 이상인 2형당뇨병콩팥병 환자에서 레닌-안지오텐신계억제제를 최대 내약용량으로 복용함에도 불구하고 알부민뇨가 지속된다면 비스테로이드무기질부신피질호르몬수용체길항제를 투여하도록 권고하였다[11,13]. 다만 KDIGO 지침과 달리 당뇨병콩팥병 진료지침에서는 혈청포타슘에 대한 조건을 따로 제시하지 않았는데[11], 약물 사용에 따른 고칼륨혈증의 위험에 대해서는 주기적인 감시와 더불어 식이요법 교육, 병용 약물의 검토 및 이뇨제, 탄산수소소듐(sodium bicarbonate) 혹은 포타슘결합제 등 포타슘 농도를 낮출 수 있는 약물의 사용을 통하여 혈청포타슘을 조절할 수 있을 것으로 보았기 때문이다[11,13]. 무기질부신피질호르몬수용체(mineralocorticoid receptor)는 심혈관계 세포 및 조직에도 존재하므로 이를 억제함으로써 혈관내피세포 기능 이상, 섬유화, 염증 등의 병태생리를 조절하여 콩팥 및 심혈관 보호 효과가 발휘되는 것으로 생각되고 있지만[40], 콩팥에서의 무기질부신피질호르몬수용체는 수분과 소듐 조절을 통한 혈압과 체액 유지에 있어 중요한 생리 역할을 담당하고 있다는 점을 감안하면 무기질부신피질호르몬수용체길항제는 레닌-안지오텐신계억제제, SGLT2억제제와 더불어 콩팥에 직접적으로 작용하는 콩팥병 치료제로 볼 수 있겠다(Fig. 3).
사구체여과율과 알부민뇨 분류에 따라, 예를 들어 알부민뇨 300 mg/g 이상, 추정사구체여과율 30 mL/min/1.73 m2 미만 또는 추정사구체여과율이 30-44 mL/min/1.73 m2이면서 알부민뇨 30-299 mg/g 범주인 경우에 신장전문의에게 의뢰하자는 기준 등이 제시되었기는 하지만[41], 이 기준에 대하여 객관적인 연구 근거가 있는 것은 아니다. 오히려 그러한 범주에 있는 환자들은 콩팥병 진행 위험이 이미 매우 높은 상태(very high risk)인 경우가 대부분이다[13,15]. 즉 기존 지침들에서 제시하고 있는 신장전문의 의뢰 기준은 콩팥 기능이 이미 70% 이상 상실된 상태이기 때문에 이를 기준으로 하여 신장전문의에게 당뇨병콩팥병 환자를 의뢰하는 것은 너무 늦다는 지적이 있어 왔다[42]. 게다가 사구체여과율이 60 mL/min/1.73 m2 이상이더라도 알부민뇨가 30-299 mg/g인 환자 혹은 알부민뇨가 30 mg/g 미만이라도 사구체여과율이 45-59 mL/min/1.73 m2인 환자 모두 이미 콩팥병 진행 위험이 중등도로 높아진 상태(moderately increased risk)에 놓여 있다는 점을 상기할 필요가 있다[13,15]. 이에 당뇨병콩팥병 진료지침에서는 성인 당뇨병 환자의 경우 알부민뇨가 있거나 추정사구체여과율이 60 mL/min/1.73 m2 미만이라면 콩팥 손상의 원인 감별과 향후 관리를 위하여 신장 전문의 협진이 필요하다고 하였다[11]. 적절한 시점에 콩팥병 환자가 신장전문의에게 의뢰 혹은 협진되지 않으면 사망률, 이환율, 입원 기간 및 의료비용 상승뿐 아니라 말기콩팥병에 대한 미흡한 치료, 신대체요법 준비의 어려움, 응급 투석 요법의 증가 등의 결과로 이어진다고 보고된 바 있다[43]. 또한 알부민뇨 발생이 선행하여 발병하는 전형적인 당뇨병콩팥병 외에 최근 수십여 년 사이에는 알부민뇨 혹은 단백뇨 발생 없이 사구체여과율만 점진적으로 감소하는 형태의 당뇨병콩팥병도 늘고 있어서[44], 당뇨병콩팥병의 다양한 병태생리 기전을 고려한다면 신장전문의 관점도 필요할 것이다. 또한 의뢰나 협진 시기를 고려할 때 사용되고 있는 기준인 추정사구체여과율이나 알부민뇨 외에도 kidney failure risk evaluation과 같은 말기콩팥병 위험 예측 공식을 활용한다면 신장전문의 협진 시점을 결정하는 데 있어 도움을 받을 수 있을 것이다[45]. 한편, 소아청소년 당뇨병 환자의 경우 당뇨병 진단 후의 이환 기간이 길어지게 되므로 콩팥 합병증의 발병과 진행을 최대한 늦추기 위해서는 보다 세밀한 관리가 필요하므로 성인보다도 조기에 소아청소년 신장전문의에게 의뢰하는 것이 필요하다. 이에 소아청소년 당뇨병 환자의 경우 혈당과 혈압을 최적으로 조절함에도 불구하고 알부민뇨, 추정사구체여과율 90 mL/min/1.73 m2 미만 혹은 원인이 불분명한 콩팥병의 소견을 보이는 경우 소아청소년 신장전문의에게 의뢰하도록 권고하였다[11]. 당뇨병의 다른 합병증과 마찬가지로 당뇨병콩팥병은 조기에 인지하고 필요한 치료를 조기에 적용하는 것이 중요하다[42]. 이를 위해서는 궁극적으로 신장전문의를 포함한 여러 전문가 집단에 의한 상호 협조적이고 통합적인 관리 접근이 필요하다고 하겠다.
당뇨병콩팥병 진료지침은 우리나라 당뇨병콩팥병의 현황부터 소아청소년 당뇨병콩팥병의 진단과 치료에 이르기까지 당뇨병콩팥병과 관련된 거의 모든 영역을 포함하였다. 특히 치료 분야에서는 최근 만성콩팥병의 치료제로서 주목을 받고 있는 SGLT2억제제나 비스테로이드무기질부신피질호르몬수용체길항제 등의 적응증과 기존 약물과의 병용 요법에 대한 권고를 제시하였다. 본 진료지침이 성공적으로 정착함으로써 당뇨병콩팥병 환자의 일선 진료 현장에 잘 적용된다면 그 임상에 미치는 효과는 서서히, 그렇지만 명확하게 나타날 것이며, 궁극적으로는 10년 후 예상되는 만성콩팥병 환자 수의 증가를 억제하고, 더 나아가 말기콩팥병 유병 환자 수를 감소시키고자 하는 최종 목표를 달성할 수 있을 것이다. 물론 이를 위해서는 의료진과 환자뿐 아니라 보건당국, 정책 입안자 및 관련 전문가들의 협력이 필요하다. 이 모든 과정에 있어 본 진료지침이 첫 발을 내딛는 역할을 함으로써 당뇨병이 동반된 만성콩팥병 환자의 임상 결과를 향상시키고 삶의 질을 개선시키며 우리나라 국민의 건강 수준 향상에 있어 큰 도움이 되기를 기대한다.
Notes
CONFLICTS OF INTEREST
The author is currently serving as Director of The Clinical Practice Guidelines Committee of The Korean Society of Nephrology (2022-2024). No other competing interests are declared.
Acknowledgements
Figure 3 was created with BioRender.com (confirmation of publication and licensing rights agreement number: YK26197G6U).
REFERENCES
1. GBD Chronic Kidney Disease Collaboration. Global, regional, and national burden of chronic kidney disease, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet 2020;395:709–733.


2. Jager KJ, Kovesdy C, Langham R, Rosenberg M, Jha V, Zoccali C. A single number for advocacy and communication-worldwide more than 850 million individuals have kidney diseases. Nephrol Dial Transplant 2019;34:1803–1805.


3. Kovesdy CP. Epidemiology of chronic kidney disease: an update 2022. Kidney Int Suppl (2011) 2022;12:7–11.



5. Sarnak MJ, Levey AS, Schoolwerth AC, et al. Kidney disease as a risk factor for development of cardiovascular disease: a statement from the American Heart Association Councils on Kidney in Cardiovascular Disease, High Blood Pressure Research, Clinical Cardiology, and Epidemiology and Prevention. Circulation 2003;108:2154–2169.


6. Health Insurance Review & Assessment Service (HIRA). 2021 National Health Insurance Statistical Yearbook [Internet]. Wonju (KR): HIRA, c2022 [cited 2022 Nov 30]. Available from: https://www.hira.or.kr/bbsDummy.do?pgmid=HIRAA020045020000/&brdScnBltNo=4&brdbrdBl=2314&pageIndex=1&pageIndex2=1
7. Aitken GR, Roderick PJ, Fraser S, et al. Change in prevalence of chronic kidney disease in England over time: comparison of nationally representative cross-sectional surveys from 2003 to 2010. BMJ Open 2014;4:e005480.



8. Ahn JH, Yu JH, Ko SH, et al. Prevalence and determinants of diabetic nephropathy in Korea: Korea national health and nutrition examination survey. Diabetes Metab J 2014;38:109–119.



9. The Korean Society of Nephrology Korean Renal Data System (KORDS) Committee. Trends in epidemiologic characteristics of end-stage renal disease from 2022 KORDS [Internet]. Seoul (KR): The Korean Society of Nephrology, c2023 [cited 2023 Jul 31]. Available from: https://www.ksn.or.kr/bbs/index.php?code=report
10. United States Renal Data System (USRDS). 2022 annual data report: epidemiology of kidney disease in the United States [Internet]. Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases, c2022 [cited 2022 Oct 31]. Available from: https://usrds-adr.niddk.nih.gov/2022
11. The Korean Society of Nephrology Clinical Practice Guideline Committee. Korean Society of Nephrology 2023 practical recommendations for the management of diabetic kidney disease [Internet]. Seoul (KR): The Korean Society of Nephrology, c2023 [cited 2023 Jul 11]. Available from: https://ksn.or.kr/bbs/?code=guideline_k
12. Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group. KDIGO 2020 clinical practice guideline for diabetes management in chronic kidney disease. Kidney Int 2020;98:S1–S115.


13. Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group. KDIGO 2022 clinical practice guideline for diabetes management in chronic kidney disease. Kidney Int 2022;102:S1–S127.


14. Navaneethan SD, Zoungas S, Caramori ML, et al. Diabetes management in chronic kidney disease: synopsis of the KDIGO 2022 clinical practice guideline update. Ann Intern Med 2023;176:381–387.


15. Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney Int Suppl 2013;3:1–150.
16. Kidney Disease: Improving Global Outcomes (KDIGO) Lipid Work Group. KDIGO clinical practice guideline for lipid management in chronic kidney disease. Kidney Int Suppl (2011) 2013;3:259–305.

17. Kidney Disease: Improving Global Outcomes (KDIGO) Blood Pressure Work Group. KDIGO 2021 clinical practice guideline for the management of blood pressure in chronic kidney disease. Kidney Int 2021;99:S1–S87.


18. Ruospo M, Saglimbene VM, Palmer SC, et al. Glucose targets for preventing diabetic kidney disease and its progression. Cochrane Database Syst Rev 2017;6:CD010137.



19. Duckworth W, Abraira C, Moritz T, et al. Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med 2009;360:129–139.


20. Action to Control Cardiovascular Risk in Diabetes Study Group, Gerstein HC, Miller ME, et al. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med 2008;358:2545–2559.



21. Shurraw S, Hemmelgarn B, Lin M, et al. Association between glycemic control and adverse outcomes in people with diabetes mellitus and chronic kidney disease: a population-based cohort study. Arch Intern Med 2011;171:1920–1927.


22. Low S, Zhang X, Wang J, et al. Impact of haemoglobin A1c trajectories on chronic kidney disease progression in type 2 diabetes. Nephrology (Carlton) 2019;24:1026–1032.


23. Heerspink HJL, Stefánsson BV, Correa-Rotter R, et al. Dapagliflozin in patients with chronic kidney disease. N Engl J Med 2020;383:1436–1446.


24. Bhatt DL, Szarek M, Pitt B, et al. Sotagliflozin in patients with diabetes and chronic kidney disease. N Engl J Med 2021;384:129–139.


25. The EMPA-KIDNEY Collaborative Group, Herrington WG, Staplin N, et al. Empagliflozin in patients with chronic kidney disease. N Engl J Med 2023;388:117–127.



26. Nuffield Department of Population Health Renal Studies Group; SGLT2 inhibitor Meta-Analysis Cardio-Renal Trialists' Consortium. Impact of diabetes on the effects of sodium glucose co-transporter-2 inhibitors on kidney outcomes: collaborative meta-analysis of large placebo-controlled trials. Lancet 2022;400:1788–1801.


27. Mosenzon O, Raz I, Wiviott SD, et al. Dapagliflozin and prevention of kidney disease among patients with type 2 diabetes: post hoc analyses from the DECLARE-TIMI 58 trial. Diabetes Care 2022;45:2350–2359.



28. Kraus BJ, Weir MR, Bakris GL, et al. Characterization and implications of the initial estimated glomerular filtration rate 'dip' upon sodium-glucose cotransporter-2 inhibition with empagliflozin in the EMPA-REG OUTCOME trial. Kidney Int 2021;99:750–762.


29. Oshima M, Jardine MJ, Agarwal R, et al. Insights from CREDENCE trial indicate an acute drop in estimated glomerular filtration rate during treatment with canagliflozin with implications for clinical practice. Kidney Int 2021;99:999–1009.


30. Koh ES, Kim GH, Chung S. Intrarenal mechanisms of sodium-glucose cotransporter-2 inhibitors on tubuloglomerular feedback and natriuresis. Endocrinol Metab (Seoul) 2023;38:359–372.



31. Tomson CRV, Cheung AK, Mann JFE, et al. Management of blood pressure in patients with chronic kidney disease not receiving dialysis: synopsis of the 2021 KDIGO clinical practice guideline. Ann Intern Med 2021;174:1270–1281.


32. SPRINT Research Group, Wright JT Jr, Williamson JD, et al. A randomized trial of intensive versus standard blood-pressure control. N Engl J Med 2015;373:2103–2116.



33. Bress AP, King JB, Kreider KE, et al. Effect of intensive versus standard blood pressure treatment according to baseline prediabetes status: a post hoc analysis of a randomized trial. Diabetes Care 2017;40:1401–1408.


34. Nazarzadeh M, Bidel Z, Canoy D, et al. Blood pressure-lowering treatment for prevention of major cardiovascular diseases in people with and without type 2 diabetes: an individual participant-level data meta-analysis. Lancet Diabetes Endocrinol 2022;10:645–654.


35. Keane WF, Brenner BM, de Zeeuw D, et al. The risk of developing end-stage renal disease in patients with type 2 diabetes and nephropathy: the RENAAL study. Kidney Int 2003;63:1499–1507.


36. Makino H, Haneda M, Babazono T, et al. Prevention of transition from incipient to overt nephropathy with telmisartan in patients with type 2 diabetes. Diabetes Care 2007;30:1577–1578.


37. Bakris GL, Agarwal R, Anker SD, et al. Effect of finerenone on chronic kidney disease outcomes in type 2 diabetes. N Engl J Med 2020;383:2219–2229.


38. Pitt B, Filippatos G, Agarwal R, et al. Cardiovascular events with finerenone in kidney disease and type 2 diabetes. N Engl J Med 2021;385:2252–2263.


39. Agarwal R, Filippatos G, Pitt B, et al. Cardiovascular and kidney outcomes with finerenone in patients with type 2 diabetes and chronic kidney disease: the FIDELITY pooled analysis. Eur Heart J 2022;43:474–484.



40. Lv R, Xu L, Che L, Liu S, Wang Y, Dong B. Cardiovascularrenal protective effect and molecular mechanism of finerenone in type 2 diabetic mellitus. Front Endocrinol (Lausanne) 2023;14:1125693.



41. de Boer IH, Khunti K, Sadusky T, et al. Diabetes management in chronic kidney disease: a consensus report by the American Diabetes Association (ADA) and Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int 2022;102:974–989.


42. Martínez-Castelao A, Soler MJ, Górriz Teruel JL, et al. Optimizing the timing of nephrology referral for patients with diabetic kidney disease. Clin Kidney J 2020;14:5–8.



43. Wavamunno MD, Harris DC. The need for early nephrology referral. Kidney Int Suppl 2005;67:S128–S132.


44. Pugliese G, Penno G, Natali A, et al. Diabetic kidney disease: new clinical and therapeutic issues. Joint position statement of the Italian Diabetes Society and the Italian Society of Nephrology on “The natural history of diabetic kidney disease and treatment of hyperglycemia in patients with type 2 diabetes and impaired renal function”. Nutr Metab Cardiovasc Dis 2019;29:1127–1150.


Annual expenses per capita per year (Korean Won) for hypertension, diabetes, cardiac disease, cerebrovascular disease, malignancy, liver disease, arthritis, and chronic kidney disease (from left to right) in Korea. In September 2023, the KRW-US dollar exchange rate was 1,333.4 KRW per 1 US dollar, based on the daily exchange rates provided by Woori Bank.
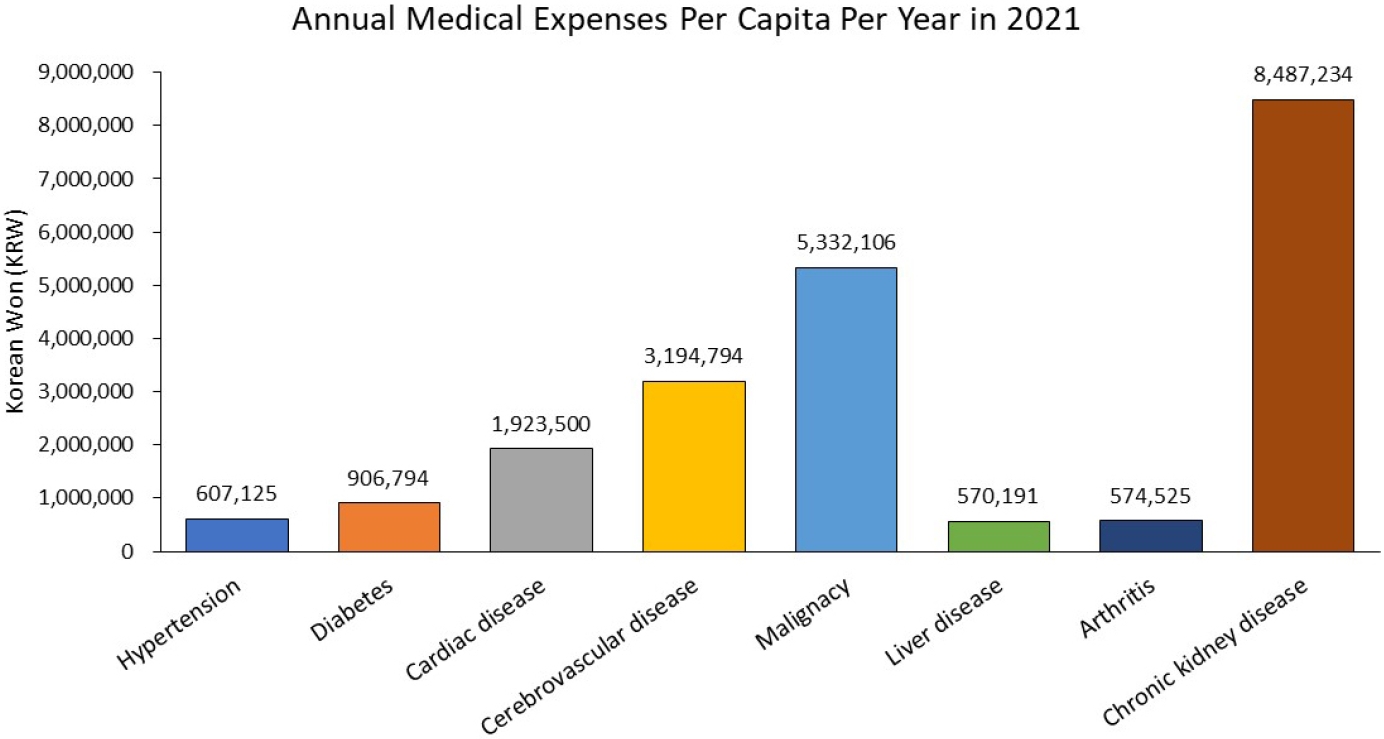
Figure 1.
Incidence and prevalence of ESKD, proportion of annual ESKD incidence, and causes of ESKD in Korea. Adopted from The Korean Society of Nephrology Korean Renal Data System [9] with permission from the Korean Renal Data System Registry Committee of The Korean Society of Nephrology. ESKD, end-stage kidney disease; HD, hemodialysis; PD, peritoneal dialysis; KT, kidney transplantation; DM, diabetes mellitus; HTN, hypertension; Chronic GN, chronic glomerulonephritis.
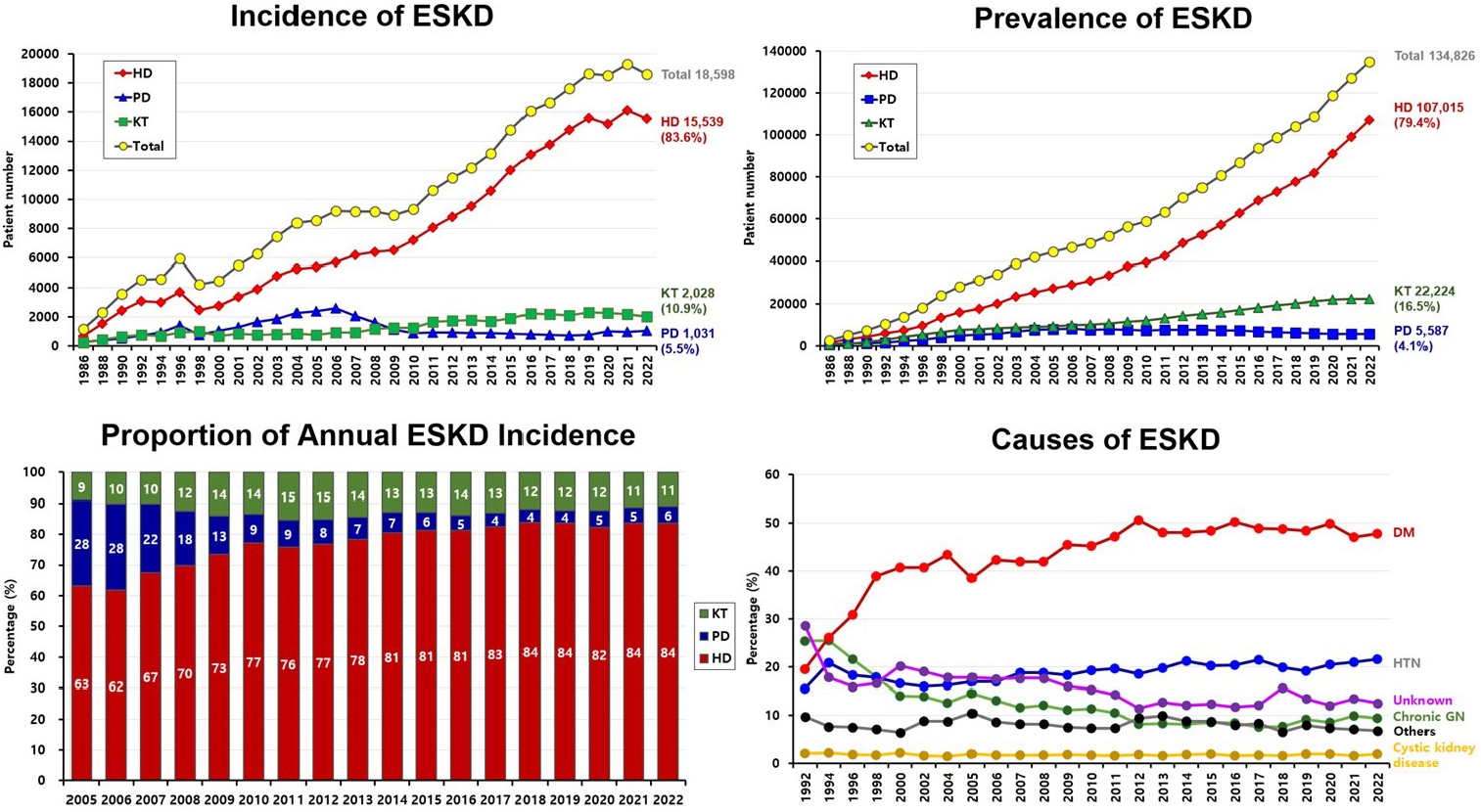
Figure 2.
Mechanisms of action of medications used to treat diabetic kidney disease, focusing on renin-angiotensin system inhibitors, SGLT2 inhibitors, and mineralocorticoid receptor antagonists. Renin-angiotensin system inhibitors, such as angiotensin-converting enzyme inhibitors and angiotensin receptor blockers, reduce glomerular capillary pressure by decreasing arterial pressure and selectively dilating efferent arterioles via inhibition of the angiotensin II AT1 receptor. In diabetes, the expression of SGLT2 in the proximal tubules of the kidneys is upregulated by increased glycosuria, leading to excessive sodium reabsorption. SGLT2 inhibitors enhance the distal delivery of sodium chloride by inhibiting SGLT2. At the macula densa, the Na+-K+-2Cl- cotransporter (NKCC2) detects an increase in the luminal NaCl concentration, triggering the release of adenosine from the macula densa, which in turn affects arterioles. The expression and transport of the ENaC in the collecting duct are regulated by aldosterone, which binds to an intracellular MR, leading to increased transcription and expression of several genes, including ENaC and the Na+-K+-ATPase). Mineralocorticoid receptor antagonists such as finerenone target the MR, thereby inhibiting sodium influx through ENaC. SGLT2, sodium-glucose cotransporter-2; ENaC, epithelial sodium channel; AT1 receptor, angiotensin II type 1 receptor; MR, mineralocorticoid receptor; Na+-K+-ATPase, sodium-potassium- ATPase.
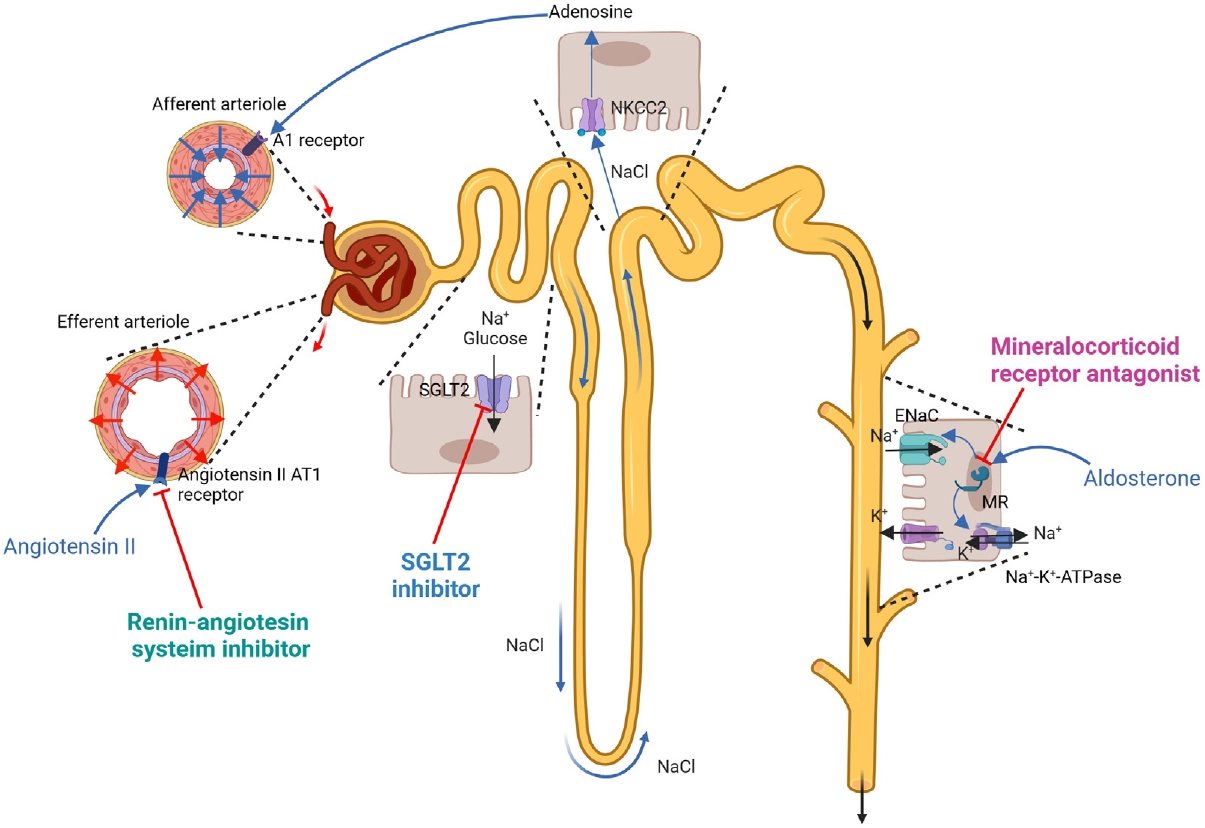
Figure 3.
Table 1.
Summary of the recommendation statements in the KSN 2023 practical recommendations for the management of diabetic kidney disease
-
METRICS

-
- 1 Crossref
- 0 Scopus
- 1,166 View
- 138 Download



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



