당뇨병 치료약제와 심혈관 질환
Anti-Diabetic Drugs in Cardiovascular Disease
Article information
Trans Abstract
Diabetes is one of the important risk factors in cardiovascular disease associated with atherosclerosis, and cardiovascular disease is the leading cause of death in patients with diabetes mellitus. Recent randomized placebo-controlled cardiovascular outcome trials of all new antidiabetic drugs have linked SGLT-2 inhibitors and GLP1-agonists to not only increased cardiovascular stability but significant reduction of cardiovascular disease. These results have led to preferential selection of the most effective and beneficial antidiabetic drugs with the evidence of cardiovascular safety and efficacy. Herein, we address cardiovascular stability and the effectiveness of antidiabetic drugs, focusing on recently developed ones.
서 론
당뇨는 동맥경화와 관련된 심혈관 질환의 가장 중요한 인자 중 하나로, 당뇨병이 있는 경우 심혈관 질환의 위험률이 2-3배 이상 증가한다. 심혈관 질환은 당뇨병 환자의 주요 사망 원인 중 하나이며, 특히 심혈관 질환의 위험률은 당뇨의 유병 기간에 따라 증가하고 고혈압, 이상지질혈증, 대사증후군, 만성 신장 질환과 같은 동반 질환 유무에 영향을 받는다[1]. 따라서 당뇨 환자에서 심혈관 질환의 예방과 치료는 매우 중요하다. 당뇨 치료약제 중 하나인 로시글리타존(rosiglitazone)이 심혈관 질환의 위험을 증가시킨다는 것이 확인된 후 미국식품의약국(Food and Drug Administration, FDA)은 2008년부터 모든 당뇨 치료약제에 대한 심혈관 질환 발생 자료를 요구하였다[2,3]. 이에 따라 DPP-4 억제제(dipeptidyl peptidase 4 inhibitor, DPP4-inhibitor)를 시작으로 새로운 당뇨 치료약제들 모두에서 심혈관 질환 발생에 대한 임상 연구를 통해 당뇨 치료약제들의 심혈관 안정성에 대한 임상적 근거가 제시되었다. 이러한 가운데 최근 개발된 당뇨병 약제인 SGLT-2 억제제(sodium-glucose cotransporter 2 inhibitor, SGLT2 inhibitor)와 GLP-1 수용체 작용제(glucagon-like peptide 1 receptor agonist, GLP-1 agonist)는 심혈관 안정성이 있을 뿐 아니라 심혈관 질환의 발생을 감소시키는 데 명백한 이점이 있음이 확인되었고 이를 토대로 가이드라인의 변화 및 임상에 많은 변화가 일어났다[4]. 과거에 당뇨병 치료 목표가 혈당의 적절한 조절에 있었다면 최근에는 심혈관 질환의 위험도 경감에 더 초점이 맞춰져 있으며, 당뇨 치료약제의 선택에 있어 심혈관 안정성 및 심혈관 유효성의 증거가 있는 약제를 추천해야 하는 치료 패러다임의 변화를 가져온 것이다. 이에 따라 최근 미국당뇨병학회(American Diabetes Association, ADA)에서는 심혈관 질환이 있거나 다수의 심혈관 질환 위험인자가 있는 경우 이 2가지 약제를 처방하라고 권고하고 있다[1,4]. 이에 본고에서는 최근 개발된 당뇨 치료 약제를 중심으로 심혈관 안정성과 효과를 요약하고 임상적 적용을 소개하고자 한다.
본 론
최근 개발된 당뇨 치료약제에는 DPP-4 억제제, GLP-1 수용체 작용제, SGLT-2 억제제가 있다. 각 약제의 심혈관 안정성을 확인하는 무작위 위약 대조 심혈관 질환 발생 연구(randomized placebo-controlled CV outcome trials)에서 일차 연구 종말은 심혈관계 관련 사망, 비치명적 심근경색 또는 비치명적 뇌졸중으로 정의되는 3-point 주요 심혈관계 관련 사건(major adverse cardiovascular event, MACE)으로 정의되었고, 추가적으로 심부전에 의한 입원, 불안정성 협심증에 의한 입원, 총 사망의 종합 혹은 각각의 결과를 통해 안정성 및 효과를 확인하였다. 그 결과 일부 약제 연구에서는 심혈관 안정성 확인과 함께 심혈관 질환 예방 효과까지 확인이 되면서 추가적인 연구들이 진행되고 있다. 아래에 각 약제별로 연구 임상 연구 결과를 서술하고 표로 정리하였다.
DPP-4 억제제(dipeptidyl peptidase 4 inhibitor, DPP-4 inhibitor)
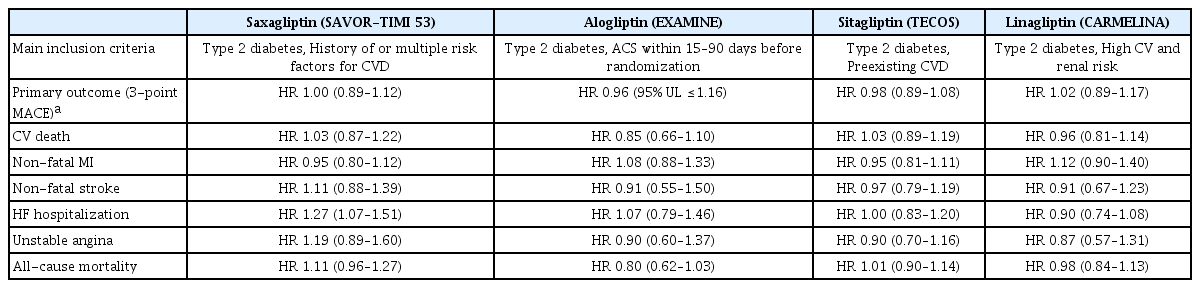
DPP-4 억제제는 중등도의 당 강화 효과가 있고 저혈당의 위험이 낮아 많은 환자에서 사용되는 당뇨 치료약제 중 하나이다. DPP-4 억제제는 소장에서 분비되는 인크레틴(incretin)인 glucagon-like-peptide 1 (GLP-1)을 분해하여 불활성화 시키는 효소인 DPP-4를 억제하는 역할을 하며, 이를 통해 인슐린 분비를 촉진하고 인슐린 작용 시간을 증가시키며 글루카곤 분비를 억제함으로써 혈당을 감소시킨다[5]. 가장 먼저 발표된 Saxagliptin Assessment of vascular Outcomes Recorded in Patients with Diabetes Mellitus-Thrombolysis in Myocardial Infarction 53 (SAVOR-TIMI 53) 연구에서는 3-point MACE에 대해 saxagliptin 사용군과 대조군 간의 유의한 차이가 없었고, 이후 발표된 alogliptin군과 대조군을 비교한 Examination of Cardiovascular Outcomes with Alogliptin versus Standard of Care (EXAMINE) 연구와 sitagliptin군과 대조군을 비교한 Trial to Evaluate Cardiovascular Outcomes After Treatment With Sitagliptin (TECOS) 연구, linagliptin군과 대조군을 비교한 The Cardiovascular and Renal Microvascular Outcome Study With Linagliptin (CARMELINA) 연구 모두에서도 심혈관 질환에 대한 유의한 차이를 보이지 않았다(Table 1) [6-9]. 이들은 모두 비열등성 임상 연구로써, 이 연구 결과로 DPP-4 억제제의 심혈관 안정성이 입증되었다. 다만, linagliptin과 sitagliptin에서는 유의하지 않았지만 SAVOR-TIMI 53 연구 결과 saxagliptin이 대조군에 비해 심부전에 의한 입원을 27%가량 의미 있게 증가시키는 것이 확인되었고, 이후 DPP-4 억제제의 심부전에 의한 입원 증가 문제가 대두되면서 진행된 alogliptin의 하위 연구에서는 심부전을 기저에 진단받았던 환자에서는 alogliptin 투약군과 대조군 간에 심부전에 의한 입원에 대해 유의한 결과를 보이지 못하였으나, 기저에 심부전을 진단받지 않았던 환자에서는 alogliptin을 사용한 군에서 대조군에 비해 심부전으로 인한 입원을 76% 증가시키는 것이 확인되었다[7,10]. 결국 당뇨 환자에서 DPP4 억제제는 심혈관 안정성은 입증되었으나 심혈관 질환 예방에 유의한 효과는 없으며, 일부에서는 심부전으로 인한 입원 증가의 위험이 있다.
GLP-1 수용체 작용제(glucagon-like peptide 1 receptor agonist, GLP-1 agonist)
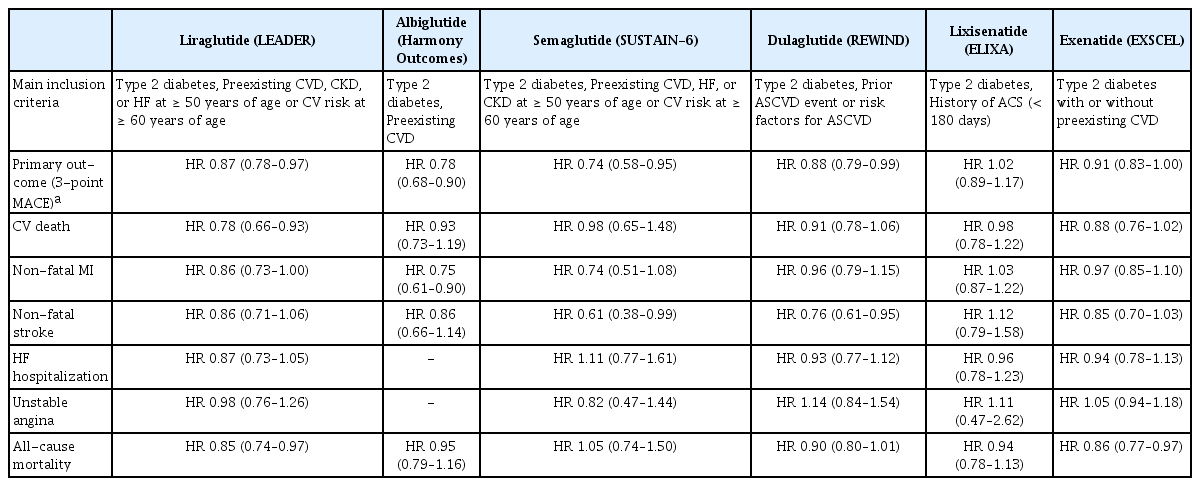
GLP-1 수용체 작용제는 피하주사제 당뇨 치료약제로 DPP-4 억제제와 유사하게 인크레틴의 작용을 증가시켜 혈당 강하 효과를 보인다[11]. GLP-1 수용체 작용제는 당뇨 치료약제 중 심혈관 안정성에 대한 입증과 함께 심혈관 질환 예방에 효과가 있는 최초의 약제로 대두되었다. GLP-1 수용체 작용제 중 대표적 약제인 liraglutide의 임상 연구(Liraglutide Effect and Action in Diabetes: Evaluation of Cardiovascular Outcome Results, LEADER)에서는 liraglutide의 심혈관 질환에 대해 안전할 뿐 아니라 치료군이 대조군과 비교하여 유의하게 3-point MACE를 감소시키는 것을 확인하였다[12]. 또한, 다른 GLP-1 수용체 작용제인 semaglutide를 사용한 Trial to Evaluate Cardiovascular and Other Long-term Outcomes With Semaglutide in Subjects With Type 2 Diabetes (SUSTAIN-6) 연구, albiglutide와 대조군을 비교한 Albiglutide and cardiovascular outcomes in patients with type 2 diabetes and cardiovascular disease (Harmony) 연구 그리고 dulaglutide와 대조군을 비교한 Researching Cardiovascular Events With a Weekly Incretin in Diabetes (REWIND) 연구에서도 모두 심혈관 안정성과 함께 심혈관 질환 예방에 긍정적인 결과를 보였다(Table 2) [13-15]. 또한, GLP-1 수용체 작용제가 혈당 조절 외에도 인슐린 저항성 개선, 체중 감소 및 이상지질혈증의 개선 등을 통해 당뇨병 자체의 발생 위험을 낮추고 대사증후군의 개선에도 도움을 주는 것이 확인되어 이로 인한 심혈관 질환 예방 효과도 있는 것으로 생각된다[16]. 그러나 GLP-1 수용체 작용제 중 lixisenatide와 exenatide를 사용한 Evaluation of Lixisenatide in Acute Coronary Syndrome (ELIXA) 연구 및 Exenatide Study of Cardiovascular Event Lowering (EXSCEL) 연구에서는 심혈관 안전성은 검증되었으나 심혈관 질환 예방 효과는 입증하지 못하였다[17,18]. 따라서 현재 ADA에서는 특히 심혈관 질환이 있는 환자 및 다수의 심혈관 질환 위험인자가 있는 환자의 경우 심혈관 질환 예방효과가 있는 4가지 약제(liraglutide, albiglutide, semaglutide, dulaglutide)의 투약을 권고하고 있다[1].
SGLT-2 억제제(sodium-glucose cotransporter 2 inhibitor, SGLT2 inhibitor
SGLT-2 억제제는 콩팥의 근위부 세뇨관에서 당의 재흡수를 담당하는 SGLT-2 수용체를 억제하여 소변으로 당 배설을 촉진시키고 그 결과 혈액 내 혈당을 감소시키는 약제이다[19]. SGLT-2 억제제 중 최초로 보고된 empagliflozin에 대한 안정성 연구인 Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes trial (EMPA-REG OUTCOME) 결과를 보면 empagliflozin을 투약한 군에서 대조군에 비해 3-point MACE가 14% 감소되었고 심혈관계 사망 단독에 대해서는 38%의 감소를 보였다[20]. 또한, Canagliflozin을 사용한 Canagliflozin Cardiovascular Assessment Study (CANVAS) 연구에서도 마찬가지로 3-point MACE에 대해 유의한 감소를 보였으며 만성 신부전 환자를 대상으로 한 CANVASRenal (CANVAS-R) 및 Canagliflozin and Renal Events in Diabetes with Established Nephropathy Clinical Evaluation (CREDENCE) 연구에서는 canagliflozin 투약군에서 대조군에 비하여 유의하게 위험성이 감소하였다[21-23]. 한편, dapagliflozin 투약군과 대조군을 비교한 연구(dapagliflozin effect on cardiovascular events-thrombosis in myocardial infarction 58, DECLARE-TIMI 58)에서는 3-point MACE의 발생을 유의하게 감소시키지는 못하였으나 심혈관계 사망률과 심부전에 의한 입원 각각에 대해서는 유의한 감소를 확인하였다[24]. 이 3가지 약제에 대한 임상 연구의 결과로 SGLT-2 억제제는 심혈관 안정성은 물론이고 신장 질환자에 대한 안정성도 보여주었으며, 심혈관 질환 예방효과 역시 뛰어남을 보여주었다(Fig. 1). 특히, SGLT-2 억제제는 혈당의 감소 외에도 삼투압성이뇨(osmotic diuresis) 및 나트륨성이뇨(natriuresis)로 인한 중등도의 이뇨 효과를 보여 심혈관 질환과 별개로 심부전 환자에서 긍정적 작용을 하리라 기대하였던 약제로 실제 안정성 연구에서 심부전에 대한 긍정적 효과가 확인되면서 SGLT-2 억제제의 심부전에 대한 효과를 확인하는 임상 연구가 진행되었다. Dapagliflozin의 심부전에 대한 효과를 확인하였던 Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction (DAPA-HF) 연구에서 좌심실 박출률이 감소된 심부전 환자에서 dapagliflozin이 심혈관계 사망 및 심부전에 의한 입원을 감소시키는 것을 확인하였고 대상 환자의 50%가 비 당뇨 환자로 당뇨의 유무 상관없이 그 효과가 있음이 입증되었다. 이후 진행된 empagliflozin의 심부전에 대한 효과를 본 Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure (EMPEROR-REDUCED) 연구에서도 마찬가지의 결과를 입증함으로써 SGLT-2 억제제는 당뇨 치료약제를 넘어 새로운 심부전 치료약제로 각광받게 되었다(Table 3) [25,26]. 또한, SGLT-2 억제제도 GLP-1 수용체 작용제처럼 인슐린 저항성 개선, 체중감소 등의 효과가 있어 심혈관 질환 위험인자의 개선에 도움을 주며 이로 인한 심혈관 질환의 예방 효과도 보인다[19]. 이러한 결과로 인해 아직 가이드라인에 반영되지는 않았으나 국내외 전문가들은 기저 심장 질환이 있는 환자에서 SGLT-2 억제제를 메트포르민 대신 당뇨 치료의 일차 약제로 고려할 것을 권고하고 있다[25,26].
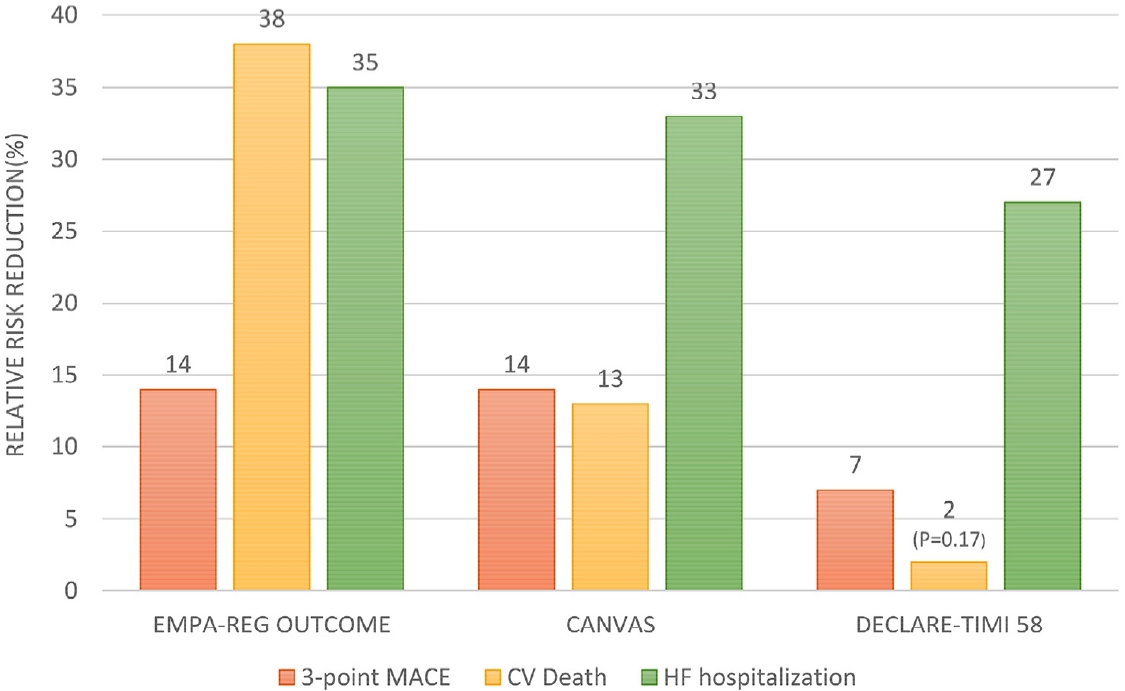
Cardiovascular outcome trials of SGLT2-Inhibitors. EMPA-REG OUTCOME trial for empagliflozin, CANVAS trial for canagliflozin, DECLARE-TIMI 58 trial for dapagliflozin. All relative risk reduction is statistically significant (p < 0.05) except CV death in DECLARE-TIMI 58. 3-point MACE, composite of death from cardiovascular causes, nonfatal myocardial infarction, or nonfatal stroke; CV, cardiovascular; HF, heart failure.

SGLT-2 inhibitors in patients with reduced ejection fraction: the results of DAPA-HF and EMPEROR-REDUCED Trial
이러한 연구 결과를 바탕으로 대한당뇨병학회에서는 관상동맥 질환, 심근경색 등과 같은 심장 질환이 있는 고위험군에서는 SGLT-2 억제제 중 심혈관 예방효과가 입증된 약제를 우선 고려하도록 권고하고 있고 미국과 유럽당뇨병학회에서도 죽상경화성 심혈관 질환(atherosclerotic cardiovascular disease, ASCVD)을 동반한 당뇨병 환자에게는 SGLT-2 억제제 혹은 GLP-1 수용체 작용제를 처방하는 것을 권고하고 있다[1]. 게다가 미국 FDA에서는 dapagliflozin을 당뇨병 환자의 심부전 예방약 및 심부전 치료제로, canagliflozin을 당뇨병성 신질환을 동반한 제2형 당뇨병 치료제로 승인한 바 있다. 다만, 아직까지 국내 보험 급여 기준은 당뇨 환자에서 메트포르민 혹은 인슐린과 병용 투약하거나 당화혈색소(HbA1c)가 7.5% 이상인 경우만 급여 인정이 되고, 당화혈색소(HbA1c)가 7.5% 미만의 경우 환자 본인 전액부담으로 처방이 가능한 상태이다. 따라서 아직까지는 이를 임상에 적용하기에는 제한점이 많다.
요약 및 향후 기대효과
당뇨 치료약제의 심혈관 질환 안정성 연구는 초기에는 잠재적으로 심혈관 질환의 위험성이 있는 당뇨 치료약제를 막기 위해 시작되었으나 결국에는 새로운 약제들의 심혈관 질환 예방효과가 입증되면서 당뇨병뿐만 아니라 심혈관 질환 치료 지침에도 변화를 불러오고 있다. 현재까지의 연구 결과로 보아 DPP-4 억제제는 심혈관 안정성은 증명되었으나 심혈관 질환에 대한 예방효과는 확실치 않으며, 일부 약제의 경우 심부전 악화의 위험성이 있다. 반면, 3개의 SGLT-2 억제제(empagliflozin, canagliflozin, dapagliflozin)와 4개의 GLP-1 수용체 작용제(liraglutide, albiglutide, semaglutide, dulaglutide)는 심혈관 안정성이 확인되었을 뿐 아니라 유의하게 심혈관 질환의 발생을 감소시킨다는 것이 확인되어 이 두 가지 약제의 심혈관 질환 예방효과는 분명하다[27]. 특히 SGLT-2 억제제는 만성 신부전 환자에서 신기능 개선의 효과를 보이고 비 당뇨 환자에서도 심부전에 의한 입원률 감소 및 신장기능 개선에도 효과가 있으며 특히 좌심실 박출이 감소된 심부전 환자에서 심혈관계 사망 및 심부전에 의한 입원을 감소시키는 결과를 보여 임상적으로 여러 환자군에서 서로 다른 효과를 기대하며 적용할 수 있겠다. 따라서 특정 환자군에서 SGLT-2 억제제의 효과를 확인하는 연구들이 필요할 것으로 생각되며, 현재 좌심실 박출률이 보존된 심부전 환자나 급성 심근경색 환자, 관상동맥 질환 환자를 대상으로 한 연구가 진행되어 곧 발표 예정에 있다. 또한, GLP-1 수용체 작용제는 체중감량에 있어 뛰어난 효과를 보여 새로운 비만 치료제로 떠오르고 있어 향후 당뇨 치료약제를 넘어선 새로운 영역의 치료제로서의 역할도 기대된다. 한편, SGLT-2 억제제와 GLP-1 수용체 작용제를 함께 투약하였을 때의 추가적인 효과는 아직 알려진 바가 없어 향후 이에 대한 연구도 필요할 것으로 보인다.
결 론
당뇨 치료약제의 심혈관계 질환 안정성 연구는 초기에 잠재적으로 유해한 약제를 확인하는 것에서 확장되어 새로운 약제에 대한 연구 결과로 인해 당뇨 및 심혈관 환자에서 입증된 안정성뿐만 아니라 심혈관 질환을 예방 혹은 치료하는 분야까지 확장되었다. 이와 같은 결과는 당뇨 치료약제의 선택에 있어 심혈관 안정성 및 심혈관 유효성의 증거가 있는 약제 특히 GLP-1 수용체 작용제와 SGLT-2 억제제를 추천해야 하는 치료 패러다임의 변화를 가져왔다. 향후 추가적인 연구를 통해 환자의 심혈관 질환의 위험도, 질환 유무에 따른 약제 선택이 가능해질 것으로 예상되며 당뇨병 치료 목표가 단순한 당뇨 조절이 아닌 더 나아가 효과적인 심혈관 질환의 예방 및 사망률 감소에 이르게 될 것으로 예상된다.