증 례
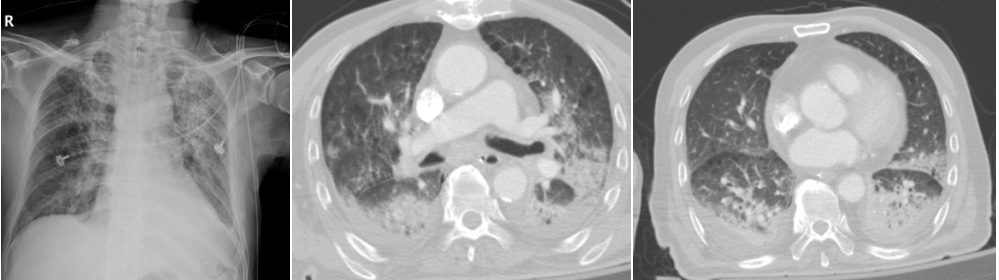
80세 남자가 고열과 호흡곤란으로 응급실에 내원하였다. 5일 전부터 기침과 가래가 있었으며 호흡기 증상은 점점 더 심해졌다고 한다. 혈압 90/40 mmHg, 호흡수 25회/분, 심박수 120회/분, 체온 39℃, 체중 50 kg이었다. 생리식염수 1L 정주와 동시에 혈중 젖산 농도를 포함한 일반화학 및 혈액배양 검사를 같이 시행하였다. 산소 투여 전 동맥혈 검사는 pH 7.324, pCO2 44.6 mmHg, pO2 58.8 mmHg, SpO2 89%였으며, 젖산 농도는 3.8 mmol/L였다. 진찰 시 qSOFA는 높은 호흡수와 낮은 혈압으로 3점 중 2점이었다. 양 폐에서 악설음이 들렸으며 단순가슴촬영사진에서 양측성 폐경화 소견이 보였으며 가슴 전산화단층촬영술을 시행하였다(Fig. 1). 비강을 통하여 2 L/분의 산소 투여 후 산소 포화도는 95% 이상 유지되었다. 폐렴에 의한 패혈증 진단 후 세프트리악손(ceftriaxone)과 레보플록사신(levofloxacin)을 정주하였다. 응급실 내원 후 1시간 동안 환자는 총 1.5 L의 생리식염수 투여 후 활력 징후는 혈압 120/80 mmHg, 호흡수 21회/분, 심박수 90회/분으로 안정되었다.
서 론
중환자실 입실 환자의 25-30%를 차지하는 패혈증은 여전히 30-50%의 높은 사망률을 보이고 있지만 실제 임상 현장에서 패혈증을 정확히 진단하는 것은 어렵다. 최근 국내에서 다기관으로 시행된 후향적 연구[1]에 따르면 한 달이라는 특정 기간 동안 응급실을 방문한 환자에서 패혈증 유병률을 조사한 결과, 인구 1,000명당 15.2명, 약 1.5%였고 이 중 36.5%의 환자가 패혈성 쇼크(septic shock)에 합당하였다. 사망률은 패혈증의 경우 약 25%, 패혈성 쇼크에서는 약 40%로 나타났는데, 유병률은 소득이 비슷한 다른 나라와 비교해서 유사하였지만 사망률은 보다 높았다는 점에서 시사하는 바가 있으며, 이는 등록된 환자의 나이가 고령이었기 때문일 수 있음을 저자들은 언급하였다.
패혈증의 정의(2016 Sepsis-3)
가장 최근 개정된 패혈증의 정의는 2016년 2월 미국과 유럽 중환자학회(Society of Critical Care Medicine/European Society of Intensive Care Medicine)가 공동으로 발표한 새로운 합의 지침인 “Sepsis-3”에서 찾을 수 있다[2]. 여기서 패혈증은 의심 또는 명백한 감염에 의해 발생한 생명을 위협하는 장기부전으로 정의하였고, 특히 기존의 중환자에서 예후 예측을 위한 장기부전 점수로 측정하였던 sequential organ failure assessment (SOFA) 점수가 2점 이상 증가한 경우로 구체화하였다. 패혈성 쇼크는 패혈증의 정의에 기존과 마찬가지로 혈압의 기준이 포함된 것으로 적절한 수액 치료에도 불구하고 평균 동맥압 65 mmHg을 만족하기 위하여 승압제가 필요하면서 혈청 젖산 농도가 2 mmol/L 이상인 경우이다.
초기 패혈증의 정의는 이미 널리 알려진 바 있듯이 “전신성 염증 반응 증후군(systemic inflammatory response syndrome, SIRS)”에 기초하였다. 이것은 1992년 처음 발표된 개념[3]으로, 4가지 임상기준 중 2가지 이상(체온 > 38℃ 혹은 < 36℃, 심박수 > 90회/분, 호흡수 > 20회/분 혹은 동맥혈 이산화탄소 분압 < 32 mmHg, 백혈구 수 > 12,000개/mm3 혹은 < 4,000개/mm3)을 만족시킬 때 해당하며 SIRS와 더불어 확인된 또는 의심되는 감염증이 있을 때 패혈증이라고 정의하였다. 이후 2003년에 발표된 Sepsis-2 정의에서는 중증 패혈증(severe sepsis)이라는 개념으로 장기부전이 진행된 경우를 별도로 분류하였으나 2016년 Spesis-3에서는 병의 분류를 단순화하여 진단의 오류를 줄이고자 중증 패혈증은 삭제되었다[2,4].
Sepsis-3가 도입된 배경은 다음의 몇 가지를 제시할 수 있다. 우선 Sepsis-2에서 패혈증 정의 문제는 SIRS가 감염증에 의해서 뿐만 아니라 췌장염, 수술, 화상 등에서도 기준을 만족하므로 패혈증의 병태생리를 설명하는 데 제한적이며, 패혈증을 설명하는 데 민감도와 특이도가 낮다는 것이었다. 한편, 패혈증의 장기부전을 제시하는 도구로 SIRS, SOFA, logistic organ dysfunction (LODS) 등을 비교한 연구가 있었는데[5], 3가지의 도구 중 LODS는 24시간 소변량을 모아야 하므로 계산하기가 어렵다는 단점이 있었고, SIRS와 SOFA 중에서 병원 내 중환자실 사망률을 예측하는 데 있어 SOFA가 유의하였으며, Sepsis-3에서 새롭게 제안된 quick sepsis related organ failure assessment (qSOFA)의 경우, 병원 내 비중환자실 환자의 사망률 예측도에서는 4가지 도구 중 오히려 SOFA보다 qSOFA가 높게 보고되었다. 하지만 선별 도구로서 유용한 qSOFA는 Sepsis-3 정의에 포함되지는 않았다. qSOFA의 내용은 표 1과 같으며, 2점 이상 충족 시 병원 내 사망률 및 예후가 더 나쁘다[5].
패혈증의 묶음(bundle) 치료
2001년 Rivers 등[6]이 제시한 조기 목표 지향 치료(early goal directed therapy, EGDT)는 패혈증의 사망률을 낮추는 데 많은 기여를 하였다. EGDT의 핵심은 6시간 내에 패혈성 쇼크 및 중증 패혈증에서 충분한 수액을 공급하는 데 있었다. 하지만 최근 ARISE study (호주), ProCess study (미국), ProMISe study (영국) 3가지 대규모 임상 연구를 통하여 EGDT의 실질적 효과가 입증되지는 못하였는데[7-9], 그럼에도 불구하고 세 연구 모두 무작위 배정 전에 이미 충분한 수액 공급(> 30 mL/kg)과 항생제가 조기에 투여되어 EGDT를 부정하기에는 제한점이 있는 것으로 평가되고 있다.
2002년에 처음 소개된 “surviving sepsis campaign (SSC)”은 패혈증에 대한 국제 임상 진료 지침으로 4년마다 갱신되고 있으며 2012년부터는 묶음 치료를 함께 제시하고 있다. 첫 묶음 치료로 3시간 내에 젖산의 측정, 항생제 투여 전 혈액배양, 광범위 항생제의 투여, 젖산 ≥ 4 mmol/L 혹은 저혈압에서 결정질(crystalloid) 수액의 투여 4가지를 패혈증 환자에서 시행할 것을 권고하였는데, 이후 치료 시간이 6시간에서 3시간으로 단축이 되었으며 이것은 그만큼 빠르고 적절한 치료가 패혈증 환자에서 중요하다는 것을 의미한다. 결국 가장 최근에 발표된 2018년 지침에서는 1시간 안에 묶음 치료할 것을 권고하였는데, 1시간 패혈증 묶음 치료의 내용을 요약해서 나타내면 표 2와 같다[10].
EGDT에서는 수액 치료의 목표를 중심 정맥압(central venous pressure, CVP)과 중심 정맥 산소포화도(central venous oxygen saturation, SCVO2)로 보았지만, 이러한 정적인 지표만을 목표로 환자의 소생과 수액 치료의 반응성을 보는 것은 여러 제한점이 있음이 알려졌다. 따라서, 특히 조직 저산소증의 교정을 위하여 여러 가지 역동적 도구로 실시간 모니터링하여 환자를 적절히 치료하라는 것이 새롭게 개정된 진료 지침의 또 다른 주된 내용이다. 이런 역동적 도구에는 수동적 다리 들기법(passive leg raise test), 호흡에 따른 하대정맥 크기 혹은 동맥압 변화성 등이 있는데, 이를 위해서는 실제로 다양한 새로운 기술과 의료기기의 도입이 필요하므로 현재 국내에서 널리 사용되기에는 제한적이다[11-13]. 특히 역동적 도구 중 중요한 것이 초음파를 이용한 환자의 용적 상태 평가인데[14], 수액 공급 이후에도 평균 동맥압이 65 mmHg 이하일 경우, 승압제로 노르에피네프린이 첫번째로 고려되지만[15], 결국 혈압(blood pressure, BP)은 심박출량(crdiac output, CO)과 전신혈관저항(systemic vascular resistance, SVR)의 곱(BP = CO × SVR)으로 나타낼 수 있으므로 CO와 SVR 각각을 측정할 수 있다면 수액 또는 승압제 투여를 보다 선별할 수 있는데, 이 과정에서 중환자 침상 옆에서의 초음파가 유용하다. 예를 들어 CO를 나타내는 확장기말용적(end diastolic volume)이 감소하였을 때는 결정질 수액의 공급이 적절하며, SVR이 떨어졌을 때는 노르에피네프린의 투여가 바람직할 것이다. 또한, 폐초음파를 이용하여 수액 투여 전 B-line이 없던 환자에서 충분한 수액 공급 후에도 저혈압 시 폐초음파를 재검하여 B-line이 보인다면 혈압 교정을 위하여 승압제 치료를 고려해 볼 수 있을 것이다.
Table 1.
Quick sequential organ failure assessment criteria
| 1. Altered mental status (Glasgow coma scale < 15) |
| 2. High respiratory rate (≥ 22 breaths/min) |
| 3. Low blood pressure (systolic BP ≤ 100 mmHg) |
Table 2.
2018 surviving sepsis campaign: hour-1 bundle
패혈성 쇼크 환자에서 스테로이드 치료에 대한 연구
수액 요법 및 승압제 투여에 반응하지 않는 패혈성 쇼크 환자에서 스테로이드 투여는 현재까지 2016 SSC 지침에서 약한 수준으로 충분한 수액과 승압제 치료에도 불구하여 혈역학적으로 불안정한 패혈성 쇼크 환자에서 히드로코르티손(hydrocortisone)을 하루 200 mg 정주할 것을 권고한 바 있다[15]. 이후 가장 최근 대규모로 진행된 두 가지의 무작위 배정 임상시험인 ADRENAL study와 APROCCHSS study [16,17]에서 기대하였던 것과 달리 패혈증에서의 스테로이드 치료효과가 두 연구에서 동일한 결과를 보여주지 못하였기 때문에 여전히 패혈성 쇼크에서 스테로이드 치료에 대해서 확립된 지침은 나오지 않았다. 하지만 최근 미국의학회지에서 8,000명 이상의 환자를 메타분석 하였을 때 스테로이드 치료가 패혈성 쇼크 환자에서 28일 사망률을 줄이는 것으로 보고되었기에 이 결과는 주목할 만하며[18], 추후 개정되는 합의된 진료 지침에서는 이 결과까지 반영되어 스테로이드 치료의 권고를 더 높일 수 있을 것으로 기대되고 있다.
패혈증 기타 치료제 연구
2017년 비타민 C, 히드로코르티손, 비타민 B1 (thiamine)을 중증 패혈증과 패혈성 쇼크에 투여하였을 때 병원 내 사망률과 승압제 투여 기간이 단축되었다는 연구가 처음 보고되면서[19], 부작용은 크지 않으면서 항산화효과로 알려진 비타민이 패혈증에서의 대안적 치료제로 주목받기 시작하였다. 하지만 이 연구는 후향적 연구라는 큰 한계가 있었고 이후 현재까지 매우 많은 무작위 임상시험이 진행되는 가운데 2019년 44개의 기존 연구에 대한 메타분석 연구가 발표되었는데, 현재까지는 비타민 C의 투여로 인한 병원 내 사망률과 중환자실 재원 기간의 단축은 보이지 않았다[20]. 하지만 이 연구는 패혈증 환자만을 대상으로 한 연구가 아닌 전반적인 중환자실 환자를 대상으로 하였기 때문에 패혈증에서 비타민의 유용성 여부에 대해서는 아직 연구가 더 필요하다.
한편, 패혈증 관련 응고병증(sepsis-associated coagulopathy)이 있는 환자군을 대상으로 인간 재조합 수용성 트롬보모듈린(recombinant human soluble thrombomudulin, rhsTM)의 투여가 패혈증의 생존율을 낮추는지에 대한 연구(SCARLET trial)가 진행되어[21], 최근 2019년 미국의학회지에 발표가 되었으나 28일간 사망률인 일차 결과 변수에서 rhsTM은 패혈증에서의 사망률을 유의미하게 감소시키지 못하였다. 심부정맥혈전증을 예방하기 위하여 이미 헤파린이 투여되고 있는 환자가 약 25% 정도 같이 등록되었다는 제한점 등이 있었지만 결국 다기관 연구에서 음성의 결과를 보인 결과이며 앞으로 패혈증의 치료제로 응고병증을 목표로 한 또 다른 연구들이 계속해서 진행되고 있다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






