 |
 |
| Korean J Med > Volume 91(2); 2016 > Article |
|
ėė―
ę°ėļíŽė ėė ėė ë§Īė° ë뎞ëĐ° ėžë°ė ėļ ėė ėė ëđíī ėíę° ëķëíëĪ. ė§ëĻ ëđė ëĶžíė ė ėī ë° ę° ė ėīëĨž ëë°í ęē―ė°ę° ë§ė ėīėđëĢëĄ íėííėëēė ėííë ęē―ė°ę° ë§ė§ë§ íėŽęđė§ ė ëĶ―ë íėííėëēė ė ėë ë° ėëĪ. ëí ëŽļí ëģīęģ ė ë°ëĨīëĐī ę·ļ íĻęģžę° ėė ėė ëđíī ėĒė§ ėëĪ. ëģļ ėĶëĄë ęĩëīėė HER2 ėėąė ëģīėļ ę°ėļíŽė ėė ėė ėēŦ ėĶëĄėīëĪ. ęļ°ėĄī íėííėëēė HER2 íė ėđëĢė ėļ trastuzumabė ėķę°íėŽ ėŽėĐíėęģ íėŽ ëģĩëķ ė ė°íëĻėļĩėīŽė ë° AFP ęēėŽė íļė ėęēŽė ëģīėīęģ ėëĪ.
Abstract
Gastric hepatoid adenocarcinoma is a rare adenocarcinoma that develops in the stomach. The prognosis of gastric hepatoid adenocarcinoma is poorer than that of ordinary gastric adenocarcinoma. Here, we report the first case of human epidermal growth factor receptor 2 (HER2)-positive gastric hepatoid adenocarcinoma in Korea. A 57-year-old male presented with abdominal distension and underwent endoscopic gastric biopsy and percutaneous core needle liver biopsy. The pathological findings were consistent with HER2-positive gastric hepatoid adenocarcinoma. He received six cycles of chemotherapy with cisplatin-capecitabine plus trastuzumab, which is a HER2 targeted agent. After chemotherapy, a follow-up abdominal computed tomography scan showed a partial tumor response. This case emphasizes the importance of using trastuzumab in a patient with HER2-positive gastric hepatoid adenocarcinoma.
ę°ėļíŽė ėė ė(hepatoid gastric adenocarcinoma)ė 1985ë
Ishikura ëą[1]ė ėíī ëŠ
ëŠ
ëėžëĐ° ę°ėļíŽė ëķíė ėííėëĻë°ą(Alphafetoprotein, AFP)ė ėėąíë íđė§ė ę°ė§ëĪ. íė ëĪė Ishikura ëą[1]ė AFPëĨž ėėąíė§ ėë ę°ėļíŽė ėė ėė ëģīęģ íėėžëĐ° íėŽ ė§ëĻė íėĪ AFP ėļĄė ėđëģīëĪë ėĄ°ė§íė íđė§ė ęļ°ë°íėŽ ėīëĢĻėīė§ęģ ėëĪ[2]. ė ėēī ėėė 0.38-1%ëĨž ė°Ļė§íë ęēėžëĄ ëģīęģ ëėėžëĐ°, ė§íë ėíėė ė§ëĻëë ęē―ė°ę° ë§ęģ ęļ°í ėėė ëđíī ëķëí ėíëĨž ëģīėļëĪ. íėŽ ė§íí ę°ėļíŽė ėė ėė ëí íėííėëēė ė ëĶ―ë ë°ę° ėëĪ. ėžë°ė ėļ ėė ėė 5-fluorouracil, cisplatin ëģėĐėëēė ėĢžëĄ ėŽėĐíęģ ėėžëĐ° Kang ëą[3]ėī ëģīęģ í ë°ė ë°ëĨīëĐī capecitabineęģž cisplatin ëģėĐėëē ėė ë§ėĄąėĪëŽėī ėđëĢ íĻęģžëĨž ëģīėŽ ë§ėī ėŽėĐëęģ ėëĪ. ę°ėļíŽė ėė ė ėĪ ėļę°ėížėĶėėļėėėĐėēī2 (human epidermal growth factor receptor type 2, HER2) ėėąėžëĄ trastuzumabė íĩíī ėđëĢí ę°ėļíŽė ėė ėė ę° ė ėī 1ėëĨž ęē―ííėęļ°ė ëŽļíęģ ė°°ęģž íĻęŧ ëģīęģ íë ë°ėīëĪ.
57ėļ ëĻėę° ëīė 10ėž ė ëķí° ëģĩëķ í―ë§ę°ėī ë°ėíėŽ í ëģėėė ėíí ëģĩëķ ėīėíėė ę°ëī ėĒ
ęīīę° ęīė°°ëėī ëīėíėëĪ. íë Ĩ ė§íë íė 140/90 mmHg, ë§Ĩë° 98í/ëķ, íļíĄ 18í/ëķ, ėēīėĻ 36.4âėėžëĐ° ęģ íėėžëĄ ėīė ëí ė―뎞 ėŽėĐ ėĪėīėęģ ėīėļė ęļ°í ęģžęą°ë Ĩ ë° ė―뎞 ëģĩėĐë Ĩė ėėëĪ. ė ėēī ęēė§ėė ė ė ėíë ęąīę°íī ëģīėęģ ėėė ëŠ
ëĢíėëĪ. ëęē―ëķ, íëķ ė§ė°°ėė íđėī ėęēŽė ėėėžëĐ° ëģĩëķ ė§ė°°ė ëģĩëķ í―ë§ėī íėļëėëĪ. ë§ėī íėĄ ęēėŽėė ë°ąíęĩŽ 7,600/mm3, íėė 9.5 g/dL, íėí 581,000/mm3ėęģ , íėē ėíí ęēėŽėė ėī ëĻë°ą 6.4g/dL, ėëķëŊž 2.5 g/dL, ėī ëđëĶŽëĢĻëđ 3.4 mg/dL, ė§ė ëđëĶŽëĢĻëđ 3.2 mg/dL, AST 210 IU/L, ALT 164 IU/L, ALP 1,017 IU/L, gamma glutamyl transpeptidase 714 IU/LėëĪ. ėĒ
ė íė§ė ęēėŽėėë AFP 7,330 ng/mL, proteins induced by vitamin K absence or antagonist-II test (PIVKA-II) 147 mAu/mL, carcinoembryonic antigen (CEA) 3,869 ng/mL, carbohydrate antigen 19-9 (CA 19-9) 128 U/mLėëĪ. Bí ę°ėž íëĐīíėė ėėąėīėęģ íëĐīíėēī ėėąėīėėžëĐ° Cí ę°ėž íėēī ė ëģ ęēėŽ ėėąėīėëĪ. ëģĩëķ ė ė°íëĻėļĩėīŽėėė ę° ëŽļë§Ĩė ėĒ
ė íė ė ëë°í ęą°ë ëĪęē°ė ėą ėĒ
ęīīę° ęīė°°ëėęģ ëë ·í ëë§Ĩęļ° ėĄ°ė ėĶę° íđė ëŽļë§Ĩęļ° ėĄ°ė ę°ėëĨž ëģīėīė§ë ėėëĪ. ėíëķ ėēīëē―ė ëķę·ėđí ëđíëĨž ëģīėėžëĐ° ėĢžëģëķ ëĶžíė ėĒ
ëę° ęīė°°ëėëĪ. ė ė ėė ėëĻėļĩėīŽėėė ę°ëī ę·ļëĶŽęģ ėė ė ëķė ëėŽę° ėĶę°ë ëģëģėī íėļëėī ė
ėą ėĒ
ėėī ėėŽëėęģ ė ėĢžëģ ëĪėė ė ėīėą ëĶžíė ėī ęīė°°ëėëĪ. ėëėëīėęē―ėėë ėė ė ëķ 3 cm íŽęļ°ė ęķĪėėą ėĒ
ęīīę° íėļëėī ėĄ°ė§ęēėŽëĨž ėííėęģ (Fig. 1), ę°ëī ėĒ
ęīīė ëíėŽ ėĪėŽë°ëėęēė ėííėëĪ. ę°ėĒ
ęīīė ėĪėŽë°ëėęē ėĄ°ė§ė íëŊļęē― ėęēŽė, ė ëķíė ė
ėą ė ėëŽžëĄ ę°ėļíŽė ëķíė ė ëķíę° íĻęŧ ęīė°°ëėėžëĐ°(Fig. 2), ė ëīėęē― ėęēėĄ°ė§ėėë ė ëķíė ę°ėļíŽė ėėĒ
ėī ęīė°°ëėëĪ(Fig. 3). ę° ėęēėĄ°ė§ė ę°ėļíŽė ëķíëĨž ëģīėīë ëķëķęģž ė ėęēėĄ°ė§ė ė ëķí ėėĒ
ė AFP ëĐīėėĄ°ė§ííėžėėė ėėą ėęēŽė ëģīėëĪ. ę°ėļíŽė ėė ėė ę° ė ėīëĄ ėĩėĒ
ė§ëĻëėëĪ. ėëīėęē― ėęēėĄ°ė§ ë° ę° ėęēėĄ°ė§ėė ėķę°ëĄ ėíí HER2 ëĐīėėĄ°ė§íí ėžėėė ę°ėėąėī íėļëėëĪ. ę° ė ėīëĨž ëë°í íėëĄ cisplatin, capecitabineė trastuzumabė ėķę°íėŽ íėííėëēė 3ėĢž ę°ęēĐėžëĄ ėííėęģ 2ëŽ ę°ęēĐėžëĄ ëģĩëķ ė ė°íëĻėļĩėīŽėė ėķė ęīė°°íėëĪ. íėíí ėđëĢëĨž ėííë ëė 10ėĢžęļ° ėīí 2ëĻęģė ë§ėīė ęē―ëģėĶėī ë°ėíėŽ cisplatinė ėĪëĻíėėžëĐ° capecitabine ë° trastuzumabė ę°ë ëë ėĪëĻ ėėī ė ė§íėëĪ. ėđëĢ ę°ė ė í ęēėīíļėŽėĨíėĄíėĪėšė ėííėęģ ėŽėĨë
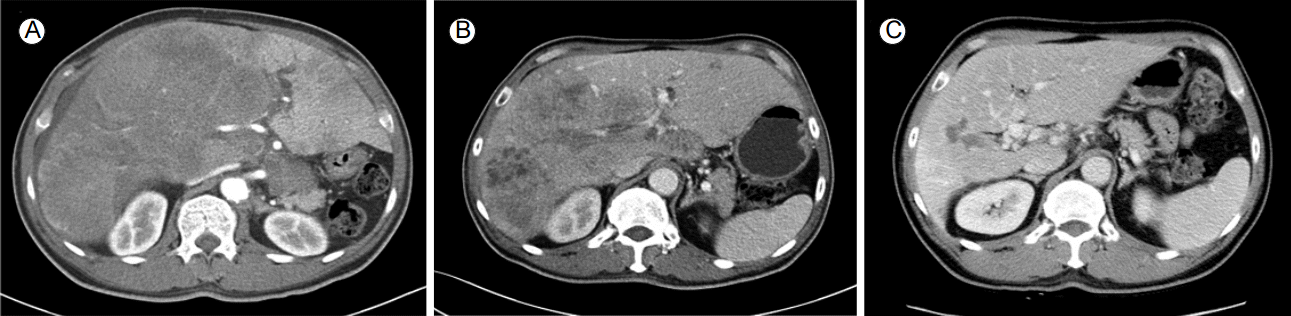
ėąė íėļëė§ ėėëĪ. ėī 16ėĢžęļ°ė íėíí ėđëĢëĨž ėííėėžëĐ° ę°ëī ė ėīėą ėĒ
ėė íŽęļ°ę° ëė ëęē ę°ėíėęģ 1ë
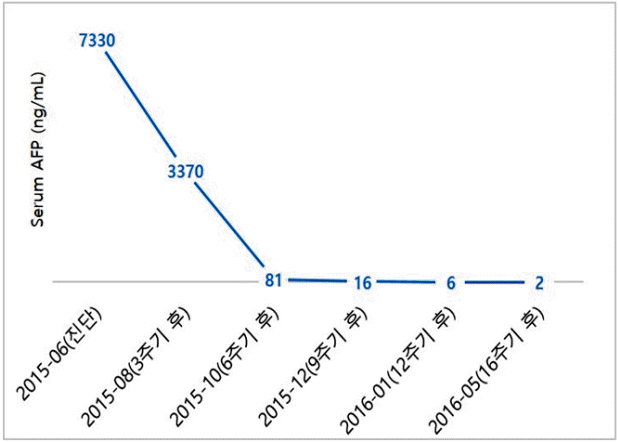
ėīė ëŽīė§í ėėĄīė ė ė§íęģ ėëĪ(Fig. 4). ëí ėīęļ° 7,330 ng/mLėīë AFP ėė 2 ng/mLęđė§ ę°ėíėëĪ(Fig. 5).
ę°ėļíŽė ėė ėė íę· ë°ëģ ė°ë đė 63.5ėļėīëĐ° ėŽėąė ëđíī ëĻėąėė íļë°íë ęēėžëĄ ëģīęģ ëėëĪ(2.32:1) [4]. ėėė íļë°íëĐ°(83.9%) ëīë(3.7%), ėęķ(3.2%), í(2.3%) ę·ļëĶŽęģ ë뎞ė§ë§ ėë ë° ëģĩë§ėėë ë°ėíëĪ. ėžë°ė ėļ ėė ėė ëđíī ëķëí ėíëĨž ëģīėīëë° Liu ëą[5]ė 1ë
, 3ë
, 5ë
ėėĄīėĻė ę°ę° 53%, 35%, 28%ëĄ ëģīęģ íėëĪ. ėīë AFPëĨž ëķëđíė§ ėë ęļ°í ėėė 95%, 57%, 38%ęģž ëđęĩíėŽ ëķëíëĪ. ę°ėļíŽė ėė ėė ėíę° ëķëí ėīė ė ëíī ëŠ ę°ė§ ę°ėĪėī ė ėëėëĪ. Inagawa ëą[6]ė ę°ėļíŽė ėė ėėī AFPė ëëķėī ėí-1 ííļëĶ―ė ë° ėí-1 ííĪëŠĻíļëĶ―ė ė ëķëđíë ęēė ëģīęģ íėëĪ. ėī 뎞ė§ėī ëĐīė ėĩė ėėĐė íëĐ° ëĻë°ąëķíīíĻė ėĩė ëĨž íĩíī ėĢžė ėĄ°ė§ėžëĄė ėđĻíŽėąėī ëėė§ęģ ėīė ë°ëž ė ë§Ĩ ėđĻëēėī ë§ėžëĐ° ëí ę° ė ėīę° íí ęēėžëĄ ėę°ëëĪ. ëģļ ėĶëĄėėë ę°ëŽļë§Ĩė ėĒ
ė íė ė ëë°íęģ ėėëĪ. ëí ėđëĢė ė ė ė ėī ëķę°ëĨí ęē―ė° ëėą ëķëíë° ėī ęē―ė° ėžë°ė ėļ ėė ėė ėėĄī ėĪėę°ėļ 9.3-10.5ę°ėėļ ęēė ëđíī[3] ę°ėļíŽė ėė ėė ėėĄī ėĪėę°ė 2.7-8.0ę°ėė ëķęģžíëĪ[4,7]. ėė ėī ëķę°ëĨí ęē―ė° íė ėđëĢę° ėĢžë ėđëĢė§ë§ ėė§ęđė§ ë§ėĄąí ë§í ėđëĢ íĻęģžëĨž ëģīėļ ėę° ėėī ėžë°ė ėļ ėė ėė íėííėëēė ęļ°ë°íėŽ ėđëĢíęģ ėëĪ. 5-fluorouracil, cisplatin ëģėĐėëēęģž capecitabine, cisplatin ëģėĐėëēė ėĢžëĄ ėŽėĐíëĐ° ėīėļėë S-1 ëĻë
ëë paclitaxel, cisplatin ëģėĐėëē íėííėëēė ėííëĪ[4]. íė§ë§ íėŽ íĻęģžė ėļ íėííėëēėī ė ëĶŽëė§ ėė ėđëĢíëë° ėīë Īėė ęēŠęģ ėëĪ. ęĩëīėėë ėė í 1ë
ë§ė ėŽë°í ėĶëĄę° ėėęģ [8], Baek ëą[7]ė ėíëĐī íėííėëēė ëķëķë°ė ėīėė ëģīėļ ęē―ė°ę° 8.3%ė ëķęģžíë° ęĩëī ėžë°ė ėļ ėė ėė ëķëķë°ėëĨ 32-46%ė ëđíī ë§Īė° ëķëíëĪ[3]. ėļęĩ ëģīęģ ėėë ë§ė°Žę°ė§ëĄ ëķëí ėíëĨž íėļí ė ėëĪ. Lin ëą[4]ėī ëģīęģ í ë°ė ë°ëĨīëĐī 87.1%ė íėę° ė§ëĻ ëđė ëĶžíė ė ėīë ėęēĐė ėīëĨž ëë°íęģ ėėėžëĐ°, 5-fluorouracil ęļ°ë°ė íėííėëēė ėííė§ë§ ėĪė ėėĄī ęļ°ę°ė 7.2ė ëķęģžíëĪ. Su ëą[9]ėī ėíí ëĐíëķėėėë ėėĄī ėëĢę° íėļë íė 125ëŠ
ėĪ 51.2%ė íėę° ė§ëĻ 12ę°ė ëīė ėŽë§íėëĪ. íėŽęđė§ ë°íë ëģīęģ ėë HER2 ėėąė ëģīėļ ėĶëĄę° ėėžëĐ° trastuzumabė ėŽėĐí ė ėė ėëĪ. ëģļ ėĶëĄë ę°ėļíŽė ėė ėėė HER2 ėėąė ëģīėļ ėēŦ ėĶëĄėīëĪ. Bang ëą[10]ė ė§íí ėžë°ė ėļ ėė ėėė HER2 ėėąėž ęē―ė° ęļ°ėĄī íėííėëēė trastuzumabė ėķę°íë ęēėī ėĒ ë ė°ėí ėđëĢ íĻęģžëĨž ëíëīë ęēėžëĄ ëģīęģ íėëĪ. ėīė ëģļ ėĶëĄėėë trastuzumabė ėŽėĐíėęģ ëŽīė§í ėėĄīė 1ë
ėīė ė ė§íęģ ėëĪ. ę°ėļíŽė ėė ė íė ėĪ 8.3%ë§ėī íėíí ėđëĢė ë°ėíėęģ ėėĄī ėĪėę°ėī 8ę°ė ëŊļë§, 1ė°Ļ íėíí ėđëĢė ëŽīė§í ėėĄīę°ėī 5ę°ė ëŊļë§ėė ęģ ë ĪíëĐī ë§ėĄąí ë§í ėđëĢ ęē―ęģžëĄ íëĻí ė ėëĪ. ėžë°ė ėžëĄ ę°ėļíŽė ėė ėė ėđëĢ ėąė ėī ėĒė§ ėė§ë§ ëģļ ėĶëĄėėė ę°ėī HER2 ëĐīė íí ęēėŽëĨž ėííęģ íė ėđëĢė ėļ trastuzumabė ėŽėĐíĻėžëĄėĻ ėĒ ë ėĒė ėđëĢ ėąė ė ęļ°ëíī ëģž ė ėëĪ.
REFERENCES
1. Ishikura H, Fukasawa Y, Ogasawara K, Natori T, Tsukada Y, Aizawa M. An AFP-producing gastric carcinoma with features of hepatic differentiation. A case report. Cancer 1985;56:840â848.


2. Ye MF, Tao F, Liu F, Sun AJ. Hepatoid adenocarcinoma of the stomach: a report of three cases. World J Gastroenterol 2013;19:4437â4442.



3. Kang YK, Kang WK, Shin DB, et al. Capecitabine/cisplatin versus 5-fluorouracil/cisplatin as first-line therapy in patients with advanced gastric cancer: a randomised phase III noninferiority trial. Ann Oncol 2009;20:666â673.


4. Lin CY, Yeh HC, Hsu CM, Lin WR, Chiu CT. Clinicopathologial features of gastric hepatoid adenocarcinoma. Biomed J 2015;38:65â69.


5. Liu X, Cheng Y, Sheng W, et al. Clinicopathologic features and prognostic factors in alpha-fetoprotein-producing gastric cancers: analysis of 104 cases. J Surg Oncol 2010;102:249â255.


6. Inagawa S, Shimazaki J, Hori M, et al. Hepatoid adenocarcinoma of the stomach. Gastric Cancer 2001;4:43â52.


7. Baek SK, Han SW, Oh DY, Im SA, Kim TY, Bang YJ. Clinicopathologic characteristics and treatment outcomes of hepatoid adenocarcinoma of the stomach, a rare but unique subtype of gastric cancer. BMC Gastroenterol 2011;11:56.



8. Moon JY, Kim GH, Cheong JH, Lee BE, Ryu DY, Song GA. A case of hepatic metastasis of gastric hepatoid adenocarcinoma mistaken for primary hepatocellular carcinoma. Korean J Gastroenterol 2012;60:262â266.


Esophagogastroduodenoscopy reveals a 3-cm ulcerative mass lesion at the distal antrum lesser curvature-anterior wall.
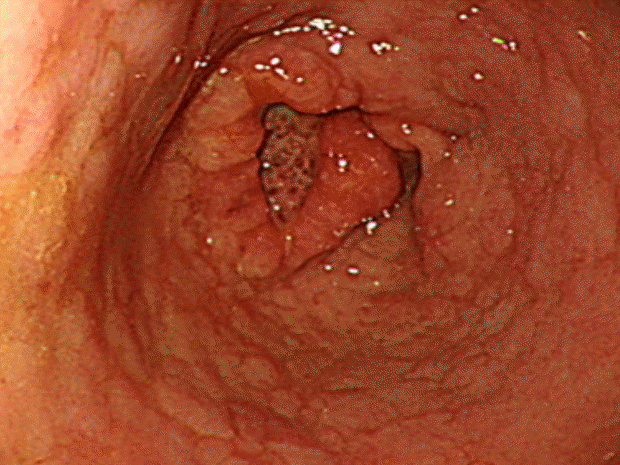
Figure 1.
Histological findings of the liver biopsy. (A) Core needle biopsy specimen is composed of solid sheet and glandular patterns of polygonal cells with eosinophilic and occasional clear cytoplasm. (Hematoxylin and eosin stain, Ã200). The tumor cells were positive for (B) alpha fetoprotein (AFP) (AFP immunohistochemical stain original magnification, Ã200) and (C) human epidermal growth factor receptor 2 (HER2) (HER2 immunohistochemical stain, Ã200).
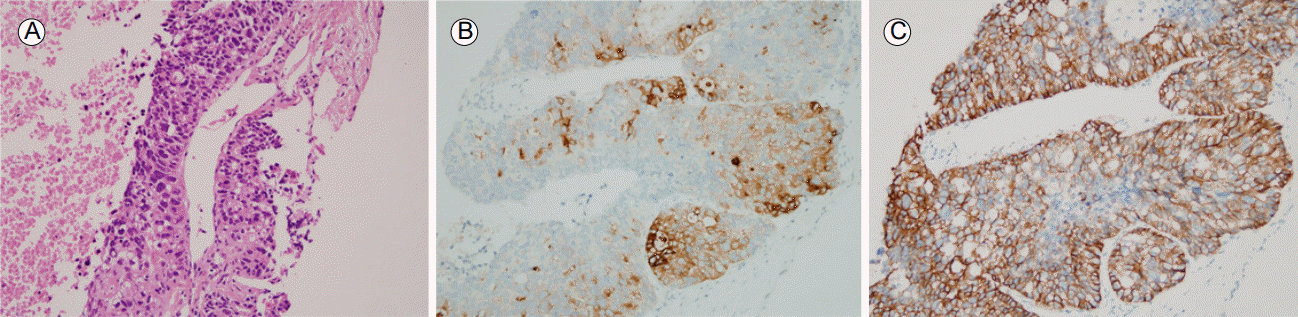
Figure 2.
Histological findings of the stomach biopsy. (A) Tumor cells consist of a solid sheet of large polygonal cells with eosinophilic cytoplasm resembling hepatocellular carcinoma. (Hematoxylin and eosin stain, Ã200). (B) The tumor cells were positive for alpha fetoprotein (AFP) (AFP immunohistochemical stain original magnification, Ã200) and (C) human epidermal growth factor receptor 2 (HER2) (HER2 immunohistochemical stain, Ã200).
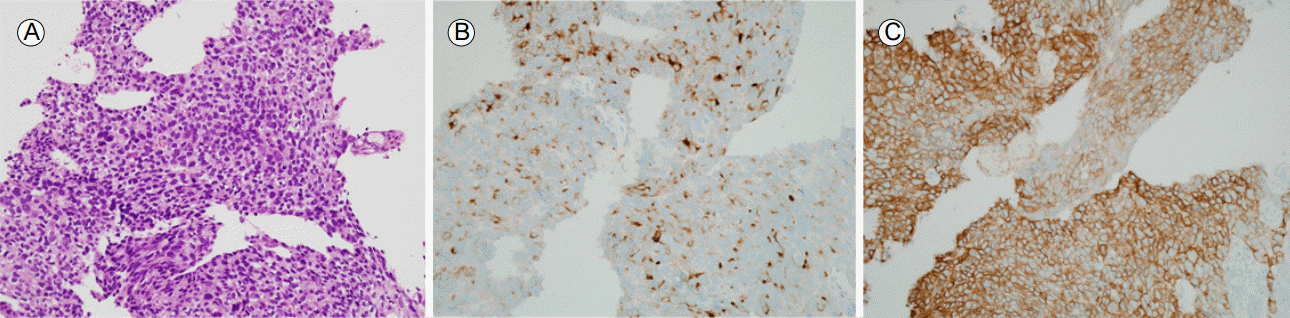
Figure 3.
-
METRICS

-
- 1 Crossref
- 0 Scopus
- 7,597 View
- 158 Download



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



