žĄú Ž°†
Ūėąž≤≠žöĒžāįŽÜ掏ĄÍįÄ 6.8 mg/dL žĚīžÉĀžĚľ ŽēĆ Í≥†žöĒžāįŪėąž¶ĚžĚīŽĚľ ŪēėÍ≥† žĄłŪŹ¨žôłžē°žóź žöĒžāįžóľžĚī Í≥ľŪŹ¨ŪôĒžÉĀŪÉúÍįÄ ŽźėŽ©ī ž°įžßĀžóź monosodium urate Í≤įž†ē ŪėēŪÉúŽ°ú žĻ®žį©ŽźėžĖī ŪÜĶŪíćÍ≥ľ ÍįôžĚÄ žßąŪôėžĚī ŽįúžÉĚŪēėÍ≤Ć ŽźúŽč§[1,2]. ž†ēžÉĀ žč†žě•ÍłįŽä•žĚĄ ÍįĞߥ ŪÜĶŪíćŪôėžěźžóźžĄú Í≥†žöĒžāįŪėąž¶ĚžúľŽ°ú žöĒžāįž†ÄŪēėž†úŽ•ľ žā¨žö©Ūē† ŽēĆ žĚľŽįėž†ĀžúľŽ°ú žĻėŽ£ĆžĚė Ž™©ŪĎúŽäĒ Ūėąž≤≠žöĒžāįžĻėŽ•ľ 6.0 mg/dL ŽĮłŽßĆžúľŽ°ú žú†žßÄŪēėŽŹĄŽ°Ě ŪēúŽč§[1,3]. žě•ÍłįÍįĄ žöĒžāįžĚė Ž∂Äž†Āž†ąŪēú ž°įž†ąŽ°ú žĚłŪēī žīąŽěėŽźú ŽßĆžĄĪ Í≤įž†ēžĄĪ ŪÜĶŪíć ŽįŹ žöĒžāįÍ≤įžĄĚÍ≥ľ ÍįôžĚÄ ŪÜĶŪíćžĚė Ūē©Ž≥Ďž¶Ě ŽįúžÉĚ žčúžóźŽäĒ žöĒžāįž†ÄŪēėžĻėŽ£ĆÍįÄ ŪēĄžöĒŪēėŽč§. AllopurinolžĚÄ žöĒžāįÍįēŪēėž†úŽ°ú ÍįÄžě• ŽßéžĚī žā¨žö©ŽźėžĖī žė® žēĹž†úŽ°ú žč†žě• ÍłįŽä•žóź ŽĒįŽĚľ žö©ŽüČ ž°įž†ąžĚĄ ŪēĄžöĒŽ°ú ŪēúŽč§[4]. febuxostatžĚÄ ŽĻĄŪﮎ¶įÍ≥Ą žĄ†ŪÉĚž†Ā xanthine oxidase (XO) žĖĶž†úž†úŽ°úžĄú Ūﮎ¶į ŽįŹ ŪĒľŽ¶¨ŽĮłŽĒė ŽĆÄžā¨Í≥ľž†ēžóź ÍīÄžó¨ŪēėŽäĒ Žč§Ž•ł Ūö®žÜĆŽď§žóź žĶúžÜĆŪēúžĚė žėĀŪĖ•ŽßĆ ŽĮłžĻúŽč§[5]. Febuxostatžóź ÍīÄŪēú žóįÍĶ¨ÍįÄ žĚīŽ£®žĖīžßÄÍ≥† ÍīĞ訞Ěī ž¶ĚÍįÄŪēėÍ≥† žěąŽäĒ žÉĀŪô©žóźžĄú, žĶúÍ∑ľ ž†ÄžěźŽď§žĚÄ ŽßźÍłįžč†Ž∂Äž†ĄžúľŽ°ú Ž≥ĶŽßČŪą¨žĄĚžĚĄ ŪēėŽäĒ ŪôėžěźžóźžĄú žě¨ŽįúŪēėŽäĒ Í≤įž†ąžĄĪ ŪÜĶŪíć žĻėŽ£Ćžóź febuxostatžĚĄ žĚīžö©Ūēėžó¨ Ūėąž≤≠žöĒžāįŽÜ掏ĄŽ•ľ 6.0 mg/dL ŽĮłŽßĆžúľŽ°ú žú†žßÄŪē† žąė žěąžóąŽćė 1žėąŽ•ľ Í≤ĹŪóėŪēėžėÄÍłįžóź Ž¨łŪóĆÍ≥†žįįÍ≥ľ Ūē®ÍĽė Ž≥īÍ≥†ŪēėŽäĒ ŽįĒžĚīŽč§.
ž¶Ě Ž°Ä
Ūôė žěź: 29žĄł Žā®žěź
ž£ľ žÜĆ: Í≤įž†ēžĄĪ ŪÜĶŪíćžúľŽ°ú žĚłŪēú žĖϞܟ(Rt. wrist & thumb, Lt. 4th finger)žĚė Í∑Ļžč¨Ūēú ŪÜĶž¶Ě ŽįŹ ÍīÄž†ąžöīŽŹôžě•žē†
Í≥ľÍĪįŽ†•: ŽßźÍłįžč†Ž∂Äž†Ą, Í≥†Ūėąžēē, Í≤įž†ąžĄĪ ŪÜĶŪíć
ÍįÄž°ĪŽ†•: ŪäĻžĚīžā¨Ūē≠ žóÜžĚĆ.
žßĄžįį žÜĆÍ≤¨: Žāīžõź ŽčĻžčú Ž≥ĶŽßČŪą¨žĄĚ 4ŽÖĄžį®Ž°ú ŽßĆžĄĪ Ž≥ĎžÉȞ̥ Ž≥īžĚīÍ≥† žěąžóąÍ≥† ŪôúŽ†• žßēŪõĄŽäĒ Ūėąžēē 150/90 mmHg, ŪėłŪĚ° 18ŪöĆ/Ž∂Ą, Žß•Žįē 80ŪöĆ/Ž∂Ą, ž≤īžė® 36.5‚ĄÉ ŽįŹ žĚėžčĚžĚÄ Ž™ÖŽ£ĆŪēėžėÄŽč§. žĖĎ ŪŹźžēľžóźžĄú žąėŪŹ¨žĚĆžĚīŽāė ž≤úŽ™ÖžĚĆžĚÄ Žď§Ž¶¨žßÄ žēäžēėÍ≥† žč¨žě°žĚĆžĚÄ žóÜžóąžúľŽ©į Ž≥ĶŽ∂ÄŽäĒ ŪĆĹžįĹžÜĆÍ≤¨ ŽįŹ žēēŪÜĶžĚīŽāė ŽįėŽįúŪÜĶžĚÄ ÍīÄžįįŽźėžßÄ žēäžēėŽč§. žöįžł° žÜź žóĄžßÄžôÄ žÜźŽ™©Ž∂ÄžúĄ ŽįŹ žĘĆžł° žÜź 4Ž≤ąžßł žÜźÍįÄŽĚĹ ŽßąŽĒĒÍįÄ tophiŽ°ú žĚłŪēī Ž∂ďÍ≥† Žįúž†ĀžĚī žěąžúľŽ©į žēēŪÜĶžĚī ŪôēžĚłŽźėžóąŽč§.
Í≤Äžā¨žč§ žÜĆÍ≤¨: Žāīžõź ŽčĻžčú žčúŪĖČŪēú ŽßźžīąŪėąžē° Í≤Äžā¨žóźžĄú ŽįĪŪėąÍĶ¨ 4,400/mm3, ŪėąžÉČžÜĆ 8.6 g/dL, ž†ĀŪėąÍĶ¨ žö©ž†ĀŽĻĄ 26.0%, ŪėąžÜĆŪĆź 115,000/mm3žĚīžóąŽč§. Ūėąž≤≠ žÉĚŪôĒŪēô Í≤Äžā¨žóźžĄú BUN 96.4 mg/dL, ŪĀ¨Ž†ąžēĄŪčįŽčĆ 18.5 mg/dL, ŽāėŪ䳎•® 140 mM/L, žĻľŽ•® 5.1 mM/L, žīĚ Žč®ŽįĪ 5.1 g/dL, žēĆŽ∂ÄŽĮľ 3.4 g/dL, AST 17 IU/L, ALT 13 IU/L, ALP 128 U/L, Uric acid 9.8 mg/dLžĚīžóąŽč§.
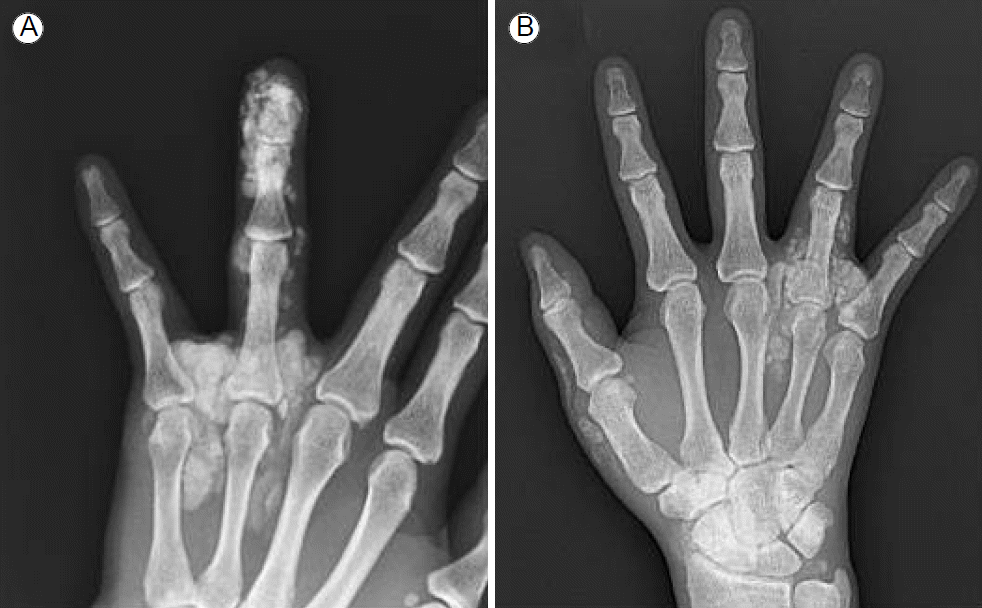
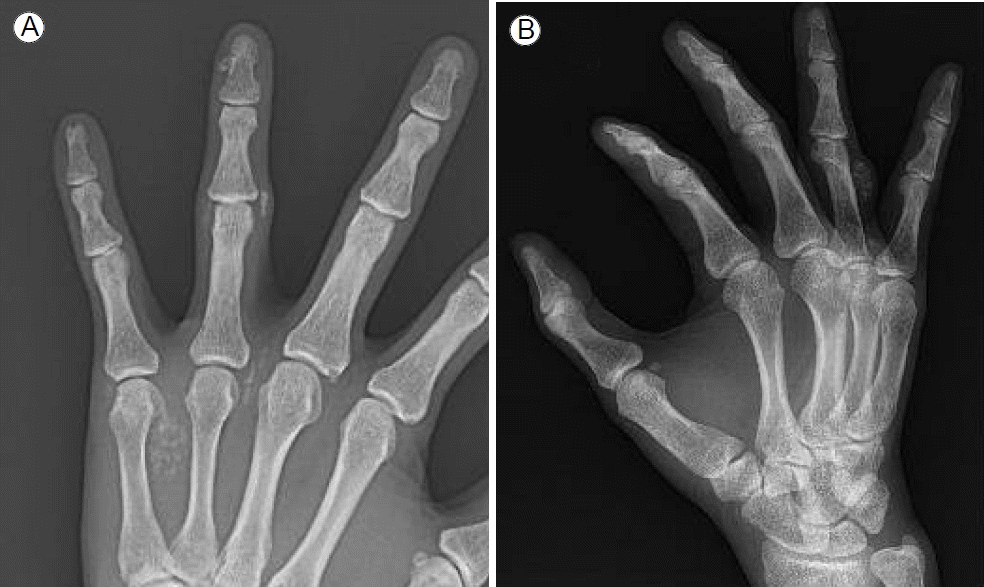
žěĄžÉĀ Í≤ĹÍ≥ľ ŽįŹ žĻėŽ£Ć: žôłŽěėžóźžĄú Í≥†žöĒžāįŪėąž¶Ě(uric acid 7.6-9.2 mg/dL)žúľŽ°ú žēĄžĻ®žóź Ūēú Ž≤ą allopurinol 50 mgžĚĄ 2ŽÖĄ ž†ēŽŹĄ žßÄžÜ枆ĀžúľŽ°ú Ž≥Ķžö©Ūēī žė§Žćė ž§ĎžĚīžóąžĚƞ󟎏Ą Ž∂ąÍĶ¨ŪēėÍ≥† Žāīžõź žčú both hands x-rayžÉĀ žóįž°įžßĀŽ∂Ä tophi ŪôēžĚłŽźėžĖī Žč§žĚĆ Žā† excisional biopsy žąėžą†žĚī žßĄŪĖČŽźėžóąŽč§(Fig. 1). žą† ŪõĄ ž¶ĚŽüČŽźú allopurinol 100 mgžĚĄ ŪēėŽ£® Ūēú Ž≤ą Ž≥Ķžö©ŪēėžėÄžúľŽāė 3ÍįúžõĒ Ží§ Žč§žčú Í≤įž†ēžĄĪ ŪÜĶŪíćžĚī žě¨ŽįúŪēėžó¨ 2žį® ž†úÍĪį žąėžą†žĚĄ ŪēėÍ≥†, žąėžą† ŪõĄ 1žĚľžį®Ž∂ÄŪĄį febuxostat 40 mg Í≤ĹÍĶ¨ 1ŪöĆ žöĒŽ≤ēžĚĄ žčúžěĎŪēėžėÄŽč§. Ž≥Ķžö© žčúžěĎ ŪõĄ 3ÍįúžõĒ Ží§ Ūėąž≤≠žÉĚŪôĒŪēô Í≤Äžā¨Í≤įÍ≥ľ BUN 62.8 mg/dL, ŪĀ¨Ž†ąžēĄŪčįŽčĆ 15.9 mg/dL, ŽāėŪ䳎•® 134 mM/L, žĻľŽ•® 4.8 mM/L, žīĚ Žč®ŽįĪ 5.6 g/dL, žēĆŽ∂ÄŽĮľ 3.8 g/dL, AST 17 IU/L, ALT 11 IU/L, ALP 178 U/L, Ūėąž≤≠žöĒžāį ŽÜ掏ĄÍįÄ 5.9 mg/dLÍĻĆžßÄ ÍįźžÜĆŪēėžėÄÍ≥† žßÄžÜ枆ĀžúľŽ°ú febuxostat 40 mg ŪēėŽ£® Ūēú Ž≤ą Ž≥Ķžö©žĚĄ žú†žßÄŪēī 20ÍįúžõĒžĚī žßÄŽāú ŪėĄžě¨ÍĻĆžßÄ žě¨ŽįúžĚĄ Ž≥īžĚīžßÄ žēäžēėŽč§(Fig. 2).
Í≥† žįį
ŽßĆžĄĪ Í≤įž†ēžĄĪ ŪÜĶŪíćžĚÄ žě•ÍłįÍįĄžĚė Í≥†žöĒžāįŪėąž¶ĚžúľŽ°ú žĚłŪēėžó¨ žöĒžāįÍ≤įž†ēžĚī ÍīÄž†ą, žóįž°įžßĀ, žĚłŽĆÄ, ŽľąŽŹĆÍłį ŽďĪžóź žĻ®žį©Žźú žÉĀŪÉúŽ°ú ž†ĀÍ∑Ļž†ĀžĚł žēĹŽ¨ľ žĻėŽ£ĆÍįÄ žöįžĄ†žčú ŽźúŽč§. žēĹŽ¨ľ žĻėŽ£ĆžóźŽŹĄ Ž∂ąÍĶ¨ŪēėÍ≥† ÍłįŽä•žě•žē†ÍįÄ žßÄžÜ掟ėÍĪįŽāė ÍįźžóľžõźžĚī Žź† Í≤Ĺžöį ŽėźŽäĒ žč†Í≤Ĺ ŽďĪ ž£ľŽ≥Ä ÍĶ¨ž°įŽ•ľ žēēŽįēŪē† Í≤Ĺžöįžóź žąėžą†ž†Ā žĻėŽ£ĆŽ•ľ Í≥†Ž†§ŪēėÍ≤Ć ŽźúŽč§. ŪÜĶž¶ĚžĚė ÍįźžÜĆ, ŽĮłžö©žÉĀžĚė Ž™©ž†ĀžĚĄ žúĄŪēī ž†úŪēúž†ĀžúľŽ°ú žąėžą†žĚĄ ŪēėÍłįŽŹĄ ŪēėŽ©į ž£ľŽ≥Ä ž°įžßĀžúľŽ°úŽ∂ÄŪĄį tophiŽ•ľ žôĄŽ≤ĹŪēėÍ≤Ć ž†úÍĪįŪēėÍłįŽäĒ žĖīŽ†§žöįŽĮÄŽ°ú žě•Íłįž†ĀžúľŽ°ú žöĒžāįŽÜ掏ĄŽ•ľ ž†ēžÉĀžúľŽ°ú žú†žßÄŪēėŽäĒ Í≤ÉžĚī ŽćĒ ž§ĎžöĒŪēėŽč§[6]. AllopurinolÍ≥ľ febuxostatžĚė žēąž†ēžĄĪÍ≥ľ žú†Ūö®žĄĪžĚĄ ŽĻĄÍĶźŪēú žóįÍĶ¨ÍįÄ ŽßéžĚÄŽćį Í∑ł ž§Ď Ž¨īžěĎžúĄ Žįįž†ē žĚīž§Ď ŽßĻÍ≤Ä 3žÉĀ CONFIRMS trial [1]žóźžĄúŽäĒ 6ÍįúžõĒÍįĄ 2,269Ž™ÖžĚė ŪôėžěźŽ•ľ ŽĆÄžÉĀžúľŽ°ú žčúŪóėŪēú Í≤įÍ≥ľ, alliopurinol 200/300 mg Ž≥Ķžö©ÍĶį ŽįŹ febuxostat 40 mg Ž≥Ķžö©ÍĶįŽ≥īŽč§ febuxostat 80 mg Ž≥Ķžö©ÍĶįžĚī primary end pointžĚł Ūėąž≤≠žöĒžāįŽÜ掏Ą 6.0 mg/dL ŽĮłŽßƞ̥ ŽćĒ ŽßéžĚī Žč¨žĄĪŪēėžėÄŽč§. ŽćĒžöĪžĚī Í≤ĹŽŹĄžóźžĄú ž§ĎŽďĪŽŹĄžĚė žč†ÍłįŽä• Ž∂Äž†ĄžĚł ŪôėžěźŽď§žóźžĄúŽŹĄ febuxostat 40 mgžúľŽ°ú allopurinolŽ≥īŽč§ ŽćĒ Ūö®Í≥ľž†ĀžúľŽ°ú žöĒžāįŽÜ掏ĄŽ•ľ Žāģž∂ú žąė žěąžóąŽč§.
AllopurinolžĚÄ Ūﮎ¶įÍ≥Ą XO žĖĶž†úž†úŽ°ú žöĒžāįÍįēŪēėž†úŽ°úžĄú ÍįÄžě• ŽßéžĚī žā¨žö©ŽźėžĖī žė® žēĹž†úžĚīŽč§. žö©ŽüČžĚÄ ž≤ėžĚĆ 100 mg (ŪŹČÍ∑† 300 mg/day)žúľŽ°ú žčúžěĎŪēėžó¨ ŪēĄžöĒžóź ŽĒįŽĚľ 800 mgÍĻĆžßÄ ž¶ĚŽüČŪē† žąė žěąŽč§. Žč®, ŪôúžĄĪŽĆÄžā¨žāįŽ¨ľžĚł oxipurinolžĚī žč†žě•žúľŽ°ú ŽįįžĄ§ŽźėŽĮÄŽ°ú žč†žě• ÍłįŽä•žóź ŽĒįŽĚľ žö©ŽüČ ž°įž†ąžĚĄ Ūēīžēľ ŪēúŽč§[4,5]. ŽďúŽ¨ľžßÄŽßĆ Ž∂ÄžěĎžö©žúľŽ°ú ŪĒľŽ∂ÄŽįúžßĄžĚī žěąžóąŽćė ŪôėžěźÍįÄ Žč§žčú allopurinolžóź ŽÖłž∂úŽźėŽ©ī Í≥ľŽĮľŽįėžĚĎ(hypersensitivity syndrome)žĚĄ žĚľžúľŪā¨ žąė žěąŽäĒŽćį Stevens-Johnson syndrome ŽėźŽäĒ ŽŹÖžĄĪŪĎúŪĒľÍīīžā¨žö©Ūēī(toxic epidermal necrolysis) ŽďĪ žÉĚŽ™ÖžĚĄ žúĄŪėĎŪēėŽäĒ žĻėŽ™Öž†ĀžĚł Í≤ĹžöįŽŹĄ ŽįúžÉĚŪē† žąė žěąŽč§[6]. FebuxostatžĚÄ allopurinolÍ≥ľ Žč¨Ž¶¨ ž£ľŽ°ú ÍįĄžóźžĄú ŽĆÄžā¨ŽźėžĖī ͳĎ£®ŪĀ¨Ž°úŽāėžĚīŽďú(glucuronide)Ž•ľ ŪėēžĄĪŪēėŽĮÄŽ°ú žč†ÍłįŽä• ž†ÄŪēė žčúžóźŽŹĄ žě•ÍįĄ Žāī žąúŪôėžĚĄ ŪÜĶŪēī ŽĆÄŽ≥ÄžúľŽ°ú ŽįįžĄ§ŪēėŽäĒ žĖĎžĚī ž¶ĚÍįÄŪēī žč†Ž∂Äž†Ą ŪôėžěźŽāė ŽÖłžĚłžóźžĄú žö©ŽüČ ž°įž†ąžĚė žĖīŽ†§žõÄžĚī žóÜŽč§. ŽėźŪēú xanthinežóźžĄú žöĒžāįžúľŽ°ú ž†ĄŪôėžĚĄ Žß§ÍįúŪēėŽäĒ XO Ūö®žÜĆŽäĒ žāįŪôĒŪėēÍ≥ľ ŪôėžõźŪėēžĚī žěąŽäĒŽćį, allopurinolžĚÄ žāįŪôĒŪėēŽßĆ žĖĶž†úŪēėŽäĒ ŽįėŽ©ī febuxostatžĚÄ Ž™®ŽĎź žĖĶž†úŪē† žąė žěąžĖī Ūö®Í≥ľž†ĀžĚīŽč§[5]. ž†ēžÉĀ žč†žě•ÍłįŽä• ŪôėžěźžôÄ ŽĻĄÍĶźŪēėžó¨ ž§ĎŽďĪŽŹĄžĚė žč†žě•ÍłįŽä• ž†ÄŪēėŪôėžěźžóźžĄú febuxostat Ž∂ÄžěĎžö© ŽĻąŽŹĄÍįÄ ŽćĒ ŽÜížßÄŽäĒ žēäžēėŽč§Í≥† ŪēėŽ©į žēĹŽ¨ľžĚĄ ž§ĎŽč®ŪēėÍ≤Ć ŽźėŽäĒ ž£ľžöĒ žõźžĚłžúľŽ°úŽäĒ ÍįĄÍłįŽä• žąėžĻė žÉĀžäĻ, ͳȞĄĪ ŪÜĶŪíć ŽįúžěĎ(gout flares), žĄ§žā¨, ŽįúžßĄžĚī žěąÍ≥† Í∑ł žôł ÍĶ¨žó≠, ÍĶ¨Ū܆, ŽĎźŪÜĶ, žĖīžßÄŽüľž¶Ě, ÍīÄž†ąŪÜĶ ŽďĪžĚė Ž∂ÄžěĎžö©žĚī ŽďúŽ¨ľÍ≤Ć žÉĚÍłł žąė žěąŽč§[7].
ž¶ĚŽ°ÄžĚė Í≤Ĺžöį ŽßźÍłį žč†Ž∂Äž†ĄžúľŽ°ú Ž≥ĶŽßČŪą¨žĄĚžĚĄ ŪēėŽäĒ ŪôėžěźŽ°ú žĖϞܟ ÍīÄž†ąžóź žÉĚÍłī tophiŽ°ú žĚłŪēī ŪÜĶž¶ĚžĚī žč¨ŪēėÍ≥† ÍīÄž†ąžöīŽŹôžĚī ž†úŪēúŽźėžĖī žĚľžÉĀžÉĚŪôúžóź žßÄžě•žĚī žěąžĖī žąėžą†žĚĄ ŪēėžėÄÍ≥†, allopurinolžĚĄ ž¶ĚŽüČŪēėžó¨ Ž≥Ķžö©ŪēėžėÄžĚƞ󟎏Ą 3ÍįúžõĒ Ží§ Žč§žčú žě¨ŽįúŪēú tophiŽ°ú žĚłŪēī 2žį® ž†úÍĪį žąėžą†žĚĄ ŪēīžēľŽßĆ ŪēėžėÄŽč§. žĚīžĖī žąėžą† ŪõĄ 1žĚľžį®žóź febuxostat 40 mg žēĄžĻ®žóź Ūēú Ž≤ą Ž≥Ķžö©žúľŽ°ú ž†ĄŪôėŪēėžėÄÍ≥† Ž≥Ķžö© ŪõĄ 3ÍįúžõĒ žį®žóź Ūėąž≤≠žöĒžāįŽÜ掏ĄÍįÄ 5.9 mg/dLÍĻĆžßÄ ÍįźžÜĆŪēėžėÄÍ≥† 20ÍįúžõĒžĚī žßÄŽāú ŪėĄžě¨žóźŽäĒ Ūėąž≤≠žöĒžāįžĻėÍįÄ 5.3-5.5 mg/dL ž†ēŽŹĄŽ•ľ žú†žßÄŪēėÍ≥† žěąŽč§. Febuxostat Ž≥Ķžö©ÍłįÍįĄ ž§Ďžóź žēĆŽü¨žßÄ ŽįėžĚĎžĚīŽāė Ž≤ĒŪėąÍĶ¨ÍįźžÜĆž¶ĚžĚÄ ÍīÄžįįŽźėžßÄ žēäžēėžúľŽ©į 40 mgžĚė ž†ĀžĚÄ žö©ŽüČžúľŽ°úŽŹĄ Ūö®Í≥ľž†ĀžúľŽ°ú žöĒžāį ŽÜ掏ĄŽ•ľ Žāģž∂ú žąė žěąžóąŽč§.
ŽĮłÍĶ≠ žčĚžēĹž≤≠žóźžĄú febuxostat Ž≥Ķžö©ŽüČ(2009ŽÖĄ)žĚĄ 40-80 mg/dayŽ°ú ŽįúŪĎúŪĖąÍ≥†, žĚľŽ≥łžĚė Í≤Ĺžöį(2011ŽÖĄ) žú†žßÄžöĒŽüȞ̥ 40 mg/day, ŪēėŽ£® žĶúŽĆÄžö©ŽüȞ̥ 60 mg/dayŽ°ú žäĻžĚłŪēėžėÄŽč§. žĚľŽ≥łžóźžĄú 2013ŽÖĄ ŽįúŪĎúŪēú Ūēú žóįÍĶ¨[8]žóź ŽĒįŽ•īŽ©ī ŽßźÍłį žč†Ž∂Äž†ĄžúľŽ°ú Ūėąžē°Ūą¨žĄĚŪēėŽäĒ Í≥†žöĒžāįŪėąž¶Ě Ūôėžěź 5Ž™ÖžĚĄ ŽĆÄžÉĀžúľŽ°ú žĚīž†Ąžóź žöĒžāįÍįēŪēėž†úŽ•ľ Ž≥Ķžö©Ūēúž†Ā žóÜŽäĒ 3Ž™ÖžĚÄ febuxostat 10 mgžĚĄ, ŪēėŽ£® Ūēú Ž≤ą allopurinol 50-100 mgžĚĄ Ž≥Ķžö©ŪĖąŽćė 2Ž™ÖžĚÄ febuxostat 20 mgžĚĄ Ž≥Ķžö©Ūēėžó¨ 4ÍįúžõĒ ŽŹôžēą Ūėąž≤≠žöĒžāįŽÜ掏ĄÍįÄ 6.0 mg/dL ŽĮłŽßĆžúľŽ°ú žú†žßÄŽźėŽ©īžĄú ͳȞĄĪ ŪÜĶŪíćŽįúžěĎžĚī ŽāėŪÉÄŽāėžßÄ žēäžēėŽč§ŽäĒ Ž≥īÍ≥†ÍįÄ žěąžóąŽč§. FebuxostatžĚÄ ŽßźÍłį žč†Ž∂Äž†ĄžúľŽ°ú Ūą¨žĄĚŪēėŽäĒ ŪôėžěźžóźžĄú ž†ĀžĚÄ žö©ŽüČžúľŽ°úŽŹĄ žě¨ŽįúŪēėŽäĒ ŪÜĶŪíćžóź Ūö®Í≥ľž†ĀžúľŽ°ú žĻėŽ£ĆÍįÄ ÍįÄŽä•ŪēėÍ≥† Íłįž°īžĚė žĻėŽ£Ćž†úžĚł allopurinolžóź ŽįėžĚĎŪēėžßÄ žēäÍĪįŽāė Ž∂ąŽāīžĄĪžĚł Í≤ĹžöįžóźŽŹĄ ŽĆÄž≤īŪē† žąė žěąŽäĒ žĘčžĚÄ žēĹž†úžĚīŽč§. Žč§ŽßĆ žĻėŽ£Ć žīąÍłį ͳȞĄĪ ŪÜĶŪíćŽįúžěĎžĚī ŽįúžÉĚŪē† žąė žěąžĖī non-steroidal anti-inflammatory drug ŽėźŽäĒ žĹúŪěąžĻú(colchicines)žĚĄ žėąŽį©ž†ĀžúľŽ°ú 6ÍįúžõĒÍįĄ Ž≥ĎŪĖČŪē† Í≤ɞ̥ ž∂Ēž≤úŪēėŽ©į žēĹŽ¨ľ žÉĀŪėłžěĎžö©žĚĄ Í≥†Ž†§Ūēėžó¨ XO žĚėž°ī ŽĆÄžā¨Ž•ľ ÍĪįžĻėŽäĒ theophylline, azathioprine, mercaptopurine, didanosine ŽďĪžĚė žēĹž†úŽäĒ ŽŹôžčú Ž≥Ķžö©žĚĄ ŪĒľŪēėŽäĒ Í≤ÉžĚī žĘčŽč§. žēĄžßĀ žßĀž†Ďž†ĀžĚł žÉĀÍīÄÍīÄÍ≥ĄÍįÄ ŽįĚŪėÄžßĞߥ žēäžēėžúľŽāė febuxostatÍ≥ľ žč¨ŪėąÍīÄ Ūėąž†ĄžÉČž†Ąž¶Ě žúĄŪóėžĄĪžĚī žĖłÍłČŽźėŽĮÄŽ°ú Ž≥Ķžö© ž§Ďžóź žč¨Í∑ľÍ≤ĹžÉČžĚīŽāė ŽáĆž°łž§Ď žßēŪõĄÍįÄ Ž≥īžĚīŽäĒžßÄ Ž©īŽįÄŪēú ÍīÄžįįžĚī ŪēĄžöĒŪēėŽ©į ž£ľÍłįž†ĀžúľŽ°ú žč¨ž†ĄŽŹĄ ŽįŹ Ūėąžē°Í≤Äžā¨Ž•ľ žčúŪĖČŪēėŽŹĄŽ°Ě ŪēúŽč§[7,9].
Í≥†žöĒžāįŪėąž¶ĚžĚÄ Ž¨īž¶ĚžÉĀ žÉĀŪÉúžóźžĄúŽŹĄ Ž≥ĎŽ¶¨žÉĚŽ¶¨Ūēôž†ĀžúľŽ°ú Ž≥ÄŪôĒŽ•ľ žú†ŽįúŪēėŽäĒŽćį Ž†ąŽčĆ-žēąžßÄžė§ŪÖźžč† žčúžä§ŪÖúžĚė ŪôúžĄĪŪôĒžôÄ žā¨ÍĶ¨ž≤ī žó¨Í≥ľžú® ÍįźžÜĆ, ŽāīŪĒľ žĄłŪŹ¨žĚė ÍłįŽä•ž†ÄŪēė ŽįŹ nitric oxidežĚė žÉĚžĄĪ ÍįźžÜĆ, ŪėąÍīÄ ŪŹČŪôúÍ∑ľ žĄłŪŹ¨ ž¶Ěžč̞̥ žěźÍ∑ĻŪēėŽäĒ ŽďĪ arterioležóź ÍĶ¨ž°įž†Ā Ž≥ÄŪôĒŽ•ľ žú†ŽįúŪēėžó¨ žč†žě•ÍłįŽä• ž†ÄŪēėŽ•ľ žú†ŽįúŪēúŽč§. ŽėźŪēú žč¨ŪėąÍīÄÍ≥ĄžßąŪôėžĚė žúĄŪóėžĚłžěźŽ°ú ŽßĆžĄĪžč†Ž∂Äž†Ą 4-5Íłį ŪôėžěźŽď§žóźÍ≤ĆžĄú žč¨ŪėąÍīÄžßąŪôėžúľŽ°ú žĚłŪēú žā¨ŽßĚ žúĄŪóėŽŹĄŽ•ľ ž¶ĚÍįÄžčúŪā®Žč§[5,10]. ŽĒįŽĚľžĄú žĚľŽ≥łžóźžĄúŽäĒ Ž¨īž¶ĚžÉĀ Í≥†žöĒžāįŪėąž¶Ě(> 8.0 mg/dL) žÉĀŪÉúžóźžĄúŽŹĄ febuxostat žā¨žö©žĚĄ ž∂Ēž≤úŪēėÍ≥† žěąŽč§[8].
FebuxostatžĚÄ ŽßźÍłį žč†Ž∂Äž†ĄžúľŽ°ú Ž≥ĶŽßČŪą¨žĄĚžĚĄ ŪēėŽäĒ ŪôėžěźžóźžĄú ŽįėŽ≥ĶŽźėŽäĒ ŽßĆžĄĪÍ≤įž†ēžĄĪŪÜĶŪíćžĚė žĻėŽ£Ćžóź žú†Ž¶¨ŪēėŽ©į Ūėąž≤≠žöĒžāįŽÜ掏ĄŽ•ľ 6.0 mg/dL ŽĮłŽßĆžúľŽ°ú ŽāģÍ≤Ć žú†žßÄŪēėŽäĒ Žćį Ūö®Í≥ľž†ĀžĚīžóąŽč§. ŽāėžēĄÍįÄ ŽāėžĚīÍįÄ ž†äžĚÄ Ūą¨žĄĚŪôėžěźžóźžĄú ŪĖ•ŪõĄ žč¨ŪėąÍīÄÍ≥Ą Ūē©Ž≥Ďž¶ĚžĚĄ ž§ĄžĚľ žąė žěąŽäĒ ŽćįžóźŽŹĄ ŽŹĄžõÄžĚī Žź† Í≤ÉžĚīŽĚľ Ž≥īžĚīŽ©į, žĚīžóź ÍīÄŪēīžĄúŽäĒ žě•ÍłįÍįĄ Í∑úŽ™®ÍįÄ žěąŽäĒ žóįÍĶ¨ÍįÄ ŽćĒ ŪēĄžöĒŪē† Í≤ÉžĚīŽč§. FebuxostatžĚÄ Ž∂ąžĚĎžĄĪ ŪÜĶŪíćžĚīŽāė ŽßĆžĄĪ Í≤įž†ēžĄĪŪÜĶŪíć žú†Ž≥Ϟ̥ ž§Ąžó¨ž§Ą ÍįÄŽä•žĄĪžĚĄ žčúžā¨ŪēėŽ©į, žě•ÍłįÍįĄ Ūą¨žĄĚžĚĄ ŪēėŽäĒ ŪôėžěźžóźŽŹĄ Ūö®Í≥ľž†ĀžĚł žöĒžāįÍįēŪēėž†úŽ°úžĄú žā¨žö©žĚī ŽćĒ ŽäėžĖīŽā† Í≤ÉžúľŽ°ú žā¨Ž£ĆŽźúŽč§.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






