서 론
폐암은 전 세계적으로 암 사망률 1위이며 국내에서도 2006년 이후로 1위를 차지하고 있다[1-3]. 표피성장인자 수용체(epidermal growth factor receptor, EGFR) 티로신 활성효소 억제제(tyrosin kinase inhibitor, TKI)인 gefitinib과 erlotinib은 비소세포폐암에 대한 표적치료제로 사용되고 있다[4]. 진행암으로 운동이 제한되고 있는 환자에서 혈전증의 발생률은 일반인에 비해 약 4.1배 높고, 항암치료를 하는 경우는 약 6.5배 높은 것으로 보고되고 있다[5]. 와파린은 혈전증의 예방 및 치료제로 흔히 사용되며 이는 다른 약제와 함께 투여될 때에 상호작용을 일으켜서 혈전 및 출혈의 합병증을 유발시킬 수 있다. 와파린이 gefitinib과 함께 투여될 때에 두 약제의 상호작용으로 PT-INR이 연장되었다는 보고[5,6]가 있었고, gefitinib과 화학적 구조가 유사한 erlotinib과 와파린도 같은 반응을 보일 것이라는 이론적 가능성과 실험 결과[7-10]는 제시되었지만 임상 증례보고는 아직 없는 실정이다. 저자들은 3차 폐암치료로 erlotinib이 투여되고 있던 환자에서 정맥혈전증의 치료를 위하여 와파린을 병용함에 따라 PT-INR이 연장되었던 증례를 경험하였기에 문헌고찰과 함께 보고하는 바이다.
증 례
환 자: 50세 남자
주 소: 이틀 전부터 심해진 호흡곤란 및 양측 상지의 부종
과거력 및 현병력: 비소세포 폐암(편평상피세포암, T4N3M0, IIIB)으로 진단받은 후 동시 항암방사선 치료 및 3회의 공고화학요법을 시행하였다. 이후 안정성 병변으로 외래에서 추적 관찰을 시행한 지 7개월 후, 우측 기관주위 종괴의 크기가 약간 증가하였으며, 뇌의 좌측 측두엽에 단발성 전이와 다발성 골전이가 발견되었다. 자기수행능력은 ECOG 1이었으므로 뇌전이 병변에 대한 사이버나이프 및 2차 약제로 항암치료(gemcitabine, carboplatin)를 시행하였다. 1개월 후에 왼쪽 상지 부종을 호소하였고, CT 검사상 왼쪽 팔머리 정맥(Lt. bracheocephalic v.)의 혈전증이 발견되어 저 분자량 헤파린 피하주사 치료 후 경구 와파린 유지하다가 심한 빈혈 및 위장관 출혈로 중지하였다. 2개월 후 양측 두개골 및 두피의 다발성 전이로 통증을 호소하여 진행성 병변으로 판단하고 항암치료를 중단하기로 하였으며 전뇌 방사선치료와 함께 erlotinib을 사용하기 시작하였다. 환자는 점차 자기수행능력이 저하되면서 전신 쇄약감, 흉부 불쾌감과 양측 상지의 부종을 호소하였다.
이학적 소견: 신체활력 징후는 혈압 130/90 mmHg, 맥박 95회/분, 체온 37.3℃, 호흡수 20회/분이었다. 신장 173 cm, 몸무게 78.5 kg였고, 영양 상태는 양호해 보였다. 신체 검사상 양측 상지의 부종이 관찰되었으며, 특히 이전에 팔머리 정맥혈전증이 있었던 좌측 상지에 정맥혈전증의 재발이 의심되었다.
검사실 소견: 말초혈액검사에서 Hb 9.4 g/dL, Hct 29.2%, MCV 95.4fl, MCHC 30.7 pg, M.C.H.C. 32.2%로 정구정색성 빈혈이 관찰되었고, 백혈구 12,070/mm3 (호중구 87.5%), 혈소판 150,000/mm3, 프로트롬빈시간 12.0초(INR 1.20), 활성화부분트롬보플라스틴시간(aPTT) 25.8초이었다. 단백 5.46 g/dL, 알부민 3.12 g/dL, AST 22 IU/L, ALT 10 IU/L, 총 빌리루빈 1.60 mg/dL, ALP 140 IU/L, LDH 875 IU/L, BUN 13.4 mg/dL, Cr 1.28 mg/dL이었다. 혈장 전해질 수치는 Na 137 mEq/L, K 4.1 mEq/L, Cl 95 mEq/L이었고, Ca 6.7 mg/dL, P 1.56 mg/dL이었다. D-dimer는 492 ug/L (참고치 0-200 ug/L)로 이전에 비해 상승되어 있었다.
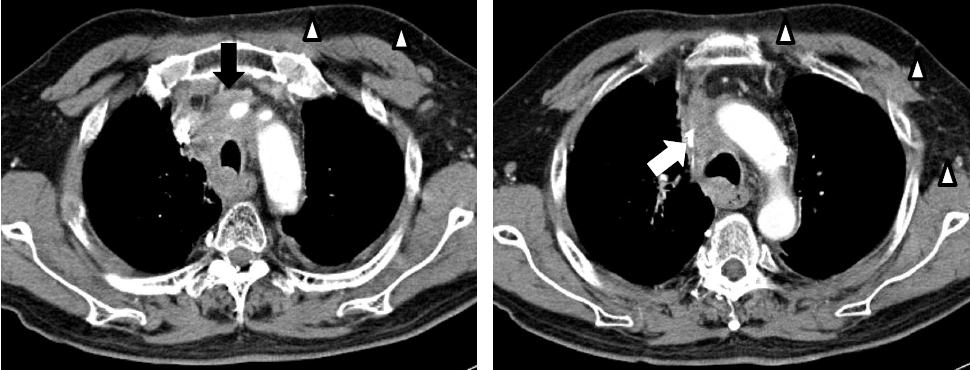
방사선학적 소견: 흉부 단순 촬영에서는 우측 기관주위 종괴의 크기가 증가 이외의 특이소견은 보이지 않았다. 흉부 전산화 단층 촬영에서는 우측 상부 종격동 림프절 종대에 의하여 상대 정맥의 내강이 협착되어 있었고, 왼쪽 팔머리 정맥의 혈전증 및 흉벽으로 측부 혈관들이 발달되어 있었다(Fig. 1).
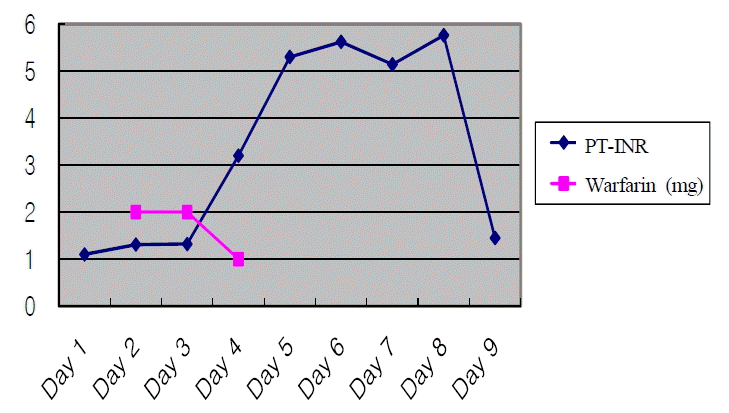
임상경과 및 치료: 팔머리정맥 혈전증에 대한 항응고 치료를 중단한 병력이 있었고, 왼쪽 상박부의 부종악화 및 D-dimer가 상승되어 있는 것으로 보아 혈전증 재발이 의심되어 저분자량 헤파린 주사 및 와파린 2 mg을 투여하였고, 종양에 의한 상대정맥의 내강 협착에 대하여 혈관촬영술 및 풍선에 의한 경피적 확장술을 시행하였다. 경구 와파린을 사용한 지 3일째 INR 3.2로 연장되어 1 mg으로 줄였으나 4일째 5.3으로 더욱 연장되어 와파린 투여를 중지하였다. 이후에도 2일간 지속적으로 연장되어 비타민 K 정주 후에 1.45로 되었다(Fig. 2).
고 찰
표피성장인자 수용체 티로신 활성효소 억제제(epidermal growth factor receptor tyrosine kinase inhibitors, EGFR TKIs)는 분자표적 치료제로서 비소세포성폐암에 대하여 현재 임상에서 쓰이고 있는 대표적인 약제로는 gefitinib과 erlotinib이 있다. 이는 진행성 비소세포폐암 환자에서 2차 또는 3차 약제로 사용되고 있으며, 자기수행능력이 저하되어 있는 환자에서는 1차 약제로 선택되기도 한다[4,9,10]. Gefitinib은 서양인보다 동양인, 특히 여성, 비흡연자, 조직학적으로 선암은 반응이 좋을 것으로 예측이 되는 인자이며 우리나라를 비롯한 아시아 지역에서는 진행성 비소세포폐암 환자에게 투여하였을 때에 서양인에 비하여 효과적인 것으로 보고되고 있으며[11], erlotinib은 표준치료에 실패한 비소세포폐암환자에서 위약과 비교한 무작위 3상 연구결과에서 생존기간에 있어서 통계적으로 유의한 연장을 보여 FDA의 승인을 받았고, 현재 서구에서 진행성 비소세포폐암에 대한 2차 요법제로 쓰이고 있다[12]. 두 약제는 비슷한 화학적 구조를 가지고 있으며 유사한 효과와 부작용을 보이는 것으로 알려져 있다[10].
진행성 암환자는 혈전 발생의 고 위험군으로, 특히, 항암치료, 입원, 빈혈에 대한 조혈인자의 사용 등으로 혈전발생의 위험성은 더욱 증가하게 되며, 와파린을 예방적 항 혈전치료로 쓸 수 있다[13]. 와파린은 다른 약제와 함께 사용할 경우, 그의 약물 역동학적 특성이 변화되어 출혈 및 혈전발생의 위험이 증가할 수 있는 약제이다[14]. 와파린은 경구 복용하면 위장관을 통해 혈중으로 흡수되며 혈중에서 알부민과 결합하며, 간에서 cytochrome P450효소에 의해서 대사되는데, 와파린의 CYP 대사과정과 관련된 약물을 복용하거나, 혈중에서 알부민에 결합하여 와파린을 치환시키는 약물 또는 대장 정상 세균총을 변화시키는 항생제를 복용한 경우 와파린의 항 응고작용에 영향을 주어 출혈소인이 증가할 수 있다[14]. 와파린과 상호작용을 하는 항암제로는 5-FU [15]나 capecitabine [16]이 보고되었고, 분자표적치료제로서는 최근에 gefitinib [5]과 sorafenib [17]이 보고되었다.
Arai 등[5]는 비소세포암으로 gefitinib을 쓰고 있는 12명의 환자에서 와파린을 함께 사용하였을 때 50%에서 INR이 연장되는 것을 발견하였다. 와파린은 CYP2C9, CYP1A2, CYP3A4에 의해서 대사가 이루어지며, gefitinib도 주로 CYP3A4에 의해 대사되므로 와파린과 경쟁적으로 작용할 수 있다[10,14]. 따라서 gefitinib이 동시에 투여되면 와파린의 대사속도가 느려지므로 혈중에서 작용시간이 늘어나게 되고 결과적으로 INR이 연장된다. 또한 와파린과 gefitinib은 혈중에서 알부민과 결합하므로 상호 경쟁적으로 결합하게 되어 동시에 투여 시 알부민에 결합되지 못한 와파린이 증가하게 되어 저트롬빈혈증을 초래하여 INR을 연장시킨다[10,14]. 또한 간기능 부전이나 항암치료에 따른 설사와 점막염으로 비타민 K의 흡수가 불충분한 경우 등도 INR을 연장시키는 원인이 될 수 있다[14].
Sorafenib [17]은 티로신 활성 억제제이면서 혈관 내피 세포 성장 억제제(vascular endothelial growth factor inhibitor)로서 종양의 증식을 억제하는 동시에 혈관생성을 억제하는 역할을 하며 주로 간암의 치료로 사용되는데, 약물대사 중 CYP3A4이 관련되어 와파린과 함께 사용하면 출혈 경향을 더욱 가중시킬 수 있다. 그러나 만성 B형 간염과 간암으로 인한 간기능 부전에 의해서도 INR의 연장이 초래될 수 있음을 고려해야 할 것이다. 본 증례의 환자는 간기능 지수는 정상 범위였고, 설사나 점막염이 의심되는 증상은 보이지 않았다. 또한 와파린과 작용하여 INR을 연장시킬 수 있는 다른 약물도 투여되지 않는 상황이었으므로 이 환자에게서 보이는 INR의 연장은 erlotinib에 의한 것이라고 할 수 있고, 약제간의 상호작용 연관성을 평가하는 객관적인 지표인 Naranjo ADR probability scale [18]에 적용하면 score 6점으로 probable에 해당되어 두 약제의 상호작용으로 INR이 연장 되었다고 할 수 있다. 또한 와파린은 erlotinib과 대사과정에서 상호경쟁적으로 작용하여 erlotinib의 대사율이나 종양 반응률에도 영향을 미칠 수 있다. Arai 등[5]에 따르면 와파린과 gefitinib을 같이 사용한 경우의 종양 반응률은 54.5%이라고 하였으며, 이는 gefitinib 단독으로 사용했을 경우에 비하여 우월한 결과임을 제시하였다[19]. 결과적으로 와파린과 gefitinib을 함께 투여하더라도 gefitinib의 종양억제 효과가 떨어지지 않는다고 하였지만 환자의 수가 적고, 동양인에 국한되어 있는 점을 고려할 때 두 약제의 동시 사용에 따른 암에 대한 치료 효과에 대해서는 단정적으로 결론을 지을 수는 없다.
활동성이 저하된 진행성 암환자에서 혈전증의 발생위험이 높고, 심방세동 등의 빈도가 증가할 수 있으며, 특히 비소세포폐암인 경우에는 와파린을 투여하면서 EGFR TKI 표적치료제를 사용하는 경우가 더욱 증가할 것을 고려할 때에 이 논문의 의의는 크다고 볼 수 있다. 결론적으로 와파린과 gefitinib 및 erlotinib을 같이 쓸 경우에는 이와 같은 잠재적인 상호작용을 고려하여 INR의 변화를 주의 깊게 관찰해야 하며 필요한 경우에는 와파린의 용량을 조절해야 한다. 또한 와파린이 erlotinib과 함께 투여될 때 erlotinib의 종양 반응률에 영향을 알고자 하는 향후 대규모의 연구도 필요하다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






