 |
 |
| Korean J Med > Volume 80(3); 2011 > Article |
|
요약
전신성 홍반성 루푸스 자체에 의한 간염은 드물게 발생하며, 자가면역성 간염과 감별을 요한다. 저자들은 자가면역성 간염과 유사하게 표현된 루푸스 간염에서 간 조직검사의 중요성을 경험하였기에 문헌고찰과 함께 보고하는 바이다.
Abstract
Patients with systemic lupus erythematosus(SLE) have a 25% to 50% incidence of abnormal findings on liver function tests. The main causes of abnormal liver function in patients with SLE are viral hepatitis, drug-induced toxic hepatitis, and fatty liver. However, hepatic involvement due to the pathogenic process of SLE is rare. In such conditions, lupus-related hepatitis must be distinguished from autoimmune hepatitis, which is a type of primary liver disease characterized by similar clinical manifestations and autoimmune profiles. Relationships between hepatic involvement of SLE and autoimmune hepatitis remain to be elucidated. We report a case of lupus-related hepatitis mimicking autoimmune hepatitis. (Korean J Med 2011;80:360-364)
전신성 홍반성 루푸스(이하 루푸스)는 자가 항체 및 면역복합체로 인해 일어나는 자가면역질환으로 전신을 침범하는 질환이지만 병적인 면역반응에 의한 간 침범은 드문 것으로 알려져 있다. 루푸스 환자의 25~50%에서 간 기능 이상소견을 보일 수 있으나, 대부분 일시적이며 증상발현이 거의 없어, 임상적으로 명백한 간질환으로의 이행은 드물다. 간 기능 이상소견을 보이는 루푸스 환자에서 간 기능 이상의 주요 원인으로 바이러스성 간염이나 간독성 약물에 의한 간염이 알려져 있지만 이를 배제할 경우, 루푸스 간염과 자가면역성 간염을 고려하여야 한다. 이들은 다른 예후를 가지는 반면, 임상양상과 자가항체와 같은 혈액검사소견에서 많은 공통점을 공유하고 있어 감별이 중요하면서도 어려운 것으로 알려져 있다[1,2].
환 자: 이○○, 여자, 52세
주 소: 오심, 복부 팽만감
현병력: 2006년 구강궤양, 피부발진 및 혈액검사상, 범혈구 감소증, 항 핵항체 양성, 항 ds-DNA 항체 양성, 단백뇨로 전신성 홍반성 루푸스 진단받고, 타병원에서 면역억제제(Cyclosporine, Azathioprine), 항말라리아제 복용한 과거력이 있으며, 피부발진 및 구강궤양 등의 임상양상이 호전되어 자의로 복용을 중단하였다. 2007년 본원 내원하여 시행한 검사상, 간 기능 이상소견을 보여 정밀검사 시행결과, 간염 바이러스 음성, International Autoimmune Hepatitis Group (IAHG) score 10점으로[6] ‘Probable’ 자가면역성 간염에 해당하였으나, 항 Smooth muscle 항체 양성으로 간 조직검사 없이 자가면역성 간염으로 추정하고 고용량 스테로이드 치료 후 호전되었다. 이후 외래 추적 검사상 AST 45~70 IU/L, ALT 45~100 IU/L 범위를 유지하며 지속적으로 상승되어 있고 간헐적인 혈관염성 피부발진의 재발 등으로 인해 Prednisone 15 mg/day 복용을 유지하였으며, 내원 2주 전부터 오심, 복부 팽만감 발생하여 응급실 내원하였다.
과거력: 당뇨, 고혈압, 결핵의 병력은 없었으며, 음주력이나 흡연력, 다른 약제 복용력도 없었다. 수혈 받은 적은 없었다.
가족력 및 사회력: 특이소견 없었다.
신체검진 소견: 내원 당시 활력징후는 혈압 135/87 mmHg, 맥박 84회/분, 호흡수 20회/분, 체온 36.5℃였다. 의식은 명료하였으며 급성병색을 보였다. 두경부 소견상, 안면발진, 구강 내 궤양은 보이지 않았고, 촉지되는 림프절은 없었다. 흉부청진상에서 심잡음은 청진되지 않았으며, 천명음이나 수포음도 청진되지 않았다. 복부 장음은 항진되어 있었으며, 복부 촉진에서 간비대는 관찰되지 않았으며, 압통은 없었다. 사지진찰상 함요부종 소견은 보이지 않았다.
검사 소견: 일반혈액 검사상, 백혈구 5,250/uL, 혈색소 13.6 g/dL, 혈소판 189,000/uL, 적혈구침강속도 14 mm/h였다. 혈액응고검사 PT/PTT는 9.7/19.6 sec였다. 일반화학검사상, 나트륨 142 mmol/L, 칼륨 4.2 mmol/L, 칼슘 9.1 mmol/L, 인 4.7 mmol/L, 혈액요소질소 21.1 mg/dL, 크레아티닌 0.69 mg/dL, 총 단백질 6.7 g/dL, 알부민 3.9 g/dL, LDH 556 IU/L, CPK 30 IU/L, 총 빌리루빈 0.53 mg/dL, ALP 223 IU/L, 요산 5.5 umol/L이었으며, AST 69 IU/L, ALT 169 IU/L로 간 효소 수치는 정상보다 상승되어 있었다. 요분석검사상, 요단백 음성, 적혈구 4-9/HPF였고, 24시간 요 단백량 374 mg이었다. 일반혈청검사상, C 반응성 단백질 < 0.02 mg/L, HBs 항원 음성, HBs 항체 양성, HCV 항체 음성, IgM 항 HAV 음성이었다. 혈액은행검사상, 직접 Coombs 검사 양성, 간접 Coombs 검사 음성이었고, 망상적혈구 2.38%이었다. 면역화학검사상, 면역글로불린 G, A, M, E 모두 정상이었으며, 혈청 보체 C3 8.0 g/L, C4 1.8 g/L, Haptoglobin < 30 mg/dL, Ceruloplasmin 170 mg/dL였다. 자가면역혈청검사상, 항 핵항체 양성(1:100, nuclear & cytoplamic type), 항 ds-DNA 항체 38.4 IU/mL, 항 Cardiolipin 항체 음성, 항 Ro 항체 양성, 항 Ribosomal-P Protein 항체 양성, 항 Smooth muscle 항체 음성, 항 SLA/LP 항체 음성, 항 LKM-1 항체 음성, 항 LC-1 항체 음성, 항 미토콘드리아 항체 음성이었다.
방사선학적 소견: 단순 흉부 및 복부 촬영에서는 특이소견 보이지 않았으며, 복부 컴퓨터단층촬영에서 간 및 비장 종대, 복수 등의 특이소견은 보이지 않았다.
병리조직학적 소견: 간 효소 수치가 지속적으로 상승하고 2007년 검출되었던 항 Smooth muscle 항체가 내원 당시 검출되지 않아, 기존에 추정 진단하였던 자가면역성 간염보다는 루푸스 자체에 의한 간염일 가능성을 고려하여 간 조직검사를 시행하였다. 간 조직검사상 조각괴사 소견은 보이지 않았으며, 경증의 문맥주위 염증세포 침윤과 소엽에 경미한 염증반응 및 경한 간 섬유화 소견이 관찰되었다(Fig. 1A and 1B).
이후 Prednisone을 25 mg/day로 증량하고, Mycophenolate mofetil 1 g/day을 추가로 투여하였으며, Prednisone은 25 mg/day에서 1주일 간격으로 5 mg/day씩 감량하였다. Mycophenolate mofetil 추가 후 2주일 뒤 외래에서 시행한 혈액검사에서 AST 31 IU/L, ALT 78 IU/L로 호전되었으며, 오심과 복부팽만감도 호전되었다.
현재 환자는 Mycophenolate mofetil 1 g/day, Prednisone 15 mg/day 복용 중으로 위장관계 증상 없이 외래에서 추적관찰 중이다.
루푸스는 근골격계, 피부, 신장, 폐, 심혈관계, 중추신경계 등 전신을 침범하는 자가면역질환으로, 질병의 경과 중 25~30%에서 간 기능 이상소견을 보일 수 있으나, 이는 임상적으로 명백한 간질환으로 간주되는 경우는 흔치 않고, 루푸스의 진단기준에도 역시 포함되지 않는다[7]. 루푸스 환자에서의 간 기능 이상은 용혈성 빈혈에 의한 황달, 약물치료로 인한 간독성, 바이러스 간염이 동반된 경우에 주로 나타나며, 다른 자가면역 질환이 동반되어 있는 경우에도 나타날 수 있으나, 루푸스 자체에 의한 간기능 이상 소견은 8% 정도로 드문 것으로 알려져 있다[1,2]. 간 기능 이상을 보이는 루푸스 환자에서 루푸스 간염과 가장 쉽게 오인되는 것은 비슷한 임상양상과 자가항체가 나타나는 자가면역성 간염이다. 자가면역성 간염은 1956년 Mackay 등이 루푸스와 비슷한 임상양상을 보이고, LE 세포현상을 보이는 만성 활동성 간염을 ‘루푸스양 간염(Lupoid hepatitis)’ 라고 언급한 것에서 시작되었으며, 이후 이 용어는 비정상적인 면역반응에 의한 원인불명의 만성 진행성 염증성 간질환을 뜻하는 자가면역성 간염으로 발전하였다. 1993년 International Autoimmune Hepatitis Group (IAHG)에서는 자가면역성 간염 진단을 위한 점수체계를 정립하였으며, 점수체계는 임상양상, 면역학적 소견(자가항체), 병리조직학적인 소견, 그리고 생화학적소견(고감마글로불린혈증, 면역글로불린 G)을 바탕으로 구성되었다. 이러한 점수체계가 정립되면서, 자가면역성 간염의 진단은 더욱 명확해졌지만, Oka 등에 의하면 자가면역성 간염 환자의 3%에서 루푸스의 진단기준을 만족하기 때문에[8] 루푸스 간염은 자가면역성 간염으로 오인될 수 있어 진단이 어렵다. 이처럼 두 질환은 감별진단이 어려움에도 불구하고, 합병증과 치료 관점에서 다른 것으로 알려져 있어, 두 질환을 감별하는 것이 중요하다[6]. 말기 간질환으로 진행하는 빈도에 있어 루푸스 간염의 경우, 간경화, 간성혼수, 문맥고혈압 등 말기 간질환으로 진행하는 경우가 드물지만[9], 자가면역성 간염의 경우 5년 사망률 50%, 치료받지 않을 경우 10년 사망률 90%로 말기 간질환으로 진행하는 빈도가 높다[10,11]. 치료적 측면에 있어, 자가면역성 간염의 경우 Glucocorticoid와 Azathioprine의 병합요법이 65~80% 정도 효과가 있다고 알려져 있으며, 재발 시 저용량의 Glucocorticoid 혹은 Azathioprine을 장기간 사용할 수 있다[10,12]. 반면 루푸스 자체에 의한 간염은 루푸스에 의한 다른 임상양상을 치료하는 것과 같으며, Glucocorticoid 치료에 반응이 좋은 것으로 알려져 있다[13].
두 질환을 감별하는데 있어, 자가항체와 같은 혈청학적 검사와 간 조직 병리소견에 대한 중요성이 강조되고 있으며, 이에 대한 여러 연구들이 진행되었다. 혈청학적 검사 측면에서 항 핵항체는 두 질환 모두에서 나타날 수 있으나, 항 Smooth muscle 항체는 자가면역성 간염 환자의 67~81%에서 검출되며, 루푸스 간염에서도 30% 정도에서 검출될 수 있다[11]. 항 LKM-1 항체는 자가면역성 간염 환자에서만 검출되며, 루푸스 환자에서는 일반적으로 검출되지 않는다. 이와 대조적으로 항 ds-DNA 항체, 항 Ribosomal-P protein 항체 등의 존재는 루푸스 간염 진단의 중요한 소견이다[10]. 항 Ribosomal-P protein 항체는 Elkon & Foster에 의해서 처음 언급된 항체로, 루푸스 환자의 16%에서 검출되며[11,14], Bonfa, The 등의 연구와 Koren, Hulsey, Ohira 등의 연구에 의하면 이 항체는 루푸스 간염에서만 나타났고, 자가면역성 간염에서는 검출되지 않았다[14-18].
Kooy 등은 두 질환을 감별하는데 있어 간 조직검사의 필요성을 강조하였으며, 간의 조직병리학적 소견은 활동성 루푸스 환자에서 간수치 상승이 있을 때, 루푸스 간염과 자가면역성 간염을 진단할 때 중요한 지표가 될 수 있다[3,11]. 루푸스 간염의 조직학적 형태는 다양하게 나타나며, 대부분 경한 염증반응을 보인다. Gibson 등에 의하면 대부분의 경우, 소엽과 문맥주위에 소수의 림프구 침윤을 보였으며, 지방침윤과 염증세포의 침윤이 없는 다발성 국소성 간 괴사 소견을 보였다. 이러한 문맥주위의 림프구 침윤에 의한 문맥 간염은 질병의 활성도를 반영할 수 있으며, 때로는 소엽 간염 형태로 나타날 수 있다[11]. 이에 비해 자가면역성 간염은 조각괴사(piecemeal necrosis)를 특징으로 하며, 활동성 간염, 간세포의 Rossetting, 림프구 침윤 등의 소견을 보일 수 있다. 자가면역성 간염은 대부분 루푸스 간염에 비해 심한 염증반응을 보이며, 특징적인 병리조직학적 소견인 조각괴사의 유무가 두 질환을 감별하는 데 중요한 역할을 한다[3].
본 증례의 경우, 2007년 처음 간 기능 이상 소견을 보였을 당시 혈청검사상, 항 핵항체 양성, 항 Ribosomal P-protein 항체 양성 소견과 함께 항 Smooth muscle 항체 양성 소견을 보여 IAHG score 10점이었음에도 항 Smooth muscle 항체 검출로 인해 임상적으로 자가면역성 간염으로 진단하였다. 반면, 2009년 다시 간 기능 이상으로 입원하였을 당시, IAHG score 7점이었으며, 자가면역성 간염에 특이적인 항 Smooth muscle 항체, 항 SLA/LP 항체, 항 LKM-1 항체 등은 검출되지 않으면서 루푸스 간염에 비교적 특이적이라고 알려진 항 Ribosomal P-protein 항체가[14-18] 검출되었다(Table 1). 한 연구에 의하면 자가면역성 간염에서 항 핵항체나 항 Smooth muscle 항체가 혈액검사 소견과 병리조직 소견이 호전될 경우 76%에서 음전될 수 있다고 하였으나[19], 본 증례는 루푸스의 진단기준을 만족하면서 전신성 홍반성 루푸스 질병 활성도 지수(Systemic Lupus Erythematousus Disease Activity Index (SLEDAI)) 10점(혈뇨, 농뇨, 탈모증)으로 활성화된 루푸스 양상을 보이고[20], 간 조직검사상 조각괴사가 보이지 않고, 소엽과 문맥 주위에 소수의 림프구 침윤 소견을 보이는 루푸스 간염에 합당한 소견을 보였다.
본 증례는 2007년 내원 시 IAHG score 10점으로 ‘Probable’ 자가면역성 간염 소견을 보이면서, 항 Smooth muscle 항체가 검출되어 혈청학적 측면에서 자가면역성 간염과 유사하나 확진을 위한 간 조직검사는 시행하지 않고 자가면역성 간염으로 오인하였던 예이다. 이번 증례를 통해서 자가면역성 간염과 루푸스 자체에 의한 간염을 감별하는 것은 어렵지만, 항 Ribosomal P-protein 항체, 항 LKM-1 항체, 항 Smooth muscle 항체 등의 자가항체와 간 조직검사가 두 질환을 감별하는 데 중요하며, 자가항체가 전형적으로 분류되어 나오지 않거나 IAHG 점수가 비교적 높더라도, 간 조직검사 소견이 두 질환을 감별하는데 중요한 의미를 가진다는 것을 알 수 있다.
REFERENCES
1. Lu MC, Li KJ, Hsieh SC, Wu CH, Yu CL. Lupus-related advanced liver involvement as the initial presentation of systemic lupus erythematosus. J Microbiol Immunol Infect 2006;39:471–475.

2. Miller MH, Urowitz MB, Gladman DD, Blendis LM. The liver in systemic lupus erythematosus. Q J Med 1984;53:401–409.

3. Yoon JU, Park SH, Kim EJ, et al. Two cases of autoimmune hepatitis associated with systemic lupus erythematosus. Korean J Hepatol 2003;9:231–235.

4. Chang HK, Kim SY, Park YS. A case of autoimmune hepatitis associated with systemic lupus erythematosus. J Korean Rheum Assoc 2000;7:410–414.
5. Park KT, Kim KY, Kim IY, et al. A case of autoimmune hepatitis accompanied by systemic lupus erythematosus. Korean J Med 2007;72:160–163.
6. Johnson PJ, McFarlane IG. Meeting report: International Autoimmune Hepatitis Group. Hepatology 1993;18:998–1005.


7. Hochberg MC. Updating the American College of Rheumatology revised criteria for the classification of systemic lupus erythematosus. Arthritis Rheum 1997;40:1725.


8. Oka H. The survey of autoimmune hepatitis in Japan. Annual report of the study group on severe hepatitis. Japanese Ministry of Health and Welfare 1988;235–241.
9. Chowdhary VR, Crowson CS, Poterucha JJ, Moder KG. Liver involvement in systemic lupus erythematosus : case review of 40 patients. J Rheumatol 2008;35:2159–2164.


10. Obermayer-Straub P, Strassburg CP, Manns MP. Autoimmne hepatitis. J Hepatol 2000;32(1 Suppl):S181–S197.


11. Kaw R, Gota C, Bennett A, Barnes D, Calabrese L. Lupus-related hepatitis: complication of lupus or autoimmune association? Case report and review of the literature. Dig Dis Sci 2006;51:813–818.


12. Usta Y, Gurakan F, Akcoren Z, Ozen S. An overlap syndrome involving autoimmune hepatitis and systemic lupus erythematosus in childhood. World J Gastroenterol 2007;13:2764–2767.

13. Malnick S, Melzer E, Sokolowski N, Basevitz A. The involvement of the liver in systemic diseases. J Clin Gastroenterol 2008;42:69–80.


14. Elkon KB, Parnassa AP, Foster CL. Lupus antoantibodies target ribosomoal P proteins. J Exp Med 1985;162:459–471.



15. Hulsey M, Goldstein R, Scully L, Surbeck W, Reichlin M. Anti-ribosomal P antibodies in systemic lupus erythematosus: a case-control study correlating hepatic and renal disease. Clin Immunol Immunopathol 1995;74:252–256.


16. Bonfa E, Golombek SJ, Kaufman LD, et al. Association between lupus psychosis and anti-ribosomal P protein antibodies. N Engl J Med 1987;317:265–271.


17. Teh LS, Isenberg DA. Antiribosomal P protein antibodies in systemic lupus erythematosus: a reappraisal. Arthritis Rheum 1994;37:307–315.


18. Koren E, Schnitz W, Reichlin M. Concomitant development of chronic active hepatitis and antibodies to ribosomal P proteins in a patient with systemic lupus erythematosus. Arthritis Rheum 1993;36:1325–1328.

(A) Liver biopsy shows predominantly lobular inflammation, including mild focal necrosis and fatty change. Piecemeal necrosis is not noted in portal areas (H&E stain, ×200). (B) Liver biopsy shows mild portal inflammation and expansion of portal spaces by inflammatory cells with fibrosis (light green staining) (Masson’s trichrome stain, ×100).
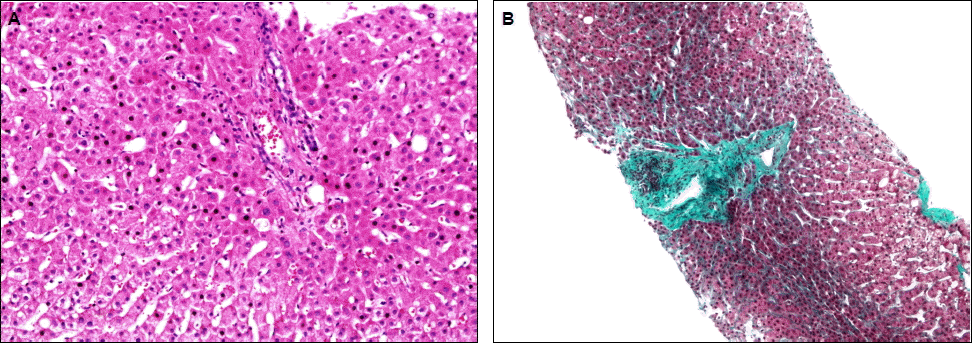
Figure 1.
Table 1.
| Clinical Feature | Admission in 2007 | Admission in 2009 |
|---|---|---|
| Female gender | +2 | +2 |
| ALP:AST ratio | 0 | +2 |
| +2: < 1.5 | ||
| +0: 1.5~3.0 | ||
| -2: > 3.0 | ||
| Serum globulin or IgG above normal | ||
| +3: > 2.0 | +2 | +1 |
| +2: 1.0~1.5 | ||
| +1: < 1.0 | ||
| ANA, SMA, LKM-1 | +3 (ANA, SMA) | +3 (ANA) |
| +3: > 1:80 | ||
| Illicit drug use history | -4 | +1 |
| -4: Positive | ||
| +1: Negative | ||
| Average alcohol intake | +2 | +2 |
| +2: < 25 g/d | ||
| Histological findingb) | -5 | |
| Other autoimmune disease | +2 | +2 |
| Hepatitis viral markers | +3 | +3 |
| +3: Negative | ||
|
|
||
| Total scorec) | 10 | 7 |
a) Scoring system for autoimmune hepatitis defined by the International Autoimmune Group [6].
- TOOLS
-
 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link XML Download
XML Download Full text via DOI
Full text via DOI-
 Download Citation
Download Citation
 Print
Print-
Share :








