체액량 평가와 수액요법: 실제적인 면 중심으로
Evaluation and Management of Volume Status: A Practical View
Article information
Trans Abstract
Objective, rapid, and accurate assessment of volume status is important in the early management of acute, critical illnesses, as inappropriate therapy may lead to interventions with fatal outcomes. Traditionally, the history and physical examinations have been used for this assessment, but have limitations. Radioisotopic measurement or invasive hemodynamic monitoring is impractical, complicated, and expensive. Recently developed technologies offer rapid, accurate estimation of volume status with the potential to improve clinical outcome. This review discusses the methods available for volume assessment, including ultrasound, bioimpedance, and the historical tools. (Korean J Med 2011;80:1-7)
서 론
체액량이 과다 혹은 부족한 환자의 증상은 매우 다양하면서도 복잡하다. 경우에 따라서는 부종은 심하지만, 순환 혈류량은 감소한 복합한 장애를 보일 수도 있어 이를 평가하는 것은 중요하지만, 쉽지 않은 진단작업이다. Wuerz와 Meador가 시행한 연구를 보면, 급성 심부전악화가 의심되는 환자를 정해진 알고리듬에 따라 구급차 후송 이전에 미리 진단하고, furosemide, nitroglycerin, morphin 등의 응급처치를 미리 투여하도록 프로토콜을 만들어 그 효과를 평가하였다[1]. 최종적으로 심부전으로 확인된 환자 중 48%는 이러한 초기치료로 생존율이 2.5배 증가하였으나, 심부전이 아니었으나 심부전으로 분류되어 초기치료를 받은 환자의 경우 오히려 사망률이 3.6배 증가하였다. 이와 같이 초기 환자의 체액량 평가가 이후 진행되는 치료와 독립적으로 중요하다는 것을 알 수 있다.
체액량 평가 방법 중 혈액량 평가의 절대적 표준검사는 적혈구 혹은 알부민에 방사성 동위원소 표지자를 붙여 측정하는 방법들이 있으나, 이를 임상에서 이용하는 것은 어렵고, 신속하지 않으며, 경제적 비용 문제가 있다. 본론에서는 흔히 임상에서 적용하고 있는 전통적인 체액량 평가 방법에 대한 평가와 최근 발전하고 있는 기기들의 임상활용방안 그리고 평가를 토대로 수액요법을 시행할 때 고려해야 할 원칙들에 대해 언급하고자 한다.
체액량 평가
1. 병력 청취
병력 및 신체검진으로 체액량 과다를 진단할 때, 그 정확도와 신뢰도를 평가한 연구가 최근에 있었다(표 1)[2]. 1966년부터 2005년까지 18개 연구를 메타분석한 연구에서 환자가 호소하는 증상 및 신체검진을 통해 얻은 소견을 통해 체액과다 여부를 평가한 것이다. 증상 중에서 운동 시 호흡곤란이 가장 민감한 지표였고, 발작성 야간 호흡곤란이 특이도가 가장 높은 지표였다[2]. 그 외 좌위호흡(orthopnea), 부종이 체액과다의 특이적인 지표였다. 이러한 증상은 특히 심부전으로 인한 체액과다를 진단할 때 반드시 확인해야 한다. 반대로 체액량 감소의 경우는 Gross 등이 평가한 38개의 임상지표들 중에서 다음의 지표가 체액량 감소와 유의한 관련성을 보였다: 설건조증(tongue dryness), 세로 균열혀(longitudinal tongue furrows), 구강점막 건조, 상체 근위약감, 혼동(confusion), 언어장애(speech difficulty), 눈주위 함몰(sunken eyes)[3]. 갈증은 탈수의 정도와 큰 관련성은 없었다.
기립성 증상 혹은 저혈압도 저혈량 상태를 나타낼 수 있다. 간혹 심부전, 신경계 장애 혹은 혈관확장을 초래하는 상황에서 감별이 필요한 경우도 있다. 기립성 증상은 어지러움증, 호흡곤란, 위약감, 쇠약감 등이 가능하고, 심한 경우, 실신하기도 한다. 이런 증상은 서있을 때 악화되고, 누운 상태에서 호전되는 특징이 있어야 한다.
2. 신체검진
신체검진 역시 체액량을 평가할 때 매우 유용하다. 폐음, 말초 부종, 경정맥 확대(jugular venous distention, JVD), 간-목 반사(hepatojugular reflux, HJR) 및 비정상적 심음등의 소견이 체액과다를 시사한다. 특히 JVD는 우심방압의 증가와 유의한 관련을 가지고 있다[4]. 폐모세혈관쐐기압(pulmonary capillary wedge pressure, PCWP)>18 mmHg를 체액량 과다로 정의한 경우, JVD와 HJR 검진의 정확성이 81% 이상이었다[5]. 폐음의 경우, 체액과다를 예측하는 양성 예측도가 100%에 이르렀지만, 음성예측도는 35%에 불과하였다[6]. 한편, 심박출량이 낮은 만성적인 심부전 환자를 대상으로 한 전향적 연구에서는 폐음, 부종, JVD 증가 소견이 PCWP가 증가한 환자의 절반에서 관찰되지 않은 결과도 있어 대상 환자에 따라 신체검진 지표의 해석에 주의가 필요하다[7].
구토, 설사, 경구 섭취 감소 등의 저혈량 환자에서 액와부 건조가 양성 예측도 2.8배 높았고(2.8; 95% 신뢰구간, 1.4~5.4), 젖은 구강점막, 균열없는 혀(tongue without furrows)는 음성예측도가 높았다(0.3 95% 신뢰구간, 0.1~0.6)[8]. 피부반점형성(skin mottling)은 심부전으로 인한 말초 순환 장애를 나타내는 징후로서, 입원 환자의 경우 17.5배의 높은 사망률을 나타내는 지표이다[9].
3. 기립성 생체징후 및 심음
기립성 생체징후는 맥박과 혈압의 자세에 따른 변화를 평가하는 방법이다. 쉽게 측정할 수 있고, 신속하게 수행할 수 있고, 침습적이지도 않다. 정확도를 높이기 위해서는 최소 3분 이상 누운 상태에서 기저의 맥박과 혈압을 측정한 다음, 3분 동안 일어선 자세를 유지하고 맥박과 혈압을 다시 측정한다. 이때 혈압의 10 mmHg 이상 감소, 맥박의 20/분 이상 증가한 경우, 유의한 것으로 판정한다.
오랫동안 저혈량의 지표로 널리 사용되었던 이 지표의 정확성에 대한 연구결과는 다소 의외이다. 132명의 정상 체액량 환자를 측정하였을 때, 맥박의 변화는 -5에서 +39/분이었고, 수축기 혈압 변화는 -20에서 +26 mmHg였다[10]. 앞서 언급한 기준으로 판정하자면 43% 환자에서 위양성을 보였다. 502명의 노인을 대상으로 한 연구에서 하루 3회 위의 지표를 시행하였을 때 68% 환자에서 하루 한 번 이상 양성의 소견을 보였다. 하지만, 검사 시간에 따른 결과의 재현성이 낮았고, 저녁 이후는 오히려 기립성 저혈압의 유병률이 떨어졌다. 이러한 결과는 기립성 생체징후를 판정할 때 반복적인 측정으로 신중하게 판단해야 함을 시사한다[11].
출혈이 의심되는 환자를 대상으로 한 기립성 생체징후 평가에 관한 연구에서 기립성 어지러움증, 기립 시 맥박 30/분 이상 증가 등은 매우 유용한 지표였다. 하지만, 소량의 혈액소실이 의심되는 경우, 기립성 생체징후의 예측력은 22%에 불과하였다. 1 L 이상의 혈액소실이 있을 때는 기립성 생체징후의 민감도 및 특이도는 각각 97%, 98%이었고, 이는 누운 상태에서 측정한 저혈압 및 빈맥에 비해서는 월등히 우수한 정확성을 보였다[8].
심음은 체액량 과다를 진단할 때 흔히 확인하는 검사이다. 제 3심음(S3)은 충만압(filling pressure)이 증가하였을 때 순응도(compliance)가 나쁜 심실에서 급속 충만 시 발생하는 심음이다. 이것은 심실기능장애 및 좌심실 충만압의 증가에 매우 특이적인 지표로서, 심부전에서 나쁜 예후인자이며, JVD와 함께 고려한 경우 심부전으로 인한 입원율 및 사망률 등을 예측하는 인자이다[12]. 그러나 높은 양성 예측도에 비해 음성예측도는 유의하지 않으며[2], 특히, 만성 폐색성 폐질환, 비만 등의 질환이 동반되어 있을 때는 민감도가 떨어진다.
4. 추가 검사를 이용한 체액량 평가방법
이상과 같은 병력 및 신체검진은 초기 진단에 매우 중요한 방법이긴 하지만, 정확성에 있어서 많은 제한점이 있다. 특히, 심부전이나 패혈증 등이 동반되어 있는 경우 체액량을 정확히 평가하는 것은 더욱 어려울 수 있어 보다 객관적인 지표에 대한 방법이 요구되고 있다.
1) 흉부 방사선 촬영
전통적으로 흉부 방사선 촬영은 환자의 체액량 평가를 위해 가장 먼저 시행하는 검사 중 하나이다. 체액량 감소에서는 유용성이 떨어지지만, 체액량 과다의 경우 매우 유용하다. 상엽혈관의 확장(dilated upper lobe vessels), 심비대, 간질부종, 폐동맥 확장, 흉막삼출액, 폐포 부종, 상대정맥 돌출, Kerley선 등은 매우 특이적인 징후이다[13]. 이러한 방사선학적 소견들은 체액량 과다의 정도가 심할수록 보다 많은 소견을 관찰할 수 있다. 심비대 소견 또한 심부전이 의심되는 환자에서 심-흉곽비 소견이 유용할 수 있는데, 심-흉곽 비가 60% 이상인 경우 5년 사망률이 증가하였다[14].
하지만, 방사선 촬영에서 이상소견과 임상적인 효과 간에 수시간의 지연이 있을 수 있어 치료반응을 평가할 때 주의해야 한다. 또한, 방사선촬영결과가 정상이더라도 좌심실 기능이상을 완전히 배제할 수 없다. 심장이 흉곽 내에서 회전된 경우, 심비대가 있어도 심-흉곽 비가 정상으로 보일 수 있고, 심초음파 연구에 따르면 이러한 경우가 약 22%에서 보고되었다[15]. 흉부 방사선 촬영을 할 때 환자의 상태나 검사법에 따라서도 정확도에 차이를 보일 수 있다. 방사선 촬영을 이동식으로(portably) 하였을 때, 체액량과다의 민감도는 현격히 떨어진다. 환자가 기관삽관 상태로 누워있다면, 흉수가 발견되지 않을 수도 있다. 요약하면, 흉부 방사선 촬영은 체액량 과다를 진단할 때 유용하고 흔히 사용할 수 있으나, 체액량 부족 시 혹은 경도의 체액량 과다 등의 경우 민감도가 떨어질 수 있다.
2) 나트륨이뇨 펩티드(Natriuretic peptide, NP)
뇌 나트륨이뇨 펩티드(BNP), N-말단 proBNP, 심방 나트륨이뇨 펩티드는 심근 스트레스가 있을 때 상승하고, 체액과다에서도 증가한다. 특히 NP 값이 감소한 경우, 심부전을 배제하기 위한 음성 예측력이 매우 뛰어나다. 하지만 체액증가와 무관한 심근 스트레스의 원인은 매우 많기 때문에 NP의 상승은 임상상과 함께 해석해야 한다. 또한 비만(NP의 감소와 관련), 신부전(NP의 증가와 관련)에서도 해석에 유의해야 하고, 환자의 체액량 상태가 변함에 따라 NP 값도 변화하므로 해석에 주의가 필요하다.
3) 생체 임피던스 분석(Bioimpedance analysis, BIA)
전신 임피던스는 세포내 및 세포외를 모두 통과하는 전류에 대한 저항 R 값과 세포막과 조직 경계면에 의해 생성되는 용량(capacitance, Xc) 값의 조합으로 구성된다. 이러한 차이를 이용하여 체액량을 측정할 수 있는데, 그 오차는 2~4%이내이다[16].
BIA는 여러 체액상태(간 질환, 신장 질환, 심장 질환 등)에서 타당성에 관한 연구가 진행되었고, 이를 통해 3,000명 이상의 혈액투석 환자 연구에서 연조직 수분상태에 따른 사망률의 예측력을 보여주었다[17]. 또한, 292명을 대상으로 한 전향적 연구에서는 BIA와 BNP를 함께 측정한 경우 환자의 체액량 상태를 보다 정확하게 예측할 수 있음을 보여주었다[18]. 인공신장센터, 중환자실, 응급실, 심장센터 등 다양한 영역에서 적용가능하며, 이에 근거한 수액요법에 대한 연구들이 진행 중에 있다. 하지만, BIA를 통해 심장 내 혹은 흉곽 내, 복수 등 구획별 체액량을 예측할 수는 없고, 서구 유럽인을 대상으로 표준화가 이루어졌기 때문에 추후에 보다 많은 연구가 필요하다.
4) 초음파 검사
흉곽 초음파는 폐내 수분을 측정할 수 있다. B-라인으로 알려진 인공음영(artifact)은 간질의 비후 혹은 체액-충만 폐포(alveoli)를 시사하며[19], PCWP 혹은 혈관외 폐 수분 증가와 연관성을 보인다[20]. 초음파를 통한 하대정맥 직경측정도 체액량 평가에 이용할 수 있다. 450 mL의 헌혈자 및 혈액투석 환자를 대상으로 한 연구에서 하대정맥 직경이 혈액 및 체액량의 변화를 반영하는 것으로 알려졌다[21,22].
5) 기타
혈액량 측정의 절대적 표준방법은 방사면역측정법에 의한 객관적 혈액량 측정 방법이 있지만, 이것은 측정시간이 오래 걸리고, 방사선 검사를 위해 환자를 옮겨야 하는 불편함이 있어 임상에 적용하기엔 무리가 있다. 음향 심장검사법(acoustic cardiography)은 마이크로폰 심전도 유도(lead)를 통해 심음을 디지털로 기록하는 기술로서 제 3심음을 발견하는데, 유용할 수 있으나, 민감도가 떨어지는 것으로 보고되었다[23].
혈역학적 상태를 평가하기 위한 전통적인 방법은 심장가까이 도관을 삽입하는 침습적인 방법이었는데, 최근 비침습적인 방법으로 개발된 방법들 중 impedance cardiography (ICG)가 있다[24]. ICG 측정은 고주파 전류가 흉곽을 통해 흐르고 이때 측정한 임피던스를 통해 흉곽의 폐포 내와 간질내 체액량 변화를 감지한다. 심전도와 함께 얻어진 시간별 측정값의 변화를 통해 얻어진 심박출량은 thermodilution 기법과 같이 침습적인 방법을 통해 얻은 값과 비교해 비교할 만하다. 연속적인 측정이 가능하고 재현성이 뛰어나다.
체액량 평가의 실제
1. 체액량 감소
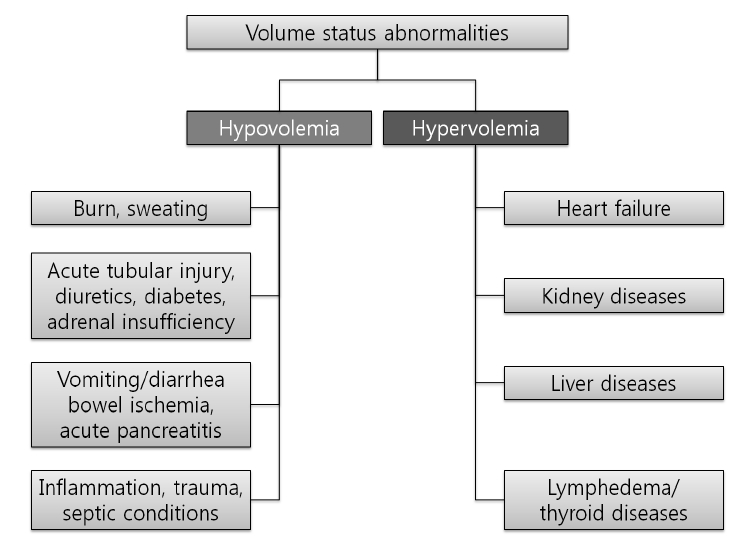
체액량 감소의 원인은 신장 소실과 신장외 소실로 구분해볼 수 있다. 신장 소실은 경우는 이뇨제 사용, 염분 소실 신증, 염류 코르티코이드 결핍, 급성 세뇨관 괴사에서 삼투성이뇨 등을 통한 염분의 신장소실이 가능하고, 신장외 소실은 위장관, 호흡기, 피부, 발열, 패혈증을 통한 소실 혹은 체액축적(third space accumulation) 등이 원인일 수 있다(그림 1). 체액량 감소의 증거는 먼저 병력 및 신체검진에서 찾아볼 수 있다. 증상은 대개 비특이적인데, 갈증, 피로, 위약감, 근육 경련, 기립성 어지러움증 등이 나타날 수 있다. 또한 경정맥압 저하, 기립성 저혈압 혹은 빈맥 등을 확인할 수 있다. 피부 긴장도 감소, 및 구강 점막 감소는 간질액 감소의 지표이다. 보다 많은 체액이 손실되었다면, 혈관내 체액량 감소로 인한 장기의 관류장애를 시사하는 소견(의식저하, 핍뇨, 말초 청색증 등) 혹은 보상적 기전에 의한 증상(빈맥, 빈호흡, 발한, 털 세움 등)이 쇽의 증상으로 나타날 수 있다.
요 삼투압 증가, 요 소디움 감소, 체액감소로 인한 알칼리증 등이 나타날 수 있으나, 손실된 체액의 성분 혹은 체액소실의 원인 질환에 따라 다양하게 보일 수도 있다. 높은 혈청 소디움 값은 체내 소디움 양을 반영하기보다 대부분 수분결핍을 반영한다. 상대적으로 혈색소의 증가 및 알부민 농도의 증가 등도 보일 수 있다.
체액 감소량을 정확히 측정하기 어려우므로 치료는 대부분 경험적으로 진행한다. 먼저 치료의 목표는 혈관내 체액량을 등장성 수액으로 보충하고, 이후 체내 수분 균형을 회복시키는 것이다. 생리 식염수(0.9% NaCl)를 초기에 처방하는데, 특히 저혈압 혹은 쇽이 있을 때는 더욱 그러하다. 투여한 수액의 1/3~1/4가 혈관 내 분포하고, 나머지는 간질액으로 이동하므로, 치료도중 체액량 상태를 자주 확인해 봐야 한다. 추천되는 방법 중 한 가지 안전한 방법을 예로 들자면, 등장액 1~2 L를 체액량 결핍 정도에 따라 정맥내 대량주입(bolus)으로 투여한 이후 체액량 평가를 다시 하고, 이러한 주기를 반복해서 수액을 투여하는 것이다. 특히 경정맥 확장 등 우심부전이 의심되거나 심근경색이 의심되는 경우에는 한번에 투여하는 수액을 250~500 mL 정도의 작은 양으로 시작하는 것도 유용할 수 있다[25].
2. 체액량 증가
체액량 증가를 일으키는 원인은 심부전, 콩팥 질환, 간질환, 악성 림프부종, 갑상선 질환 등이 있다(그림 1). 특히, 심부전 환자에서 호흡곤란이 있는 경우 병력과 신체검진을 통해먼저 체액량을 평가한다. 좌위호흡은 모세혈관 쐐기압의 상승을 반영하는 민감도 및 특이도가 높은 증상이다[7]. 말초부종은 비보상성 심부전 환자의 50%에서 동반한다. 교대맥(pulsus alterans)는 좌심부전이 있을 때 나타날 수 있다. 폐수포음은 새로 발생한 심부전 혹은 울혈성 심부전에서 충만압(filling pressure)의 급격한 상승을 나타낸다. 폐동맥압 상승으로 제 2심음 (폐부분)이 증가하고, 제 3심음 심실성 갤럽이 나타난다[26]. 경정맥 확장과 복부-경부 반사도 보일 수 있다.
혈액검사, 소디움, 포타시움, 혈당, 혈액요소질소, 크레아티닌, 트로포닌 I, 동맥혈 가스검사를 시행할 수 있다. 나트륨이뇨펩티드는 특히 100~400 pg/mL 이하로 감소하였을 때, 음성 예측력이 뛰어나며, 충만압의 변화와 높은 연관성을 보인다[27]. 흉부 방사선 촬영은 신속하게 수행 가능하지만, 심부전 환자의 20% 가까이에서 위음성을 보일 수 있다[28]. 기관지주위 둘러쌈(peribronchial cuffing, peribronchial thickening or bronchial wall thickening)이 있는 경우 심부전의 특이도가 특히 높다[29]. 흉부 초음파가 일반 방사선 촬영보다 흉막삼출 진단이 훨씬 민감해서 100 mL 이하의 양도 측정 가능하다[30]. 하대정맥의 확장이 제한된 경우, 체액량 과다를 시사할 수 있다. 호흡에 따른 변화가 15% 이내인 경우를 기준을 할 때, 심부전 진단의 민감도 92%, 특이도 84%에 다다른다. 하대정맥의 직경 10 mm라는 기준을 추가하면 특이도가 91%로 상승한다[31]. 폐동맥 도관 삽입 시 심박출량과 충만압을 측정할 수 있어서 혈역학적으로 불안정한 환자, 울혈과 저관류가 공존하는 환자, 체액량 상태가 불분명한 환자 등에서 시도해 볼 수 있다[32]. 비침습적인 방법으로 BIA를 통해 체질량 및 수분 구성을 평가해 볼 수 있다. 이것은 체액량 이상이 의심되는 환자에게서 매우 중요할 수 있다. 예를 들어 심부전 환자에서 체질량을 고려하지 않고 체중만 고려한 경우는 영양부족으로 인해 근육 혹은 지방질량이 감소한 경우는 필요 이상의 체액을 줄일 위험이 있다. 실제로, 심부전으로 인해 체액량 과다인 환자에서 BIA에서 측정한 저항값(resistance)이 BNP 값 및 New York Heart Association 호흡곤란 단계와 유의한 연관성을 보였고, 임피던스와 중심정맥압 사이에도 유의한 연관성을 보고한 연구가 있다[33]. BIA의 치료반응 평가를 위한 연구를 한 예로 들면, 심부전 악화로 내원한 환자에서 이뇨제 치료로 수액량을 조절한 환자에서 초기, 24시간, 72시간째 정기적으로 BNP 값, BIA 및 초음파로 측정한 caval index와 vascular pedicle width 등을 측정하였을 때, 치료를 통해 환자가 호전되었을 때 모든 지표가 정상화되는 것을 관찰하였다[34].
전신적 체액 과다의 증거가 명백한 경우 이뇨제를 투여해볼 수 있다. Furosemide 20~40 mg 정맥주사를 초기 처방으로 추천할 수 있다[32]. 신장 기능, 수축기 혈압, 이전의 이뇨제 사용병력 등에 따라서 용량은 조절해 볼 수 있다. 하지만, 신기능의 저하가 우려될 수 있기 때문에 초기부터 고용량을 사용하는 것은 주의가 필요하다. 폐부종이 있고, 수축기 혈압이 140 mmHg 이상인 경우, 흔히 정상 체액량 혹은 체액량 감소인 경우가 있으므로(예를 들어, 실제로 체액량 과다는 아니지만, 이완기 장애로 인해 전신 체액의 재분포가 일어난 경우) 이뇨제를 사용하는 대신 nitrates와 같은 혈관확장제로 치료해 볼 수도 있다.
결 론
체액량을 객관적이고 신속하면서도 정확하게 평가하는 것은 매우 중요하다. 특히 환자의 상태가 위급하고 불안정할 때, 체액량 평가에서 오류를 범하는 것은 환자에게 치명적일 수 있다. 전통적으로 병력, 신체검진을 비롯하여 간단한 생화학적 혹은 방사선학적 검사들이 체액량 평가를 위해 시행되어 왔지만, 제한점이 있었다. 최근의 기술적인 발전으로 초음파 및 BIA 등 간편하면서도 정확성을 높인 진단기구들이 개발되어 임상적인 효율성에 대한 연구들이 보고되고 있다.