서 론
Sirolimus는 mTOR (mammalian target of rapamycin) inhibitor로 calcineurin inhibitor보다 신독성과 이식 후 종양발생이 적고 피부에 발생한 카포시 육종을 치료하는 효과가 있어 calcineurin inhibitor의 대체 면역억제제로 부각되고 있다1). 그러나 sirolimus의 투여로 인한 부작용으로 백혈구 감소증, 혈소판 감소증, 고지혈증, 수술부위의 창상지연 등 또한 보고되고 있다2).
이 중 sirolimus-induced pneumonitis는 Mahalati 등에 의해 2000년에 처음 보고되었으며3), intersticial pneumonitis, bronchitis obliterans, organizing pneumonia, alveolar proteinosis 등의 형태로 보고되고 있다4). 아직 국내에서는 sirolimus가 보험적용을 받지 못하여 일부 환자에게만 제한적으로 투여되고 있어 sirolimus에 의한 폐렴이 보고된 적이 없다. 이에 저자들은 51세 남자가 신장 이식 후 3개월간 sirolimus를 복용한 후에 발생한 폐렴을 경험하였기에 문헌고찰과 함께 보고하는 바이다.
증 례
환 자: 51세, 남자
주 소: 기침, 객담
현병력: 신세포암으로 우측신절제술을 시행한 자로, 이후발생한 신기능 악화로 2004년 9월부터 혈액투석을 시행하였고, 2006년에 부인으로부터 신장을 받아 이식했으며, HLA 불일치는 4/6였다. 내원 한 달 전부터 시작된 기침, 객담과 3주 전부터 시작된 열감을 주소로 내원하였다.
과거력 및 투약력: 환자는 신이식 후 면역억제제로 tacrolimus, deflazacort, mycophenolic acid를 사용하던 중 혈중크레이아틴 수치 상승 소견을 보여 2008년 8월 신장 조직검사를 시행하였고, 이때 chronic allograft nephropathy (CAN) grade 1 소견이 확인되었다. CAN은 이식신장 기능상실의 주요한 원인이며, calcineurin inhibitor toxicity와 관계있는 것으로 알려져 있어, tacrolimus를 중단하고 2008년 9월 4일부터 sirolimus를 2 mg/day로 복용을 시작하여, 혈중농도를 확인하면서 증량하였고, 내원 당시에 sirolimus 5 mg, deflazacort 6 mg, mycophenolic acid 1,000 mg을 복용 중이었다
신체검진 소견: 내원시 활력징후는 혈압 148/84 mmHg, 맥박 117회/분, 호흡수 20회/분, 체온 36.6℃였고, 급성 병색을 보이고 있었다. 두경부 소견상 임파선 종대나 인후 발적 소견은 보이지 않았다. 흉부검사 소견상 양측 폐부에서 악설음이 청진되었으며, 심음은 정상이었다. 복부검사소견상 이식신부위의 압통이나 반발통은 없었다.
검사실 소견: 혈액검사상 백혈구 5,760/μL (호중구 58.7%, 호산구 9.2%, 림프구 21.7%), 혈색소 10.0 g/dL 혈소판 188,000/μL 로 확인되었으며 동맥혈검사상 pH 7.42, pCO2 27.7 mmHg, paO2 105 mmHg, HCO3 17.9 mEq/L로 확인되었고, 생화학검사상 CRP 7.35, 크레아티닌 2.11 mg/dL이었고, 그 밖의 생화학적검사와 전해질검사, 소변검사는 정상 범위였다. 내원시 확인한 sirolimus level은 8.6 ng/mL이었고, 환자 혈청학적 검사상에서 cytomegalo virus RT PCR (-), BK virus RT PCR (-), mycoplasma IgM (-), legionella Ag (-)로 확인되었다.
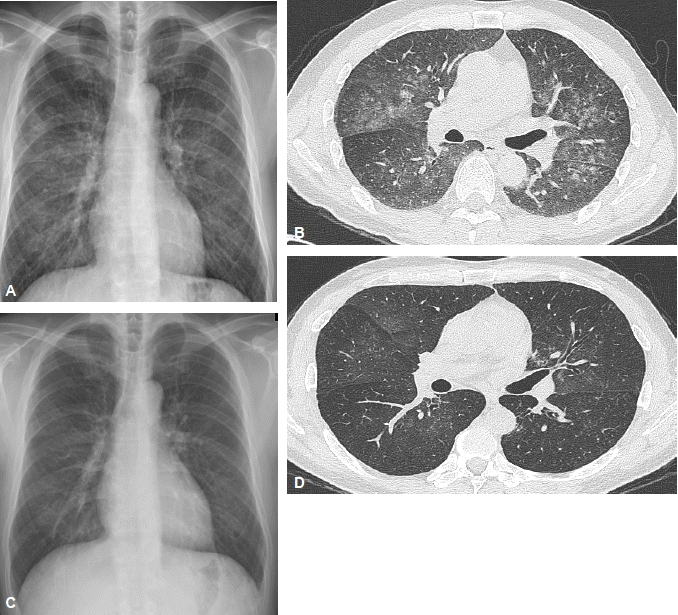
방사선학적 소견: 내원시 확인한 단순흉부사진(그림 1A)상 젖빛 유리 모양 음영이 다발성으로 양측 중하엽에서 확인되었다. 흉부고해상도 전산화단층촬영(HRCT) (그림 1B)상, 다발성 젖빛 유리 모양 음영이 양측 폐엽에서 기관지를 따라 분포된 양상이었다.
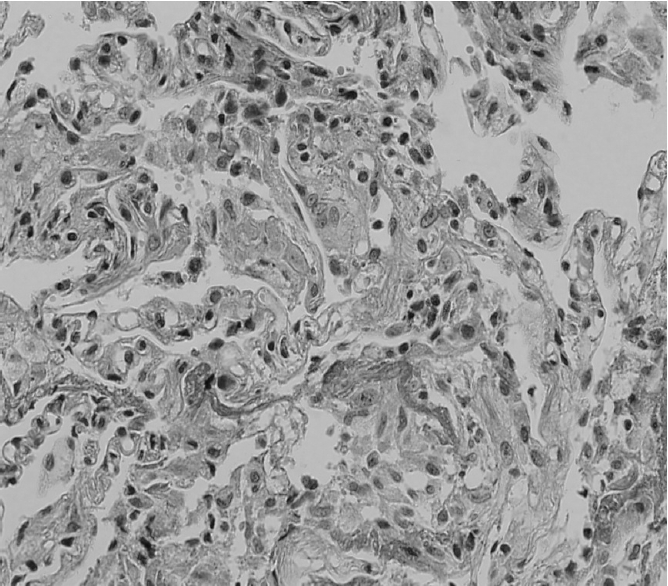
기관지내시경: 환자 내원 다음날 기관지 내시경으로 기관지폐포세척술, 경기관지폐생검을 시행하였다. 기관지폐포세척술 소견(그림 2)상으로는 림프구와 대식세포 일부가 관찰되었고, methenamine silver, PAS, Ziehl-Neelsen 염색 검사상에서 세균감염원이 확인되지 않았고, candida, aspergillosis, pneumocystis carini 등의 진균감염도 확인되지 않았다. 경기관지폐생검 소견은 섬유성 삼출액의 침윤과 함께 호산구와 비반 세포를 폐포내에서 관찰할 수 있었다.
치료 및 임상경과: 환자 내원시 확인한 방사선학적 소견상 바이러스성 폐렴, 폐포자충 폐렴 의심하에 gancyclovir와 bactrim을 2병일부터 투여하였다. 그러나 sirolimus를 3개월전부터 사용한 과거력이 있고, 한 달 전부터 증상이 병발한 자로, 이후로 감염 증거가 확인되지 않았고, 호흡기 증상과 방사선학적 이상 소견을 보이고 있어, sirolimus induced pneumonitis 의심하에 3병일째부터 sirolimus 중단하고 tacrolimus를 2.5 mg bid로 투여하면서 동시에 Methylprednisolone 250 mg을 bid로 투여하였다. 이후로 환자의 임상증상 빠르게 호전되었고, 6병일째 추적관찰한 흉부 고해상도 전산화 단층촬영(그림 1D)상에서 이전과 비교하여 다발성 젖빛 유리 모양 음영이 현저히 감소함을 확인할 수 있었다. 환자 7병일째 prednisolone 30 mg, tacrolimus 2.5 mg bid, mycophenolic acid 1,000 mg으로 유지하면서 퇴원하였다. 일주일 후 외래 추적관찰상 증상 대부분 회복되고 단순 흉부사진상(그림 1C)에서 상당한 호전 소견 보이고 있었다.
고 찰
본 증례는 sirolimus를 복용하던 중 객담, 기침과 고열을 동반한 이식환자에서 폐렴소견을 보였으며 기관지경검사와 미생물검사를 통하여 특별한 원인균을 동정할 수 없었고, sirolimus의 투여 중지와 스테로이드 투여로 폐렴이 호전되어 sirolimus에 의한 폐렴으로 진단내렸던 증례이다. 신장 이식 환자에서 호흡기 증세가 있고 단순 흉부사진에서 폐렴이 진단될 경우, 세균, 바이러스, 진균 등의 기회감염의 가능성을 먼저 고려해 볼 수 있겠으나 siolimus를 복용하는 환자에서 상기 증세와 방사선학적 소견을 보일 때 한번쯤은 약제에 의한 폐렴의 가능성을 고려하는 것이 임상적으로 중요하다.
Siromuls에 의한 폐렴의 발생율을 종합하면 5~11%이며 발생시기는 투여 후 1~51개월 사이로 알려져 있다. Weiner 등1)에 의하면, 신이식이나 췌장이식 후 sirolimus를 사용하는 환자 115명을 대상으로 한 연구에서 13명에서 pneumonitis가 발생하여 9.6%의 발생율을 보였고, 발생시기는 약제 투여 후 1~8개월 사이로 확인되었다. 본 증례의 경우 sirolimus를 투여하고 있는 11명의 환자 중 1명에서 발생하여 언급된 것과 비슷한 발생율을 보였다.
지금까지 sirolimus에 의한 폐렴의 위험 인자는 명확하게 정립되지 않았지만, 고령, 남성, 약제의 고용량, 신이식 후 지연된 약제의 사용 등이 고려되고 있다5,6). 위 위험인자와 함께 일부 보고에서는 폐렴 발생률의 증가는 신기능의 저하와 관련있을 것으로 추정하고 있다. 즉, Weiner 등의 연구에서는 폐렴이 발생한 모든 환자들에서 상당한 신기능 저하가 동반되고 있음이 확인되었고, 본 증례의 환자에서도 혈중 크레아티닌이 2.11 mg/dL로 증가되어 있었음을 확인할 수 있었다. 이러한 신기능의 저하가 sirolimus에 의한 폐렴발생의 위험 인자인지, 아니면 단순한 sirolimus 사용 환자군의 특징적 소견인지 구분되지 않지만, calcineurin inhibitor에서 sirolimus로 바꾸는 주요 원인중의 하나가 신독성에 의한 신기능저하임을 고려할 때, 신기능 저하 환자에서의 sirolimus 사용에 있어서 앞으로 좀더 심도있는 연구와 주의가 필요하다고 하겠다.
Sirolimus에 의한 폐렴의 임상증상은 다양하지만, 현재까지 보고된 내용을 종합하면 발열이 73%로 가장 많았고 그 다음이 호흡곤란과 기침 순이었다1). 본 증례의 경우 한 달 가량의 호흡기 증세가 있었고, 미열이 3주 동안 지속되었다. 본 증례의 특징적인 것으로 일반적으로 이식환자에서 발생하는 폐렴에 비하여, 단순 흉부사진 소견에 비해 증세가 경미했다는 것을 들 수 있겠다.
진단에 있어 가장 중요한 점은 먼저 sirolimus에 대한 폐렴의 가능성을 염두에 두는 것이다. 즉, sirolimus를 사용 중인 환자에서 발열이나 호흡기 증상이 발현되었으나 명확한 감염원이 밝혀지지 않을 때 반드시 이 질환을 고려해 보아야 한다. Morelon 등은 진단기준을 다음과 같이 정하였다7). 첫째, 호흡기증상이 나타나기 전에 sirolimus의 사용이 선행되어야 한다. 둘째, 감염이나 다른 약제(azathioprine, β-blockers, ACE inhibitor, fibrates, sulfamethoxazole, trimethoprim) 등에 의한 호흡기 질환이 배제되어야 한다(이러한 약제를 계속 사용하면서 임상적 호전이 이루어져야 한다). 셋째, sirolimus를 중단한 후에 질환의 회복이 있어야 한다. 넷째, 병리학적 소견상에서 림프구의 폐포 침윤이 확인되어야 한다. 본 증례에서도 증상 발현 2개월 전부터 환자가 sirolimus를 복용하였고, 기관지 내시경과 혈액 검사를 통하여 감염 질환을 배제진단하는 한편, 병리학적으로 림프구의 폐포 침윤을 확인하였고, sirolimus를 중단한 후에 질병의 회복을 관찰할 수 있어서 진단기준에 합당하였다고 할 수 있겠다.
현재까지 sirolimus에 의한 폐렴의 발생 기전은 명확히 밝혀지지 않았다. 폐렴의 인체에 대한 상당수의 보고에서 sirolimus 혈중농도가 15 ng/mL 이상으로 확인되었고, sirolimus를 중단한 후 농도가 10 ng/mL 이하로 떨어진 뒤 증상 호전이된 결과로 보아, 직접적인 약독성과 관련있다고 판단될 수 있다. 그러나 경기관지폐생검 소견상 호산구의 상승과 비반세포의 침윤이 일부 보고에서도 확인되고 있어 sirolimus에 대한 과민반응에 의한 것으로도 추정할 수 있고7), 본 증례에서도 유사한 소견이 확인되었다. 또한 다른 보고에서는 기관지폐포세척술 상에서의 림프구 우세소견과 함께, 낮은 농도에서의 sirolimus에 의한 폐렴이 확인되고 있어 immune-mediated response 역시 배제할 수 없다. 본 증례에서도 기관지폐포세척술상에서 림프구가 확인되었고, 내원 당시 sirolimus 농도가 8.8 ng/mL로 확인되는 것은 immune-mediated response의 가능성을 시사하는 소견이라 하겠다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






