žĄú Ž°†
ž§Ďž¶Ěž≤úžčĚžĚÄ ž†Ąž≤ī ž≤úžčĚžĚė 3-10%Ž•ľ žį®žßÄŪēėžßÄŽßĆ[1,2], ž†Ąž≤ī ž≤úžčĚ ÍīÄŽ†® žĚėŽ£ĆŽĻĄžö©žĚė 60% žĚīžÉĀžĚĄ žÜĆŽ™®ŪēúŽč§[3]. žĚėŽ£ĆŽĻĄžö©žĚė ŽĆÄŽ∂ÄŽ∂ĄžĚÄ žēĹž†úŽĻĄžĚłŽćį, ž§Ďž¶Ěž≤úžčĚ ŪôėžěźžĚė ÍįúžĚłŽčĻ žĚėŽ£ĆŽĻĄžö©žĚÄ ŽčĻŽá®Ž≥ĎžĚīŽāė, ŽáĆž°łž§Ď, chronic obstructive pulmonary disease (COPD)Ž≥īŽč§ Ūõ®žĒ¨ ŽÜíŽč§[4]. ŽŅźŽßĆ žēĄŽčąŽĚľ, ž§Ďž¶Ěž≤úžčĚžóź žąėŽįėŪēėŽäĒ ž°įž†ą(control)ŽźėžßÄ žēäŽäĒ ž≤úžčĚ ž¶ĚžÉĀÍ≥ľ žě¶žĚÄ ž≤úžčĚ žēÖŪôĒŽäĒ ŪôėžěźžĚė žā∂žĚė žßąžĚĄ Žß§žöį ž†ÄŪēėžčúŪā§Í≥†, ž§Ďž¶Ěž≤úžčĚžĚė žĻėŽ£ĆŽ•ľ žúĄŪēī žā¨žö©ŪēėŽäĒ žēĹŽ¨ľ(ž†Ąžč† žä§ŪÖĆŽ°úžĚīŽďú ŽďĪ)žóź žĚėŪēú Ž∂ÄžěĎžö© žó≠žčú ŪôėžěźžóźÍ≤Ć ŪĀį Ž∂ÄŽčīžúľŽ°ú žěĎžö©ŪēúŽč§[5].
Ž≥ł Ž°†
ž§Ďž¶Ěž≤úžčĚ(severe asthma)Í≥ľ ŽāúžĻėž≤úžčĚ(difficult-to-treat asthma)žĚė ž†ēžĚė
Global iNitiative for asthma (GINA) žßÄžĻ®žóźžĄú ž†úžčúŽźú ž§Ďž¶Ěž≤úžčĚžĚė ž†ēžĚėŽäĒ 2014ŽÖĄ european respiratory society (ERS)/american thoracic society (ATS) žßÄžĻ®žóźžĄúžĚė ž†ēžĚėžôÄ ÍĪįžĚė ŽŹôžĚľŪēúŽćį, ERS/ATS žßÄžĻ®žĚÄ ž§Ďž¶Ěž≤úžčĚžĚė ž†ēžĚėŽ•ľ žĘÄ ŽćĒ ÍĶ¨ž≤īž†ĀžúľŽ°ú Íłįžą†ŪēėÍ≥† žěąŽč§[1]. žĚīžóź ŽĆÄŪēīžĄúŽäĒ Ūē®ÍĽė Í≤ƞ쨎źú ‚Äúž§Ďž¶Ěž≤úžčĚžĚė žßĄŽč®‚ÄĚ ŽÖľŽ¨łžĚĄ žįłÍ≥†ŪēėÍłį ŽįĒŽěÄŽč§. ŽėźŪēú, žöįŽ¶¨ÍįÄ ŽÖľŪēėŽäĒ ž§Ďž¶Ěž≤úžčĚžĚÄ žÉĀŽčĻŪēú ÍłįÍįĄ(žąėÍįúžõĒ žĚīžÉĀ) ŽŹôžēąžĚė ž°įž†ąž†ú(controller) žĻėŽ£ĆŽ•ľ žčúŪĖČŪēú ŪõĄžóź ŪĆźŽč®ŪēėÍłį ŽēĆŽ¨łžóź, 2007 national asthma education and prevention program žßÄžĻ®Í≥ľ 2008ŽÖĄ žĚīž†ĄžĚė GINA žßÄžĻ®žóźžĄú žÜĆÍįúŽźėÍ≥† žěąŽäĒ ž°įž†ąž†ú žú†žßÄ žĻėŽ£ĆŽ•ľ ŽįõžßÄ žēäÍ≥† žěąŽäĒ ž≤úžčĚ ŪôėžěźžóźžĄúžĚė ‚Äúž§Ďž¶Ě žßÄžÜ枥Ī ž≤úžčĚ(severe persistent asthma)‚ÄĚÍ≥ľŽäĒ Žč§Ž•īŽč§[6].
Í∑łŽ†áŽč§Ž©ī, ŽāúžĻėž≤úžčĚžĚÄ ž§Ďž¶Ěž≤úžčĚÍ≥ľ žĖīŽĖĽÍ≤Ć Žč§Ž•ľÍĻĆ? ž§Ďž¶Ěž≤úžčĚžĚÄ ŽįėŽďúžčú ž≤úžčĚžĚīžßÄŽßĆ, ŽāúžĻėž≤úžčĚžĚÄ ž≤úžčĚžĚī žēĄŽčź žąėŽŹĄ žěąŽč§. ŽėźŪēú, ŽāúžĻėž≤úžčĚžĚė ž†ąŽįė ž†ēŽŹĄŽäĒ žĶúžĘÖž†ĀžúľŽ°ú ž§Ďž¶Ěž≤úžčĚžúľŽ°ú žßĄŽč®ŽźėžßÄŽßĆ, žĚľŽ∂ÄŽäĒ ž≤úžčĚžĚī žēĄŽčąžóąÍĪįŽāė(žěėŽ™ĽŽźú žßĄŽč®žúľŽ°ú ž≤úžčĚžĻėŽ£ĆÍįÄ ž¶ĚžÉĀÍįúžĄ†žóź Ūö®Í≥ľÍįÄ žóÜžóąŽćė Í≤Ĺžöį), Žėź Žč§Ž•ł žĚľŽ∂ÄŽäĒ žąúžĚĎŽŹĄ/ŪĚ°žěÖÍłį Íłįžą†(adherence/inhaler technique)žĚė Ž¨łž†ú, ŪėĻžĚÄ ž≤úžčĚ ŽŹôŽįú žßąŪôė(comorbidities)žĚė Ž¨łž†ú, ͳȞĄĪ ž≤úžčĚ žēÖŪôĒ žúĄŪóė žĚłžěź/ž≤úžčĚ ž¶ĚžÉĀ žú†ŽįúŽ¨ľžßą(exacerbation risk factors/asthma triggers)žĚė žßÄžÜ枆ĀžĚł ŽÖłž∂ú ŽďĪžóź žĚėŪēú ŽāúžĻėž≤úžčĚžĚīžóąžúľŽāė, ž§Ďž¶Ěž≤úžčĚžóźŽäĒ ŪēīŽčĻŪēėžßÄ žēäžĚĄ žąė žěąŽč§[1,7,8].
ŽāúžĻėž≤úžčĚžĚė žĻėŽ£Ć ž†ĎÍ∑ľ
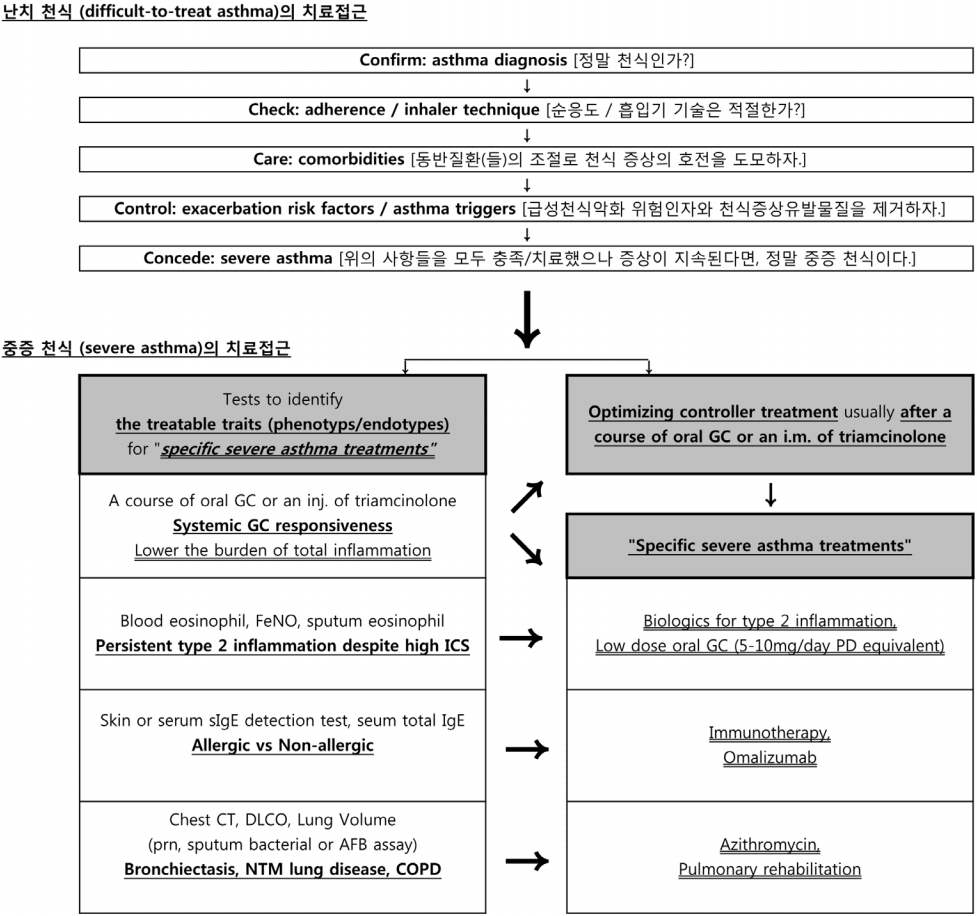
Í∑łŽ¶ľ 1žĚė žúóŽ∂ÄŽ∂Ąžóź ŽāúžĻėž≤úžčĚžĚė žĻėŽ£Ćž†ĎÍ∑ľžóź ŽĆÄŪēīžĄú žöĒžēĹŪēėžėÄŽč§. žúĄžóź Íłįžą†Ūēú ŽįĒžôÄ ÍįôžĚī ŽāúžĻėž≤úžčĚžĚÄ žēĄŽěėžôÄ ÍįôžĚÄ Žč®Í≥ĄŽ•ľ ÍĪįž≥źžĄú, ž†ēŽßź ž§Ďž¶Ěž≤úžčĚžóź ŪēīŽčĻŪēėŽäĒžßÄŽ•ľ ŪôēžĚłŪēėŽäĒ Í≥ľž†ēžĚīŽĚľ Ūē† žąė žěąŽč§.
Confirm: asthma diagnosis(ž†ēŽßź ž≤úžč̞̳ÍįÄ?)
Í≥†ÍįēŽŹĄžĚė ž≤úžčĚ žĻėŽ£ĆŽ•ľ ŪēėÍ≥† žěąžĚƞ󟎏Ą, ŪôėžěźžĚė ž¶ĚžÉĀ(ž≤úžčĚžĚė 4ŽĆÄ ž¶ĚžÉĀžĚł ÍłįžĻ®[cough], ŪėłŪĚ° Í≥§ŽěÄ[dyspnea], ž≤úŽ™Ö[wheezing], ÍįÄžäī ŽčĶŽčĶŪē®[chest tightness] ž§Ď Ūēú ÍįÄžßÄ žĚīžÉĀ) ÍįúžĄ†žĚī ŽĮłŽĻĄŪēėŽč§Ž©ī, ÍįÄžě• Ž®ľž†Ä ŪôēžĚłŪē† Í≤ÉžĚÄ Íłįž°īžóź ž≤úžčĚžĚī ŪôēžßĄ(confirm diagnosis) ŽźėžóąŽäĒžßÄ ŪôēžĚłŪēėŽäĒ Í≤ÉžĚīŽč§. ŽĻĄž°įž†ą ž≤úžčĚžĚė 10-30%ÍįÄ Í≤įÍĶ≠žĚÄ non-asthmatic conditionsŽ°ú žßĄŽč®ŽźėŽäĒ Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąŽč§[1,9,10]. ž≤úžčĚ ŪôēžßĄžĚÄ ž≤úžčĚžĚė ž¶ĚžÉĀžĚī žěąŽäĒ žÉĀŪÉúžóźžĄú ÍįÄŽ≥Äž†Ā ÍłįŽŹĄ ŪŹźžáĄ(variable airflow obstruction)ÍįÄ ŪŹźÍłįŽä• Í≤Äžā¨žóźžĄú ŪôēžĚłŽź† ŽēĆ ÍįÄŽä•ŪēėŽč§[7,11,12]. ž°įž†ąž†úŽ•ľ žā¨žö©ŪēėŽäĒ žÉĀŪÉúžóźžĄú ž≤úžčĚ ŪôēžßĄžĚī ŪēĄžöĒŪēú Í≤Ĺžöį, ‚Äúbaseline spirometry forced expiratory volume in the first second (FEV1) ‚Üí twice-daily peak expiratory flow rate (PEF) for 2 weeks (1st week: Íłįž°ī žĻėŽ£Ć; 2nd week: Íłįž°ī žĻėŽ£Ć + Í≤ĹÍĶ¨žä§ŪÖĆŽ°úžĚīŽďú Žč®ÍłįžöĒŽ≤ē [prednisolone 30-60 mg/day 5-14days]) ‚Üí follow-up spirometry (FEV1)‚ÄĚžĚė Žį©Ž≤ēžĚĄ žĚīžö©ŪēīŽ≥ľ žąė žěąŽč§.
Check: adherence/inhaler technique(žąúžĚĎŽŹĄ/ŪĚ°žěÖÍłį Íłįžą†žĚÄ ž†Āž†ąŪēúÍįÄ?)
žąúžĚĎŽŹĄ(adherence)
ŽāģžĚÄ žąúžĚĎŽŹĄ(poor adherence)ŽěÄ ŪôėžěźÍįÄ žēĹžÜćŪēú žĻėŽ£ĆŽ•ľ ŪēėžßÄ žēäŽäĒ Í≤ÉžĚīŽč§. ž≤úžčĚ ŪôėžěźžĚė 50% ž†ēŽŹĄŽäĒ žēĹž†úŽ•ľ ž†úŽĆÄŽ°ú žā¨žö©ŪēėžßÄ žēäŽäĒ žčúÍłįÍįÄ žěąŽč§[13]. Ž¨łž†úŽäĒ ŪôėžěźÍįÄ žä§žä§Ž°úžĚė žĻėŽ£Ć žąúžĚĎŽŹĄŽ•ľ ž†ēŪôēŪēėÍ≤Ć žĚīžēľÍłįŪēėžßÄ žēäžĚĄ ŽēĆÍįÄ ŽßéÍ≥†, Í∑łŽď§žĚė žąúžĚĎŽŹĄŽ•ľ Í≥ľŽĆÄŪŹČÍįÄŪēúŽč§ŽäĒ Í≤ÉžĚīŽč§[14]. žąúžĚĎŽŹĄžĚė ŪôēžĚłžĚĄ žúĄŪēī ž†ĄžěźŪĚ°žěÖÍłįŽ™®ŽčąŪĄįŽßĀžĚīŽāė Ūėąž§ĎŽÜ掏Ą žł°ž†ē(žĻėŽ£Ć žēĹŽ¨ľžĚł ŪĒĄŽ†ąŽďúŽčąžÜĒŽ°†žĚīŽāė žĹĒŪčįžÜĒ), žēĹžā¨žĚė ž°įž†úÍłįŽ°Ě ŽďĪžĚė Žį©Ž≤ēžĚī žÜĆÍįúŽźėÍłįŽŹĄ ŪēėŽāė[5,10,15], ŽįĒžĀú žěĄžÉĀ ŪėĄžě•žóźžĄú žĚīžö©ŪēėÍłįŽäĒ žČĹžßÄ žēäŽč§. ŪôėžěźžôÄ ŽąąžĚĄ Žßąž£ľžĻėÍ≥†, ŪôėžěźžĚė žĖīŽ†§žõĞ̥ žč≠Ž∂Ą žĚīŪēīŪē®žĚĄ ŪĎúžčúŪēėŽäĒ Í≥ĶÍįźž†Ā žßąŽ¨ł(empathic question)žĚĄ ŪÜĶŪēī ŪôėžěźÍįÄ žąúžĚĎŽŹĄŽ•ľ ž†ēŪôēŪěą ŽįĚŪ칎ŹĄŽ°Ě žú†ŽŹĄŪēīžēľ ŪēúŽč§[7,12]. žēĹž†úŽ•ľ ž∂ĒÍįÄŪēú ŪõĄ žĚľž†ēÍłįÍįĄ(3-6ÍįúžõĒ) žēĹž†ú žąúžĚĎŽŹĄÍįÄ žĘčžēėžĚƞ󟎏Ą Ž∂ąÍĶ¨ŪēėÍ≥† ž¶ĚžÉĀžĚīŽāė ŪŹźÍłįŽä• ÍįúžĄ†žĚī žó܎觎©ī, ž∂ĒÍįÄŪēú žēĹž†úŽ•ľ ž§ĎŽč®ŪēėŽäĒ Í≤ɞ̥ Í≥†Ž†§Ūēīžēľ ŪēúŽč§[5].
ŪôėžěźÍįÄ žēĹž†ú žā¨žö©žĚĄ Í≤ƞ̥Ž¶¨ŪēėžėÄŽč§Í≥† Í≥†ŽįĪŪēėŽ©ī, žĚėžā¨ŽäĒ ŽĻĄŽāúŪēėžßÄ žēäŽäĒ ŪÉúŽŹĄ(non-judgemental manner)Ž°ú Ūôėžěź ŽįŹ Ūôėžěź Ž≥īŪėłžěźžôÄ Ū܆Ž°†Ūēėžó¨ ŽĻĄžąúžĚĎžĚė žõźžĚłžĚĄ ŽįėŽďúžčú ŪôēžĚłŪēīžēľ ŪēúŽč§. žĚīŽü¨Ūēú Í≤Ĺžöį ŽßéžĚÄ ŪôėžěźŽ°úŽ∂ÄŪĄį žĚėŽŹĄž†ĀžĚł ŽĻĄžąúžĚĎ(intentional poor adherence)žĚĄ ŪôēžĚłŪē† žąė žěąŽäĒŽćį, ÍįÄžě• ŽßéžĚÄ Í≤ĹžöįÍįÄ ‚Äú(ž¶ĚžÉĀžĚī žóÜžĖīžßÄŽ©ī) žĻėŽ£ĆÍįÄ ŪēĄžöĒ žó܎觎äĒ žĚłžčĚ‚ÄĚÍ≥ľ ‚ÄúŽ∂ÄžěĎžö©žóź ŽĆÄŪēú ÍĪĪž†ē‚ÄĚžĚīŽč§. Ūôėžěź žä§žä§Ž°úÍįÄ žßąŪôė ŽįŹ žĻėŽ£ĆžĚė Ūö®Í≥ľŽ•ľ žĚīŪēīŪēėÍ≤Ć ŽźėŽ©ī žĻėŽ£Ć žąúžĚĎŽŹĄŽäĒ Žß§žöį ž¶ĚÍįÄŪēúŽč§[7]. ŪôėžěźžĚė žßąŪôė žĚłžč̞̥ ÍįúžĄ†žčúŪā¨ žąė žěąŽäĒ žĄ§Ž™ÖžĚė žėąŽäĒ Žč§žĚĆÍ≥ľ ÍįôŽč§: ‚Äúž≤úžčĚžĚÄ ŽčĻŽá®Ž≥ĎžĚīŽāė Í≥†ŪėąžēēÍ≥ľ ÍįôžĚÄ ŽßĆžĄĪ žßąŪôėžě֎蹎č§.‚ÄĚ, ‚ÄúžßÄÍłą žā¨žö© ž§ĎžĚł ŪĚ°žěÖž†úŽäĒ žėąŽį©žēĹ(ž°įž†ąž†ú)žě֎蹎č§. OOOŽčėžĚė ž≤úžčĚ ž¶ĚžÉĀžĚī ŽāėŪÉÄŽāėžßÄ žēäÍ≤Ć Ūēīž£ľÍ≥†, ÍįźÍłįžóź ÍĪłŽ¶¨ŽćĒŽĚľŽŹĄ žč¨ŪēėÍ≤Ć ŽāėŽĻ†žßÄžßÄ žēäÍ≤Ć žėąŽį©žčúžľúž§ćŽčąŽč§. ŽßĆžēĹ ŽčĻžč† žĚī žēĹ(ž°įž†ą)žĚĄ ž§ĎŽč®ŪēėŽ©ī, ž¶ĚžÉĀžĚÄ ŽįėŽďúžčú Žč§žčú ŽāėŪÉÄŽā©ŽčąŽč§.‚ÄĚ, ‚ÄúŪĚ°žěÖž†úžĚė Ž∂ÄžěĎžö©žĚÄ Žß§žöį ŽďúŽ≠֎蹎č§. ŽßĆžēĹ Ž∂ÄžěĎžö©žĚī žÉĚÍ≤®ŽŹĄ ŪēīÍ≤įŪē† Žį©Ž≤ē(žēĹ Ž≥ÄÍ≤Ĺ or device Ž≥ÄÍ≤Ĺ)žĚī ŽßéžúľŽĮÄŽ°ú, žĖłž†úŽď†žßÄ Ž∂ąŪéłŪēú ž¶ĚžÉĀžĚī žěąžúľŽ©ī ž†ÄŲ̄žóźÍ≤Ć žēĆŽ†§ž£ľžĄłžöĒ‚ÄĚ.
ŪĚ°žěÖÍłį Íłįžą†(inhaler technique)
ž≤úžčĚ žĻėŽ£ĆžĚė ÍįÄžě• ž§Ďžč¨ž†ĀžĚł žēĹŽ¨ľžĚÄ ŪĚ°žěÖžēĹŽ¨ľžĚīŽĮÄŽ°ú, ŪôėžěźžĚė ŪĚ°ÍłįŽ†•/žĚłžßÄ ÍłįŽä•/ŽŹôŽįė žßąŪôė ŽďĪžĚĄ žĘÖŪē©Ūēėžó¨ ŪĚ°žěÖ žĻėŽ£ĆžĚė Žį©Ž≤ē(ŪĚ°žěÖÍłį žĘÖŽ•ė)žĚĄ Í≤įž†ēŪēīžēľ ŪēúŽč§. žėąŽ•ľ Žď§žĖī Í≥†Ž†Ļ (žĚłžßÄÍłįŽä• ž†ÄŪēėÍįÄ žěąŽäĒ Í≤Ĺžöį)žĚė ÍīÄž†ąžóľžĚĄ žēďÍ≥† žěąŽäĒ ŪôėžěźžóźÍ≤ĆŽäĒ pressurized metered dose inhaler (pMDI) (+/-spacer)/dry powder inhaler (DPI)Ž≥īŽč§ ŽĄ§Ž∑łŽĚľžĚīž†łÍįÄ ž†ĀŪē©ŪēėŽč§[16]. pMDI (+/-spacer)/DPIŽ•ľ žā¨žö©ŪēėÍłįŽ°ú Í≤įž†ēŪēú Í≤Ĺžöį, ž†Āž†ąŪēú ÍĶźžú°žĚĄ ŪÜĶŪēī ŪĚ°žěÖÍłį Íłįžą†žĚĄ žäĶŽďĚŪēėŽŹĄŽ°Ě Ūēīžēľ ŪēúŽč§. ŽėźŪēú, ž≤ėžĚĆ ÍĶźžú° ŪõĄ 4-6ž£ľ žĚīŽāīžóźŽäĒ ŪôėžěźžĚė ž≤úžčĚžĚī žěė ž°įž†ąŽźėÍ≥† žěąŽćĒŽĚľŽŹĄ, Ūēú Ž≤ą ŽćĒ ŪĚ°žěÖÍłį Íłįžą†žĚĄ ž†źÍ≤ÄŪēėÍ≥†, žĚīŪõĄ ž£ľÍłįž†ĀžĚł ž†źÍ≤ÄžĚī ŪēĄžöĒŪēėŽč§. ŽßĆžēĹ, ž≤úžčĚžĚī ž°įž†ąŽźėžßÄ žēäŽäĒ žÉĀŪÉúŽ°ú ŪôėžěźÍįÄ Žį©Ž¨łŪēú Í≤ĹžöįžóźŽäĒ, žĘÄ ŽćĒ žĄłŽįÄŪēú ŪĚ°žěÖÍłį Íłįžą† ž†źÍ≤ÄžĚī ŪēĄžöĒŪēėŽč§. žĚīŽēĆŽäĒ Ž™®Ūėē ŪĚ°žěÖ ÍłįÍĶ¨(placebo inhaler)Ž•ľ ÍįÄžßÄÍ≥† žßĀž†Ď ŪôėžěźžóźÍ≤Ć žčúžóįŪēėŽŹĄŽ°Ě žßÄžčúŪēú ŪõĄ, žěėŽ™ĽŽźú Žč®Í≥ĄŽ•ľ ŪôēžĚłŪēúŽč§. Žč§žĚĆžúľŽ°ú žĚėžā¨ÍįÄ žßĀž†Ď Ž™®ŪėēžĚĄ žĚīžö©Ūēėžó¨ ŪôėžěźžóźÍ≤Ć ŪĚ°žěÖÍłįŽ•ľ ž†úŽĆÄŽ°ú žā¨žö©ŪēėŽäĒ Žį©Ž≤ēžĚĄ Ž≥īžó¨ž§Ä ŪõĄ, Ž¨łž†ú žěąŽäĒ Žč®Í≥ĄŽ•ľ ž§Ďžč¨žúľŽ°ú žā¨žö© Žį©Ž≤ēžĚĄ 2-3Ž≤ą Žč§žčú ŪôēžĚłŪēī ž£ľŽäĒ Í≤ÉžĚī ŪēĄžöĒŪēėŽč§[7,17].
Care: comorbidities(ŽŹôŽįė žßąŪôė ž°įž†ąŽ°ú ž≤úžčĚ ž¶ĚžÉĀžĚė Ūėłž†ĄžĚĄ ŽŹĄŽ™®Ūēėžěź)
ŽĻĄžóľ ŽįŹ ŽĻĄŽ∂ÄŽĻĄŽŹôžóľ, žúĄžčĚŽŹĄ žó≠Ž•ė žßąŪôė, Ž∂ąžēąžě•žē†, žč¨žě• žßąŪôė, ŽĻĄŽßĆ, ŪŹźžáĄžĄĪ žąėŽ©ī Ž¨īŪėłŪĚ°ž¶Ě ŽďĪžĚĄ ŪŹ¨Ūē®Ūēú ž≤úžčĚ ŽŹôŽįė žßąŪôėŽď§žĚÄ ž≤úžčĚ ž°įž†ąžĚĄ žēÖŪôĒžčúŪā§ÍĪįŽāė ž¶ĚžÉĀžĚė žõźžĚłžĚī Žź† žąė žěąŽč§[1,5,7,11,12]. Í≤Ĺžöįžóź ŽĒįŽĚľžĄúŽäĒ ÍįÄŽ≥Äž†Ā ÍłįŽŹĄŪŹźžáĄÍįÄ ŪôēžĚłŽźú žÉĀŪô©žóźžĄúŽŹĄ(ž≤úžčĚžĚī ŪôēžßĄŽźú žÉĀŪô©), ŽŹôŽįė žßąŪôėžĚĄ žĻėŽ£ĆŪēú ŪõĄ ŪôėžěźžĚė Ž™®Žď† ž¶ĚžÉĀžĚī žā¨ŽĚľžßÄŽäĒ Í≤ĹžöįŽŹĄ žěąŽč§ (Ž∂ąžēąžě•žē†, žč¨žě• žßąŪôė). ŽĒįŽĚľžĄú, ŽĻĄž°įž†ą ž≤úžčĚ ŪôėžěźžóźžĄú ŽŹôŽįė žßąŪôėžĚī žĚėžč¨/ŪôēžĚłŽźėŽ©ī ž†Āž†ąŪēú ŪėϞߥÍ≥ľ Žč§Ūēôž†úž†Ā ŪŹČÍįÄ/žĻėŽ£ĆŽ•ľ žč†žÜćŪěą žčúŪĖČŪēīžēľ ŪēúŽč§[5]. ŪēėžßÄŽßĆ ŽŹôŽįė žßąŪôėžĚė ž°įž†ąžĚī žĖīŽ†§žöī Í≤ĹžöįŽŹĄ ŽßéÍłį ŽēĆŽ¨łžóź(ŽĻĄŽßĆ, ŽĻĄŽ∂ÄŽĻĄŽŹôžóľ), ŽŹôŽįė žßąŪôėžĚĄ žĻėŽ£ĆŪēėŽäĒ Í≤ÉžĚī ž§Ďž¶Ěž≤úžčĚ Ūėłž†Ą žó¨Ž∂Äžóź ŽĮłžĻėŽäĒ žėĀŪĖ•žóź ŽĆÄŪēīžĄúŽäĒ žóįÍĶ¨ÍįÄ žĘÄ ŽćĒ ŪēĄžöĒŪēī Ž≥īžĚłŽč§[11]. Ž™á ÍįÄžßÄ ž§ĎžöĒŪēú ž≤úžčĚ ŽŹôŽįė žßąŪôėŽď§žĚĄ Íłįž°ī žóįÍĶ¨žôÄ ŪēĄžěźžĚė Í≤ĹŪóėžĚĄ ŽįĒŪÉēžúľŽ°ú žēĄŽěėžôÄ ÍįôžĚī ž†ēŽ¶¨ŪēīŽ≥īžēėŽč§.
ŽĻĄžóľ(ŽĻĄŽ∂ÄŽĻĄŽŹôžóľ)
ž≤úžčĚžĚė ÍįÄžě• ŪĚĒŪēú ŽŹôŽįė žßąŪôėžĚł ŽĻĄžóľ(ŽĻĄŽ∂ÄŽĻĄŽŹôžóľ)žĚÄ ž≤úžčĚ ŪôėžěźžĚė 90% žĚīžÉĀžóźžĄú ŽāėŪÉÄŽāúŽč§[18]. ŽĆÄÍįú ŽĻĄžóľžĚÄ ž≤úžčĚŽ≥īŽč§ žĄ†ŪĖČŪēėŽäĒŽćį ŽĻĄžóľ ŪôėžěźžĚė 30% ž†ēŽŹĄžóźžĄú Í≤įÍĶ≠ ž≤úžčĚžĚī ŽįúžÉĚŪēúŽč§[12] (žįłÍ≥†Ž°ú ŽĻĄžóľÍ≥ľ ž≤úžčĚžĚė žú†Ž≥ĎŽ•†žĚÄ ÍįĀÍįĀ ž†Ą žĚłÍĶ¨žĚė 10-20%, 5-10%Ž°ú žēĆŽ†§ž†ł žěąžĚĆ). ŪäĻŪěą, ž§Ďž¶Ě žßÄžÜ枥Ī ŽĻĄžóľ(severe persistent rhinitis) ŪôėžěźžóźžĄú ž≤úžčĚžĚī ŽßéžĚī ŽįúžÉĚŪēúŽč§[18]. ŽĻĄŽ∂ÄŽĻĄŽŹôžóľžĚÄ ž≤úžčĚ žēÖŪôĒžĚė žúĄŪóė žĚłžěźžĚīÍ≥†[19], ŽĻĄŽ∂ÄŽĻĄŽŹôžóľžĚė žĻėŽ£ĆŽäĒ ž≤úžčĚ ž¶ĚžÉĀžĚĄ ÍįúžĄ†žčúŪā®Žč§[20,21]. ŽĻĄžóľ(ŽĻĄŽ∂ÄŽĻĄŽŹôžóľ)žĚÄ ž†ĄŪėēž†ĀžĚł žēĆŽ†ąŽ•īÍłį ŽĻĄžóľ ž¶ĚžÉĀ(ŽßĎžĚÄ žĹߎ¨ľ[ž†ĄŽĻĄŽ£®], žĹĒŽßČŪěė, žě¨žĪĄÍłį, ŽąąÍįÄŽ†§žõÄ) žóÜžĚī, ŽĻĄž†ĄŪėēž†Ā ž¶ĚžÉĀ (ŪõĄŽĻĄŽ£®, Ž™©žĚīŽ¨ľÍįź, ÍłįžĻ®, ÍįĚŽčī)ŽßĆ ŽāėŪÉÄŽāėÍłįŽŹĄ ŪēúŽč§(ŽĻĄžēĆŽ†ąŽ•īÍłį ŽĻĄžóľ) [22]. ŪēėžßÄŽßĆ, žēĆŽ†ąŽ•īÍłį ŽĻĄžóľ/ŽĻĄžēĆŽ†ąŽ•īÍłį ŽĻĄžóľ Ž™®ŽĎź žĻėŽ£ĆžĚė ŪēĶžč¨žĚÄ ŽĻĄÍįēŽāī žä§ŪÖĆŽ°úžĚīŽďú(intranasal steroid, INS)žĚīŽĮÄŽ°ú, ŽĻĄžóľ(ŽĻĄŽ∂ÄŽĻĄŽŹôžóľ)žĚĄ ŪėłžÜĆŪēėŽäĒ ž≤úžčĚ ŪôėžěźžóźÍ≤Ć ÍłįŽ≥łž†ĀžúľŽ°ú INSŽ•ľ ž≤ėŽį©ŪēėÍ≥†, žēĆŽ†ąŽ•īÍłįŽĻĄžóľžĚė ÍįÄŽä•žĄĪžĚī ŽÜížēĄ Ž≥īžĚīŽ©ī 2žĄłŽĆÄ Ūē≠Ūěąžä§ŪÉÄŽĮľ, ŽĻĄžēĆŽ†ąŽ•īÍłį ŽĻĄžóľ ÍįÄŽä•žĄĪžĚī ŽÜížúľŽ©ī 1žĄłŽĆÄ Ūē≠Ūěąžä§ŪÉÄŽĮľžĚĄ žā¨žö©ŪēīŽ≥ľ žąė žěąŽč§. žč¨Ūēú ŽĻĄžóľ ž¶ĚžÉĀžĚī žěąžĚĄ ŽēĆ žÉĚŽ¶¨žčĚžóľžąė žĹĒžĄłž≤ôžĚīŽāė Žč®ÍłįÍįĄžĚė Í≥†žö©ŽüČ Í≤ĹÍĶ¨žä§ŪÖĆŽ°úžĚīŽďú, ŪôĒŽÜ枥Ī ŽĻĄŽ∂ÄŽĻĄŽŹôžóľžĚī ŽįúžÉĚŪēú Í≤Ĺžöį Ūē≠žÉĚž†úŽ•ľ žā¨žö©ŪēėŽäĒ Í≤ÉžĚī ŽŹĄžõÄžĚī ŽźúŽč§. ŽćĒ žěźžĄłŪēú ŽĻĄžóľžĚė žĻėŽ£ĆŽäĒ žĶúÍ∑ľ Žāėžė® ÍįÄžĚīŽďúŽĚľžĚłžĚĄ žįłÍ≥†ŪēėÍłį ŽįĒŽěÄŽč§[23].
žúĄžčĚŽŹĄ žó≠Ž•ė žßąŪôė
žúĄžčĚŽŹĄ žó≠Ž•ė žßąŪôė(gastroesophageal reflux disease, GERD)žĚÄ žěźž£ľ(Žß§žĚľ) ŽįúžÉĚŪēėŽäĒ ÍįÄžäīžďįŽ¶ľ, žč†Ž¨ľ, žĚĆžčĚŽ¨ľ žó≠Ž•ė, žÉĀŽ≥ĶŽ∂ÄžďįŽ¶ľ ŽďĪžĚė ž¶ĚžÉĀžĚĄ žĚľžúľŪā§ŽäĒ žßąŪôėžúľŽ°ú žčĚŽŹĄÍīĄŽěĶÍ∑ľžĚė ÍłįŽä•ž†ÄŪēėŽ°ú žĚłŪēī ŽįúžÉĚŪēúŽč§. ž≤úžčĚ ŪôėžěźžóźžĄú žĚľŽįėžĚłŽ≥īŽč§ 3Žįį ŽßéžĚÄ GERD ŽĻąŽŹĄŽ•ľ Ž≥īžĚłŽč§Í≥† žēĆŽ†§ž†ł žěąŽč§[11]. ž≤úžčĚ ŪôėžěźžóźžĄú GERDžĚė ž¶ĚžÉĀžĚī ŽŹôŽįėŽźú Í≤ĹžöįžóźŽäĒ GERDžĚė žĻėŽ£Ć(proton pump inhibitor, PPI)ÍįÄ ž≤úžčĚ ž¶ĚžÉĀ/žēÖŪôĒ ÍįźžÜĆžóź ŽŹĄžõÄžĚī ŽźėŽāė, GERD ž¶ĚžÉĀžĚī žóÜŽäĒ Í≤ĹžöįžóźŽäĒ ž≤úžčĚ outcomežóź žėĀŪĖ•žĚĄ ŽĀľžĻėžßÄ žēäŽäĒ Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąŽč§[24,25]. ŽĒįŽĚľžĄú ŽĻĄž°įž†ą/ž§Ďž¶Ěž≤úžč̞󟞥ú GERD ž¶ĚžÉĀžĚī žóܞ̥ ŽēĆ ž≤úžčĚ ž¶ĚžÉĀ ÍįúžĄ†žĚīŽāė žēÖŪôĒ žėąŽį©žĚĄ Ž™©ž†ĀžúľŽ°ú PPIŽ•ľ žā¨žö©Ūē† ŪēĄžöĒŽäĒ žóÜŽč§[7].
GERDŽäĒ ŽßĆžĄĪ ÍłįžĻ®žĚė žõźžĚłžĚīÍłįŽŹĄ ŪēėŽč§. GERDŽ°ú žĚłŪēú ŽßĆžĄĪ ÍłįžĻ®žĚė ž†ĄŪėēž†ĀžĚł žěĄžÉĀ žĖĎžÉĀžĚÄ ŽßĆžĄĪ ÍłįžĻ®Í≥ľ GERD ž¶ĚžÉĀžĚī Ūē®ÍĽė ŽįúžÉĚŪēėŽäĒ Í≤ÉžĚīŽāė, ÍłįžĻ®žĚī žú†žĚľŪēú ž¶ĚžÉĀžĚł Í≤ĹžöįŽŹĄ žěąŽč§(silent GERD) [26]. ŪäĻŪěą, ÍłįžĻ®žĚī ž£ľ ž¶ĚžÉĀžĚł ŽĻĄž°įž†ą ž≤úžč̞󟞥ú ŪŹźÍłįŽä•(FEV1)žĚī žĚīž†Ąžóź ŽĻĄŪēī ŽāėžĀėžßÄ žēäŽč§Ž©ī, ŽĻĄŽ∂ÄŽĻĄŽŹôžóľ žóįÍīÄ upper airway cough syndrome (UACS)žĚīŽāė GERDŽ•ľ žĚėžč¨Ūēėžó¨ Í≤ĹŪóėž†ĀžúľŽ°ú ŽĎź žßąŪôėžóź ŽĆÄŪēú žąúžį®ž†ĀžĚł žĻėŽ£ĆŽ•ľ žčúŪĖČŪēėŽäĒ Í≤ÉžĚÄ Žß§žöį Ūē©Ž¶¨ž†ĀžĚīŽĚľÍ≥† Ūē† žąė žěąŽč§[11].
ŽĻĄŽßĆ
ž≤úžčĚžĚÄ ŽĻĄŽßĆŪēú žā¨ŽěĆžóźÍ≤Ć ŽćĒ ŪĚĒŪēėŽč§[7]. ŽĻĄŽßĆŪēú ž≤úžčĚ ŪôėžěźŽäĒ ž≤úžčĚ ž¶ĚžÉĀÍ≥ľ žēÖŪôĒÍįÄ ŽćĒ žč¨ŪēėÍ≥†, ICSžĚė žĻėŽ£Ć ŽįėžĚĎžĚī žĚľŽįėžĚłžóź ŽĻĄŪēī ŽĖ®žĖīžßÄŽäĒ Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąŽč§[7]. 5-10%žĚė ž≤īž§ĎÍįźžÜĆŽßĆžúľŽ°úŽŹĄ ž≤úžčĚ ž°įž†ąÍ≥ľ žā∂žĚė žßąžĚī ŽāėžēĄžßÄŽĮÄŽ°ú[27], ŽĻĄž°įž†ą ž≤úžčĚ ŪôėžěźÍįÄ ŽĻĄŽßĆŪēėŽč§Ž©ī, ž†ĀÍ∑Ļž†ĀžĚł ž≤īž§ĎÍįźžÜĆŽ•ľ Í∂ĆÍ≥†Ūēīžēľ ŪēúŽč§.
ž†ēžč†Í≥ľž†Ā žßąŪôė: Ž∂ąžēąžě•žē†/Í≥ľŪôėÍłįž¶ĚŪõĄÍĶį/Í≥ĶŪô©žě•žē†, žöįžöłž¶Ě
Ž∂ąžēąžě•žē†(Í≥ľŪôėÍłįž¶ĚŪõĄÍĶį, Í≥ĶŪô©žě•žē†)žôÄ žöįžöłž¶ĚžĚÄ ŽĆÄŪĎúž†ĀžĚł ž≤úžčĚ žóįÍīÄ ž†ēžč† žßąŪôėžĚīŽč§. žöįžöłž¶ĚžĚÄ žĚľž†ē ÍłįÍįĄ žĚīžÉĀ žßÄžÜ掟ėŽäĒ žöįžöłŪēú ÍłįŽ∂Ą ŪėĻžĚÄ ž¶źÍĪįžõÄžĚė žÉĀžč§Ž°ú, ŪäĻŪěą ŽÖłžĚł ž≤úžčĚ ŪôėžěźžóźÍ≤Ć žěė ŽŹôŽįėŽźúŽč§. žöįžöłž¶ĚžĚÄ žěė žēĆŽ†§žßĄ ͳȞĄĪ žēÖŪôĒžĚė žúĄŪóė žĚłžěźžĚīÍ≥†, žöįžöłž¶ĚžĚė ÍīÄŽ¶¨Ž•ľ žěė ŪēėŽ©ī ž≤úžčĚŽŹĄ ŽćĒ žěė ž°įž†ąŽźėŽäĒ Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąŽč§[7,11]. Ž∂ąžēąžě•žē†ŽäĒ ž≤úžčĚžóź Ž≥ĎŽįúŪēėÍłįŽ≥īŽč§ ÍįźŽ≥ĄŪēīžēľ Ūē† ŪēĄžöĒÍįÄ ŽćĒ ŽÜížĚÄ žßąŪôėžúľŽ°ú, ž£ľŽ°ú žä§Ū䳎†ąžä§žóź ŽĮľÍįźŪēú ž†äžĚÄ(10-40ŽĆÄ) žó¨žěźžóźžĄú ŽįúžÉĚŪēúŽč§. Ž∂ąžēąžě•žē†ŽäĒ žīąž°įŪēėÍ≥† ŽĎźŽ†§žöī ŽäźŽāĆÍ≥ľ Ūē®ÍĽė ŽĻąŽß•, ŽįúŪēú ŽďĪžĚė žěźžú®žč†Í≤ĹŪē≠žßĄ ž¶ĚžÉĀžĚĄ Ž≥īžĚīŽäĒŽćį, žč¨ŪēīžßÄŽ©ī Í≥ľŪėłŪĚ°ž¶ĚŪõĄÍĶį(žč¨Ūēú Ž∂ąžēąžúľŽ°ú žĚłŪēú ŽĻ†Ž•īÍ≥† ÍĻäžĚÄ ŪėłŪĚ°žĚė ŽįėŽ≥Ķ)žĚīŽāė Í≥ĶŪô©žě•žē†(Í∑Ļžč¨Ūēú Ž∂ąžēąžúľŽ°ú žĚłŪēī ž£ĹžĚĄ Í≤É ÍįôžĚÄ ŽäźŽāĆžĚī ŽďúŽäĒ Í≤É)Ž°ú ŽāėŪÉÄŽāúŽč§[28]. Ž∂ąžēąžě•žē† žó≠žčú ž≤úžčĚžĚė ŽŹôŽįė žßąŪôėžúľŽ°ú ŽįúžÉĚŪē† žąė žěąŽč§. Í≤Ĺžöįžóź ŽĒįŽĚľžĄúŽäĒ ž≤úžčĚžēĹŽ¨ľ(Ž≤†ŪÉÄŪē≠žßĄž†ú)žĚī ŪôėžěźžóźÍ≤Ć Ž∂ąžēąžĚĄ žú†ŽŹĄŪēėÍłįŽŹĄ ŪēėŽäĒŽćį, žĚī Í≤Ĺžöį ŪôėžěźžĚė Ž∂ąžēąÍįźžĚī žēĹŽ¨ľ žĻėŽ£Ć ž†ĄŽ∂ÄŪĄį žěąžóąŽäĒžßÄ ŪôēžĚłŪēīžēľ ŪēėÍ≥† Ž≤†ŪÉÄŪē≠žßĄž†úŽ•ľ ž†úžôłŪēú ž≤úžčĚ žēĹŽ¨ľžĚĄ žā¨žö©ŪēėŽäĒ Í≤ÉžĚī žöĒŽßĚŽźúŽč§.
ŪôėžěźžĚė ž¶ĚžÉĀžĚī ž≤úžčĚŽßĆžúľŽ°ú žĄ§Ž™ÖŽźėžßÄ žēäŽäĒ Í≤É ÍįôÍ≥†, ŪäĻŪěą ž£ľÍīÄž†Ā ŪėłŪĚ°Í≥§ŽěÄžĚė ŪėłžÜĆŽäĒ žč¨ŪēėŽāė ž£ľŽ°ú žēąž†ēžčú ŪėłŪĚ°Í≥§ŽěĞ̥ žöīŽŹôžčú ŪėłŪĚ°Í≥§ŽěÄŽ≥īŽč§ žč¨ŪēėÍ≤Ć ŪėłžÜĆŪēėÍ≥†(žĚľžÉĀ žóÖŽ¨īŽäĒ žěė ŪēėŽāė ÍįĄŪ󟞆ĀžúľŽ°ú Ūėľžěź žČ¨Í≥† žěąžĚĄ ŽēĆ ŪėłŪĚ°Í≥§ŽěÄ ŽįúžÉĚ), Í≤Äžā¨(FEV1)žÉĀ ž†ēžÉĀžĚīÍ≥† ŪėłŪĚ°Í≥§ŽěÄ žôłžĚė ž≤úžčĚ ž¶ĚžÉĀ(ÍłįžĻ®, ž≤úŽ™Ö)žĚī ÍīÄžįįŽźėžßÄ žēäÍĪįŽāė žĶúÍ∑ľžóź žč¨Ūēú žä§Ū䳎†ąžä§Ž•ľ Í≤ĹŪóėŪēėžėÄŽćė Í≤Ĺžöį žöįžöłž¶ĚžĚīŽāė Ž∂ąžēąžě•žē†žĚė ŽŹôŽįė ŪėĻžĚÄ ÍįźŽ≥ĄžĚĄ Í≥†Ž†§Ūēīžēľ ŪēúŽč§[29]. žöįžöłž¶ĚžĚė Í≤Ĺžöį Ūēúžą® žČ¨Ž©īžĄú ŪÉĄžčĚŪēėŽäĒ ŪėłŪĚ°žĖĎžÉĀžĚĄ Ž≥īžĚīŽäĒŽćį ŽĻĄŪēī, Ž∂ąžēąžě•žē† ŽēĆŽäĒ ŪĚ°ÍłįÍįÄ Žćú žĚīŽ£®žĖīžßĄ ŽäźŽāƞ̥ ŪėłžÜĆŪēėŽ©īžĄú ŽįėŽ≥Ķž†ĀžúľŽ°ú žč¨ŪėłŪĚ°žĚĄ ŪēėŽäĒ Ž™®žäĶžĚĄ Ž≥īžĚłŽč§.
žĄĪŽĆÄÍłįŽä•Ž∂Äž†Ą
žĄĪŽĆÄÍłįŽä•Ž∂Äž†Ą(vocal cord dysfunction, VCD)žĚÄ ŪõĄŽĎźÍ≥ľŽĮľž¶Ě(laryngeal hyperresponsiveness)žĚī žěąŽäĒ žā¨Žěƞ󟞥ú žä§Ū䳎†ąžä§/Ž∂ąžēą, ŪõĄŽĻĄŽ£®, GERD, žöīŽŹô ŽįŹ ŽĻĄŪäĻžĚīž†Ā ÍłįŽŹĄžěźÍ∑ĻŽ¨ľžßą ŽďĪžóź žĚėŪēī ŽįúžÉĚŪēėŽäĒ ÍįĎžěϞ䧎üį žĄĪŽĆÄžĚė ÍłįŽä•ž†Ā ŪŹźžáĄŽ•ľ ŽßźŪēúŽč§[30]. ž£ľŽ°ú ž†äžĚÄ žó¨žĄĪžóźžĄú ŽįúžÉĚŪēėŽäĒŽćį, ž≤úžčĚžóź Ž≥ĎŽįúŪēėÍłįŽŹĄ ŪēėÍ≥†, ž≤úžčĚÍ≥ľ žÉĀÍīÄžóÜžĚī ŽįúžÉĚŪēėÍłįŽŹĄ ŪēúŽč§. ž¶ĚžÉĀžĚī žôĄž†ĄŪěą žÜƞ觎źėŽäĒ ŪäĻžĄĪžúľŽ°ú ŽßźŽĮłžēĒžēĄ ž≤úžčĚ ŪėĻžĚÄ ŪõĄŽĎźŪėąÍīÄŽ∂ÄžĘÖžúľŽ°ú žė§žĚłŽźėžĖī, ŪôėžěźžóźÍ≤Ć Ž∂ąŪēĄžöĒŪēú ž≤úžčĚ žĻėŽ£ĆŽāė ž†Ąžč† žä§ŪÖĆŽ°úžĚīŽďú žĻėŽ£ĆŽ•ľ ŽįõÍ≤Ć ŪēėÍłįŽŹĄ ŪēúŽč§(ÍłįÍīÄžßÄŪôēžě•ž†úŽāė žä§ŪÖĆŽ°úžĚīŽďúŽäĒ VCDžóź ž†ĄŪėÄ Ūö®Í≥ľ žóÜžĚĆ) [30]. žĄĪŽĆÄŪŹźžáĄÍįÄ ŽįúžÉĚŪēėŽ©ī, ŪėłŪĚ°Í≥§ŽěÄ, žČį Ž™©žÜĆŽ¶¨(dysphonia)žôÄ Ūē®ÍĽė ŪĚ°ÍłįžĄĪ ŪėĎžį©žĚĆ(inspiratory stridor)žĚī Ž™© ž£ľžúĄžóźžĄú Žď§Ž¶¨Í≤Ć ŽźúŽč§. ž¶ĚžÉĀžĚī žěąžĚĄ ŽēĆ flow-volume curvežóźžĄú inspiratory flatteningÍ≥ľ ŪõĄŽĎźÍ≤Ĺ Í≤Äžā¨žóźžĄú žĄĪŽĆÄžĚė žēěŽ∂ÄŽ∂Ą Žāīž†Ą(adduction)Í≥ľ Ūē®ÍĽė Ží∑Ž∂ÄŽ∂ĄžĚė Žč§žĚīžēĄŽ™¨ŽďúŽ™®žĖĎ chinking žÜĆÍ≤¨žĚī Ž≥īžĚīŽ©ī ŪôēžßĄŪē† žąė žěąžúľŽāė, ŪôēžĚłŪēėÍłįŽäĒ žČĹžßÄ žēäžēĄ ŽĆÄŽ∂ÄŽ∂ĄžĚÄ žěĄžÉĀž†Ā ž∂Ēž†ē žßĄŽč®žĚĄ ŪēúŽč§[30]. Ž™© žĚīŽ¨ľÍįźÍ≥ľ ÍłįžĻ®ŽŹĄ ŽŹôŽįėŪē† žąė žěąŽč§. ŽĆÄŽ∂ÄŽ∂ĄžĚÄ ž¶ĚžÉĀ žčúžěĎ 5-10Ž∂Ą žĚīŽāīžóź žěźžóį žÜƞ觎źėŽäĒŽćį, Ž¨ľ ŽßąžčúÍłį, žĪÖ žĚĹÍłį, žč¨ŪėłŪĚ°, ŽįúžāīŽįĒŽ≤ē, ŪóźŽĖ°ÍĪįŽ¶¨Ž©īžĄú žą®žČ¨Íłį(panting) ŽďĪžĚė žĄĪŽĆÄžóź ÍīĞ訞̥ ŽĎźžßÄ žēäŽäĒ ž£ľžĚėžāįŽßĆ(distraction) ŪôúŽŹôžĚī žĄĪŽĆÄŪŹźžáĄžĚė žĘÖŽ£Ćžóź ŽŹĄžõÄžĚī ŽźúŽč§[31]. ÍįĄŪėĻ, žč¨Ūēú ž¶ĚžÉĀžúľŽ°ú žĚĎÍłČžč§žóź ŽāīžõźŪēėžó¨ ÍłįÍīÄ žāĹÍīĞ̥ žčúŪĖČŪēú Ž≥īÍ≥†ÍįÄ žěąžúľŽāė, Ž≥łžßąž†ĀžúľŽ°úŽäĒ žěźžóį Ūėłž†ĄŽźėŽäĒ žßąŪôėžĚīŽč§. ŽĒįŽĚľžĄú, žĚĎͳȞÉĀŪô©žóźžĄúŽäĒ ŪôėžěźŽ•ľ žēąžč¨žčúŪā§Í≥†(reassurance), ŪóźŽĖ°ÍļľŽ¶¨Ž©īžĄú žą®žĚĄ žČ¨ŽŹĄŽ°Ě žú†ŽŹĄ(panting respiration)ŪēėŽ©ī ŽĆÄŽ∂ÄŽ∂Ą Ūėłž†ĄŽźúŽč§[30]. ÍįĄŪėĻ, žč¨Ūēú ŪôėžěźžĚė Í≤Ĺžöį Ūėłž†ĄŽź† ŽēĆÍĻĆžßÄ CPAPŽ•ľ ž†Āžö©ŪēīŽ≥ľ žąė žěąŽč§[32,33]. ͳȞĄĪÍłį ž¶ĚžÉĀžĚī žóÜžĖīžßĄ ŪôėžěźŽäĒ žĚĆžĄĪ žĻėŽ£Ć(speech therapy)Ž•ľ žčúŪĖČŪēėžó¨ ŽßąžĚłŽďúžĹėŪ䳎°§ ŽįŹ žĄĪŽĆÄŪŹźžáĄŽ•ľ žĘÖŽ£ĆŪē† žąė žěąŽäĒ ŪėłŪĚ°Ž≤ēžĚĄ ŽįįžöįŽŹĄŽ°Ě Ūēīžēľ ŪēúŽč§. ŽėźŪēú ŽĆÄŽ∂ÄŽ∂ĄžĚė ŪôėžěźÍįÄ žä§Ū䳎†ąžä§/Ž∂ąžēąžě•žē†Ž•ľ ÍįÄžßÄÍ≥† žěąžúľŽĮÄŽ°ú žĚīžóź ŽĆÄŪēú ž†ēžč†Í≥ľž†Ā žĻėŽ£ĆÍįÄ ŪēĄžöĒŪēėŽč§[30].
Control: exacerbation risk factors/asthma triggers (ͳȞĄĪ ž≤úžčĚ žēÖŪôĒ žúĄŪóė žĚłžěźžôÄ ž≤úžčĚ ž¶ĚžÉĀ žú†ŽįúŽ¨ľžßąžĚĄ ž†úÍĪįŪēėžěź)
ͳȞĄĪ ž≤úžčĚ žēÖŪôĒ žúĄŪóė žĚłžěź(exacerbation risk factors)
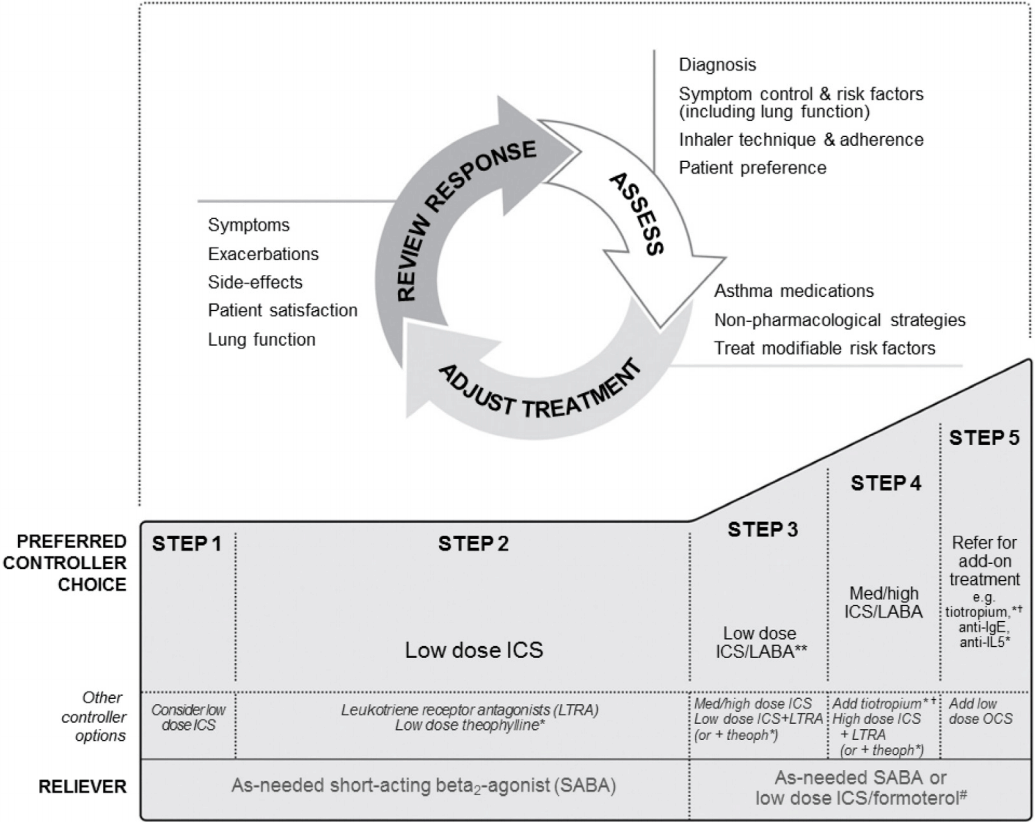
ŪĎú 1žĚÄ ÍłČžĄĪ ž≤úžčĚ žēÖŪôĒžĚė žúĄŪóė žĚłžěźžĚīŽč§[7,11]. ž≤úžčĚžúľŽ°ú žĻėŽ£Ć ž§ĎžĚł Ūôėžěźžóź ŽĆÄŪēī žĚėŽ£ĆžßĄžĚÄ 1) ŪŹČÍįÄ(assess), 2) žĻėŽ£Ć ž°įž†ē(adjust treatment), 3) ŽįėžĚĎ ŪôēžĚł(review response)žĚė Í≥ľž†ēžĚĄ ž†ēÍłįž†ĀžúľŽ°ú(Ž≥Ďžõźžóź Žį©Ž¨łŪē† ŽēĆŽßąŽč§) ŪôēžĚłŪēīžēľ ŪēúŽč§(Fig. 2) [7]. ŪäĻŪěą ŽĻĄž°įž†ą/ŽāúžĻėžĄĪ ž≤úžčĚ ŪôėžěźžóźžĄúŽäĒ ŪėĻžčú ŽÜďžĻėÍ≥† žěąŽäĒ ͳȞĄĪ žēÖŪôĒ žúĄŪóė žĚłžěźÍįÄ žěąŽäĒžßÄ Ž©īŽįÄŪēú ‚ÄúŪŹČÍįÄ(assess)‚ÄĚžôÄ ‚ÄúžĻėŽ£Ć ž°įž†ē(adjust treatment)‚ÄĚžĚī ŪēĄžöĒŪēėŽč§. žėąŽ•ľ Žď§žĖī, Ūėąžē°/ÍįĚŽčīŪėłžāįÍĶ¨Žāė ŪėłÍłį žāįŪôĒžßąžÜĆ(high FENO)Ž•ľ ŪôēžĚłŪēėžó¨ Í∑ł žąėžĻėÍįÄ ž†ēžÉĀŽ≥īŽč§ ŽÜíŽč§Ž©ī, ž†ĀÍ∑Ļž†ĀžúľŽ°ú ž°įž†ąž†ú(ICS)Ž•ľ ž¶ĚŽüČŪēīžēľ ŪēúŽč§. ŪŹźÍłįŽä•žĚī ŽāģžĚĄ ŽēĆžóźŽäĒ ŽĻĄŽ°Ě ž¶ĚžÉĀžĚī ž†ĀŽćĒŽĚľŽŹĄ(žēÖŪôĒŽäĒ ž¶ĚÍįÄŪēėŽĮÄŽ°ú) ž†ĀÍ∑Ļž†ĀžúľŽ°ú ž°įž†ąž†úŽ•ľ ž¶ĚŽüČ/ž∂ĒÍįÄŪēīžēľ ŪēúŽč§. ŽėźŪēú, ͳȞĄĪ žēÖŪôĒžĚė žúĄŪóė žĚłžěźÍįÄ žóÜžĖīžßÄžßÄ žēäžĚÄ žÉĀŪô©žóźžĄúŽäĒ žĻėŽ£ĆŽč®Í≥ĄŽāīŽ¶ľ(step down treatment)žĚÄ žč†ž§ĎŪēīžēľ ŪēėÍ≥†, ž°įž†ąž†ú(ICS)Ž•ľ žôĄž†ĄŪěą ž§ĎŽč®ŪēīžĄúŽäĒ žēą ŽźúŽč§.
ž≤úžčĚ ž¶ĚžÉĀ žú†ŽįúŽ¨ľžßą(asthma triggers)
ŪĎú 2ŽäĒ ž≤úžčĚ ž¶ĚžÉĀ žú†ŽįúŽ¨ľžßąžĚīŽč§[7,34]. ŽĻĄž°įž†ą/ŽāúžĻėžĄĪ ž≤úžčĚ ŪôėžěźžóźžĄúŽäĒ žĘÄ ŽćĒ Ž©īŽįÄŪēú žú†ŽįúŽ¨ľžßą ŪôēžĚłžĚė Í≥ľž†ēžĚī ŪēĄžöĒŪēėŽč§. žú†ŽįúŽ¨ľžßąžĚī žĚėžč¨ŽźėŽäĒ Í≤Ĺžöį, ž¶ĚžÉĀÍ≥ľ žĚėžč¨ŽźėŽäĒ Ž¨ľžßą žā¨žĚīžóź žÉĀÍīÄÍīÄÍ≥ĄÍįÄ žěąŽäĒžßÄ ŪôēžĚłŪēėÍłį žúĄŪēī ŽÖłž∂úžĚľÍłį(ŽÖłž∂ú/ŪôúŽŹô/ŪôėÍ≤Ĺ, ž¶ĚžÉĀ/PEF)Ž•ľ žďįŽäĒ Í≤ÉžĚī ŽŹĄžõÄžĚī ŽźúŽč§. žēĆŽ†ąŽ•īÍłįŽ¨ľžßą(allergen, allergic antigen)žĚÄ ŪäĻž†ē žēĆŽ†ąŽ•īÍłįžĄĪ ž≤úžč̞󟞥úŽßĆ ž¶ĚžÉĀžĚĄ žú†ŽįúŪēúŽč§. žĚīžóź ŽĻĄŪēī ŽĻĄžēĆŽ†ąŽ•īÍłįžĄĪ ÍłįŽŹĄžěźÍ∑ĻŽ¨ľžßąžĚė Í≤Ĺžöį Ž™®Žď† ž≤úžčĚ Ūôėžěź(žēĆŽ†ąŽ•īÍłįžĄĪ ŽįŹ ŽĻĄžēĆŽ†ąŽ•īÍłįžĄĪ ž≤úžčĚ)žóźÍ≤Ć ž¶ĚžÉĀžĚĄ žú†ŽįúžčúŪā¨ žąė žěąŽč§. ž≤úžčĚ ž¶ĚžÉĀ žú†ŽįúŽ¨ľžßąžĚĄ ž†úÍĪįŪēėÍĪįŽāė ŪöĆŪĒľŪēėŽäĒ Í≤ÉžĚÄ ž≤úžčĚžĚė ž°įž†ąžóź žěąžĖīžĄú Ūö®Í≥ľŽäĒ Ūôēžč§ŪēėŽč§[7,34]. ŪēėžßÄŽßĆ ž≤úžčĚžĚė ž°įž†ąžóź žĚīŽ•īÍ≤Ć Ūē† ŽßĆŪĀľ ž∂©Ž∂ĄŪěą žú†ŽįúŽ¨ľžßą ŽÖłž∂úžĚĄ ž§ĄžĚīŽäĒ Žį©Ž≤ēžóź ŽĆÄŪēīžĄúŽäĒ žēĄžßĀ ŽÖľŽěÄžĚī ŽßéÍ≥†, žú†ŽįúŽ¨ľžßąžĚĄ žôĄž†ĄŪěą ž†úÍĪįŪēėŽäĒ Í≤ÉžĚÄ žā¨žč§žÉĀ Ž∂ąÍįÄŽä•ŪēėŽč§[34]. ŽĒįŽĚľžĄú, žú†ŽįúŽ¨ľžßąžĚė ŽÖłž∂úžĚī žěąŽćĒŽĚľŽŹĄ ž≤úžčĚ ž¶ĚžÉĀžĚī ŽįúžÉĚŪēėžßÄ žēäÍ≤Ć ŪēėŽäĒ žēĹŽ¨ľ žĻėŽ£Ć(ŪäĻŪěą, ŪĚ°žěÖžēĹŽ¨ľ ž°įž†ąž†ú)ÍįÄ žú†ŽįúŽ¨ľžßąžĚė ŪöĆŪĒľ(ŪôėÍ≤ĹÍīÄŽ¶¨)Ž≥īŽč§ Ūõ®žĒ¨ ŽćĒ ž§ĎžöĒŪēėŽč§[7].
žēĆŽ†ąŽ•īÍłįŽ¨ľžßą(allergen, allergic antigen)
ŪĚĒŪēú žēĆŽ†ąŽ•īÍłįŽ¨ľžßąžĚÄ žßĎŽ®ľžßÄ žßĄŽďúÍłį, žē†žôĄŽŹôŽ¨ľžĚė ŪĄł, ŽįĒŪÄīŽ≤ĆŽ†ą, Í≥įŪĆ°žĚī, ÍĹÉÍįÄŽ£® ŽďĪžĚī žěąŽč§. Ūēú ÍįÄžßÄ ŪôėÍ≤ĹÍīÄŽ¶¨ Žį©Ž≤ē(single intervention: allergen impermeable bed cover)žúľŽ°úŽäĒ žěĄžÉĀž†Ā Ūėłž†ĄžĚĄ ÍłįŽĆÄŪē† žąė žěąžĚĄ ž†ēŽŹĄžĚė ž∂©Ž∂ĄŪěą žēĆŽ†ąŽ•īÍłįŽ¨ľžßąžĚĄ ÍįźžÜĆžčúŪā§žßÄ Ž™ĽŪēėŽäĒ Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąžúľŽāė, ŪŹ¨ÍīĄž†ĀžĚł ŪôėÍ≤ĹÍīÄŽ¶¨(multi-component intervention: allergen impermeable bed cover+HEPA filtered vacuum cleaner+HEPA filtered air cleaner+No pets+No damp area)Ž°ú žč§ŽāīžēĆŽ†ąŽ•īÍłįŪē≠žõźžóź ŽĆÄŪēú ŽÖłž∂úžĚĄ ž§ĄžĚīŽ©ī ž≤úžčĚ ÍīÄŽ†® žĚīŪôėžú®žĚĄ ÍįźžÜĆžčúŪā§ŽäĒ Ūö®Í≥ľÍįÄ žěąžóąŽč§[35]. ŪēėžßÄŽßĆ, Ž™®Žď† žóįÍĶ¨ Í≤įÍ≥ľÍįÄ žĚľÍīÄžĄĪ žěąÍ≤Ć Žāėžė§žßÄ žēäžēėÍ≥†[36], ŪôėÍ≤ĹÍīÄŽ¶¨žóź ŽďúŽäĒ ŽĻĄžö©žĚī ŽßéžēĄ ŽĻĄžö© Ūö®Í≥ľž†ĀžĚīžßÄ žēäžĚÄ Ž©īžĚī žěąžúľŽĮÄŽ°ú, žēĆŽ†ąŽ•īÍłįŽ¨ľžßą ŪöĆŪĒľ(allergen avoidance)ŽäĒ ž≤úžčĚÍīÄŽ¶¨žĚė žĚľŽįėž†ĀžĚł ž†ĄŽěĶžúľŽ°ú Í∂Ćžě•ŽźėžßÄ žēäÍ≥† žěąŽč§(GINA 2017 Appendix, Chapter 6, Non-pharmacological therapies and strategies) [7]. ŪēėžßÄŽßĆ ŪėĄžč§ž†ĀžúľŽ°ú ŽĻĄž°įž†ą/ŽāúžĻėžĄĪ ž≤úžčĚ ŪôėžěźžóźžĄúŽäĒ ž¶ĚžÉĀž°įž†ąÍ≥ľ žēÖŪôĒžėąŽį©žĚĄ žúĄŪēú Ž™®Žď† ŽÖłŽ†•žĚĄ Í≤Ĺž£ľŪēīžēľ ŪēėŽĮÄŽ°ú, ŪôėžěźÍįÄ Í≤Ĺž†úž†ĀžúľŽ°ú žó¨žú†ÍįÄ žěąŽč§Ž©ī ŪŹ¨ÍīĄž†ĀžĚł ŪôėÍ≤ĹÍīÄŽ¶¨(žēĆŽ†ąŽ•īÍłį Ž¨ľžßą ŪöĆŪĒľ)Ž•ľ ž∂Ēž≤úŪēėŽäĒ Í≤ÉžĚī Ūē©Ž¶¨ž†ĀžĚīŽĚľÍ≥† ŪĆźŽč®ŽźúŽč§.
ŽĻĄžēĆŽ†ąŽ•īÍłįžĄĪ ÍłįŽŹĄžěźÍ∑ĻŽ¨ľžßą
ŽĻĄžēĆŽ†ąŽ•īÍłįžĄĪ ÍłįŽŹĄžěźÍ∑ĻŽ¨ľžßąžóźŽäĒ žč§ŽāīÍ≥ĶÍłįžė§žóľ(VOCs/ÍįĄž†ĎŪĚ°žóį/žĚĆžčĚŽ¨ľž°įŽ¶¨žóįÍłį/ÍįĞ䧎†ąžĚłžßÄ), žč§žôłÍ≥ĶÍłįžė§žóľ(DEG/ŽĮłžĄłŽ®ľžßÄ/ŪĖ•žąė), ÍłįŪõĄ/žė®ŽŹĄ Ž≥ÄŪôĒ(žį®Í≥† ÍĪīž°įŪēú Í≥ĶÍłį) ŽďĪžĚī žěąŽč§. ž≤úžčĚžĚī žěė ž°įž†ąŽźėÍ≥† žěąŽäĒ ŪôėžěźžóźžĄú ž≤úžčĚžóź žĘčžßÄ žēäžĚÄ ŪôėÍ≤Ĺž°įÍĪīžĚĄ ŽįėŽďúžčú ŪĒľŪē† ŪēĄžöĒŽäĒ žóÜŽč§. Í∑łŽü¨Žāė ž≤úžčĚ ž°įž†ąžĚī žēą ŽźėŽäĒ ŪôėžěźŽäĒ ÍłįŽŹĄžěźÍ∑ĻŽ¨ľžßąžĚī ŽßéžĚÄ žÉĀŪÉúžóźžĄúŽäĒ žč†ž≤ī ŪôúŽŹôžĚĄ ŪĒľŪēėŽäĒ Í≤ÉžĚī ŽįĒŽěĆžßĀŪēėŽč§(GINA2017 Appendix, Chapter 6, Nonpharmacological therapies and strategies) [7]. žį®Í≥† ÍĪīž°įŪēú Í≥≥žóź žěąžĚĄ ŽēĆ ŽĎźÍļľžöī Žßąžä§ŪĀ¨Ž•ľ žā¨žö©ŪēėŽ©ī Í≥ĶÍłįŽ•ľ žäĶŪēėÍ≥† ŽĒįŽúĽŪēėÍ≤Ć ŪēėŽäĒŽćį ŽŹĄžõÄžĚī ŽźúŽč§[37].
žēĹŽ¨ľ, žčĚŪíą/žčĚŪíąž≤®ÍįÄŽ¨ľ, žßĀžóÖžĄĪ ŽÖłž∂úŽ¨ľžßą
Aspirin & NSAIDs: ž†Ąž≤ī ž≤úžčĚžĚė 7%, ž§Ďž¶Ěž≤úžčĚžĚė 15%ŽäĒ aspirin & NSAIDsžóź žĚėŪēī ž≤úžčĚž¶ĚžÉĀžĚī ŽāėŽĻ†žßą žąė žěąŽäĒ žēĄžä§ŪĒľŽ¶į žēÖŪôĒ ÍłįŽŹĄ žßąŪôė(aspirin-exacerbated respiratory disease, AERD)žóź ŪēīŽčĻŪēúŽč§[7]. žēĄžä§ŪĒľŽ¶į žēÖŪôĒ ÍłįŽŹĄ žßąŪôė(AERD)žĚÄ ž≤úžčĚ, ŽßĆžĄĪ žö©žĘÖžĄĪ Ž∂ÄŽĻĄŽŹôžóľžĚī žěąŽäĒ ŪôėžěźžóźžĄú žēĄžä§ŪĒľŽ¶į Í≥ľŽĮľžĄĪ(aspirin or NSAIDsžóź ŽÖłž∂úŽźėžóąžĚĄ ŽēĆ bronchospasmÍ≥ľ nasal congestionžĚī ŽįúžÉĚ)žĚī žěąžĚĄ ŽēĆ žßĄŽč®Ūē† žąė žěąŽč§. Í≥ľÍĪįžóźŽäĒ žēĄžä§ŪĒľŽ¶į žú†Žįú ž≤úžčĚ(aspirin-induced asthma) ŪėĻžĚÄ žēĄžä§ŪĒľŽ¶į Í≥ľŽĮľžĄĪ ž≤úžčĚ(aspirin-sensitive asthma)žĚīŽĚľÍ≥† Ž∂ąŽ†ÄžúľŽāė, žēĄžä§ŪĒľŽ¶į Í≥ľŽĮľžĄĪžĚÄ AERDžĚė Ūēú ÍįÄžßÄ ŪäĻžĄĪžóź Ž∂ąÍ≥ľŪēėÍ≥†(Ž¨ľŽ°† ž§ĎžöĒŪēú ŪäĻžĄĪžĚīžßÄŽßĆ), Íłįž†Äžóź žēĄžä§ŪĒľŽ¶įÍ≥ľ Ž¨īÍīÄŪēėÍ≤Ć žßĄŪĖČŪēėŽäĒ ž≤úžčĚÍ≥ľ ŽßĆžĄĪ žö©žĘÖžĄĪ Ž∂ÄŽĻĄŽŹôžóľžĚī žěąžúľŽĮÄŽ°ú, žĶúÍ∑ľžóźŽäĒ AERDŽ°ú Ž∂ÄŽ•īÍ≥† žěąŽč§[38,39]. AERDžĚė žßĄŽč®žĚÄ ž≤úžčĚ ŪôėžěźžóźžĄú žēĄžä§ŪĒľŽ¶įÍ≥ľŽĮľžĄĪžĚė Ž≥ĎŽ†•žĚĄ ŪôēžĚłŪē®žúľŽ°úžć® ÍįÄŽä•ŪēėŽāė, Ž≥ĎŽ†•žĚī Ž™®ŪėłŪēú Í≤Ĺžöį(žó¨Žü¨ ÍįÄžßÄ žēĹŽ¨ľžĚī Žď§žĖīÍįĄ ŪõĄ ŽįėžĚĎžĚī žÉĚÍ≤ľÍĪįŽāė, žĚľÍīÄžĄĪ žěąÍ≤Ć ŽįėžĚĎžĚī žÉĚÍłįžßÄ žēäžĚÄ Í≤Ĺžöį)žóźŽäĒ oral aspirin challenge test ŪėĻžĚÄ bronchial aspirin (lysine aspirin) challenge testŽ•ľ žčúŪĖČŪēīŽ≥ľ žąė žěąŽč§. AERDŽ°ú ŪôēžĚłŽźėŽ©ī, žßĄŪÜĶžÜƞ󾞆úŽ•ľ žā¨žö©Ūē† ŽēĆ ÍĶźžį®ŽįėžĚĎžĚī žóÜŽäĒ selective COX (cyclooxygenase)-2 inhibitorŽāė acetaminophen (Í≥†žö©ŽüČ[1ŪöĆžö©ŽüČžĚī 1,000 mg žĚīžÉĀ]žóźžĄúŽäĒ ÍĶźžį®ŽįėžĚĎ ÍįÄŽä•)žĚĄ žā¨žö©Ūēīžēľ ŪēúŽč§[40,41]. žöįŽ¶¨ŽāėŽĚľžóźžĄúŽäĒ žěė žčúŪĖČŪēėžßÄ žēäžßÄŽßĆ, aspirin desensitizationŽŹĄ Í≥†Ž†§ŪēīŽ≥ľ žąė žěąŽč§[39].
ACEi/ARB: angiotensin-converting enzyme inhibitor (ACEi)ŽäĒ ž≤úžčĚžĚė žēÖŪôĒ žóÜžĚī, ÍłįžĻ®žĚĄ žú†ŽįúžčúŪā¨ žąė žěąŽč§(ACEi žā¨žö©žěźžĚė 20%) [42]. Angiotensin receptor blocker (ARB)ŽäĒ ŽďúŽ¨ľÍ≤Ć ÍłįžĻ®žĚĄ žĚľžúľŪā¨ žąė žěąŽč§ŽäĒ Ž≥īÍ≥†ÍįÄ žěąžúľŽāė[43], ŽĆÄž≤īž†ĀžúľŽ°ú ÍłįžĻ®žĚĄ žĚľžúľŪā§žßÄ žēäŽäĒŽč§Í≥† žó¨ÍłįÍ≥† žěąŽč§[42]. ACEižóź žĚėŪēī ŽįúžÉĚŪēú ÍłįžĻ®žĚÄ ŽĆÄŽ∂ÄŽ∂Ą ž§ĎŽč®ŪēėŽ©ī 1-4ž£ľ žĚīŽāīžóź Ūėłž†ĄŽźúŽč§[42]. ŽĻĄž°įž†ą/ŽāúžĻėžĄĪ ž≤úžčĚ ŪôėžěźÍįÄ ÍłįžĻ®Í≥ľ Ūē®ÍĽė ACEiŽāė ARBŽ•ľ žā¨žö© ž§ĎžĚīŽĚľŽ©ī ACEi ‚Üí ARB, ARB ‚Üí angiotensin Ž¨īÍīÄžēĹŽ¨ľŽ°ú Ž≥ÄÍ≤ĹŪēėŽäĒ Í≤ÉžĚÄ Ūē©Ž¶¨ž†ĀžúľŽ°ú Ž≥īžĚīŽāė, 1Žč¨ žĚīŽāī ÍłįžĻ®žĚė Ūėłž†ĄžĚī žó܎觎©ī ACEiŽāė ARBžôÄŽäĒ Ž¨īÍīÄŪēėŽč§Í≥† ŪĆźŽč®Ūē† žąė žěąžúľŽĮÄŽ°ú, Ūôėžěź žÉĀŪÉúžóź ŽĒįŽĚľ ACEi/ARBžĚė žě¨žā¨žö©žĚĄ Í≥†Ž†§Ūē† žąė žěąÍ≤†Žč§.
Ž≤†ŪÉÄžį®Žč®ž†ú: Ž≤†ŪÉÄžį®Žč®ž†úŽäĒ ŽĆÄŽ∂ÄŽ∂ĄžĚė ž≤úžčĚ ŪôėžěźžóźÍ≤Ć bronchospasmžĚĄ žú†ŽŹĄŪēėÍ≥†[7], žĚīÍ≤ÉžĚÄ žÜĆŽüČ(topical beta-blocker eye drop)žúľŽ°úŽŹĄ ŽįúžÉĚŪē† žąė žěąŽč§[44]. Ž≤†ŪÉÄžį®Žč®ž†úÍįÄ ŪēĄžöĒŪēú žÉĀŪô©žóźžĄúŽäĒ Ž≤†ŪÉÄ1žĄ†ŪÉĚžį®Žč®ž†úŽ•ľ žā¨žö©Ūēīžēľ ŪēúŽč§. Í≤Ĺžöįžóź ŽĒįŽĚľžĄúŽäĒ Ž≤†ŪÉÄ1žĄ†ŪÉĚžį®Žč®ž†ú žó≠žčú bronchospasmžĚĄ žú†ŽŹĄŪēėŽĮÄŽ°ú, ž¶ĚžÉĀžĚī žěąŽäĒ ŽāúžĻėžĄĪ ž≤úžčĚ ŪôėžěźžóźžĄú ŽĆÄž≤īžēĹŽ¨ľžĚī žěąÍ≥†, Ž≤†ŪÉÄžį®Žč®ž†úŽ•ľ ŽįėŽďúžčú žā¨žö©ŪēėžßÄ žēäžēĄŽŹĄ ŽźúŽč§Ž©ī ž§ĎŽč®ŪēėŽäĒ Í≤ÉžĚī Ūē©Ž¶¨ž†ĀžĚīŽč§.
žčĚŪíą/žčĚŪíąž≤®ÍįÄŽ¨ľ(food/ food additives): ž≤úžčĚžĚė žēÖŪôĒ žöĒžÜĆŽ°úžĄú žĚĆžčĚŽ¨ľ žēĆŽ†ąŽ•īÍłįŽäĒ ŪĚĒŪēėžßÄ žēäŽč§[7]. žĚĆžčĚŽ¨ľ ŪöĆŪĒľŽäĒ Ūôēžč§Ūēú Ž≥ĎŽ†• ŪėĻžĚÄ Í≤ĹÍĶ¨žú†ŽįúžčúŪóėžúľŽ°ú žēĆŽ†ąŽ•īÍłįÍįÄ žôĄž†ĄŪěą ž¶ĚŽ™ÖŽźėÍłį ž†ĄÍĻĆžßÄŽäĒ Í∂ĆÍ≥†ŪēėžßÄ žēäŽäĒŽč§. žčĚŪíąž≤®ÍįÄŽ¨ľžĚÄ žčĚŪíąžĚė Ž≥īž°īžĚīŽāė ÍįÄÍ≥ĶÍ≥ľž†ēžóźžĄú Žď§žĖīÍįÄŽäĒ Ž¨ľžßąŽ°ú žĄ§ŪĆĆžĚīŪäł(sulfite, žēĄŪô©žāįžóľ), ŪÉÄŪ䳎̾žßĄ(tatrazine, žčĚžö©žÉČžÜĆ Ūô©žÉČ ž†ú5Ūėł), Ž≤§ž°įžāįžóľ(benzoate), ͳĎ£®ŪÉźžāįŽāėŪ䳎•®(monosodium glutamate, MSG) ŽďĪžĚī bronchospasmžĚĄ žĚľžúľŪā¨ žąė žěąŽč§Í≥† Ž≥īÍ≥†ŽźėžóąŽč§. ŪēėžßÄŽßĆ, žĶúÍ∑ľžóźŽäĒ žĄ§ŪĆĆžĚīŪäł žôłžóźŽäĒ bronchospasm žú†ŽįúžĚī žóÜŽč§Í≥† Ž≥īÍ≥† žěąŽč§[7,12] žĄ§ŪĆĆžĚīŪ䳎äĒ žôĞ̳/Žß•ž£ľ, ŽßźŽ¶į Í≥ľžĚľ/ÍĪīžĖīŽ¨ľ, ÍįÄÍ≥ĶŽźú Íįźžěź, žÉąžöįžôÄ ÍįôžĚÄ žčĚŪíąžĚė Ž≥īž°īž†ú ŽįŹ žāįŪôĒŽį©žßÄž†úŽ°ú žĚīžö©ŪēėŽäĒŽćį, žĄ≠ž∑® ŪõĄ ž¶ČÍįĀŪėē Í≥ľŽĮľŽįėžĚĎ(bronchospasm, urticaria)žĚī ŽįúžÉĚŪē† žąė žěąŽč§[34]. ž†Ąž≤ī ž≤úžčĚ ŪôėžěźžĚė 5-10%, ž§Ďž¶Ěž≤úžčĚ ŪôėžěźžĚė 10-20%žóźžĄú žĄ§ŪĆĆžĚīŪäł žĄ≠ž∑®žóź žĚėŪēī bronchospasmžĚī ŽįúžÉĚŪē† žąė žěąŽäĒ Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąŽč§[45,46]. žßĄŽč®žĚÄ Ž™ÖŪôēŪēú Ž≥ĎŽ†• ŪėĻžĚÄ žú†ŽįúžčúŪóėžĚĄ ŪÜĶŪēī ÍįÄŽä•ŪēėŽč§. žßĄŽč®ŽźėŽ©ī žčĚŪíąžĚė ž≤®ÍįÄŽ¨ľŽ°ú žĄ§ŪĆĆžĚīŪäł ž†úž†ú(sulfur dioxide, sodium sulfite, sodium bisulfite, sodium metabisulfite, potassium bisulfite, potassium metabisulfite)ÍįÄ ŪŹ¨Ūē®Žźú Í≤ÉžĚÄ žĶúŽĆÄŪēú ŪöĆŪĒľŪēėŽŹĄŽ°Ě ÍĶźžú°Ūēīžēľ ŪēúŽč§[34].
žßĀžóÖžĄĪ ŽÖłž∂úŽ¨ľžßą: žěĎžóÖžóįÍīÄž≤úžčĚ(work-related asthma, WRA)žóźŽäĒ žßĀžóÖžĄĪ ž≤úžčĚ(occupational asthma, OA)Í≥ľ žěĎžóÖžēÖŪôĒž≤úžčĚ(work-exacerbated asthma, WEA)žĚī žěąÍ≥†, OAŽäĒ ž∂ĒÍįÄž†ĀžúľŽ°ú sensitizer-induced OAžôÄ irritant-induced OAŽ°ú ŽāėŽČúŽč§[47]. Irritant-induced OAžĚė Í≤Ĺžöį Í≥†ŽÜ掏Ą ÍįÄžä§(žĄłž†ēž†ú/žÜĆŽŹÖž†ú[žóľžÜĆÍįÄžä§, žēĒŽ™®ŽčąžēĄ, ŽĻôžīąžāį, ͳĎ£®ŪÉÄŽ•īžēĆŽćįŪ칎ďú ŽďĪ])žĚė ŪėłŪĚ°Íłį ŽÖłž∂ú 24žčúÍįĄ Žāīžóź ž≤úžčĚž¶ĚžÉĀžĚī ŽįúžÉĚŪēú Ž≥ĎŽ†•žĚĄ Ž≥īÍ≥† žßĄŽč®ŪēúŽč§. Sensitizer-induced OAŽäĒ žěĎžóÖžě• žā¨žö©Ž¨ľžßą(material safety data, MSD)žĚĄ Í≤ÄŪ܆ŪēėÍ≥† work-related changeŽ•ľ serial PEF (or FEV1)Ž•ľ ŪÜĶŪēī ŪôēžĚłŪēėÍĪįŽāė, žßĀž†Ďž†ĀžĚł ÍłįÍīÄžßÄžú†ŽįúžčúŪóėžĚĄ ŪÜĶŪēī žßĄŽč®ŪēúŽč§[48]. Sensitizer-induced OAžĚė Í≤Ĺžöį žßĀžĘÖžĚė Ž≥ÄÍ≤ĹžĚī ŽįėŽďúžčú ŪēĄžöĒŪēėŽāė, irritant-induced OAžôÄ WEAŽäĒ ž†Āž†ąŪēú ŽÖłž∂úÍīÄŽ¶¨(žěĎžóÖžě• ŪôėÍ≤ĹÍīÄŽ¶¨, Žßąžä§ŪĀ¨)ÍįÄ žĚīŽ£®žĖīžßĄŽč§Ž©ī žßĀžĘÖžú†žßÄÍįÄ ÍįÄŽä•ŪēėŽč§[49]. ŽĻĄž°įž†ą/ŽāúžĻėžĄĪ ž≤úžčĚ ŪôėžěźžóźžĄú žßĀžóÖ(žßĀžĘÖ) ŽįŹ žěĎžóÖ žóįÍīÄžĄĪ(work-relatedness)žĚė ŪôēžĚłžĚÄ ŽįėŽďúžčú ŪēĄžöĒŪēėÍ≥†, žßĀžĘÖŽ≥ÄÍ≤ĹÍ≥ľ ŽÖłž∂úÍīÄŽ¶¨žóź ŽĆÄŪēú ž°įžĖł/ÍĶźžú°žĚĄ Ūēīžēľ ŪēúŽč§.
ž§Ďž¶Ěž≤úžčĚ(severe asthma)žĚė žĻėŽ£Ć ž†ĎÍ∑ľ
ŽĻĄž°įž†ą/ŽāúžĻėž≤úžčĚ Ūôėžěźžóź ŽĆÄŪēī Žč§Ž•ł žßąŪôė Žįįž†ú(diagnosis other than asthma)žôÄ ÍĶźž†ē ÍįÄŽä• žĚłžěź(potentially modifiable factors: adherence/inhaler technique, comorbidities, exacerbation risk factors/asthma triggers)žóź ŽĆÄŪēú ž°įžĻėŽ•ľ ž†ĀÍ∑Ļž†ĀžúľŽ°ú žčúŪĖČŪēėžėÄžĚƞ󟎏Ą ž≤úžčĚ ž¶ĚžÉĀžĚī žßÄžÜ掟† ŽēĆ ŽĻĄŽ°úžÜĆ ž§Ďž¶Ěž≤úžčĚ žßĄŽč®žĚī Ž∂Ğ󨎟† žąė žěąŽč§(Fig. 1). ž§Ďž¶Ěž≤úžčĚžúľŽ°ú ŪôēžĚł(concede)ŽźėŽ©ī, ž°įž†ąž†ú žĻėŽ£ĆŽ•ľ Í∑ĻŽĆÄŪôĒ(žĶúž†ĀŪôĒ)Ūē®Í≥ľ ŽŹôžčúžóź treatable traits (for phenotype or endotype)Ž•ľ ŪôēžĚłŪēėÍłį žúĄŪēú Í≤Äžā¨Ž•ľ žčúŪĖČŪēīžēľ ŪēúŽč§[50]. ž°įž†ąž†ú žĻėŽ£ĆŽ•ľ Í∑ĻŽĆÄŪôĒ(žĶúž†ĀŪôĒ)ŪēėžėÄžĚƞ󟎏Ą ž¶ĚžÉĀžĚī žßÄžÜ掟ėŽäĒ ž≤úžčĚ ŪôėžěźžóźÍ≤ĆŽäĒ ŪôēžĚłŽźú treatable traits (for phenotype or endotype) Í≤įÍ≥ľŽ•ľ ŽįĒŪÉēžúľŽ°ú specific severe asthma treatmentsžĚė žčúŪĖȞ̥ Í≥†Ž†§Ūēėžó¨žēľ ŪēúŽč§. žĚī Í≤Ĺžöį žĚėŽ£ĆŽĻĄžö©žĚė ž¶ĚÍįÄ(biologics ŽďĪ)žôÄ žĻėŽ£ĆžĚė Ž∂ÄžěĎžö© ŽįúžÉĚ(ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďú žú†žßÄ žĻėŽ£Ćžóź žĚėŪēú Í≥®Žč§Í≥Ķž¶Ě ŽďĪ)žĚī ÍįÄŽä•ŪēėŽĮÄŽ°ú, Ūôėžěź/Ž≥īŪėłžěźžôÄ ŽĻĄžö©-Ūö®Í≥ľ/žúĄŪóė-žĚīžĚĶžóź ŽĆÄŪēú ž∂©Ž∂ĄŪēú ŪėĎžĚėŽ•ľ Ūēú ŪõĄ žĻėŽ£Ć žó¨Ž∂ÄŽ•ľ Í≤įž†ēŪēīžēľ ŪēúŽč§(Fig. 1). ŽėźŪēú ŽßéžĚÄ ž§Ďž¶Ěž≤úžčĚ ŪôėžěźžóźžĄú žôĄŽ≤ĹŪēú ž¶ĚžÉĀž°įž†ąžĚÄ Ž∂ąÍįÄŽä•Ūēú Í≤ĹžöįÍįÄ ŽßéžúľŽĮÄŽ°ú, ŽÜížĚÄ ž†ēŽŹĄžĚė ž¶ĚžÉĀž°įž†ąŽ≥īŽč§ŽäĒ žēÖŪôĒŽ°ú žĚłŪēú žĚĎÍłČžč§ Žį©Ž¨łžĚĄ ž§ĄžĚīŽäĒ Í≤ɞ̥ Ž™©ŪĎúŽ°ú ŪēėŽäĒ Í≤ÉžĚī ŽćĒ ŽįĒŽěĆžßĀŪē† žąė žěąŽč§[11]. ŽĆÄŽ∂ÄŽ∂ĄžĚė ž≤úžčĚžßÄžĻ®žĚÄ ž§Ďž¶Ěž≤úžčĚžúľŽ°ú ŪôēžĚłŽź† Í≤Ĺžöį Í≤ĹŪóė ŽßéžĚÄ ž≤úžčĚž†ĄŽ¨łÍįÄžóźÍ≤Ć ŪôėžěźŽ•ľ žĚėŽĘįŪē† Í≤ɞ̥ Í∂ĆÍ≥†ŪēúŽč§[1,5,7].
Optimizing controller treatment usually after a course of oral glucocorticoid (GC) or an i.m. of triamcinolone
ž§Ďž¶Ěž≤úžčĚžúľŽ°ú ŪôēžĚłŽźėŽ©ī, treatable traits (phenotyps/endotypes)žĚė ŪôēžĚłžĚĄ žúĄŪēú Í≤Äžā¨Ž•ľ žčúŪĖČŪē®Í≥ľ ŽŹôžčúžóź, ž°įž†ąž†ú(controller) žĻėŽ£ĆŽ•ľ žĶúž†ĀŪôĒ(optimization)Ūēīžēľ ŪēúŽč§. ŪėĄžě¨ ŽĻĄž°įž†ą žÉĀŪÉúžĚł Í≤Ĺžöį, ž°įž†ąž†ú žĻėŽ£ĆžĚė žĶúž†ĀŪôĒžôÄ Ūē®ÍĽė Žč®ÍłįÍįĄžĚė Í≥†žö©ŽüČ ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďú žĻėŽ£ĆŽ•ľ Í≥†Ž†§ŪēīŽ≥ľ žąė žěąŽč§.
ž°įž†ąž†ú žĻėŽ£ĆžĚė žĶúž†ĀŪôĒ(optimizing controller treatment)
ž§Ďž¶Ěž≤úžčĚŽŹĄ žĚľŽįė ž≤úžčĚÍ≥ľ Žßąžį¨ÍįÄžßÄŽ°ú ž°įž†ąžĚĄ Ž™©ŪĎúŽ°ú Žč®Í≥ĄŽ≥Ą žēĹŽ¨ľ žĻėŽ£Ć(stepwise treatment)Ž•ľ žčúŪĖČŪēúŽč§(Fig. 2) [7]. GINA step 4ÍĻĆžßÄžĚė žēĹŽ¨ľ(high ICS/LABA, tiotropium, theophylline, LTRA)žĚĄ Ž™®ŽĎź Žč§ žā¨žö©ŪēėÍ≥† žěąŽäĒ žÉĀŪÉúžóźžĄúŽŹĄ ŪôėžěźžĚė ž≤úžčĚžĚī ŽĻĄž°įž†ą žÉĀŪÉúŽĚľŽ©ī(ŽŹôžčúžóź, Žč§Ž•ł žßąŪôė Žįįž†úŽźėÍ≥†, ÍĶźž†ēÍįĎ䕞̳žěźžóź ŽĆÄŪēú Ž™®Žď† ž°įžĻėÍįÄ žĚīŽ£®žĖīžßĄ Í≤Ĺžöį) ICS žö©ŽüȞ̥ very high dose (high dosežĚė 2Žįį ž†ēŽŹĄ)ÍĻĆžßÄ žė¨Ž†§Ž≥ľ žąė žěąŽč§(very high dose: fluticasone, 1,000-2,000 őľg; budesonide, 1,600-3,200 őľg) [7,51,52]. Smaller particle ICS (beclomethasone, budesonide)Ž•ľ Íłįž°ī ICSžóź ž∂ĒÍįÄŪēėŽäĒ Žį©Ž≤ēžĚĄ žć®Ž≥ľ žąėŽŹĄ žěąŽč§[51]. ICS ž¶ĚŽüČ(as very high dose)žĚÄ ž≤úžčĚ ž°įž†ąžóź ŽŹĄžõÄžĚī Ūôēžč§Ūěą ŽźėŽāė, Ž∂ÄžěĎžö©(oral candidiasis, osteoporosis) ŽįúžÉĚžĚī ž¶ĚÍįÄŪēėŽĮÄŽ°ú, žĚīžóź ŽĆÄŪēī Ž™®ŽčąŪĄįŽßĀžĚī ŪēĄžöĒŪēėŽč§[7,53-56].
Žč®ÍłįÍįĄžĚė Í≥†žö©ŽüČ ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďú žĻėŽ£Ć(a course of oral GC or an i.m. of triamcinolone)
ž§Ďž¶Ěž≤úžčĚ ŪôėžěźÍįÄ ŪėĄžě¨ ŽĻĄž°įž†ą žÉĀŪÉúžĚł Í≤Ĺžöį type 2 inflammationžĚĄ ŪôēžĚłŪēėŽäĒ Í≤Äžā¨(blood eosinophil, FeNO, sputum eosinophil)Ž•ľ žčúŪĖČŪēú ŪõĄ, Žč®ÍłįÍįĄžĚė Í≥†žö©ŽüČ ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďú žĻėŽ£ĆŽ•ľ Í≥†Ž†§ŪēīŽ≥ľ žąė žěąŽč§(prednisolone 40 mg [30-60 mg]/day for upto 2 weeks; triamcinolone 80 mg [40-120 mg] IM once) [57-60]. Žč®ÍłįÍįĄžĚė Í≥†žö©ŽüČ ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďúŽäĒ žóľž¶ĚžĚĄ žĖĶž†úŪēėžó¨, žä§ŪÖĆŽ°úžĚīŽďú ŽįėžĚĎžĄĪžĚĄ žú†žßÄŪēėŽäĒ Žćį ŽŹĄžõÄžĚī ŽźėŽäĒŽćį, Í∑ł žĚīžú†ŽäĒ žóľž¶Ě(inflammation)žĚÄ Í∑ł žěźž≤īŽ°ú žä§ŪÖĆŽ°úžĚīŽďú ŽįėžĚĎžĄĪžĚĄ žēĹŪôĒžčúŪā§Íłį ŽēĆŽ¨łžĚīŽč§(žóľž¶ĚžĚī žěąžúľŽ©ī proinflammatory transcription factoržĚł activation protein (AP)-1žĚĄ ŪôúžĄĪŪôĒŽźėÍ≥†, IL2/IL4ÍįÄ ž¶ĚÍįÄŪē®). Žč®ÍłįÍįĄžĚė Í≥†žö©ŽüČ ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďú žĻėŽ£ĆŽäĒ ŪôėžěźžĚė žě•Íłįž†ĀžĚł ŪĚ°žěÖžä§ŪÖĆŽ°úžĚīŽďúÍįÄ Ūö®Í≥ľŽ•ľ žú†žßÄŪē† ž†ēŽŹĄŽ°ú ÍłįŽŹĄ žóľž¶ĚžĚĄ ž§ĄžĚľ žąė žěąŽč§[61,62].
Tests to identify the treatable traits (phenotyps/ endotypes) & Specific severe asthma treatments"
Persistent type 2 inflammation despite high ICS & Systemic GC responsiveness
Í≥†ÍįēŽŹĄ ž≤úžčĚ žĻėŽ£Ć(GINA step 4 treatment [high ICS/LABA] žĚīžÉĀžĚė ž≤úžčĚ žĻėŽ£Ć)Ž•ľ žčúŪĖČŪē®žóźŽŹĄ Ž∂ąÍĶ¨ŪēėÍ≥†, ŪôėžěźžĚė ž≤úžčĚžĚī ž§Ďž¶Ěž≤úžč̞̾ŽēĆ, treatable traits (phenotyps/endotypes)žĚė ŪôēžĚłžĚĄ žúĄŪēīžĄú blood eosinophil, FeNO, sputum eosinophilžĚĄ žčúŪĖČŪēīžēľ ŪēúŽč§[5]. Blood eosinophil ‚Č• 300/ul, FENO ‚Č• 20ppb, or sputum eosinophil ‚Č• 2%žĚł Í≤Ĺžöį ‚Äúpersistent type 2 inflammation despite high ICS‚ÄĚŽ°ú ŪĆźŽč®Ūē† žąė žěąŽč§[5]. Type 2 inflammationžĚĄ ŪôēžĚłŪēėŽäĒ Í≤Äžā¨ žßĀŪõĄ Í≥†žö©ŽüČžĚė ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďúŽ•ľ žĚľž†ēÍłįÍįĄ žā¨žö©Ūēú ŪõĄ ž¶ĚžÉĀÍ≥ľ ŪŹźÍłįŽä•žĚė ÍįúžĄ†žĚī žěąŽäĒžßÄ ŪôēžĚłŪēīŽ≥īŽäĒ Í≤É žó≠žčú ŪēĄžöĒŪēėŽč§(systemic GC responsiveness) [57-60]. Type 2 inflammationÍ≥ľ Í≥†žö©ŽüČ ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďú ŽįėžĚĎžĚÄ ŪėĄžě¨ žÉĀžö©ŪôĒŽźú žÉĚŽ¨ľŪēôž†Ā ž†úž†ú(biologics [omalizumab, anti-IL5])Žāė ž†Äžö©ŽüČ ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďú žú†žßÄ žĻėŽ£Ćžóź Ūö®Í≥ľÍįÄ žěąžĚĄ ÍįÄŽä•žĄĪžĚĄ ŽÜížĚīŽäĒ traitžĚīŽč§[63,64]. žĚīŽü¨Ūēú traitŽ•ľ ÍįĞߥ ŪôėžěźžóźžĄú ŽĻĄž°įž†ą ŪėĻžĚÄ žēÖŪôĒ ŽēĆŽ¨łžóź žā¨žö©ŪēėŽäĒ OCS bursts(Žč®ÍłįÍįĄžĚė Í≥†žö©ŽüČ ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďú žā¨žö©)ÍįÄ ŽĄąŽ¨ī žě¶Žč§Ž©ī(2-3ÍįúžõĒžóź 1Ž≤ą žĚīžÉĀ) ž†Äžö©ŽüČ ž†Ąžč† žä§ŪÖĆŽ°úžĚīŽďú žú†žßÄ žĻėŽ£Ć(5-10 mg/day)Žāė žÉĚŽ¨ľŪēôž†Ā ž†úž†úžĚė žā¨žö©žĚĄ žč¨ÍįĀŪēėÍ≤Ć Í≥†Ž†§Ūēīžēľ ŪēúŽč§[65]. ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďúŽäĒ ŽĻĄŽ°Ě ž†Äžö©ŽüČžĚīŽćĒŽĚľŽŹĄ žě•ÍłįÍįĄ žā¨žö©žčú Ž∂ÄžěĎžö©(Í≥®Žč§Í≥Ķž¶Ě, ŽĻĄŽßĆ[cushing], ŽčĻŽá®Ž≥Ď, žó¨ŽďúŽ¶Ą, Íįźžóľ ŽďĪ)žĚī ŽįúžÉĚŪē† žąė žěąžúľŽĮÄŽ°ú ž∂©Ž∂ĄŪēú žĄ§Ž™Ö ŪõĄ žĻėŽ£ĆŽ•ľ žčúžěĎŪēīžēľ ŪēúŽč§[7]. ŪäĻŪěą 3ÍįúžõĒ žĚīžÉĀ ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďú(ž†Äžö©ŽüČžĚīŽćĒŽĚľŽŹĄ) žā¨žö©žĚī žėąžÉĀŽźėŽäĒ Í≤ĹžöįžóźŽäĒ Í≥®Žč§Í≥Ķž¶Ě žėąŽį© žĻėŽ£Ć(calcium & vitamin D)Ž•ľ ŽįėŽďúžčú Ūēīžēľ ŪēėÍ≥†, Í≥®Žč§Í≥Ķž¶Ěžóź ŽĆÄŪēú Ž™®ŽčąŪĄįŽßĀžĚī ŪēĄžöĒŪēėŽč§[7]. ŽßĆžēĹ Í≤Ĺž†úž†ĀžúľŽ°ú žó¨žú†ÍįÄ žěąŽäĒ ŪôėžěźŽĚľŽ©ī, ž†Äžö©ŽüČ ž†Ąžč†žä§ŪÖĆŽ°úžĚīŽďú žú†žßÄ žĻėŽ£ĆŽ≥īŽč§ žÉĚŽ¨ľŪēôž†Ā ž†úž†úŽ•ľ Ž®ľž†Ä Í≥†Ž†§ŪēėŽäĒ Í≤ÉžĚī ŽįĒŽěĆžßĀŪēėŽč§(ŪėĄžě¨ žčúŪĆźž§ĎžĚł žÉĚŽ¨ľŪēôž†Ā ž†úž†úŽäĒ Ž∂ÄžěĎžö©žĚī ŽßéžßÄ žēäžĚĆ). žÉĚŽ¨ľŪēôž†Ā ž†úž†úžôÄ ÍīÄŽ†®Ūēú žěźžĄłŪēú Žāīžö©žĚÄ Ūē®ÍĽė Í≤ƞ쨎źú ‚Äúž§Ďž¶Ěž≤úžčĚžĚė žĻėŽ£Ć(žÉĚŽ¨ľŪēôž†Ā ž†úž†ú)‚ÄĚ žĘÖžĄ§ ŽÖľŽ¨łžĚĄ žįłÍ≥†ŪēėÍłį ŽįĒŽěÄŽč§.
Allergy test (skin or serum sIgE detection test, serum total IgE)
ž§Ďž¶Ěž≤úžčĚžĚė Í≤Ĺžöį Í≤Ĺž¶Ěž≤úžčĚžóź ŽĻĄŪēī žēĆŽ†ąŽ•īÍłįžĄĪ ž≤úžčĚ(allergic asthma)žĚī ŽďúŽ¨ł Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąŽč§. ŪēėžßÄŽßĆ žēĆŽ†ąŽ•īÍ≤ź(žēĆŽ†ąŽ•īÍłįŽ¨ľžßą [allergen])žóź ŽĆÄŪēú specific IgE (sIgE) ž°īžě¨Ž•ľ ŪôēžĚłŪē®žúľŽ°úžĄú ŪôėÍ≤ĹÍīÄŽ¶¨(allergen avoidance)Ž•ľ ŪÜĶŪēú ž≤úžčĚ ž°įž†ąžóź ŽŹĄžõĞ̥ ž§Ą žąė žěąžúľŽĮÄŽ°ú, allergy testžĚė žčúŪĖȞ̥ ŪÜĶŪēī žēĆŽ†ąŽ•īÍłįžĄĪ ž≤úžčĚžĚė ÍįÄŽä•žĄĪžĚī žěąŽäĒžßÄ ŽįėŽďúžčú ŪôēžĚłŪēīžēľ ŪēúŽč§[1,7].
ŽėźŪēú ŪÜĶŽÖĄžĄĪ žēĆŽ†ąŽ•īÍ≤ź(perennial allergen: dust mite, animal dander, cockcroach, or molds)žóź ŽĆÄŪēú sIgEÍįÄ ŪôēžĚłŽźú ž§Ďž¶Ěž≤úžčĚžĚė Í≤Ĺžöį omalizumabžĚĄ žā¨žö©Ūē† žąė žěąŽč§(omalizumabžĚė ž†ĀžĚĎž¶Ě: ž§Ďž¶Ěž≤úžčĚ, sIgE to a perennial allergen, 6žĄł žĚīžÉĀ, serum total IgE 30-1500 IU/mL) [5]. Omalizumab žā¨žö©žěź ž§Ď žĻėŽ£Ć ŽįėžĚĎ(ž≤úžčĚž¶ĚžÉĀžĚė Ūėłž†Ą)žĚÄ 60-70%ž†ēŽŹĄžóźžĄú Žä¶žĖīŽŹĄ žĻėŽ£Ć Íįúžčú 4ÍįúžõĒ ŽāīžóźŽäĒ ŽāėŪÉÄŽāúŽč§(responder of omalizumab) [1,66]. OmalizumabžĚÄ type 2 inflammationžĚī žěąžĚĄ ŽēĆ(persistent type 2 inflammation despite high ICS) žĻėŽ£Ć ŽįėžĚĎžĚī žĘčžĚÄ Í≤ÉžúľŽ°ú žēĆŽ†§ž†ł žěąŽč§[5].
ŽŅźŽßĆ žēĄŽčąŽĚľ, sIgEžĚė ŪôēžĚłžĚĄ ŪÜĶŪēī immunotherapy (subcutaneous immunotherapy [SCIT] or sublingual immunotherapy [SLIT])Ž•ľ žčúŽŹĄŪēīŽ≥ľ žąė žěąŽč§. Žč®, immunotherapyžĚė žčúžěĎžĚÄ ž≤úžčĚžĚī žēÖŪôĒÍįÄ žēĄŽčĆ žÉĀŪÉúžóźžĄú žčúžěĎŪēīžēľ ŪēėŽ©į, FEV1 > 70-80%žĚł žÉĀŪÉúžóźžĄú žčúŪĖČŪēėŽäĒ Í≤ÉžĚī ŽįĒŽěĆžßĀŪēėŽč§[67,68].
Chest CT, DLCO, Lung volume
ž§Ďž¶Ěž≤úžčĚžúľŽ°ú ŪôēžĚłŽźėŽ©ī, ŪĚČŽ∂Ä computed tomography (CT)Ž•ľ žčúŪĖČŪēėŽäĒ Í≤ÉžĚī ŽįĒŽěĆžßĀŪēėŽč§. 2014ŽÖĄ ERS/ATS žßÄžĻ®žóźžĄúŽäĒ ŽĻĄŪäĻžĚīž†Ā ž¶ĚžÉĀ(ÍįĚŽčīžĚī ŽßéžĚÄ Í≤Ĺžöį, ŪŹźÍłįŽä•žĚė ŽĻ†Ž•ł ž†ÄŪēė, DLCO ÍįźžÜĆ, žēĄŪ܆ŪĒľ žóÜžĚĆ)žĚĄ Ž≥īžĚľ ŽēĆŽßĆ ŪĚČŽ∂Ä CT žčúŪĖȞ̥ Í∂ĆÍ≥†ŪēėŽāė(žĚėŽ£ĆŽĻĄžö©Í≥ľ Ž∂ÄžěĎžö© ŽēĆŽ¨łžóź) [1], žöįŽ¶¨ŽāėŽĚľŽäĒ CT ŽĻĄžö©žĚī ž†ÄŽ†īŪēėÍ≥†, žĶúÍ∑ľžóźŽäĒ ž†ÄžĄ†ŽüČ ŪĚČŽ∂Ä CTÍįÄ ŽĄźŽ¶¨ žĚīžö©ŽźėŽĮÄŽ°ú, Ž™®Žď† ž§Ďž¶Ěž≤úžčĚ ŪôėžěźžóźÍ≤Ć ŪēúŽ≤ąžĚÄ ŪĚČŽ∂Ä CTŽ•ľ žčúŪĖČŪēėŽäĒ Í≤ÉžĚī Ūē©Ž¶¨ž†ĀžĚīŽĚľÍ≥† ŪĆźŽč®ŽźúŽč§. žĚľŽįėž†ĀžúľŽ°ú ž≤úžčĚ ŪôėžěźŽäĒ ŪĚČŽ∂Ä CTžóźžĄú ŽĮłŽßĆžĄĪ ÍłįŽŹĄŽ≤Ĺ ŽĻĄŪõĄ, ÍłįŽŹĄŽāīÍįēŪėĎžį©, Ž™®žěźžĚīŪĀ¨ ŪŹź ÍįźžáĄ ŽďĪžĚī ÍīÄžįįŽź† žąė žěąŽč§[69,70]. žĚīŽü¨Ūēú Ž≥ĎŽ≥ÄŽď§ žôłžóź ÍłįÍīÄžßÄŪôēžě•ž¶ĚžĚīŽāė ŪŹźžĻ®žú§(ž§Ďžč¨žÜĆžóĹžĄĪ Í≤įž†ą)žĚī ŽįúÍ≤¨ŽźėŽ©ī, ÍįĚŽčī žĄłÍ∑†/Ūē≠žāįÍ∑† ŽįįžĖĎ Í≤Äžā¨ žčúŪĖČŪēėÍ≥†, ÍĶ≠žÜĆž†ĀžĚł ÍłįŽŹĄŽ≤Ĺ ŽĻĄŪõĄ/ŪŹźžáĄÍįÄ Ž≥īžĚīŽ©ī ÍłįÍīÄžßÄŽāīžčúÍ≤Ş̥ Í≥†Ž†§Ūēīžēľ ŪēúŽč§. ŪĚČŽ∂Ä CTŽ•ľ ŪÜĶŪēī žėąžÉĀžĻė žēäžĚÄ ŽŹôŽįė žßąŪôė(Í≤įŪēĶ/ŽĻĄÍ≤įŪēĶ Ūē≠žāįÍ∑† ŪŹźžßąŪôė, ŪŹźÍłįžĘÖ, ÍłįÍīÄžßÄŪôēžě•ž¶Ě ŽďĪ)žĚī ŽįúÍ≤¨ŽźėÍĪįŽāė, ž†ĄŪėÄ Žč§Ž•ł žßĄŽč®(ÍłįŽŹĄžĚīŽ¨ľ, ÍłįŽŹĄžĘÖžĖĎ ŽďĪ)žĚī žĚīŽ£®žĖīžßÄÍłįŽŹĄ ŪēúŽč§[71]. DLCOžôÄ lung volume žł°ž†ē ŽėźŪēú ŪēĄžöĒŪēėŽč§. ŽŹôŽįė žßąŪôė ŪėĻžĚÄ ŽĆÄž≤īžßĄŽč®žúľŽ°ú ILDŽāė COPDÍįÄ ÍįÄŽä•ŪēėÍłį ŽēĆŽ¨łžĚīŽč§[1,7].
ŪĚČŽ∂Ä CT ŽįŹ DLCOžôÄ lung volume ŽďĪžĚė Í≤Äžā¨Ž•ľ ŪÜĶŪēī, Ūôėžěź ž≤úžčĚžĚė ž§Ďž¶ĚŽŹĄžóź COPDÍįÄ žÉĀŽčĻŪēú žėĀŪĖ•žĚĄ ŽĀľžĻúŽč§Í≥† ŪĆźŽč®ŽźėŽ©ī(asthma-COPD overlap [ACO]ŽĚľŽ©ī), azithomycinžĚīŽāė pulmonary rehabilitationžĚĄ Í≥†Ž†§Ūēī Ž≥ľ ŽßĆŪēėŽč§[5,72]. ŽßĆžēĹ, ŪĚČŽ∂Ä CTžóźžĄú Žč§Ž•ł ŪĀį žĚīžÉĀ žÜĆÍ≤¨žĚī žóÜžĚī ŽĮłŽßĆžĄĪ ÍłįŽŹĄŽ≤Ĺ ŽĻĄŪõĄÍįÄ Ž≥īžĚīÍ≥† žĚīÍ≤ÉžĚī ÍłįŽŹĄŪŹČŪôúÍ∑ľ ž¶ĚžčĚžóź žĚėŪēú ÍłįŽŹĄ ÍįúŪėē ŽēĆŽ¨łžúľŽ°ú žó¨Í≤®žßÄŽ©ī, bronchial thermoplastyŽ•ľ Í≥†Ž†§ŪēīŽ≥ľ žąė žěąÍ≤†Žč§[1]. ŪēėžßÄŽßĆ bronchial thermoplastyŽäĒ žēĄžßĀ ž†ēŪôēŪēú ŽįėžĚĎÍĶįžĚī ž†ēžĚėŽźėžßÄ žēäžēėÍ≥†, žĚīž†Ą žóįÍĶ¨ÍįÄ FEV1 > 60% žĚīžÉĀžĚė ŪôėžěźžóźžĄúŽßĆ ž£ľŽ°ú žčúŪĖČŽźėžóąžúľŽ©į, žčúžą† ŽŹĄž§ĎžĚė ž≤úžčĚ žēÖŪôĒŽāė ŪŹźŽ†ī ŽįúžÉĚ ŽďĪžĚė Ž∂ÄžěĎžö© ŽįúžÉĚ Ž≥īÍ≥†ÍįÄ žěąžĖīžĄú, 2014 ERS/ATS žßÄžĻ®žóźžĄú ž†ĀÍ∑Ļž†Ā žčúŪĖČŽ≥īŽč§ŽäĒ ž∂ĒÍįÄž†ĀžĚł žóįÍĶ¨ Í≤įÍ≥ľ(ŪŹźÍłįŽä• ÍįúžĄ†, žēÖŪôĒ ÍįźžÜĆžóź ŽĆÄŪēú žě•ÍłįŪö®Í≥ľ)ÍįÄ ž∂ēž†ĀŽźėÍłį ž†ĄÍĻĆžßÄŽäĒ žóįÍĶ¨ Ž™©ž†ĀžúľŽ°úŽßĆ žčúŪĖČŪēėŽŹĄŽ°Ě Í∂ĆÍ≥†ŪēėÍ≥† žěąŽč§[1].
ÍłįŪÉÄ
žúĄžĚė žā¨Ūē≠ žĚīžôłžóź ž§Ďž¶Ěž≤úžčĚ ŪôėžěźžóźÍ≤Ć Í≥†Ž†§Ūēīžēľ Ūē† žā¨Ūē≠žúľŽ°ú 1) ž≤úžčĚ ÍĶźžú°(ž≤úžčĚž†ēŽ≥īž†úÍ≥Ķ ŽįŹ žßÄžčĚŪē®žĖĎ) ŽįŹ ž≤úžčĚŪĖČŽŹôžßÄžĻ®(žěźÍłįÍīÄŽ¶¨ŪõąŽ†®) žąėŽ¶Ĺ, 2) žėąŽį©ž†ĎžĘÖ(ŽŹÖÍįź, ŪŹźÍĶ¨Í∑†) ŽďĪžĚī žěąŽč§[7,12]. ž≤úžčĚžóź žěąžĖīžĄú ŪŹźÍĶ¨Í∑†žĚė žėąŽį©ž†ĎžĘÖžĚÄ ŽŹÖÍįźŽßĆŪĀľ Íįēž°įŽźėžßÄŽäĒ žēäžúľŽāė(Í≥†Ž†ĻžěźŽāė žÜĆžēĄ žôł) [7], ž§Ďž¶Ěž≤úžčĚ ŪôėžěźžóźžĄúŽäĒ ž†ĎžĘÖŪēėŽäĒ Í≤ÉžĚī Ūē©Ž¶¨ž†ĀžĚīŽĚľÍ≥† ŪĆźŽč®ŽźúŽč§.
Macrolide Ūē≠žÉĚž†ú žú†žßÄ žöĒŽ≤ēžĚÄ ž§Ďž¶Ě COPDžóźžĄú žēÖŪôĒžėąŽį©žóź ŽŹĄžõÄžĚī ŽźėŽäĒ žēĹŽ¨ľžĚīŽč§[72]. ž§Ďž¶Ěž≤úžčĚ ŪôėžěźžóźžĄúŽŹĄ ŽĻĄŪėłžāįÍĶ¨žĄĪ traitŽ•ľ Ž≥īžĚīŽäĒ Í≤Ĺžöį macrolide žú†žßÄžöĒŽ≤ēžĚī ͳȞĄĪ žēÖŪôĒžĚė ŽĻąŽŹĄÍįźžÜĆžóź ŽŹĄžõÄžĚī ŽźėžóąŽč§[12]. ŪēėžßÄŽßĆ žēĄžßĀÍĻĆžßÄ ŽĆÄÍ∑úŽ™® žóįÍĶ¨ÍįÄ Ž∂Äž°ĪŪēėÍ≥† žóįÍĶ¨ Í≤įÍ≥ľÍįÄ žĚľÍīÄŽźėžßÄ žēäžēĄ žĚľŽįėŪôĒŪēėÍłįžóźŽäĒ žĚīŽ•ł žč§ž†ēžĚīžĖīžĄú, ž§Ďž¶Ěž≤úžč̞󟞥ú žēÖŪôĒžėąŽį©žĚīŽāė ž≤úžčĚ ž°įž†ą Ž™©ž†ĀžúľŽ°ú macrolide žú†žßÄ žöĒŽ≤ēžĚĄ Í∂ĆÍ≥†ŪēėžßÄŽäĒ žēäŽäĒŽč§[1,12]. ŽĻĄŪÉÄŽĮľ D ŽėźŪēú ž≤úžčĚ ž°įž†ąžóź ŽŹĄžõÄžĚī ŽźúŽč§ŽäĒ Ž≥īÍ≥†ÍįÄ žĚľŽ∂Ä žěąžúľŽāė, ŽĆÄÍ∑úŽ™® žóįÍĶ¨ÍįÄ Ž∂Äž°ĪŪēėÍ≥† ŽįėŽĆÄžĚė Í≤įÍ≥ľŽŹĄ žěąžĖīžĄú ŽćĒ ŽßéžĚÄ žóįÍĶ¨ÍįÄ ŪēĄžöĒŪēú žč§ž†ēžĚīŽč§[7].
Í≤į Ž°†
ž§Ďž¶Ěž≤úžčĚžĚė žĻėŽ£ĆŽäĒ ŽāúžĻėž≤úžčĚžĚė žĻėŽ£Ćž†ĎÍ∑ľžóźžĄúŽ∂ÄŪĄį žčúžěĎŪēúŽč§. ŽāúžĻėž≤úžčĚ ŪôėžěźžóźžĄú Žč§Ž•ł žßąŪôėžĚĄ Žįįž†úŪēėÍ≥†, ÍĶźž†ē ÍįĎ䕞̳ žěźžóź ŽĆÄŪēú ž°įžĻėŽ•ľ ž†ĀÍ∑Ļž†ĀžúľŽ°ú žčúŪĖČŪēėžėÄžĚƞ󟎏Ą ž≤úžčĚ ž¶ĚžÉĀžĚī žßÄžÜ掟† ŽēĆ ŽĻĄŽ°úžć® ž§Ďž¶Ěž≤úžčĚ žßĄŽč®žĚī Ž∂Ğ󨎟† žąė žěąŽč§. ž§Ďž¶Ěž≤úžčĚžúľŽ°ú ŪôēžĚłŽźėŽ©ī, ž°įž†ąž†ú žĻėŽ£ĆŽ•ľ ž†Āž†ēŪôĒŪē®Í≥ľ ŽŹôžčúžóź treatable traitsÍįÄ žěąŽäĒžßÄ ž°įžā¨ÍįÄ ŪēĄžöĒŪēėŽč§. ž°įž†ąž†ú žĻėŽ£ĆŽ•ľ Í∑ĻŽĆÄŪôĒŪēėžėÄžĚƞ󟎏Ą ž¶ĚžÉĀžĚī žßÄžÜ掟ėŽäĒ ž≤úžčĚ ŪôėžěźžóźÍ≤ĆŽäĒ ŪôēžĚłŽźú treatable traits Í≤įÍ≥ľŽ•ľ ŽįĒŪÉēžúľŽ°ú specific severe asthma treatmentsžĚė žčúŪĖȞ̥ Í≥†Ž†§Ūēėžó¨žēľ ŪēúŽč§.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






