서 론
Mycoplasma Pneumoniae은 지역사회 폐렴의 주요한 원인균 중의 하나이며, 최근 시행된 국내 연구에서 지역사회 폐렴의 원인 균 중 16.7%를 차지하였다[1]. M. Pneumoniae에 의한 폐렴은 대개는 경한 경과를 보이고 항균제 치료 없이도 저절로 좋아지는 경우도 많으나, 인공호흡기 치료를 필요로 하는 중증 폐렴은 드물다. 한편, 무균성 수막염, 피부 병변, 관절염, 심근염, 콩팥병증 등의 다양한 폐외 합병증을 동반할 수 있는데, 지금까지 국내에서는 1건의 보고만이 있었다[2]. 저자들은 마이코플라즈마에 의한 중증폐렴과 이와 동반된 횡문근융해를 가진 환자를 경험하였고 성공적으로 치료하였기에 문헌고찰과 함께 보고하는 바이다.
증 례
환 자: 23세 남자
주 소: 내원 1일 전 발생한 호흡곤란
현병력: 환자는 이전에 건강하였으며, 대전 소재에 있는 군부대에서 복무 중인 군인이었다. 내원 2일 전 발열 및 기침이 발생하였고 가래는 거의 없었다. 내원 1일 전 호흡곤란, 발열과 함께 숨을 쉴 때 마다 왼쪽 가슴의 찌르는 듯한 통증이 발생하여 군 병원으로 이송되어 중증폐렴으로 진단받고 당일 전원 되었다. 환자는 최근 강도 높은 훈련 및 야외 훈련은 없었다고 하였다.
과거력: 결핵 및 이전의 폐렴을 앓았던 적 없음.
가족력: 특이 사항 없음.
진찰 소견: 응급실 도착 시 활력 징후는 혈압 122/79 mmHg, 심박수 123회/min, 호흡수는 22회/min, 체온은 39.2℃였다. 환자는 venturi mask 50%를 적용 중이었고 산소 포화도는 89%였다. 의식은 명료하였고 급성 병색을 보였다. 결막은 창백하지 않았고, 공막에 황달소견은 없었다. 경부 및 액와부 림프절은 촉지되지 않았다. 심음은 규칙적이었고 심잡음은 들리지 않았지만 양 폐하에 수포음이 청진되었다. 복부촉진상 압통은 없었으며, 복강 내에 촉진되는 장기는 없었다. 피부에 특이소견은 없었다.
검사 소견: 일반 혈액 검사에서 백혈구 6,200/mm3, 혈색소 14.6 g/dL, 헤마토크리트 41.8%, 혈소판 171,000/mm3였고, 혈액응고검사에서 PT (INR) 1.18, aPTT 37 sec이었다. 전해질검사 결과는 Na+ 133 mmol/L, K+ 4.2 mmol/L, Cl- 102 mmol/L, total CO2 19.7 mmol/L이었고, 생화학 검사에서는 혈중 요소질소 13 mg/dL, 크레아틴 1.1 mg/dL, 총 단백 5.6 g/dL 알부민 3.1 g/dL, 아스파르테이트아미노전이효소 105 IU/L, 알라닌아미노전이효소 64 IU/L, 총 빌리루빈 1.1 mg/dL, 젖산탈 수소효소 323 IU/L (120-250 IU/L), 미오글로빈 483 ng/mL (-100 ng/mL), 크리아틴키나아제 1,271 IU/L (50-250 IU/L), 트로포닌-I < 0.05 ng/mL, 크리아틴키나아제-MB 7.6 ng/mL (-5 ng/mL), CRP 34.31 mg/dL, procalcitonin 2.16 ng/mL였다. Venturi mask 50%에서 시행한 동맥혈 가스 검사는 pH 7.47, PaCO2 32 mmHg, PaO2 45 mmHg, bicarbonate 0.4 mmEq/L, 산소포화도는 84%였다.
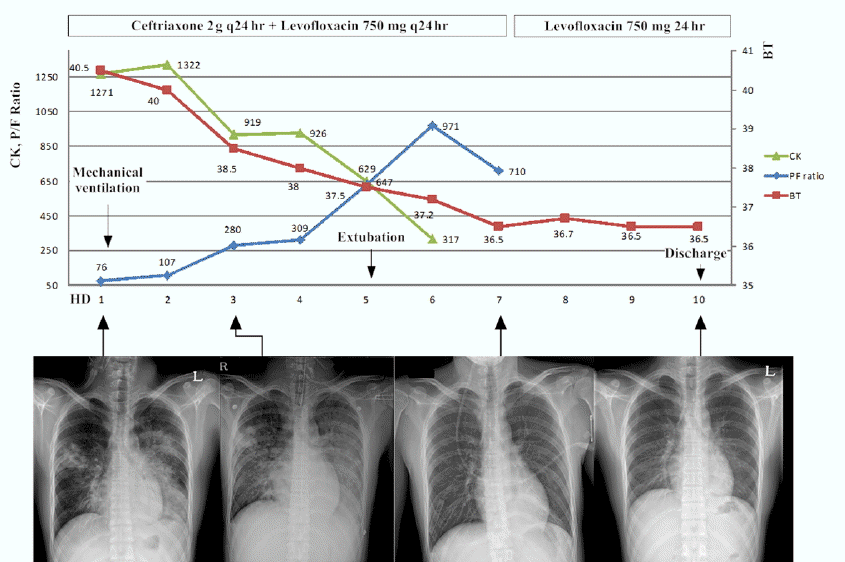
방사선 소견: 흉부 단순 촬영에서 왼쪽 폐의 중간 및 아래 영역 및 오른쪽 폐의 가운데 영역의 경화(consolidation)가 존재하였다(Fig. 1).
치료 및 임상경과: 치료 및 임상경과를 그림 1에 요약하였다. 중환자실 입실시 reservoir bag 15 L/min 적용 상태에서 시행한 동맥혈 검사상 PaO2 45 mmHg로 hypoxemia 소견을 보이고 있었다. 환자의 호흡수는 분당 34회였고, 환자는 보조 호흡근을 사용하였다. 이에 인공 호흡기를 적용하였고, ceftriaxone 2 gm과 levofloxacin 750 mg을 하루에 1회 정주로 경험적으로 투여를 시작하였다. 내원 2일째 기관지 내시경과 기관지폐포세척술(bronchoalveolar lavage, BAL)을 시행하였으며, 기관지 내시경에서 다량의 화농성 가래가 배출되었으나 출혈 소견은 없었다. 기관지폐포 세척 검사에서 시행한 fluid analysis에서 WBC 450/mm3, neutrophil 70%, lymphocyte 8%, eosinophil 1%, alveolar macrophage 21%을 보였고, BAL fluid 배양 검사에서 동정된 균은 없었다. BAL fluid에서 시행한 M. pneumoniae polymerase chain reaction (PCR) (Seeplex PneumoBacter ACE Detection, Seegene, Korea)이 양성이었고, Legionella pneumoniae, Chlamydophila pneumoniae에 대한 PCR (Seeplex PneumoBacter ACE Detection, Seegene, Korea)은 음성이었다. 호흡기 바이러스에 대한 multiplex PCR (Seeplex RV15 ACE Detection, Seegene, Korea)을 시행한 결과 adenovirus, coronavirus, enterovirus, influenza virus A/B, parainfluenza virus 1/2/3/4, respiratory syncytial virus A/B, rhinovirus, metapneumovirus에 대하여 모두 음성이었다. 또한 pneumococcal urinary antigen, legionella urinary antigen (Binax Now, Binax, Inc, Portland, ME, USA)도 음성이었다. 내원 2일째 크리아틴키나아제는 내원시 보다 상승한 1,322 IU/L였으며 혈중요소질소 14 mg/dL 크레아틴1.0 mg/dL였다. 시간당 적절한 수액요법으로 소변양은 100 cc 정도로 잘 유지되었다. 또한 FiO2 45%에서 PaO2는 108 mmHg로 산소화가 호전되었다. 내원 3일째 기계환기와 항균제 치료에 빠르게 호전되어 기계환기를 중단 하였고, 내원 5일째 발관(extubation) 후 일반 병동으로 전동하였다. 내원 6일째 크리아틴키나아제 수치는 317 IU/L까지 감소하였다. 내원 7일째부터 항균제는 levofloxacin 750 mg 하루에 1회 정주만 유지하였다. 내원 10일째 항균제를 중단 후 특별한 합병증 없이 퇴원하였다.
고 찰
마이코플라즈마 폐렴은 대체로 가벼운 경과를 보이며 대부분은 자연히 회복된다. 이러한 비교적 가벼운 임상경과로 인하여 ‘walking pneumonia’로 불리기도 한다. 하지만 드물게는 중증 폐렴을 일으키기도 한다. 현재까지 국내에서는 건강한 성인에게 발생한 M. pneumoniae 중증 폐렴이 총 2건 보고되었다.
M. pneumoniae 감염증 환자의 약 25%의 환자에서 폐외증상을 동반하는 것으로 알려져 있다. 소아들을 대상으로 한 국내 보고에서는 폐외 증상의 동반 비율은 24-66%였고, 종류로는 경련, 구토, 복통, 설사, 피부발진, 중이염 등이 있었다. 또한 심막염, 혈액응고 장애, 급성 췌장염, 간염 및 다발성 장기 부전에 동반된 횡문근 융해도 보고되었다. 성인에서는 소아보다 폐외 증상의 보고가 드물지만 용혈성 빈혈, 급성사이질 콩팥염, 심근염, Stevens-Johnson Syndrome이 국내에서 보고되었다. M. pneumoniae 감염증 시 폐외 증상이 흔한 이유는 M. pneumoniae가 혈액을 통하여 폐외 기관으로 이동하여 직접적인 장기 손상을 초래할 수 있기 때문이다. 또한 세포벽의 구성성분인 adhesion protein및 glycolipid에 대한 분자 구조가 포유류의 조직과 비슷하여, 자가면역 반응을 통해 폐외 증상을 초래할 수도 있다.
횡문근융해는 근육세포의 파괴로 정의된다. 이에 따라 myoglobin, creatine kinase, lactate dehydronage, alanine aminotransferase, aspartate aminotransferase 등이 혈액을 통하여 전신으로 퍼지며 이로 인해 다양한 장기 손상을 초래할 수 있다. Creatine kinase 수치만으로 횡문근융해를 확진할 수는 없지만, 일반적으로 creatine kinase 수치가 정상의 5배 이상이면은 횡문근융해가 동반 된 것으로 생각할 수 있다. 횡문근 융해의 주된 증상은 근육통과 위약감이지만, 횡문근 융해 환자의 50%에서만 이러한 증상이 발생하여, 임상에서 횡문근 융해를 간과할 가능성이 있다. 즉, 그동안 횡문근 융해가 동반된 중증 폐렴이 실제보다 적게 보고되었을 가능성도 있겠다. 횡문근융해의 원인은 다양하며, 대표적인 원인으로는 격렬한 근육 사용, 약물(코카인, phencyclidine 등), 외상, 알코올, 근육병증이 있다. 본 증례에서는 환자가 군인이기 때문에 훈련 등의 격렬한 신체활동에 의하여 횡문근융해가 발생하였을 가능성 고려할 수 있었다. 하지만 환자는 근래에 강도 높은 훈련을 받은 적은 없기 때문에 훈련 등과 같은 격렬한 근육사용에 의하여 횡문근융해가 발생하였을 가능성은 희박하였다. 또한 횡문근융해의 원인 중 박테리아나 바이러스와 같은 감염성 질환도 약 5%를 차지한다. Influenza virus는 바이러스 감염성 질환에 의한 횡문근융해의 가장 흔한 원인이다. 그 외에 횡문근융해를 발생시킬 수 있는 바이러스는 human immunodeficiency virus, coxsackie virus, Ebstein-Barr virus, echovirus, cytomegalovirus 등이 있다. 또한 Legionella species, Strepcococcus species, Salmonella species 등의 박테리아도 횡문근융해를 초래할 수 있다. 본 증례에서 BAL fluid로 시행한 adenovirus, coronavirus, enterovirus, influenza virus A/B, parainfluenza virus 1/2/3/4, respiratory syncytial virus A/B, rhinovirus, metapneumovirus에 대한 PCR 및 Legionella pneumoniae, Chlamydophila pneumoniae에 대한 PCR 및 pneumococcal urinary antigen, legionella urinary antigen도 음성이어서 M. pneumoniae 외에 다른 감염성 질환에 의하여 횡문근융해가 발생하였을 가능성은 낮았다. 한편 M. pneumoniae 감염에 의한 횡문근융해의 기전은 잘 밝혀지지는 않았지만 가능한 기전으로는 염증반응에 의한 종양괴사 인자의 활성화 등을 포함한 다양한 사이토카인에 의한 근육의 직접적인 손상, 자가항체에 의한 의한 근육 손상, 마지막으로 미세혈전 생성으로 인한 근육 손상 등이 제시되고 있다.
국내에서 지역사회 폐렴과 연관된 횡문근 융해는 1건이 보고되었으나, 폐렴의 원인균은 밝혀지지 않았다[3]. M. pneumoniae에 의한 지역사회 폐렴과 동반된 횡문근 융해는 국내외를 포함하여 총 9건이 보고되었고 이를 표 1에 정리하였다(Table 1). 연령대는 4-60살로 다양하였으며, 6명이 남자였다. 폐렴이 없었던 경우도 2예가 있었다. 크리아틴키나아제 수치는 792-1,074,240 Units/L로 다양하였고, 3건에서는 신부전으로 투석이 필요하였고, 4건에서는 중추신경계 합병증이 동반되었다. 본 증례와 같이 기계환기가 필요한 경우는 4예가 있었다.
마이코플라즈마 감염은 인후도말검사, 객담배양 혹은 혈청학적 검사 또는 분자생물학적 검사를 통하여 진단할 수 있다. 본 환자에서는 M. pneumoniae에 대한 배양 검사를 시행하지 않았고 또한 혈청학적 검사를 추적관찰하지 않았기 때문에 배양 검사 및 혈청학적 검사로는 마이코플라즈마 감염을 확인할 수 없었다. 하지만 BAL fluid에서 시행한 M. pneumoniae에 대한 multiplex PCR (mPCR)이 양성이어서 마이코플라즈마 폐렴으로 진단할 수 있었다. mPCR은 하나의 임상 검체로 다양한 균에 대한 검사를 시행할 수 있으며, 민감도 및 특이도도 높은 것으로 알려져 있다. Stralin 등에 따르면 하부호흡기 검체에서 mPCR 시행하였을 때 S. pneu moniae, H. influenza, M. pneumoniae에 대한 민감도를 각각 86%, 88%, 100%, 특이도는 각각 81%, 64%, 100%로 보고하였다.
본 증례는 BAL fluid 시행한 PCR에서 M. pneumoniae가 확인되었고 내원시 근육에서 유래된 효소들이 증가되어 있어 중증 마이코플라즈마 폐렴에 동반된 횡문근융해로 진단하였고, 적절한 항균제 사용과 보조적 치료를 통하여 성공적으로 치료하였기에 문헌고찰과 함께 보고하는 바이다. 따라서 임상의들은 횡문근 융해를 동반한 중증 지역 사회 폐렴의 드문 원인으로 M. pneumoniae을 기억해야겠다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print






