당뇨병성 신장병에서 염증과 섬유화 억제를 통한 심신장 보호의 새 지평: 피네레논의 임상적 의의
A New Horizon of Cardiorenal Protection through Inhibition of Inflammation and Fibrosis in Diabetic Kidney Disease: Clinical Significance of Finerenone
Article information
Trans Abstract
Non-steroidal mineralocorticoid receptor antagonists (NS-MRAs) have emerged as a novel therapeutic class while minimizing the endocrine adverse effects associated with steroidal MRAs, such as spironolactone and eplerenone. Finerenone, the first clinically approved NS-MRA, exhibits high receptor selectivity, minimal off-target hormonal activity, and exerts potent anti-inflammatory and antifibrotic actions that complement renin-angiotensin system inhibition and sodium-glucose cotransporter-2 (SGLT2) inhibitor therapy. The pivotal FIDELIO-DKD and FIGARO-DKD trials demonstrated clinically meaningful reductions in kidney disease progression and cardiovascular composite outcomes in patients with type 2 diabetes and albuminuric chronic kidney disease (urine albumin-creatinine ratio ≥ 30 mg/g), the pooled FIDELITY analysis confirmed consistent cardiorenal benefits across diverse risk strata. Hyperkalaemia remains a principal safety concern and requires potassium monitoring and dose adjustments in routine practice. Emerging short-term data on albuminuria suggest the additional benefits of concomitant SGLT2 inhibitor therapy, although definitive outcome evidence for combination strategies is still evolving. Ongoing clinical programs further extend the therapeutic scope of finerenone to heart failure with preserved ejection fraction, non-diabetic chronic kidney disease, and type 1 diabetes. Collectively, NS-MRAs provide a mechanistically distinct strategy targeting inflammation and fibrosis and represent an important therapeutic advance in integrated cardiorenal-metabolic risk reduction.
서 론
당뇨병성 신장병(diabetic kidney disease, DKD)은 전 세계 말기 신부전의 가장 흔한 원인으로[1] 신기능 저하뿐 아니라 심혈관 질환 발생 위험을 크게 높이는 주요 임상 문제이다[2]. 제2형 당뇨병 환자의 약 40%에서 DKD가 동반되며[3], 이러한 환자들은 심혈관 및 전체 사망 위험이 일반 인구보다 현저히 높다[4].
지난 수십 년간 angiotensin-converting enzyme inhibitor (ACEi)와 angiotensin II receptor blocker (ARB)를 통한 레닌-안지오텐신-알도스테론계(renin-angiotensin-aldosterone system, RAAS) 억제가 DKD 치료의 표준으로 자리 잡았고, 최근에는 sodium-glucose cotransporter-2 (SGLT2) 억제제의 도입으로 신장 및 심혈관 보호 효과가 추가적으로 입증되었다[5]. 그럼에도 불구하고 이러한 약물 치료 이후에도 여전히 신기능 악화와 심혈관 사건이 상당수 발생하며, 잔존 위험(residual risk)이 중요한 치료 과제로 남아 있다[6].
미네랄코르티코이드 수용체(mineralocorticoid receptor, MR)는 염분과 체액 항상성뿐 아니라 염증과 섬유화의 조절에 관여하는 핵심 인자로, MR의 과활성화는 신장과 심장 조직 손상을 가속화하는 주요 병리 기전으로 밝혀졌다[7,8]. 기존 스테로이드성 MR 길항제인 스피로놀락톤과 에플레레논은 일정한 효과를 보였으나 고칼륨혈증과 호르몬 부작용으로 인하여 고위험 신장병 환자에서는 사용이 제한적이었다[9]. 이러한 한계를 극복하기 위하여 개발된 비스테로이드성 미네랄코르티코이드 수용체 길항제(non-steroidal MRA, NS-MRA)는 선택적이고 균형 잡힌 MR 차단을 통해 염증과 섬유화를 억제하며, 대표 약제인 피네레논(finerenone)은 대규모 임상 연구에서 신장과 심장을 동시에 보호하는 새로운 치료 전략으로 주목받고 있다[10].
본 론
피네레논의 약리학적 특성 및 작용 기전
NS-MRA의 대표 약제인 피네레논은 기존의 스테로이드성 약제(스피로놀락톤, 에플레레논 등)와 구별되는 독특한 약리학적 특성을 지닌다. 스테로이드계 미네랄코르티코이드 수용체 길항제(mineralocorticoid receptor antagonist, MRA)는 MR뿐 아니라 안드로겐·프로게스테론 수용체에도 결합하여 성호르몬 관련 부작용을 유발할 수 있으며 체내 조직 분포가 불균형적이어서 심장보다 신장에 더 강한 영향을 미치는 경향이 있다. 반면 피네레논은 비스테로이드성 화합물로 MR에 대한 높은 선택성과 친화력을 가지며 다른 스테로이드 수용체에는 거의 작용하지 않는다[10].
피네레논은 MR에 결합하여 단순히 알도스테론의 작용을 차단하는 것을 넘어 역작용제(inverse agonist)로서 MR의 기저 활성 자체를 억제하고 병적인 전사 신호를 차단한다[11]. 이를 통해 MR 활성화로 유도되는 염증성 반응과 섬유화 신호(transforming growth factor-β, collagen-I 등)를 억제하여 신장 내 염증과 산화 스트레스를 완화하고 조직 손상을 방지한다[12]. 그 결과 피네레논은 신장과 심근의 염증, 산화 스트레스, 섬유화를 완화하여 장기 구조 손상을 방지한다[13].
또한 피네레논은 심장과 신장에 균형 잡힌 조직 분포를 보여 두 장기에서 동시에 항염증 작용과 항섬유화 작용을 발휘한다. 이러한 특성은 스피로놀락톤, 에플레레논이 심근에 비해 신장에 상대적으로 치우쳐 작용하는 것과 대조된다[14,15]. 약동학적으로는 활성 대사체가 없고 반감기가 짧으며 약물 상호작용이 적어 예측 가능한 약리 프로파일을 갖는다[16]. 그 결과 고칼륨혈증이나 성호르몬 관련 부작용의 위험이 낮아 피네레논은 기존 MRA의 한계를 극복한 차세대 심신장 보호 약물로 평가된다[10].
주요 임상 근거(FIDELIO, FIGARO, FIDELITY)
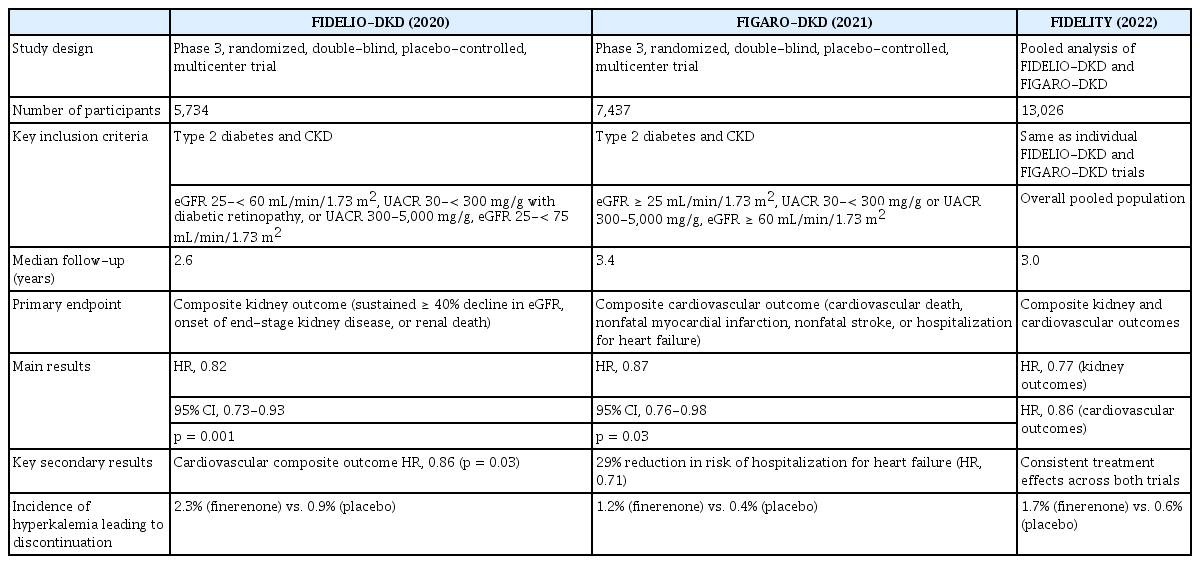
피네레논의 신장 및 심혈관 보호 효과는 두 개의 대규모 3상 임상시험인 Finerenone in Reducing Kidney Failure and Disease Progression in Diabetic Kidney Disease (FIDELIO-DKD), Finerenone in Reducing Cardiovascular Mortality and Morbidity in Diabetic Kidney Disease (FIGARO-DKD), 이들의 통합 분석인 Finerenone in Chronic Kidney Disease and Type 2 Diabetes: Combined FIDELIO and FIGARO Analysis (FIDELITY)를 통해 확립되었다[17-19]. 이 임상 연구들은 모두 제2형 당뇨병과 만성 신장병(chronic kidney disease, CKD)을 동반한 환자를 대상으로 기존의 ACEi 또는 ARB 치료를 최적 용량으로 유지한 상태에서 피네레논의 추가 효과를 평가하였다.
먼저 FIDELIO-DKD 연구는 평균 추정 사구체 여과율(estimated glomerular filtration rate, eGFR) 44 mL/min/1.73 m2, 알부민뇨가 있는 DKD 환자 5,734명을 대상으로 진행되었다[17]. 주요 평가 변수는 신장 복합 결과(지속적인 eGFR 40% 이상 감소, 말기 신부전, 신장 질환으로 인한 사망)였으며 피네레논군에서 위약군 대비 사건 발생이 18% 유의하게 감소하였다(hazard ratio [HR], 0.82; 95% confidence interval [CI], 0.73-0.93; p= 0.001). 또한 심혈관 복합 결과(심혈관 사망, 비치명적 심근경색, 비치명적 뇌졸중, 심부전 입원)는 14% 감소하였다(HR, 0.86; 95% CI, 0.75-0.99). 이러한 결과는 피네레논이 신기능 악화뿐 아니라 심혈관 사건 발생을 모두 억제함을 보여준다.
FIGARO-DKD 연구는 보다 eGFR이 높은 7,437명의 DKD 환자를 대상으로 수행되었으며 1차 평가 변수를 심혈관 복합 결과로 설정하였다[18]. 연구 결과 피네레논군에서 심혈관 사건이 13% 감소하였다(HR, 0.87; 95% CI, 0.76-0.98; p= 0.03). 특히 심부전으로 인한 입원 위험이 29% 감소하였으며(HR, 0.71; 95% CI, 0.56-0.90), 이는 피네레논의 심근 보호 효과를 강력히 시사한다. 신장 복합 결과(eGFR 40% 이상 감소, end-stage kidney disease [ESKD], 신장성 사망)는 13% 감소 경향을 보였으나 통계적 유의성에는 도달하지 않았다(HR, 0.87; 95% CI, 0.76-1.01; p= 0.07).
이후 두 연구의 통합 분석인 FIDELITY 연구는 총 13,026명을 포함하여 피네레논의 일관된 효과를 확인하였다[19]. 분석 결과 심혈관 복합 결과는 14% 감소하였고(HR, 0.86; 95% CI, 0.78-0.95; p= 0.0018) 신장 복합 결과는 23% 감소하였다(HR, 0.77; 95% CI, 0.67-0.88; p= 0.0002). 또한 피네레논의 고칼륨혈증으로 인한 치료 중단율은 약 1.7% (통합 분석 기준)로 임상적으로 관리 가능한 수준이었다.
본 연구 결과는 피네레논이 최적의 RAAS 억제 치료하에서도 잔존하는 신장 및 심혈관 위험을 추가로 감소시킬 수 있음을 보여주었으며, 일부 환자에서 SGLT2 억제제를 병용한 상황에서도 그 효과가 일관되게 관찰되었다.
피네레논-SGLT2 억제제 병용 요법: 근거와 임상 적용 전략
피네레논의 도입은 DKD 치료에 새로운 치료 옵션을 추가하였다. FIDELIO-DKD와 FIGARO-DKD 연구에서 피네레논은 RAAS 억제제 치료하에서도 신장 기능 악화 및 심혈관 사건을 유의하게 감소시켰으며 FIDELITY 통합 분석에서는 SGLT2 억제제 병용 여부와 관계없이 일관된 신장 및 심혈관 보호 효과를 보였다[17-19]. 이러한 근거를 바탕으로 DKD 치료는 RAAS 억제, SGLT2 억제제, NS-MRA, glucagon-like peptide 1 (GLP-1) 수용체 작용제로 구성된 다중 기전 기반 통합 치료(multimechanistic therapy)로 확장되고 있다. 이 중 피네레논과 SGLT2 억제제의 병용은 항염증 작용 및 항섬유화 작용과 대사/혈역학적 보호 기전이 상호 보완적으로 작용하여 추가적인 효과가 있을 가능성이 논의되고 있다[20-23].
최근 보고된 CONFIDENCE 연구에서는 RAAS 억제제 치료 중인 DKD 환자에서 피네레논과 엠파글리플로진의 초기 병용 요법이 단독 요법보다 urinary albumin-to-creatinine ratio (UACR)를 유의하게 더 크게 감소시킨다는 점을 입증하였다[24]. 6개월 시점에서 병용군은 피네레논 단독 대비 29% (least-squares mean ratio, 0.71; 95% CI, 0.61-0.82), 엠파글리플로진 단독 대비 32% (least-squares mean ratio, 0.68; 95% CI, 0.59-0.79)의 추가 감소를 보였으며, 고칼륨혈증, 저혈압, 급성 신손상 등 주요 이상 반응의 발생률은 세 군 간 유사하였다. 이러한 결과는 병용 요법이 단백뇨를 보다 빠르고 크게 감소시킬 수 있음을 보여주었다. 다만 본 연구는 1차 평가 변수가 UACR 변화인 단기 연구로서 신장 기능 악화나 심혈관 사건과 같은 임상적 예후 개선을 직접적으로 입증한 것은 아니다.
KDIGO 및 ADA-KDIGO 합의문은 RAAS 억제제와 SGLT2 억제제를 기본 축으로 하고 지속적인 알부민뇨 또는 심혈관 위험이 높은 경우 피네레논이나 GLP-1 수용체 작용제를 추가하도록 권고하고 있다[20,21,23]. 가이드라인은 약제 간 투여 순서를 명시하지 않지만 실제 임상에서는 각 약제의 근거 수준, 환자의 eGFR, 고칼륨혈증 위험, 비용 및 접근성을 고려하여 순차적 또는 조기 병용 전략을 결정한다.
피네레논과 SGLT2 억제제의 동시 병용은 단기 연구에서 양호한 안전성과 단백뇨 감소 효과를 보였으나 순차 투여와의 직접 비교 연구가 부족하여 최적의 투여 시점 및 병용 전략에 대한 근거는 아직 확립되지 않았다[25]. 현재까지는 제한된 임상 연구 및 관찰적 자료를 바탕으로 한 간접 근거가 대부분이며 향후 연구를 통해 두 접근법의 임상적 차이를 명확히 규명할 필요가 있다.
최근 문헌에서는 SGLT2 억제제와 피네레논을 신속하게 연속적으로(rapid sequence) 투여하거나 초기부터 동시에(simultaneous) 시작하는 조기 병용 전략이 개념적으로 제안되고 있다[26]. 해당 리뷰에서는 SGLT2 억제제를 먼저 시작한 뒤 피네레논의 도입 시점을 지연하지 않고 단기간 내 추가하는 방식과 두 약제를 거의 동일한 시점에서 초기 치료 전략의 일부로 함께 시작하는 방식 모두가 치료 초기의 알부민뇨 감소 반응을 앞당기고 고위험군에서 잔존 위험을 조기에 조절할 수 있다는 이론적 가능성을 제시하고 있다. 또한 SGLT2 억제제가 finerenone 관련 고칼륨혈증 위험을 일정 부분 완화할 수 있다는 가능성이 언급되며, 이러한 기전적 상보성이 조기 병용 전략의 합리성을 뒷받침하는 요소로 제시되고 있다. 다만 이는 기전적, 개념적 제안에 기반한 것이며 해당 전략 자체가 임상시험을 통해 검증된 것은 아니라는 점을 분명히 하고 있다.
이러한 점을 고려할 때 순차 투여는 각 약제의 부작용을 단계적으로 평가하며 안전성을 확보할 수 있는 장점을 가지는 반면 조기 동시 또는 신속한 연속 투여 전략은 치료 반응을 조기에 유도할 잠재적 이점을 갖는 것으로 이해된다. 그러나 이는 아직 개념적 제안의 수준에 머물고 있으며, 실제 임상적 권고로 정립되기 위해서는 충분한 규모와 기간을 갖춘 전향적 연구가 필요하다.
고칼륨혈증 관리 전략
피네레논 투여 시 고칼륨혈증은 가장 중요한 안전성 고려 사항이다. FIDELIO-DKD 연구에서 혈청 칼륨 농도 > 5.5 mmol/L의 발생률은 피네레논군에서 21.7%, 위약군에서 9.8%로 보고되었다. 그러나 치명적인 고칼륨혈증(fatal hyperkalemia)은 관찰되지 않았으며, 이는 적절한 모니터링과 용량 조절을 통해 고칼륨혈증을 관리할 수 있음을 시사한다[17]. 고칼륨혈증 위험은 기저 칼륨 상승, eGFR 감소(< 45 mL/min/1.73 m2), 중증 알부민뇨, 베타-차단제 사용에서 증가하며 루프·티아지드 이뇨제 및 SGLT2 억제제는 위험을 완화하는 보호 인자로 작용한다[27].
SGLT2 억제제 병용은 신세뇨관의 나트륨 전달을 증가시켜 칼륨 분비를 촉진하며, 실제 분석에서도 피네레논 단독 대비 고칼륨혈증 위험이 높아지지 않거나 오히려 낮은 경향을 보였다[28]. CONFIDENCE 연구에서도 초기 병용군에서 고칼륨혈증 발생률은 단독 요법군과 유사하거나 낮게 나타나 두 약제 병용 시 고칼륨혈증 위험이 적어도 증가하지 않으며 기전적 상보성에 기반한 위험 완화 가능성이 제시되고 있다[29].
실제 임상 진료지침에서는 치료 전 칼륨 ≤ 5.0 mmol/L와 eGFR ≥ 25 mL/min/1.73 m2 여부를 확인하고 시작 후 4주 이내 및 이후 4-6주 간격으로 칼륨 및 신기능을 모니터링할 것을 권고한다[20,23,27]. 고칼륨혈증 발생 시 칼륨 5.5-6.0 mmol/L에서는 일시 중단 후 10 mg으로 재개하고 칼륨 > 6.0 mmol/L에서는 즉시 중단 및 표준 치료 후 재평가한다. 저칼륨 식이, 이뇨제 조절, 칼륨 결합제 등 보조 전략은 재발 위험이 높은 환자에서 유용하다. 그러나 실제 임상에서는 다약제를 복용하는 고령 환자가 많아 고칼륨혈증 관리는 지속적인 모니터링과 약제 조절을 필요로 하는 중요한 임상적 고려 사항으로 남아 있다.
eGFR dip 현상과 관리
피네레논은 투여 초기 신세뇨관/사구체 혈역학 조정에 따른 경도의 eGFR 감소를 유발할 수 있다. FIDELIO-DKD에서는 치료 시작 후 첫 4개월 동안 eGFR 감소가 위약군 -0.73 mL/min/1.73 m2에 비해 피네레논군 -3.18 mL/min/1.73 m2로 더 크게 보고되었다[17,30]. 이러한 초기 감소는 hemodynamic changes로 해석되며 이후 장기 추적에서는 피네레논 치료군의 만성 eGFR 감소 속도가 위약군보다 완만해지는 acute dip 이후 slope 개선 패턴이 관찰되었다. 따라서 초기 경도 eGFR 감소는 치료 중단의 근거가 되지 않으며, 30% 이상 급격한 감소가 나타나는 경우에만 탈수, 약물 상호작용, 급성 신손상 등 다른 원인을 평가해야 한다.
SGLT2 억제제와의 병용에서는 두 약물의 혈류역학적 효과가 중첩되어 dip 크기가 더 커질 수 있으나 CONFIDENCE 연구에서는 평균 5-10% 수준으로 임상적으로 허용 가능한 범위 내에서 관찰되었다[24,31].
eGFR 25 미만에서의 피네레논 투여
피네레논은 FIDELIO-DKD 연구에서 eGFR 25 이상의 환자를 대상으로 시작되었으나 시험 프로토콜에서 eGFR이 25 미만으로 감소하였다는 이유만으로 치료를 중단하도록 규정하지는 않았다[17]. 또한 ADA-KDIGO 컨센서스는 혈청 칼륨이 허용 범위 내이고 내약성이 유지되는 경우 eGFR 25 미만에서도 치료를 지속할 수 있음을 언급하였다[23]. 유럽 제품 설명서 역시 eGFR 25 미만에서는 시작을 권고하지 않되 eGFR 15 이상에서는 혈청 칼륨에 기반한 용량 조절하에 치료 지속이 가능하며, eGFR 15 미만으로 진행 시에는 제한된 임상 자료를 근거로 중단을 권고한다[32].
다만 현재까지 eGFR 25 미만으로 하강한 이후 지속 투약군 및 투약 중단군을 직접 비교하여 임상 예후를 확증한 전향적 근거는 부족하므로 eGFR 25 미만으로 진행하는 경우에는 급성 콩팥 손상 가능성을 우선 평가하고 혈청 칼륨 및 신기능 모니터링을 강화하면서 칼륨 상승이나 임상적 내약성 문제 발생 시 증량 보류, 감량 또는 일시 중단 후 재개를 포함한 안전성 중심의 개별화 전략이 요구된다. 이러한 접근은 무작위 시험을 대체하는 근거는 아니지만 일본에서 시행된 120명 규모의 단일 기관 후향적 관찰 연구에서 피네레논 시작 후 초기 eGFR 변화가 동반될 수 있음에도 장기 추적에서 eGFR 기울기(slope) 개선과 UACR 감소가 관찰되었다는 보고가 있어[33] eGFR 변화만으로 자 동 중단을 결정하기보다는 임상 맥락에서 재평가한다는 해석을 보조적으로 뒷받침한다.
피네레논 치료의 적응증 및 고이득 환자군
현재까지의 임상 근거를 바탕으로 KDIGO 2022 가이드라인은 최대 허용 용량의 RAAS 억제 치료에도 불구하고 잔존 알부민뇨(UACR ≥ 30 mg/g)가 지속되는 제2형 당뇨병성 CKD 환자에서 eGFR ≥ 25 mL/min/1.73 m2이고 혈청 칼륨이 정상 범위인 경우 피네레논 추가를 권고한다[20]. 피네레논의 신장 및 심혈관 보호 효과는 주요 임상시험(FIDELIO-DKD, FIGARO-DKD) 및 통합 분석(FIDELITY) 전반에서 일관되게 관찰되었으나 절대적 이득은 고위험군에서 특히 크게 나타난다.
첫째, 요단백이 높은 환자(UACR ≥ 300 mg/g)에서 피네레논의 신장 보호 효과는 더욱 뚜렷하게 관찰되었다. FIGARO-DKD의 사후 분석에 따르면 고도 알부민뇨군(UACR ≥ 300 mg/g)에서는 eGFR ≥ 40% 감소 또는 EKSD로 구성된 신장 복합 결과의 위험이 유의하게 감소한 반면(HR, 0.74; 95% CI, 0.62-0.90) 중등도 알부민뇨군(UACR 30-< 300 mg/g)에서는 통계적으로 유의한 감소가 확인되지 않았다(HR, 1.16; 95% CI, 0.91-1.47; p_interaction = 0.02) [34]. 또한 eGFR ≥ 57% 감소 복합 결과에서도 고도 알부민뇨군에서 보다 일관된 위험 감소가 보고되었다. 한편 eGFR 수 준에 따른 피네레논의 신장 및 심혈관 보호 효과는 FIDELIO-DKD, FIGARO-DKD 및 FIDELITY 분석 전반에서 일관되게 유지되었으며 낮은 eGFR에서 피네레논의 신장 및 심혈관 보호 효과에 차이가 나타난다는 근거는 보고되지 않았다[17-19,35].
둘째, 연령, 성별, 인종에 따른 유의한 이질성은 보고되지 않았고 65세 이상 고령이나 아시아인을 포함한 다양한 하위군에서 일관된 혜택이 관찰되었다[31,36,37]. 다만 75세 이상에서는 신장 사건의 통계적 유의성이 제한적으로 나타났으나 표본 크기와 경쟁 위험의 영향을 고려할 때 실제 효과가 없다고 보기는 어렵다.
셋째, body mass index나 병용 약제(GLP-1 수용체 작용제, SGLT2 억제제)와 무관하게 단백뇨 감소 및 신장 보호 효과가 유지되었다[19,31,37].
반면 비단백뇨(UACR < 30 mg/g) 환자나 DKD 초저위험군에 대해서는 피네레논의 효과를 평가한 임상시험 자료가 거의 없으며 현재의 근거는 알부민뇨가 동반된 DKD에 국한되어 있다. 주요 무작위 대조 시험(FIDELIO-DKD, FIGARO-DKD, CONFIDENCE) 역시 모두 UACR ≥ 30 mg/g 환자를 대상으로 설계되었고[17,18,24], 이에 따라 KDIGO 2022 가이드라인 역시 지속적인 알부민뇨(≥ 30 mg/g)가 남아 있는 중등도 이상 위험군에서만 피네레논 추가를 권고한다[20]. 따라서 현시점에서 가장 명확한 임상적 이득은 중등도 이상의 알부민뇨를 동반한 DKD 환자, 특히 고알부민뇨의 고위험군에서 기대된다.
실제 세계 근거(real-world evidence)
실제 임상 환경에서도 피네레논의 효과를 평가한 관찰 연구들이 보고되고 있다. 일본에서 시행된 120명 단일 기관 후향적 관찰 연구에서는 피네레논 투여 후 연간 eGFR 감소 속도의 둔화가 관찰되었고(-4.99 to -0.59 mL/min/1.73 m2) UACR이 약 50% 감소하였으며 고칼륨혈증은 대부분 경미하였고 중대한 이상 반응은 보고되지 않았다[33]. 다만 해당 연구는 단일 기관, 비무작위, 소규모 연구로 선택 및 정보 편향의 가능성이 존재한다. 중국에서 수행된 단일 기관 후향적 연구에서는 비당뇨병성 CKD 환자를 대상으로 피네레논을 투약하였을 때 1년간 의미 있는 단백뇨 감소와 안정적인 eGFR을 보였고 고칼륨혈증 발생 역시 거의 없었다[38]. 그러나 해당 연구 역시 소규모 비무작위 관찰 연구로 무작위 대조 3상 임상시험과 직접 비교하기에는 근거 수준에 한계가 있다. 심부전 분야에서도 유사한 결과가 제시되었는데 수축기 기능 저하성 심부전(heart failure with reduced ejection fraction) 및 경도 저하성 심부전(heart failure with mildly reduced ejection fraction, HFmrEF) 환자에서는 N-terminal pro-B-type natriuretic peptide 감소와 좌심실 기능 개선이 관찰되었고 보존성 심부전(heart failure with preserved ejection fraction, HFpEF) 환자를 대상으로 한 성향 점수 매칭을 적용한 후향적 비교 연구에서는 스피로놀락톤 대비 사망률 및 심부전 입원 감소와 더 낮은 고칼륨혈증 및 급성 신손상 위험이 보고되었다[39]. 이러한 분석은 통계적 보정을 시도하였으나 잔여 교란을 완전히 배제하기는 어렵다. 이러한 실제 세계 자료는 DKD뿐 아니라 비당뇨병성 CKD 및 심부전 환자에서의 잠재적 임상 적용 가능성을 시사한다. 다만 대부분 후향적, 비무작위 연구에 기반하고 있어 무작위 대조 3상 임상시험과 동일한 수준의 근거로 해석하기에는 명확한 한계가 있다.
피네레논의 한계와 해석상의 고려점
피네레논은 FIDELIO-DKD, FIGARO-DKD 및 FIDELITY 프로그램을 통해 일관된 신장 보호 효과와 심부전 관련 사건 감소를 입증하였으나 모든 심혈관 및 사망 지표에서 완전한 일관성을 보인 것은 아니다. FIDELIO-DKD에서 신장 1차 복합 결과와 ≥ 40% eGFR 감소는 유의한 감소를 보였으나 개별 지표 중 말기 신부전과 eGFR <15 mL/min/1.73 m2 지속 감소는 통계적으로 유의하지 않았다. 심혈관 영역에서도 key secondary composite은 유의한 감소를 보였지만 심근경색, 뇌졸중, 심혈관 사망 등 개별 사건은 모두 중립적이었다. 이는 피네레논의 효과가 주로 복합 지표에서 나타나며 개별 단일 사건 감소 효과는 일관되지 않음을 시사한다[17]. FIGARO-DKD에서는 1차 심혈관 복합 결과가 주로 심부전 입원 감소에 의해 유의하게 개선된 반면 심근경색과 뇌졸중 개별 사건은 중립적이었고 신장 복합 결과는 HR이 0.87 (p= 0.07)로 경향성 수준에 머물렀다[18]. 이러한 결과는 피네레논이 죽상경화성 사건보다는 심부전 악화와 같은 비허혈성 심혈관 경과를 억제하는 데 상대적으로 더 뚜렷한 효과를 나타내며, 신기능 보호 효과는 FIDELIO-DKD 연구에서와 같이 중등도 이상의 CKD와 단백뇨가 동반된 환자군에서 보다 분명하게 관찰되는 경향을 시사한다.
한편 최근 발표된 CONFIDENCE trial은 SGLT2 억제제와 피네레논의 조기 병합 전략을 평가하였으나 1차 평가 변수가 UACR 변화로 설정된 단기 연 구로서 중 간 지 표(surrogate marker)를 평가한 연구이며 신기능 악화나 심혈관 사건과 같은 실제 임상 경과를 확인한 확증적 연구는 아니다[24]. 따라서 조기 병용의 생리적 이점은 확인되었으나 이를 임상적 예후 개선으로 일반화하기에는 근거가 충분하지 않다.
결 론
피네레논은 DKD에서 신장과 심장을 동시에 보호하는 치료 선택지로 RAAS 억제제와 SGLT2 억제제 치료 이후에도 남아 있는 잔존 위험을 추가로 감소시킬 수 있는 근거가 축적되어 왔다. 현재까지의 확립된 근거는 알부민뇨를 동반한 제2형 당뇨병성 CKD 환자에 국한된다. FIDELIO-DKD와 FIGARO-DKD, FIDELITY 프로그램을 통해 피네레논은 알부민뇨를 동반한 DKD 환자에서 신장 기능 악화와 심부전 악화 사건을 유의하게 감소시키는 결과를 보고하였으며[17-19], 고칼륨혈증 발생 위험은 증가하지만 적절한 환자 선별과 정기적인 모니터링을 통해 임상적으로 관리 가능하다는 점이 보고되었다[27]. 이러한 근거를 바탕으로 피네레논은 DKD 환자에서 RAAS 억제제 및 SGLT2 억제제와 더불어 신장-심혈관 보호를 위한 다중 기전 기반 통합 치료 전략의 한 축을 구성하게 되었다. 이러한 통합 치료 전략의 맥락에서 SGLT2 억제제와의 병용 요법에 대한 연구도 이루어지고 있다. 다만 해당 병용 전략은 주로 UACR 변화를 평가한 단기 연구에 근거하고 있어 장기 신장 및 심혈관 예후 개선에 대한 확증적 근거는 아직 축적 중이다.
한편 FINEARTS-HF 3상 연구에서는 좌심실 수축기능이 보존되었거나 경도 저하된 심부전(HFmrEF/HFpEF) 환자에서 피네레논이 위약 대비 심부전 악화 사건과 심혈관 사망의 복합결과를 유의하게 감소시켰으며[29], 특히 총 심부전 악화 사건 발생률을 약 18% 낮추는 효과(rate ratio, 0.82; 95% CI, 0.71-0.94)를 보여 심부전 영역에서의 잠재적 적용 가능성을 시사하였다. 비당뇨병성 CKD를 대상으로 한 FIND-CKD 3상 연구가 진행 중이며[40], 제1형 당뇨병 동반 CKD 환자를 대상으로 한 FINE-ONE 연구에서 6개월간 UACR 25% 감소와 양호한 안전성 프로파일이 보고되는 등[41,42] 피네레논의 항염증, 항섬유화 기전이 전통적인 DKD를 넘어 보다 다양한 신장, 심혈관 질환에서 적용될 가능성이 제기되고 있다. 향후 장기 임상 결과와 실제 임상 근거(real-world evidence)가 축적된다면 피네레논은 신장내과와 심장내과를 아우르는 통합적 심신장 보호 약제로서 임상적 역할이 더욱 확대될 것으로 기대된다.
Notes
CONFLICT OF INTEREST
No potential conflict of interest relevant to this article was reported.
FUNDING
This research was supported by the Chungnam National University Hospital Research Fund, 2024 (2024-CF-007).
AUTHOR CONTRIBUTIONS
K.P. contributed to the literature search, data curation, and writing of the original draft. D.E.C. contributed to the conceptualization, supervision, and critical revision of the manuscript. Both authors reviewed and approved the final version of the manuscript.
ACKNOWLEDGEMENTS
None.