혈뇨의 진단과 치료
Diagnosis and Treatment of Hematuria
Article information
Trans Abstract
Hematuria is a common manifestation caused by various factors such as infection, inflammation, trauma, urinary stone and malignancy. Hematuria reflects pathological state of urinary system. Isolated microscopic hematuria without any abnormalities besides of hematuria on urine microscopic examination usually presents a good clinical course or outcome. However, significant proteinuria or hypertension, which accelerates renal dysfunction, can often develop during follow-up period in patients with isolated microscopic hematuria. Compared with non-glomerular hematuria, glomerular hematuria shows several characteristic findings such as dysmorphic red blood cell (RBC) or RBC casts or significant proteinuria on urinalysis. If glomerular hematuria is strongly suspected, a kidney biopsy may be required to differentiate the cause of glomerulonephritis. In this review, we tried to review the differential diagnosis and diagnostic approach and treatment of hematuria.
증례: 54세 남자가 심한 몸살감기 이후 회복되지 않고 내원 일주일 전부터 점차 악화되는 복통과 양하지를 포함한 전신 피부 발진, 수일 전 혈변과 혈전을 동반하지 않은 검붉은색 소변을 보여 응급실에 내원하였다. 환자는 알코올간경화증 이외에 특이 병력이 없는 환자로 응급실 내원 시 생체 징후는 150/90 mmHg, 심박수 95회/분, 호흡 18회/분, 체온 37.0℃였다. 신체 진찰 소견은 우측 복부의 심한 압통 및 전반적으로 팽만된 복부를 보였고 양하지의 경미한 오목부종을 보였으나 늑골척추각압통(costovertebral angle tenderness)은 없었다. 청진 시 이상 소견은 없었다. 검사실 소견은 소변 시험지봉 검사(urine dipstick test)에서 blood 2+, protein 2+를 보였고 소변 현미경 관찰법(urine microscopic examination)에서 90% 이상의 이형 적혈구(dysmorphic red blood cell [RBC])가 보였으며 적혈구 many/고배율 시야(high power field, HPF), 백혈구 many/HPF를 보였고 적혈구 원주(RBC cast)도 관찰되었다. 소변 시험지봉 검사에서 단백뇨가 관찰되어 시행한 소변 단백-크레아티닌 비(urine protein-creatinine ratio, UPCR)와 소변 알부민-크레아티닌 비(urine albumin-creatinine ratio, UACR)는 각각 4.3 g/g과 3.5 g/g로 증가된 양상을 보였다. 혈청학적 검사에서 혈청 크레아티닌 0.95 mg/dL, 헤모글로빈 10.0 g/dL, 혈소판 89,000/μL, 혈청 알부민 2.3 g/dL였고 항중성구세포질항체(anti-neutrophil cytoplasmic antibody) 및 항핵항체(antinuclear antibody)는 음성이었으며 혈청보체(serum complement 3 [C3] and 4 [C4])는 모두 감소한 소견을 보였다. 대장 내시경 검사에서는 횡행결장을 따라 발적을 동반한 궤양성 점막 병변이 관찰되었으며 복부 컴퓨터단층촬영(computed tomography, CT)에서는 전 대장의 심한 부종이 확인되었다(Fig. 1). 입원 중 지속적인 혈청 크레아티닌 수치의 증가가 보여 혈소판 수치가 감소하였음에도 신기능의 저하의 원인을 알고 적절한 치료를 위하여 신장 조직 검사를 시행하였고 신장 조직 검사 소견은 사구체의 모세혈관 내 세포의 증식(endocapillary proliferation)과 세포성 반월상(cellular crescents)을 동반한 메산지움의 세포 증식이 보였다(Fig. 2). 면역형광현미경(immunofluorescence microscopy) 염색에서 메산지움의 면역글로불린A (immunoglobulin A, IgA)와 C3에 대해 강한 양성 반응을 보였다. 위의 결과를 토대로 전신혈관염(systemic vasculitis)과 연관된 사구체 질환인 IgA혈관염(IgA vasculitis) 또는 헤노흐-쉔라인자반증신염(Henoch Schönlein purpura nephritis)에 의한 급속 진행 사구체신염(rapid progressive glomerulonephritis)으로 진단하였고 급격한 염증세포의 증가를 막고 신기능 악화를 막기 위해서 고용량 스테로이드 및 cyclophosphamide 치료를 시작하였으나 면역억제제 치료 중 위장 출혈 및 폐렴의 발병으로 면역억제제 치료를 중단하였으며 수개월 후 신기능의 악화를 보여 결국 혈액 투석을 시작하였다. 혈액 투석 치료 후 환자의 요독 증상은 호전되어 현재 유지 혈액 투석을 받고 있다.

Findings of computed tomography (CT) of the abdomen and colonoscopy. CT of the abdomen revealed a severely edematous colon (white arrows) and kidneys with normal contours (black arrowheads) and size, without signs of hydronephrosis. Colonoscopy identified multiple intermittent ulcerative lesions throughout the entire colon.
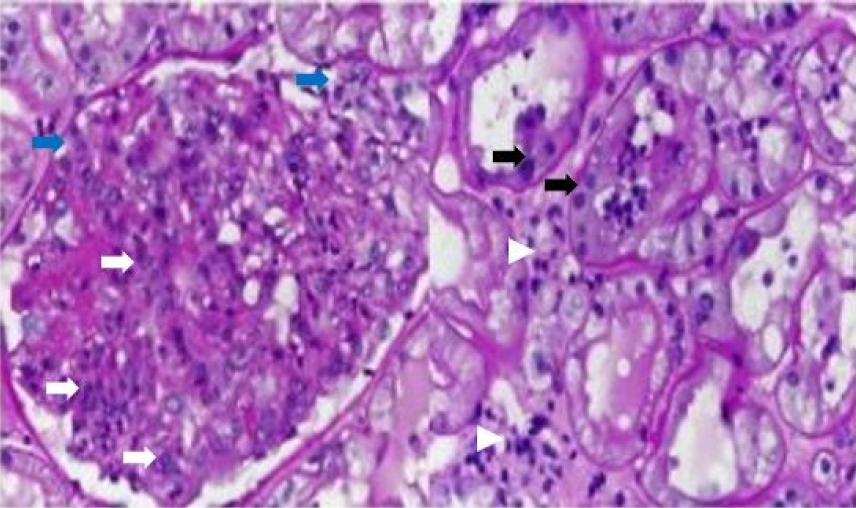
The light microscopic findigns of the kidney biopsy (hematoxylin-eosin stain, ×400). Most glomeruli showed occluded capillary lumens due to endocapillary proliferations (white arrows), composed of neutrophils, lymphocytes, and endothelial cells. Cellular crescents were observed in several glomeruli (blue arrows). The interstitium showed infiltration by lymphocytes and neutrophils (white arrowheads), leading to the formation of tubulitis in the tubules (black arrows).
본 론
혈뇨의 정의 및 감별 진단
혈뇨는 일반적으로 소변 현미경 관찰법으로 진단되는 현미경적 혈뇨(microscopic hematuria)와 육안으로 진단되는 육안적 혈뇨(gross hematuria)로 구분할 수 있다. 임상에서 흔히 말하는 성인의 혈뇨는 소변에서 HPF당 3개 이상의 적혈구가 소변 현미경 관찰법을 통해서 관찰될 때로 정의한다. 육안적 혈뇨는 소변 현미경 관찰법을 통해서 많은 수의 적혈구가 소변에서 보이므로 당연히 혈뇨의 범주 안에 있겠다. 혈뇨는 비뇨기과적 진단 및 치료를 위해서 내원하는 환자의 20%를 차지할 만큼 높은 유병률을 보이는 비뇨기과적 문제라고 생각할 수 있지만 비뇨기계 이상 이외에도 사구체질환의 초기 증후일 수도 있기에 원인에 대한 접근이 중요하다[1]. 이전 대규모 연구는 혈뇨 환자의 약 10%에서 비뇨기계 암(urologic malignancy)이 진단되었다고 보고하였으며 육안적 혈뇨를 보이는 환자의 약 13%에서 비뇨기계 암이 진단되었다고 보고하였다[2]. 또한 건강한 성인에서는 약 2.4-31.1%에서 현미경적 혈뇨가 보인다고 보고하였으며 현미경적 혈뇨를 보이는 환자의 2-3%에서 비뇨기계 암이 진단되었다고 보고하기도 하였다[1,3]. 따라서 혈뇨의 정확한 원인에 대한 감별 진단은 임상적으로 중요하다. 증례에서 언급된 것처럼 붉은색 소변이 보이는 경우 진성 혈뇨(true hematuria)와 가성 혈뇨(pseudohematuria)를 먼저 구분하여야 한다. 붉은색 소변이면서 소변 시험지봉 검사(urine dipstick test)에서 잠혈(occult blood) 또는 heme 양성이고 소변 현미경 관찰법에서 RBC 또는 RBC cast가 관찰되는 경우 진성 혈뇨라고 할 수 있다. 소변 시험지봉 검사에서 잠혈은 양성이지만 소변 현미경 관찰법에서 적혈구가 관찰되지 않는 경우는 혈색소뇨(hemoglobinuria)와 미오글로빈뇨(myoglobinuria)가 있으며 이는 육안적으로는 붉은색 소변이나 가성 혈뇨라고 할 수 있다. 심한 바이러스 감염 및 무리한 운동 또는 심한 근육 손상 후에 발생하는 급성 신손상의 원인인 횡문근융해증(rhabdomyolysis)의 경우 붉은색 소변을 보일 수 있다. 붉은색 소변은 미오글로빈이 소변으로 배출되면서 발생하며 이때 붉은색 소변은 소변 시험지봉 검사의 잠혈 반응은 양성이지만 현미경 관찰법에서 적혈구가 보이지 않는 가성 혈뇨의 한 예라고 할 수 있겠다. 소변 시험지봉 검사의 잠혈 반응에 음성인 붉은색 소변 역시 가성 혈뇨이며 리팜핀, 페니토인 같은 약물 또는 비타민C, 뿌리채소인 비트, 당근 등 케로틴을 포함한 일부 음식을 통해서 나타날 수 있다. 또한 빌리루빈, 요산, 인산이 소변을 통해서 많이 분비되는 경우에도 붉은색 소변이 보일 수 있으나 소변 시험지봉 검사에서 잠혈 반응은 음성으로 나타난다(Fig. 3).

Diagnostic approach and differential diagnosis of red urine. RBC, red blood cell; HPF, high power field.
따라서 혈뇨의 감별 진단을 위해서 시험지봉 검사와 소변 현미경 관찰법을 같이 시행하는 것이 중요하다. 소변 현미경 관찰법은 진성 혈뇨의 진단에서 가장 중요한 검사 방법이며 적혈구 수, 적혈구 모양, 적혈구 원주 및 결정체(crystal)와 같은 요침사(urinary sediments)를 확인할 수 있어 진성 혈뇨의 병적 원인의 감별 진단에 중요하다. 혈뇨가 의심되는 환자에서 소변 시험지봉 검사만 시행되었다면 반드시 소변 현미경 관찰법을 시행하여 실제 적혈구를 확인하여야 한다. 소변 현미경 관찰법을 포함한 소변 검사에서는 폐경 전 여성의 생리, 바이러스 감염, 운동, 발열, 외상 등과 같은 상황에서도 일과성 혈뇨(transient hematuria)가 보일 수 있기에 병적인 상태를 의미하는 진성 혈뇨를 진단하기 위해서는 상기의 위양성을 유발하는 임상 양상이 호전된 후 적어도 3번 이상의 소변 검사에서 3개 이상의 적혈구가 HPF에서 관찰되는 경우에 지속적 혈뇨(persistent hematuria)라고 한다. 이러한 지속적 혈뇨 환자의 약 9% 이상에서 신장이나 비뇨기계 병변을 보인다는 연구가 있기 때문에 지속적 혈뇨가 보이는 경우 혈뇨의 병적인 원인 감별을 위한 추가 검사를 시행하여야 한다. 하지만 한 번의 소변 현미경 관찰법에서 100개 이상의 적혈구가 관찰되거나 육안적 혈뇨가 보이는 경우에는 반복적인 소변 검사 없이 진성 혈뇨의 원인 감별을 위한 추가 검사를 바로 시행할 수 있겠다[2,4]. 이처럼 소변 검사는 혈뇨 진단을 위한 첫 번째 단계이며 농축된 산성뇨의 상태에서 가장 정확한 결과를 얻을 수 있기 때문에 12시간 금식 후 아침 첫 소변으로 검사를 진행하는 것이 좋다.
진성 혈뇨의 진단적 접근
진성 혈뇨의 원인을 진단하기 위해서 우선적으로 환자의 성별, 나이, 기저질환, 사회력 및 약물력 등에 대한 확인이 필요하며 신체 진찰을 통해서 피부 발진, 전신 부종 또는 하지의 오목부종 유무, 양측 늑골척추각 압통 유무, 복부 혈관의 잡음(abdominal bruit), 심장의 잡음 및 부정맥의 확인, 고령 남성의 경우 전립선 비대의 유무 등을 확인하는 것이 좋다. 또한 통증을 동반하는 경우 통증의 양상도 확인하여야 하겠으며 특별히 현미경적 혈뇨가 아닌 육안적 혈뇨를 보이는 경우에는 소변의 색깔과 혈전의 동반 여부 및 특성을 구분하는 것이 좋다. 일반적으로 비뇨기계 이상에 의한 혈뇨는 육안적으로 혈전 등을 동반하는 경우가 많고 소변도 선홍색 계열의 붉은색으로 나타나는 경우가 많다. 이에 반해 사구체 이상에 의한 혈뇨는 혈전을 동반하지 않으며 주로 선홍색 보다는 검붉은색을 나타내는 경우가 많고 혈뇨 발생 전 피부 발진 및 바이러스 또는 세균성 감염에 의한 상기도 감염의 증상과 같은 전신 증상을 동반하는 경우가 있으니 이를 통한 감별을 일차적으로 고려하여야 한다.
별다른 증상이 없고 육안적으로 보이지 않는 무증상 현미경적 혈뇨(asymptomatic microscopic hematuria)의 경우에도 일과성 혈뇨가 배제되고 지속적 혈뇨, 즉 진성 혈뇨로 판단되면 혈뇨의 원인 판단을 위해서 소변 현미경 관찰법과 소변 시험지봉 검사를 시행하여야 한다. 2023년 대한신장학회에서 보고된 현미경적 혈뇨 근거 기반 진료지침에 따르면 현미경적 혈뇨가 확인된 환자에서 원인 감별을 위해서 최초 검사로 이형 적혈구(dysmorphic RBC), 적혈구 원주, 농뇨(pyuria), 요 질산염(nitrite) 및 백혈구 원주(white blood cell [WBC] cast) 등의 유무를 확인하고 단백뇨 정량 검사로 UACR 또는 UPCR의 측정을 권고하고 있다. 또한 위의 소변 검사 이외에도 혈액 혈색소, 혈소판 및 혈청 알부민 측정, 혈청 크레아티닌을 통한 추정 사구체여과율(estimated glomerular filtration rate)도 측정하도록 하고 있다[5]. 의미 있는 단백뇨가 확인되고 이형 적혈구 또는 적혈구 원주 등이 확인된다면 사구체성 혈뇨를 강하게 의심하여야 한다. 만약 상기 검사 소견이 사구체성 혈뇨를 의심할 만한 소견이 없다면 즉 단백뇨, 이형 적혈구, 적혈구 원주 등의 소견을 보이지 않고 감염의 증후 또한 보이지 않는다면 신장 및 비뇨기과 종양에 의한 혈뇨를 배제하기 위한 추가 검사를 고려하여야 하겠다. 이와 관련하여 최근 2020년에 제시된 미국비뇨기과학회 가이드라인에 따르면 무증상 현미경적 혈뇨를 동반한 환자에서 비뇨기계 종양의 가능성을 배제하기 위하여 침습적 검사(방광경 검사)를 포함한 비뇨기과적 검사를 무조건 시행하는 것보다는 환자 개인의 계층화된 암 발생 위험도에 맞추어 검사를 시행하도록 권고하고 있다. 구체적으로 60세 이상의 성인, 30갑년 이상의 흡연력, HPF당 25개 이상의 적혈구가 보이는 경우 또는 육안적 혈뇨를 보이는 경우를 비뇨기계 암 발생 고위험 요소(high risk factors)로 정하여 이 중 적어도 한 개 이상이 해당된다면 방광경 검사 및 상부 요관을 확인할 수 있는 CT-urography를 시행하도록 규정하고 있다[6]. 2023 현미경적 혈뇨 근거 기반 진료 지침에서도 성인 현미경적 혈뇨 환자에서 요로암의 위험도에 따라 진단 방법을 다르게 할 것을 권고하고 있으며 요로암의 위험인자로 미국비뇨기과학회 가이드라인에서 제시한 인자를 포함하여 하부 요로의 자극적인 증상, 골반부 방사선 치료 과거력, cyclophosphamide 계열의 항암제 치료력, 벤젠 화학 물질 또는 방향족 아민(aromatic amine)에 대한 직업적 노출력, 가족력, 장기간 요로에 이물질을 거치하는 경우 등을 추가적으로 제시하고 있다. 또한 위의 요로암 위험 인자가 없는 저위험군의 현미경적 혈뇨의 경우에는 공동 의사결정 과정을 거쳐서 6개월 이내에 소변 검사를 다시 시행하거나 방광경 검사와 콩팥 초음파 검사를 시행하여 평가하도록 권고하고 있으며 6개월 이내에 재시행된 소변 검사에서 지속적인 현미경적 혈뇨가 확인되면 위의 과정을 반복하는 것이 좋고 다른 원인 질환의 배제를 위해서 콩팥 초음파 검사를 시행하여 도움을 받을 수 있다고 제시하고 있다[5]. 종합하면 진성 혈뇨의 원인 진단을 위해서는 환자의 병력 청취 및 신체 진찰을 통해서 증상의 유무 등을 우선적으로 파악하고 증상이 없는 무증상 현미경적 혈뇨의 경우에도 소변 시험지봉 검사 및 소변 현미경 관찰법 그리고 소변 배양 검사를 시행하여 그 결과를 정확하게 해석하고 혈뇨의 원인을 진단하기 위한 영상 검사, 혈청학적 검사 그리고 병리학적 검사가 필요하다면 선택적으로 진행하는 것이 좋겠다(Fig. 4).
고립성 혈뇨(isolated hematuria)
종종 소변 검사에 혈뇨는 보이지만 단백뇨, 원주, 결정체 또는 다른 세포를 동반하지 않는 고립성 혈뇨(isolated hematuria) 가 지속적으로 보이는 경우가 있다. 이러한 경우에는 신장-비뇨기계 결석, 종양, 외상성 출혈, 응고 장애(coagulation disorders), 사구체신염(glomerulonephritis) 등을 의심하여야 한다. 고립성 혈뇨 환자에서 사구체신염과 그 외의 다른 병적인 상태를 구분하기 위해서 소변 현미경 관찰법을 통한 적혈구 이형성(dysmorphism) 여부 및 적혈구 원주를 확인하는 것이 많은 도움이 될 수 있다. 소변 현미경 관찰법에서 이형 적혈구 또는 적혈구 원주를 보이면서 고립성 현미경적 혈뇨(isolated microscopic hematuria)가 보이면 고립성 사구체성 혈뇨(isolated glomerular hematuria)를 강하게 의심할 수 있다. IgA신병증(IgA nephropathy), 얇은기저막병(thin basement membrane disease), 알포트증후군(Alport’s syndrome)과 같은 유전성 신염(hereditary nephritis)이 고립성 사구체성 혈뇨의 대표적인 질환이며 이 중 IgA신병증이 가장 흔하다. IgA신병증 및 얇은기저막병에 의한 혈뇨는 종종 육안적 혈뇨를 보일 수도 있다. 이처럼 고립성 사구체성 혈뇨는 사구체신염의 초기 징후일 수 있다. 이전 연구에 의하면 증상이 없는 고립성 사구체성 혈뇨를 가진 환자를 장기간 추적하였을 때 40% 이상에서 혈뇨의 소견이 사라졌으며 10% 내외에서는 단백뇨를 동반하였으나 신기능의 저하의 악화로 인한 말기 신장병으로 이행된 환자는 없었다고 보고하였다. 따라서 고립성 사구체성 혈뇨를 보이는 환자의 예후는 전반적으로 양호하다고 할 수 있다[7,8]. 고립성 현미경적 혈뇨의 자연 경과를 확인한 연구에서도 고립성 현미경적 혈뇨를 지닌 환자의 신장 조직 검사 결과 IgA신병증이 가장 흔하였으며 메산지움증식사구체신염(mesangial proliferative glomerulonephritis), 사구체미세변화(glomerular minor lesion), 얇은기저막병 순으로 진단되었고 장기간 추적하였을 때 예후가 좋았고 추적 관찰 기간 중 단백뇨가 동반된 경우는 6%, 고혈압이 동반된 경우는 5%였다[9]. 이러한 사구체 질환 이외에도 결석, 종양, 외상성 출혈, 응고 장애 등에 의해서도 고립성 혈뇨는 발생할 수 있다. 결석, 외상성 출혈 등은 일반적으로 증상을 동반하기에 증상 없는 고립성 혈뇨(asymptomatic isolated hematuria) 의 경우 고립성 사구체성 혈뇨가 아니라면 그 원인으로 응고 장애, 종양을 고려하여야 한다. 요약하면 고립성 현미경적 혈뇨의 경우 단백뇨가 동반된 혈뇨에 비해서 대체적으로 좋은 임상 예후를 보였으며 장기간 추적 과정 중 많은 예에서는 정상화되기도 하지만 일부에서는 단백뇨 또는 고혈압이 동반되는 양상을 보일 수 있기에 정기적인 소변 검사의 추적이 필요하다. 추적 과정 중 하루에 소변의 총 단백이 500 mg 이상 지속적으로 관찰되거나 신기능의 이상이 발생한다면 정확한 원인 진단을 위한 신장 조직 검사가 필요하며 증상이 없는 고립성 현미경적 혈뇨의 환자 중 비뇨기계 암의 고위험 인자가 많다면 비뇨기계 종양의 감별을 위한 추가 검사가 요구된다(Fig. 4).
사구체성 혈뇨(glomerular hematuria)
진성 혈뇨 중 사구체성 혈뇨는 사구체 여과장벽(glomerular filtration barrier)의 손상에 의해 발생하며 이는 소변 현미경 관찰법을 통해 요침사를 확인하여 일차적으로 의심할 수 있다. 적혈구를 포함한 적혈구 원주 또는 적혈구와 백혈구가 동반된 소견 즉 세포성 원주(cellular casts)가 소변 현미경 관찰법을 통해서 관찰되거나 유극 적혈구(acanthocytes)와 같은 이형 적혈구가 관찰되면 일차적으로 사구체성 혈뇨를 의심할 수 있다. 적혈구 원주를 포함한 요원주(urine casts)는 사구체성 혈뇨를 진단하는 데에 있어서 특이도가 높은 검사이지만 한편으로 민감도가 낮은 검사이기도 하다. 또한 일부 연구에서는 적혈구 원주를 포함한 세포성 원주는 보다 심한 사구체 손상에 의한 혈뇨에서 발생한다고 보고하기도 하였다[9]. 이처럼 소변의 요침사만으로는 사구체성 혈뇨를 정확하게 진단하기 어렵다. 사구체성 혈뇨는 사구체 여과장벽의 손상에 의해 발생하기에 사구체성 혈뇨는 의미 있는 알부민뇨(albuminuria)를 일반적으로 동반한다.
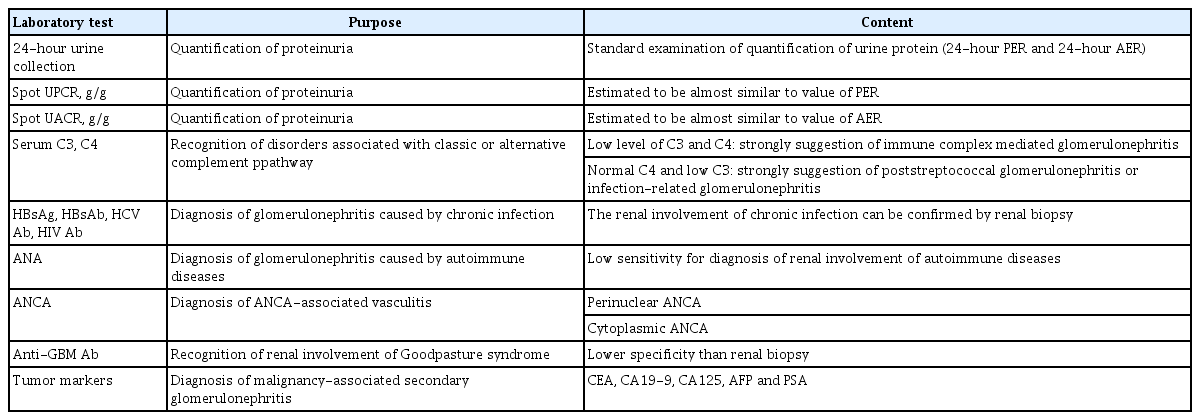
알부민은 혈청 단백질 중 가장 풍부하며 정상적으로 하루에 약 1 g의 혈청 알부민이 사구체를 통해서 여과될 수 있다. 하지만 대부분의 여과된 알부민은 세뇨관에서 재흡수된다. 따라서 신장 세뇨관의 손상의 발생한 경우에도 소변에서 알부민뇨가 나타날 수 있기에 소변 시험지봉 검사에서 단백뇨 즉 알부민뇨 양성 하나의 결과만으로 사구체성 혈뇨를 진단할 수는 없다. 범람 단백뇨(overflow proteinuria)의 원인질환인 단세포군감마글로불린병증(monoclonal gammopathy)의 경우에도 파라단백혈증(paraproteinemia)에 의해 여과된 면역글로불린 유리경쇄(immunoglobulin free light chain)가 신장 세뇨관의 손상을 유발하여 알부민뇨가 발생할 수 있으므로 단백뇨 정량 검사를 통한 상당히 의미 있는 양의 알부민뇨를 확인하지 못하면 사구체성 혈뇨를 확진할 수 없다. 일반적으로 소변에서 하루 총 단백이 500 mg 이상이면서(24-hour urine protein excretion rate [PER] > 500 mg) 소변 알부민/단백 비율(urine albumin/protein ratio)이 40%를 초과하는 경우에 사구체 손상에 의한 의미 있는 단백뇨라고 생각할 수 있다[10]. 하루 소변의 단백 정량 검사의 가장 표준화된 방법은 24시간 소변 채집을 통한 PER 또는 알부민 배설률(albumin excretion rate, AER)을 확인하는 방법이나 임상적으로는 UPCR (PER과 유사) 또는 UACR (AER과 유사)을 통하여 손쉽게 24시간 소변의 총 단백과 알부민을 추정할 수 있다(Table 1). 증례에서는 이형 적혈구 및 적혈구 원주를 동반한 붉은색 소변을 보임과 동시에 UPCR 과 UACR이 의미 있게 증가한 소견을 보였기에 사구체성 혈뇨를 강하게 의심할 수 있었으며 이에 대해서 사구체성 혈뇨의 감별 진단을 위해서 혈청학적 검사 및 신장 조직 검사를 추가적으로 진행하였다.
사구체성 혈뇨가 의심되는 상황에서는 일차성 사구체신염(primary glomerulonephritis)에 의한 혈뇨인지 아니면 환자의 기저질환에 의한 이차성 사구체신염(secondary glomerulonephritis) 에 의한 혈뇨인지를 감별하기 위한 혈청학적 검사를 우선적으로 시행하여야 한다. 이차성 사구체신염은 주로 만성 B형 또는 C형 간염 및 사람면역결핍바이러스(human immunodeficiency virus) 감염과 같은 만성 감염질환에 의하여 발생할 수 있으며 전신홍반루푸스(systemic lupus erythematosus) 및 류마티스관절염(rheumatoid arthritis)과 같은 자가면역성 질환, 급성 감염 그리고 본 증례처럼 전신혈관염(systemic vasculitis)에 의해서도 드물게 발생할 수 있다. 간경화 환자에서 IgA의 활성화에 의한 면역복합제 연관 사구체신염(immune complex mediated glomerulonephritis)이 전신 혈관염의 신장 침범의 한 형태로 발생할 수 있기에 이를 고려한 일차적 혈청학적 검사를 진행하는 것이 좋다(Table 1). 또한 당뇨, 악성 종양 등도 이차성 사구체신염의 원인이 될 수 있으므로 혈당 및 당화혈색소를 측정하여 당뇨가 진단된 환자에서는 당뇨병망막병증(diabetic retinopathy)의 유무를 확인하고 나이, 성별 및 암 발생의 위험 인자가 동반된 경우에는 선별 검사로 종양 표지자 검사를 시행하는 것이 좋다. 이러한 혈청학적 검사 결과 이차성 사구체신염의 가능성이 높지 않거나 추적 관찰 중에 신기능의 급격한 악화 등의 소견이 보이는 경우 정확한 사구체신염의 원인을 파악하고 사구체 침범 여부를 확인하기 위해 신장 조직 검사를 시행하는 것이 좋다[11].
혈뇨의 원인에 따른 치료
일반적으로 고립성 현미경적 혈뇨의 경우에는 별다른 약물 치료 없이 소변의 추적 검사를 통해 단백뇨 발생 여부를 면밀히 관찰하는 것이 필요하다. 이때 고혈압 및 신기능의 감소 여부를 검사실 검사 등을 통해 확인하는 것이 중요하다. 추적 중 단백뇨가 발생하거나 고혈압이 발생한다면 추후 신기능의 감소를 막기 위해 하루 나트륨 섭취를 2 g 미만으로 줄인 저염 식이(low-salt diet) 및 항고혈압 약제를 사용한 치료가 중요하다. 항고혈압 약제는 안지오텐신전환효소억제제(angiotensin converting enzyme inhibitor, ACEi) 또는 안지오텐신II수용체차단제(angiotensin II receptor blocker, ARB)를 사용하는 것이 좋으며 이러한 약제는 사구체의 수출세동맥(efferent arteriole)의 확장을 통해 사구체 압력을 효과적으로 줄여서 혈역학적으로 단백뇨의 발생을 감소시킬 수 있기에 단백뇨를 보이는 환자에서 일차적으로 선택될 수 있다. 상기 약제를 사용하여 단백뇨를 보이는 환자에서 혈압을 130/80 mmHg 미만으로 조절하는 것이 좋다. 최근에는 나트륨포도당공동수송체2차단제(sodium-glucose cotransporter 2 inhibitor, SGLT2i) 및 비스테로이드성 미네랄코르티코이드수용체차단제(nonsteroidal mineralocorticoid receptor antagonists, ns-MRA)가 혈역학적 그리고 항염증(anti-inflammatory) 등의 기전을 통하여 당뇨병콩팥병 환자를 포함한 단백뇨를 동반한 만성 콩팥병 환자에서 단백뇨를 효과적으로 줄일 수 있음을 확인하였다. 따라서 당뇨병콩팥병 환자에서 소변의 이상 및 의미있는 단백뇨를 보이는 경우에는 ARB를 포함한 SGLT2i가 일차적으로 권장되며 ARB 제제를 통해서도 조절되지 않는 단백뇨 환자의 경우에는 ns-MRA 제제를 선택적으로 추가할 수 있다[12].
임상적으로 의미 있는 단백뇨를 동반한 혈뇨의 경우에는 신장 조직 검사를 통해서 사구체성 혈뇨의 정확한 원인을 진단할 수 있다. 일차성 사구체신염의 흔한 원인으로 IgA신병증(IgA nephropathy), 미세변화병(minimal change disease), 국소 분절성 사구체경화증(focal segmental glomerulosclerosis), 막신병증(membranous nephropathy), 막증식사구체신염(membranoproliferative glomerulonephritis) 등이 있으며 각 질환마다 치료가 상이하나 일반적으로 원인이 면역복합제 연관 사구체신염(immune complex mediated glomerulonephritis)인 경우에는 스테로이드 기반의 면역 억제제 치료를 시행할 수 있다. 또한 혈청학적 검사 및 신장 조직 검사를 통해 이차성 사구체성 혈뇨로 진단된 경우에는 사구체성 혈뇨를 유발한 전신질환에 대한 치료를 시행한다.
결 론
혈뇨의 진단은 소변의 육안적 성상을 확인하고 정확하고 자세한 병력 청취 및 신체 진찰을 시행하는 것에서부터 시작한다. 더불어 소변 시험지봉 검사 및 소변 현미경적 검사를 통해서 일차적으로 가성 혈뇨와 진성 혈뇨를 감별하고 진성 혈뇨의 경우 사구체성 기원의 혈뇨와 비사구체성(non-glomerular) 기원의 혈뇨를 구분하는 것이 중요하다. 이를 위해서는 소변 시험지봉 검사 및 소변 현미경 관찰법의 세포 및 요침사 소견의 해석이 중요하며 소변 시험지봉 검사에서 알부민뇨 양성의 경우 단백 정량 검사를 통한 알부민뇨의 양적 평가를 시행하는 것이 중요하다. 단백뇨 및 농뇨 등의 이상 소견 없이 혈뇨만 관찰되는 고립성 현미경 혈뇨의 경우 대부분 예후가 좋으나 추적 관찰 중 단백뇨 또는 고혈압이 발생할 수 있으므로 정기적인 소변 검사 및 진찰이 중요하다. 소변 현미경적 검사에서 적혈구 침사 또는 이형 적혈구가 관찰되며 의미 있는 알부민뇨가 동반되어 사구체성 혈뇨가 의심되는 경우에는 이차성 사구체 질환에 의한 혈뇨를 감별하기 위해 혈청학적 검사의 시행을 고려한다. 이차성 사구체 질환에 의한 혈뇨의 가능성이 높지 않거나 추적 중 신기능의 급격한 감소가 보이는 경우에는 일차성 사구체신염의 정확한 진단 또는 신기능의 급격한 감소의 원인을 파악하기 위해서 신장 조직 검사를 시행하여 원인 질환에 따른 개별적 치료를 시행하도록 한다.
위의 진단적 접근을 본 증례에 적용하면 다음과 같다. 증례는 간경화 환자였으며 신체 진찰 소견으로 양측 늑골척추각 압통은 없었으나 전신의 피부발진 및 양하지의 경미한 오목부종이 있었고 소변은 육안적으로 검붉은색의 혈전을 동반하지 않는 소견을 보였다. 소변 시험지봉 검사에서 알부민뇨와 잠혈 양성 소견을 보였고 소변 현미경적 검사에서 많은 적혈구 및 적혈구 원주(RBC cast) 소견과 함께 90% 이상의 이형 적혈구(dysmorphic RBC)도 확인할 수 있었다. 또한 정량적인 알부민뇨 평가에서 의미 있는 단백뇨 소견(UACR, 3.5 g/g)을 보였기에 증례의 붉은색 소변은 사구체성 기원의 혈뇨임을 의심할 수 있었다. 사구체성 혈뇨의 경우 이차성 사구체신염을 배제하여야 하며 이와 관련된 혈청학적 검사에서 본 증례의 경우 혈청보체를 제외한 대부분의 검사는 음성 소견을 보였다. 바이러스를 포함한 감염질환 및 자가면역질환을 포함한 이차성 사구체 질환에 의한 혈뇨의 가능성은 낮으나 알코올성 간경화, 양 하지를 포함한 전신의 특징적인 피부발진 그리고 대장 내시경 소견에서 보이는 점막의 광범위한 부종 및 발진 소견 등은 만성 간질환과 연관된 전신혈관염(systemic vasculitis)의 신장 침범 가능성을 배재할 수 없었으며 증례의 경우 내과적 치료 중 급격한 신기능의 감소를 보였기에 신장 조직 검사를 시행하였다. 조직 검사를 통해서 혈뇨의 원인으로 간경화와 연관된 헤노흐-쉔라인자반증신염(Henoch-Schönlein purpura nephritis)이 진단되어 적극적인 면역 억제제 치료를 시행할 수 있었으며 이후 치료에 대한 반응 및 예후를 예측하여 치료할 수 있었다.
임상에서 혈뇨의 정확한 진단 및 감별 진단은 쉽지 않다. 또한 혈뇨는 본 증례처럼 내과적 질환 이외에도 비뇨의학 및 산부인과학 분야의 질환에 의해서도 발생할 수 있기 때문에 종종 다양한 일차의료기관에서 확인되어 진단적 접근이 이뤄지기도 한다. 이처럼 혈뇨는 다학제적 접근이 필요한 질환이며 관련된 의학 분야의 다양한 진단 가이드라인을 참고하여 혈뇨의 정확하게 정의하고 원인 감별을 위한 진단적 접근 방법을 종합하여 제시하는 것은 그 의미가 매우 크다고 할 수 있겠다.
Notes
CONFLICTS OF INTEREST
No potential conflict of interest relevant to this article was reported.
FUNDING
None.
AUTHOR CONTRIBUTIONS
Conception and design: JHJ.
Acquisition of data: JHJ.
Analysis and interpretation of data: JHJ.
Drafting of the manuscript: JHJ.
Critical revision for intellectual contents: JHJ.
Final approval of the manuscript: JHJ.
Acknowledgements
This article was supported by the Wonkwang University fund in 2023.