 |
 |
| Korean J Med > Volume 99(3); 2024 > Article |
|
Abstract
Subclinical hypothyroidism (SCH) is characterized by elevated serum thyroid-stimulating hormone (TSH) levels and normal free thyroxine levels. The Korean Thyroid Association recently issued guidelines for managing SCH. Based on the Korea National Health and Nutrition Examination Survey (2013-2015), a serum TSH level of 6.8 mIU/L is the reference value for SCH. SCH is classified as mild (TSH 6.8-10.0 mIU/L) or severe (TSH > 10.0 mIU/L), and patients are categorized as adult (age < 70 years) or elderly (age ≥ 70 years). Levothyroxine treatment (LT4-Tx) is not recommended for mild or even severe SCH in elderly patients. Immediate LT4-Tx can be given to adults in most cases, but not to women who are pregnant, patients with progressive disease, or patients with underlying coronary artery disease, heart failure, or dyslipidemia.
무증상 갑상선기능저하증은 혈중 갑상선호르몬 수치는 정상이면서 갑상선자극호르몬(thyroid stimulating hormone, TSH)만 증가된 상태이다. 무증상 갑상선기능저하증은 진료 현장에서 드물지 않게 접하게 되는데 건강 검진 등에서 우연히 발견되거나 모호한 증상을 호소하는 환자에서 여러 가지 검사를 하던 중 TSH 증가만 확인되기도 한다. 무증상 갑상선기능저하증은 중증 질환은 아니지만 비교적 흔하게 진단되므로 적절한 관리와 치료가 필요하다. 본고에서는 최근 발표된 2023 대한갑상선학회 무증상 갑상선기능저하증 진료 권고안(이하 2023 권고안)에 근거하여 진단 및 관리에 대한 최신 지견들을 소개하고자 한다.
2023 권고안[1]에서는 제6기 국민건강영양조사(이하 국건영) 결과를 바탕으로[2,3] 우리나라의 TSH 참고 구간을 0.6-6.8 mIU/L로 새롭게 제시하였다. 기존의 TSH 참고 구간(0.4-4.0 mIU/L)은 1990-2000년대 초반 미국과 유럽의 코호트 연구를 통해 제시된 기준을 그대로 적용한 것이다. 그러나 한국인의 정상 혈중 TSH 농도 범위에 관한 국내 연구들[2-6]의 결과에 따르면(Table 1) 한국인의 혈중 TSH 상한선은 다른 나라에 비해 높으며 연령 증가에 따른 TSH 농도 증가 형태도 다른 나라가 주로 선형인 것에 반해 U자형을 보이는 등 뚜렷한 차이를 보인다. 이는 우리나라의 요오드 섭취 형태와 연관성이 높다고 해석되고 있다. 따라서 우리나라 실정에 맞춘 TSH 참고 구간을 제시할 필요성에 따라 2023 권고안에 적용하게 되었다. 이에 따르면 그간 정상을 벗어난 것으로 생각되던 TSH 4.0-6.8 mIU/L 미만 구간은 더 이상 무증상 갑상선기능저하증이 아니다. 이제 임상의들은 우리나라의 TSH 상한선 기준이 다른 나라의 기준에 비해 높다는 점을 기억할 필요가 있다. TSH의 경미한 증가만으로도 과도하게 불안해하는 환자를 안심시키고 불필요한 검사나 치료의 부담을 줄이는 데 있어 새롭게 제시된 2023 권고안은 중요한 근거가 된다.
여기서 한 가지 유의할 점은 TSH 측정값이 측정 kit에 따라 차이를 보인다는 점이다. 제6기 국건영 자료는 전기화학발광 면역분석법(electrochemiluminescence immunoassay)을 활용하는 단일한 TSH 측정 kit (Roche, Basel, Switzerland)를 이용하여 얻어진 결과에 근거한다. 따라서 Roche 제품 외의 다른 Kit를 사용하여 측정한 TSH 수치에 대해 위의 기준을 그대로 적용하기엔 제한이 있다. 이에 따른 혼란을 최소화하기 위하여 대한갑상선학회 진료지침제정위원회에서는 TSH 측정값 평가위원회를 구성하여 국내에서 다빈도로 사용되고 있는 총 8개의 TSH 시약의 결과를 비교 분석하고 각 kit별 추정치를 제시하였다[7]. 이에 따르면 Roche kit에 대한 나머지 7개 시약의 상관계수는 모두 0.99 이상을 보였고 무증상 갑상선기능저하증의 새로운 진단 기준인 6.8 mIU/L에 해당하는 각 시약별 추정치는 Abbott (Lake County, IL, USA) 5.2 mIU/L, Riakey (SHINJIN MEDICS, Goyang, Korea) 5.3 mIU/L, Brahms (Hennigsdorf, Germany) 5.7 mIU/L로 낮고 Siemens (Munich, Germany) 6.9 mIU/L, BeckmanRIA (Beckman Coulter, Brea, CA, USA) 7.4 mIU/L로 높게 측정되었다(Table 2). 또한 무증상 갑상선기능저하증을 경증, 중증으로 나누는 기준인 TSH 10 mIU/L도 측정 kit에 따라 다른 추정값을 갖는다(Table 2). 예를 들어 Abbott로 측정한 TSH 값이 10.0 mIU/L면 갑상선호르몬 치료를 적극적으로 고려하지만 Siemens나 Beckman-RIA로 측정한 결과가 10.0 mIU/L인 경우에는 투약 없이 일단 추이를 관찰하는 것도 가능하다. 즉 임상의는 갑상선기능 검사 결과를 해석할 때 사용 중인 TSH 측정 kit의 종류를 확인하고 검사실에서는 시약별로 적절한 참고 구간을 제공하는 것이 바람직하다. 이와 같은 측정 Kit별 차이는 기존의 참고 구간인 0.4-4.0 mIU/L에서도 마찬가지로 고려되어야 했던 사안이었으나 그동안 간과되다가 새로운 TSH 참고 구간 제시와 함께 재고되었다고 볼 수 있다.
2023 권고안에서는 TSH의 범위에 따라 무증상 갑상선기능저하증을 경증(TSH 6.8-10.0 mIU/L)과 중증(TSH > 10.0 mIU/L)으로 나누어 관리할 것을 제안하고 있다. 기존의 진료 지침들에서는 TSH 4.0-10.0 mIU/L [8] 또는 4.5-7.0 mIU/L와 7.0-10.0 mIU/L로 보다 세분하여 관리할 것을 권하기도 하였는데[9] 2023 권고안에서는 새로운 TSH 참고 구간에 근거하여 위와 같이 구분하고 있다. 경증과 중증의 구분이 필요한 이유는 TSH 증가 정도에 따라 현성 갑상선기능저하증으로 악화될 위험이 다르기 때문이다. 무증상 갑상선기능저하증이 현성으로 진행하는 데 관련된 임상 인자로는 첫 진단 시 중증(TSH > 10.0 mIU/L) 상태이거나 추적 관찰 시 TSH 지속적 상승, 여성, 만성 자가면역성 갑상선염을 시사하는 소견(갑상선 초음파에서 에코 저하 혹은 염증 소견이 있는 경우, 갑상선과산화효소[thyroid peroxidase, TPO] 항체 양성 등), 갑상선엽절제술의 과거력, 경부 방사선 치료 병력 등이 알려져 있다.
실제 임상에서 만나는 무증상 갑상선기능저하증의 90%는 경증에 해당하고 TSH 측정값 또한 여러 가지 요인(일중변동, 약제, 수면 등)에 따라 일시적으로 변화할 수 있어 충분한 간격으로 두고 재측정하였을 때 다시 정상으로 확인되는 경우도 드물지 않다. 2023 권고안에서 무증상 갑상선기능저하증이 진단되었을 때 투약 없이 2-3개월 후 TSH 재검사를 권하고 있는 이유도 여기에 있다. 즉 무증상 갑상선기능저하증 관리의 첫 단계에서는 일과성 또는 경증과 현성 갑상선기능저하증으로 진행할 위험이 높은 중증의 환자들을 구분하는 것이 중요하다.
무증상 갑상선기능저하증과 관련된 가장 흔하고 중요한 갑상선질환은 만성 자가면역성 갑상선염이다. 따라서 2023 권고안에서는 만성 자가면역성 갑상선염 여부 확인을 위한 TPO 항체 측정 검사를 권고하고 있다. TPO 항체 양성인 무증상 갑상선기능저하증은 음성에 비해 현성 갑상선기능저하 증으로의 이환율이 2배 이상인 것으로 알려져 있고 높은 요오드 섭취와 관련하여 만성 자가면역성 갑상선질환의 빈도가 높은 우리나라에서는 특히 중요하다.
일부 TPO 항체 음성인 환자에서는 갑상선글로불린 항체 측정도 도움이 될 수 있다. 또한 갑상선 초음파 소견(갑상선 실질 에코의 변화, 거친 표면, 전후 방향 길이의 증가 혹은 감소, 결절형 경계, 미세결절화 소견 등)은 자가면역성 갑상선염 조기 진단에 유용하며 그 밖에도 만성 갑상선질환의 가족력, 과거 갑상선기능 검사에서 경미한 이상이 반복되었다는 병력 등도 단서가 될 수 있다.
자가면역성 갑상선염의 진단이 확인된 경우라면 갑상선 호르몬 치료를 시작하지 않더라도 정기적인 갑상선기능 추적 검사가 필요하다. TSH 측정 간격은 TSH의 범위와 환자의 상태에 따라 다르지만 일반적으로 6개월 내 재측정을 권하며 중증의 경우에는 더 일찍 검사해 볼 수 있다. 그리고 저요오드 식이에 대한 교육이 필요하며 가임 연령의 여성에서는 계획 임신, 임신 시 적극적 치료의 중요성에 대해 당부하도록 한다.
무증상 갑상선기능저하증에서 갑상선호르몬 치료가 필요한 환자는 어떻게 결정할까? 적절한 치료 시작 시점은 언제일까? 이에 대한 해답을 제공할 수 있는 대단위 임상 연구는 아직 충분치 않지만 지금까지 가용한 연구 결과에 입각하여 결론부터 요약하면 첫째, 70세 이상의 고령에서는 경증 및 중증을 통틀어서 무증상 갑상선기능저하증의 치료 효과가 입증된 바 없으므로 치료를 고려하지 않는다. 둘째, 70세 미만 성인에서는 중증에서, 특히 기저 관상동맥질환 또는 심부전, 이상지질혈증과 동반되어 있는 경우에만 levothyroxine (LT4) 치료의 효과를 일부 기대할 수 있을 뿐 경증에서는 치료를 권할 만한 근거가 없다.
관련된 주요 대단위 연구 결과를 소개하면 다음과 같다. 먼저 고령에서 진행한 대규모 무작위 대조군 연구로 thyroid hormone replacement for untreated older adults with subclinical hypothyroidism (TRUST) 연구가 있다[10]. 총 737명의 65세 이상 무증상 갑상선기능저하증 환자들을 모집하여 갑상선호르몬 치료군(용량 중앙값 50 μg/day)과 위약군으로 나누고 심혈관질환, 인지기능, 사망률 등을 비교하였는데 두 군 간 차이가 없음을 확인하였다. 80세 이상 고령 무증상 갑상선기능저하증 환자 251명을 대상으로 한 대규모 무작위 대조군 연구인 institute for evidence based medicine in old age (IEMO)에서도 LT4 치료는 심혈관질환 및 전체 사망률을 감소시키지 않았다[11]. 이에 근거하여 고령에서 갑상선호르몬 치료는 권고하지 않는다. 아직까지 성인 연령 단독의 대단위 무작위 대조군 연구 결과는 충분하지 않지만 성인 연령 75,000명 이상을 대상으로 하여 무증상 갑상선기능저하증과 심혈관계 질환의 관련성을 확인한 thyroid studies collaboration 코호트 연구의 메타분석[12-15]에 따르면 심방세동, 심부전, 뇌졸중, 관상동맥질환, 심혈관질환에 의한 사망 및 전체 사망률의 증가와의 연관성은 입증하지 못하였다 하지만 TSH >10.0 mIU/L의 중증에서는 심부전, 관상동맥질환, 관상동맥질환으로 인한 사망의 위험도가 정상 대비 유의하게 상승함을 확인하였다. 이에 근거하여 성인 연령에서 심혈관질환과 연관된 경우에는 치료를 고려할 수 있는 것으로 제안하고 있다[1].
무증상 갑상선기능저하증에 치매나 우울증이 동반된 경우 갑상선호르몬 치료로 이들 질환이 호전될 수 있는지 여부에 대한 대규모 무작위 대조군 연구나 메타 분석은 아직 없지만 지금까지 확인된 소규모 연구 결과들은 치료 효과를 기대할 수 없다는 결론을 내리고 있다[16]. 따라서 치매나 우울증을 호전시킬 목적으로 무증상 갑상선기능저하증 환자에서 갑상선호르몬을 처방하는 것은 근거가 없다. 또 하나 애매한 상황은 ‘무증상’ 갑상선기능저하증의 ‘증상 개선’을 목적으로 갑상선호르몬을 처방하는 경우이다. 전신 무력감, 피로, 처지는 느낌 등 모호한 전신 증상들을 호소하는 상태에서 무증상 갑상선기능저하증이 진단되면 갑상선호르몬 처방으로 일련의 증상들이 호전될 것을 기대하기도 한다. 실제로 일부 과거의 진료지침에서는 환자의 증상 여부에 따라 치료 시작을 결정하도록 권하기도 하였으나[8,9,17] 지금까지의 연구 결과에서 갑상선호르몬 치료가 증상 개선에 효과가 있다는 증거를 찾지 못했다[10,11,18]. 따라서 2023 권고안에서는 증상 개선 목적의 갑상선호르몬 치료도 권하지 않고 있다.
그림 1은 무증상 갑상선기능저하증 환자의 관리에 대한 요약 도표이다. 무증상 갑상선기능저하증으로 진단된 경우 먼저 추적 검사를 실시하고 지속 또는 악화되는 경우에는 원인 질환, 특히 갑상선 수술 병력이나 만성 자가면역성 갑상선염 여부와 함께 동반 질환, 특히 심혈관계 질환을 확인하는 것이 중요하다. 진료지침의 흐름은 TSH 증가폭에 따라 경증과 중증으로 나누고 환자의 연령에 따라 고령과 성인으로 나누어 진행한다.
70세 이상 고령에서는 치료를 서두를 필요가 없다. 동반 질환이나 경증, 중증 구분과 상관없이 보수적으로 접근하는 것이 바람직하며 추적 검사를 통해 현성 갑상선기능저하증으로 진행하는지 확인하는 것으로 충분하다. 성인에서도 경증에서는 치료를 서두르지 않으며 중증, 즉 TSH 10.0 mIU/L 이상이면서 심혈관질환 및 심부전, 고지혈증이 동반되어 있을 때 치료를 고려할 수 있다. 하지만 과거 갑상선 절제술이나 방사선 치료 후 상태로 지속적인 갑상선호르몬 분비능 저하가 예상되는 경우, 추적 검사에서 TSH 증가폭이 커지는 등 현성 갑상선기능저하증으로 진행이 거의 확실시될 경우에는 치료를 고려한다. 이처럼 성인 연령에서도 제한적인 치료만이 권고되고 있으나 한 가지 예외 사항은 가임 연령 여성이다. 이와 관련된 내용은 2023 대한갑상선학회의 임신 중 및 산후 갑상선질환의 진단 및 치료 권고안 개정안에 상세하게 소개되어 있다[19]. 이에 따르면 지역적 특성을 고려한 임신 분기별 TSH의 정상 범위가 설정되어 있지 않다면 임신 1기 혈중 TSH의 정상 상한선은 기존의 4.0 mIU/L로 제안하고 있으며 갑상선기능 저하 상태로 진행할 위험성이 높은 경우 LT4 치료를 고려하도록 제시하고 있다. 갑상선호르몬은 태아의 뇌, 심장, 갑상선 등 중요한 기관의 형성 및 발달에 중요하다. 이들 기관의 발달이 시작되는 임신 1기에는 태아의 갑상선호르몬 합성이 시작되기 이전이므로 반드시 모체로부터 갑상선호르몬을 공급받아야 한다. 따라서 이 시기 모체의 경미한 갑상선기능 저하도 태아의 성장 발전에 부정적인 영향을 미칠 수 있다. 즉 임신을 고려 중이거나 시도하고 있는 가임 연령 여성에서는 무증상 갑상선기능저하증에 대한 보다 적극적인 치료와 감시가 요구된다.
2023 권고안은 국내 첫 무증상 갑상선기능저하증 진료지침으로 국내 연구 자료를 바탕으로 TSH 참고치의 새로운 상한선을 제시하여 한국형 진단 기준을 명시했다는 점에서 의미를 가진다. 또 이전의 몇몇 진료지침에서 환자의 증상에 따른 치료를 권했던 것과 달리 더 이상 환자의 모호한 증상에 연연하여 치료 방침을 고민하지 않아도 될 근거이기도 하다. 이제 TSH의 경미한 증가 소견만으로 갑상선호르몬을 처방하거나 모호한 증상을 호소한다는 이유로 불필요한 검사를 반복하는 등의 과잉 진료를 막을 수 있을 것으로 기대한다.
TSH 상승 소견은 주로 고령에서 발견되지만 고령의 환자에서 갑상선호르몬 처방은 극히 제한적임을 명시한 것도 이번 진료지침에서 반드시 주목해야 할 부분이다. 고령을 대상으로 한 일부 종단 연구 결과[20,21] 갑상선호르몬 투여군에서 TSH 억제와 함께 심방세동, 골다공증의 위험 증가 및 사망률에 미치는 영향 등이 보고된 바 있고 고령에서는 갑상선 호르몬의 체내 대사 속도가 현저히 지연된다는 점과[22] 노인에서 다약제 처방에 따르는 각종 문제점 등을 고려하였을 때 투약에 더욱 신중을 요한다. 즉 고령의 무증상 갑상선기능저하증은 처방없이 검사만 추적하는 보수적 접근이 원칙임을 반드시 기억할 필요가 있다.
하지만 고령이 아닌 경우, 특히 가임 연령 여성, 임신 중이거나 현성 갑상선기능저하증으로 진행이 뚜렷한 예에서는 적극적 갑상선호르몬 치료를 주저할 이유가 없다. 이번 권고안이 작성된 시점에는 젊은 연령의 성인을 대상으로 한 대단위 연구나 메타 분석 자료가 충분치 않았으므로 향후 관련 연구가 더해지고 임상적 유용성이 입증되면 치료 방침이 보완, 개선될 여지도 충분하다. 갑상선호르몬을 처방하지 않은 무증상 갑상선기능저하증에서 적절한 추적 검사 기간이나 갑상선호르몬 처방 시 치료 효과 평가의 기준, 적절한 치료 기간, 치료 종료 시점을 정하는 임상적 지표 등에 대한 연구는 아직 부족하다. 무증상 갑상선기능저하증의 관리에 대한 국내 연구 또한 충분하지 않으므로 향후 이와 관련된 대단위 임상 연구들이 이어진다면 보다 유용한 한국형 진료안을 개정 보완할 수 있을 것으로 기대한다.
REFERENCES
1. Chung HK, Ku EJ, Yoo WS, et al. 2023 Korean Thyroid Association management guidelines for patients with subclinical hypothyroidism. Int J Thyroidol 2023;16:32–50.

2. Kim WG, Kim WB, Woo G, et al. Thyroid stimulating hormone reference range and prevalence of thyroid dysfunction in the Korean population: Korea National Health and Nutrition Examination Survey 2013 to 2015. Endocrinol Metab (Seoul) 2017;32:106–114.


3. Park SY, Kim HI, Oh HK, et al. Age- and gender-specific reference intervals of TSH and free T4 in an iodine-replete area: data from Korean National Health and Nutrition Examination Survey IV (2013-2015). PLoS One 2018;13:e0190738.



4. Kim M, Kim TY, Kim SH, et al. Reference interval for thyrotropin in a ultrasonography screened Korean population. Korean J Intern Med 2015;30:335–344.



5. Choi HS, Park YJ, Kim HK, et al. Prevalence of subclinical hypothyroidism in two population based-cohort: Ansung and KLoSHA cohort in Korea. J Korean Thyroid Assoc 2010;3:32–40.
6. Jang YY, Kim CY, Hwang TY, Kim KD, Lee CH. Reference interval of serum thyroid hormones in healthy Korean adults. J Prev Med Public Health 2008;41:128–134.


7. Yoo WS, Kim S, Park YJ, et al. Comparison of thyroid-stimulating hormone results from eight different reagents and assay-specific Korean reference interval for subclinical hypothyroidism treatment. Int J Thyroidol 2023;16:166–174.

8. Garber JR, Cobin RH, Gharib H, et al. Clinical practice guidelines for hypothyroidism in adults: cosponsored by the American Association of Clinical Endocrinologists and the American Thyroid Association. Thyroid 2012;22:1200–1235.


10. Stott DJ, Rodondi N, Kearney PM, et al. Thyroid hormone therapy for older adults with subclinical hypothyroidism. N Engl J Med 2017;376:2534–2544.

11. Mooijaart SP, Du Puy RS, Stott DJ, et al. Association between levothyroxine treatment and thyroid-related symptoms among adults aged 80 years and older with subclinical hypothyroidism. JAMA 2019;322:1977–1986.



12. Rodondi N, den Elzen WP, Bauer DC, et al. Subclinical hypothyroidism and the risk of coronary heart disease and mortality. JAMA 2010;304:1365–1374.


13. Chaker L, Baumgartner C, den Elzen WP, et al. Subclinical hypothyroidism and the risk of stroke events and fatal stroke: an individual participant data analysis. J Clin Endocrinol Metab 2015;100:2181–2191.



14. Gencer B, Collet TH, Virgini V, et al. Subclinical thyroid dysfunction and the risk of heart failure events: an individual participant data analysis from 6 prospective cohorts. Circulation 2012;126:1040–1049.



15. Baumgartner C, da Costa BR, Collet TH, et al. Thyroid function within the normal range, subclinical hypothyroidism, and the risk of atrial fibrillation. Circulation 2017;136:2100–2116.



16. Feller M, Snel M, Moutzouri E, et al. Association of thyroid hormone therapy with quality of life and thyroid-related symptoms in patients with subclinical hypothyroidism: a systematic review and meta-analysis. JAMA 2018;320:1349–1359.



17. Pearce SH, Brabant G, Duntas LH, et al. 2013 ETA guideline: management of subclinical hypothyroidism. Eur Thyroid J 2013;2:215–228.



18. Razvi S, Ingoe L, Keeka G, Oates C, McMillan C, Weaver JU. The beneficial effect of L-thyroxine on cardiovascular risk factors, endothelial function, and quality of life in subclinical hypothyroidism: randomized, crossover trial. J Clin Endocrinol Metab 2007;92:1715–1723.

19. Yi KH, Ahn HY, Kim JH, et al. 2023 revised Korean Thyroid Association guidelines for the diagnosis and management of thyroid disease during pregnancy and postpartum. Int J Thyroidol 2023;16:51–88.

20. Mammen JS, McGready J, Oxman R, Chia CW, Ladenson PW, Simonsick EM. Thyroid hormone therapy and risk of thyrotoxicosis in community-resident older adults: findings from the baltimore longitudinal study of aging. Thyroid 2015;25:979–986.



Algorithm for levothyroxine treatment (LT4-Tx) in patients with subclinical hypothyroidism. TSH, thyroid stimulating hormone.
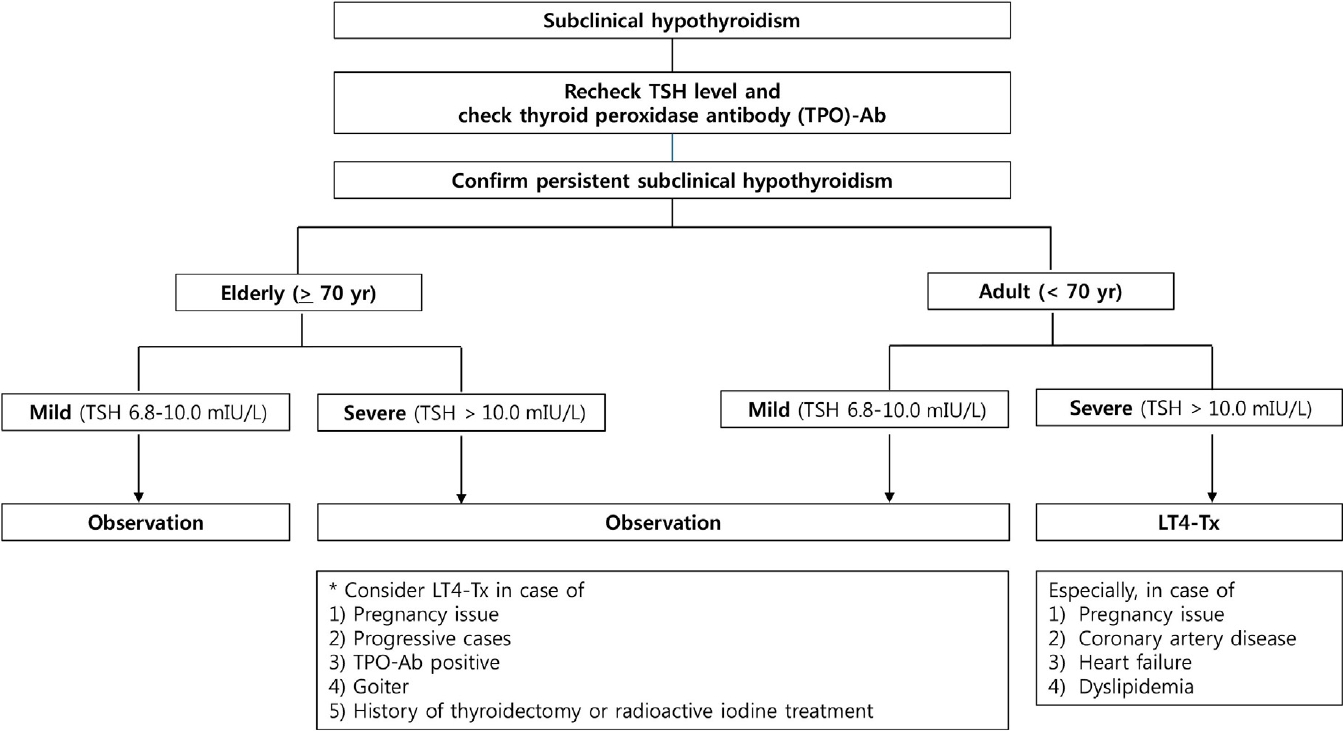
Figure 1.
Table 1.
Research findings on serum TSH concentrations in the normal healthy Korean population
| Study | Number of patients | TSH, mIU/La | Reference range, mIU/Lb |
|---|---|---|---|
| The 6th KNHANES (2017) [2,3] | 6,564 | 2.23 (IQR, 1.55-3.18) | 0.62-6.86 |
| AMC data from health Check-ups (2014) [4] | 5,778 | 2.38 (95% CI, 0.72-7.79) | 0.73-7.06 |
| Ansung cohort, KLoSHA (2010) [5] | Ansung, 3,399 | Ansung, 2.53 ± 3.31 | NA |
| KLoSHA, 940 | KLoSHA, 3.49 ± 7.12 | ||
| YNU-MC data from health check-ups (2008) [6] | 1,591 | 1.37 ± 1.95 | Men, 0.38-4.35 |
| Women, 0.35-6.42 |
Table 2.
Correlation coefficient and estimated TSH medical decision points (MDP) for each reagent compared with the Roche results
-
METRICS

-
- 1 Crossref
- 0 Scopus
- 18,009 View
- 744 Download



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



