악성흉수의 진단과 치료
Diagnosis and Management of Malignant Pleural Effusion
Article information
Trans Abstract
Malignant pleural effusions (MPEs) are an important clinical problem in patients with neoplastic disease. They can occur as the initial presentation of cancer, a delayed complication in patients with previously diagnosed malignancies, or the first manifestation of cancer recurrence after therapy. Common cancer types causing MPEs include lymphomas, mesotheliomas, and carcinomas of the breast, lung, and ovaries. However, almost all tumor types have been reported to cause MPEs. Regardless of the etiology, the median survival from clinical recognition is 4 months. New imaging modalities assist the evaluation of patients with a suspected MPE. However cytologic or tissue confirmation of malignant cells is necessary to establish a diagnosis. Management of an MPE remains palliative. Managements are directed toward removing pleural fluids and when appropriate, performing pleurodesis or initiating long-term drainage to prevent fluid reaccumulation. Talc pleurodesis is still the choice of treatment although concerns about its safety remain. Several factors such as performance status, expected survival, lung re-expansion following pleural fluid drainage and co-morbidities should be considered before the treatment. (Korean J Med 2011;81:167-173)
서 론
악성흉수는 흉수에서 악성 세포가 발견되는 것으로 악성종양 환자에서 이환율의 중요한 원인이다. 악성흉수는 악성종양의 초기에 발현될 수 있으며, 악성종양의 합병증 또는 치료 후 재발의 징후로 발현될 수 있다. 악성흉수의 발생률에 관한 연구는 미비하나, 한 사후 부검 연구에서는 악성종양으로 사망한 환자의 15%에서 악성흉수가 발견되었다[1].
악성종양 환자에서 흉수는 다양한 원인에 의하여 발생된다(Table 1) [2]. 일부 연구에서는 종양에 의한 혈관신생으로 혈관내피성장인자에 의한 혈관 투과성 증가와 액체의 혈관 누출에 의하여 흉수가 생성됨을 설명하고 있다[2,3]. 거의 모든 악성종양이 악성흉수의 원인이 될 수 있으나, 75% 이상의 악성흉수는 폐암, 유방암, 난소암, 림프종 등에 의하여 발생되며, 10% 내외에서는 원인 종양이 확인되지 않는 경우도 있다[2,4]. 악성흉수 환자의 예후는 불량하여 원인 종양 질환과 무관하게 중앙 생존 기간은 4개월로 알려져 있으며[5], 이와 같은 이유로 새로 개정된 폐암 TNM병기에서도 악성흉수는 M1a로 재분류되었다[6]. 악성흉수의 원인 질환에 따른 예후를 보면 폐암 환자가 가장 짧은 생존기간을 보였고 난소암 환자의 경우 생존기간이 길었으며, 원인이 불명확한 경우 중간 정도의 생존기간을 보였다[7,8]. 또한 Karnofsky performance scale 점수가 낮을수록, pH 7.20 미만, glucose 60 mg/dL 미만을 보일 경우 예후가 불량한 것으로 알려져 있다[5].
본 특집에서는 최근 문헌고찰을 통하여 악성흉수 환자의 진단 및 치료에 대하여 정리하고자 한다.
악성흉수의 진단
임상양상
악성흉수 환자의 50% 이상의 환자에서 발생하는 흔한 증상은 호흡곤란이다. 그 외에도 기저 악성종양에 의한 체중감소, 식욕부진, 권태감과 기침 등을 호소할 수 있으나, 증상이 없이 우연히 영상의학적 검사에서 발견되는 경우도 있다[2,9]. 악성 중피종의 경우는 60% 환자에서 지속적인 둔한 또는 간헐적인 국소 흉막통을 호소하며 육종 환자에서 발생한 악성흉수에서는 기흉이 동반되는 경우도 있다[9].
영상의학적 검사
대부분의 환자에서 흉부방사선 사진상 중등도 이상의 흉수 양(500-2,000 mL)을 보이며, 한 쪽 흉부 전체를 차지하는 대량 흉수의 원인질환은 대부분 악성종양인 경우가 흔하다[10]. 대량의 흉수는 “흉벽 측면에 흉수의 흔적이 있는 반달모양(meniscus) 징후, 반대측으로 종격동 이동, 횡격막의 역위” 등의 소견이 흉부방사선 사진에서 관찰될 수 있다[11].
흉부 초음파 검사는 적은 양의 흉수(5 mL)를 발견할 수 있어 흉강천자와 흉관삽입을 위한 가장 좋은 위치를 아는 데 도움을 준다[12]. 악성흉수를 시사하는 초음파 소견으로는 “고체형의 흉막 밀도, 불규칙하거나 명확치 않은 경계를 지닌 저에코의 흉막비후, 종양이 흉막에서 이웃 장기로 침범” 등이 있다[9].
흉부 전산화 단층촬영은 악성흉수가 진단 혹은 의심되는 환자에서 원발 종양을 발견하는 데에 유용한 정보를 제공하여 준다[11]. 악성흉수를 시사하는 소견으로는 “환상(circumferential) 흉막비후, 결절성 흉막비후, 1 cm 이상의 벽쪽 흉막비후, 원발 종양의 종격동 흉막 침범” 등이 있다[13].
흉부 자기공명영상은 악성 종양의 흉벽 또는 횡격막의 침범 여부를 확인하는데 전산화 단층촬영보다 더 좋은 영상을 제공하고, 소량의 흉수를 발견하는데 높은 민감도를 보이나, 폐 실질에 대한 영상은 흉부 전산화 단층촬영보다 효과적이지 못하여 이용이 제한적이다[9]. 양전자방출 단층촬영(PET)을 이용한 악성흉수 진단의 민감도는 93-100%, 음성 예상치 94-100%, 양성 예상치 63-94%로 알려져 있으며[14], 이는 흉수 세포학적 검사가 음성일 때 양전자방출 단층촬영의 음성 결과는 악성흉수를 배제하는데 유용하다고 한다.
흉수분석
흉부 영상의학기술의 발전에도 불구하고, 악성흉수를 확진하기 위해서는 흉수에서 세포학적 혹은 조직학적 검사에서 암세포를 확인하는 것이 필수적이다.
원인 감별을 위해 흉수천자가 필요하며 진단적 흉수검사에서는 세포수와 백분율 산정(total cell count with differential), 화학검사(total protein, lactate dehydrogenase, pH, glucose, albumin 등), 세포학적 검사 등이 필요하다. 대부분의 악성흉수는 삼출액이지만 3-10%에서는 저알부민증, 간경화, 또는 만성 심부전 등과 같은 동반된 질환이 있는 경우에 여출액으로 나타날 수도 있다[15,16]. 악성흉수를 시사하는 특징을 표 2에 정리하였다. 흉수에서 암 표지자(carcinoembryonic antigen, carbohydrate antigens 15-3, 19-9, 549, neuron-specific enolase, squamous cell carcinoma antigen, cytokeratin 19 fragments 등)의 유용성에 대한 연구들에서 암 표지자의 평균치가 악성흉수에서 높았지만 양성과 악성을 구분하는 임계수준 전후에서 중복되는 경향이 있어서 확진을 위해서는 침습적인 검사가 필요할 것이다[2,17,18].
흉수에서 세포학적 검사는 악성흉수를 진단하는 가장 쉬운 방법이나, 진단율은 원인 종양의 자연경과, 병변 분포에 따라 50-90%로 다양하며[19], 암세포의 감별을 위해 유전자 또는 면역조직화학 검사 등이 추가로 필요할 수 있다. 최근 진단율을 높이기 위하여 유전자 분석, DNA 메틸화, 염색체 분석 등을 이용한 연구가 활발히 진행되고 있다[2,9,20].
흉막 조직검사
악성흉수가 의심되지만 세포학적 검사가 음성일 때, 흉막 조직검사가 필요하다. 악성흉수를 진단하는 데 있어 세포학적 검사가 흉막 조직검사보다 더 민감하며, 흉막 조직검사의 진단율은 약 40-75%이다[20]. 영상 유도하에 시행되는 흉막 조직검사는 합병증을 줄일 수 있고 악성흉수를 진단함에 있어서 민감도(76-86%)와 특이도(100%)를 향상시킬 수 있으며, 5 mm의 두께의 적은 흉막액에서도 성공적으로 조직검사를 시행할 수 있는 장점이 있다[21].
경직성 또는 반경직성 흉강경을 이용한 내과적 흉강경 검사와 비디오 흉강경 수술을 이용한 조직검사에서는 더 많은 조직을 정확히 얻을 수 있으며, 민감도를 90-100%로 향상시킬 수 있다[9,22]. 비디오 흉강경 수술의 높은 진단율에도 불구하고, 비악성 흉수에 대한 확진에 있어서는 덜 효과적이며, 침습적이고 전신마취가 필요하다는 단점이 있다. 따라서 삼출액 흉수가 있는 환자에서 임상적으로 악성흉수가 의심되는 경우 또는 한 달 이상 지속된 증상, 열이 없는 경우, 혈성 흉수, 악성을 암시하는 흉부 전산화 단층촬영 소견이 있는 경우 비디오 흉강경 검사를 고려하도록 추천하고 있다[23].
기관지내시경
원인 미상의 흉수에서 기관지내시경 검사는 진단율이 낮아서 기본 검사로 추천되지 않는다. 객혈, 무기폐, 반대쪽으로 종격동 이동이 없는 대량 흉수의 경우처럼 기관지내 병변이 의심되는 경우에 기관지내시경을 시행한다[20].
악성흉수의 치료
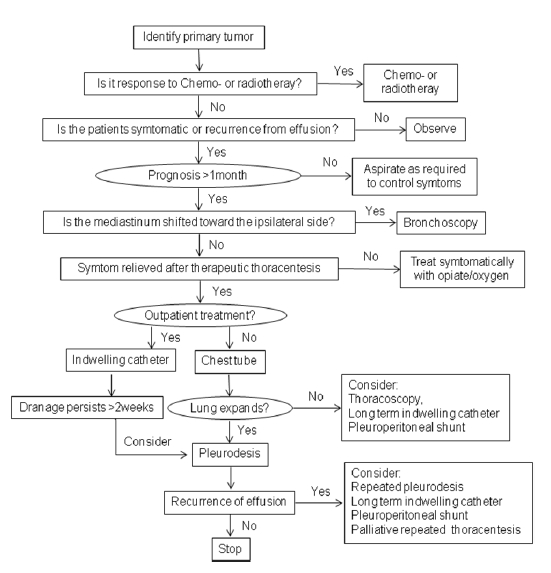
악성흉수에 대한 보존적 치료는 암 환자의 생존율을 향상시키지 못하기 때문에 원인이 되는 종양에 대한 치료가 중요하다. 흉수에 의한 호흡곤란과 같은 증상, 전반적인 건강상태, 수행능력, 기대수명 등을 종합적으로 고려하여 악성흉수에 대한 고식적 치료를 결정한다. 치료의 가장 중요한 목적은 흉수 제거와 재축적 방지를 통하여 호흡곤란 등의 증상을 완화시키는 것이다. 따라서 무증상이면서 원인이 되는 악성종양에 대한 치료가 가능한 환자에서는 경과관찰을 추천한다(Table 3, Fig. 1) [4].
치료적 흉강천자
호흡곤란과 같은 증상이 있는 악성흉수 환자에서 흉수 제거 후 호흡곤란의 개선 정도를 평가해야 한다. 많은 양의 흉강천자에도 호흡곤란과 같은 증상의 호전이 없다면, 림프관성 암종, 혈전증, 무기폐, 심장질환 등 호흡곤란을 유발할 수 있는 다른 원인을 생각해야 한다[9,19].
일반적으로 흉강천자 후 호흡곤란은 호전될 수 있으나, 98-100%의 환자는 30일 이내에 흉수가 재축적되어 증상이 재발하게 된다. 이 경우 반복적인 흉강천자를 하면 유착, 소방형성, 감염 등의 위험성이 증가된다[24]. 따라서 치료 목적의 반복적 흉강천자는 흉수가 서서히 재축적되는 경우, 전신적 치료에 악성종양이 반응하는 경우, 1-3개월 미만의 기대수명이 예상되는 경우, 흉막유착술과 같은 다른 방법으로 흉수를 조절할 수 없는 경우 등에서 고려해야 한다[9,20,22].
화학 흉막유착술
화학 흉막유착술은 화학물질을 이용하여 흉막에 염증, 섬유소 침착에 의한 유착을 초래하여 흉수의 재축적을 방지하여 호흡곤란을 호전시키고자 하는 방법이다[2,19]. 이런 흉막유착술은 흉수에 의한 호흡곤란 등 호흡기 증상이 있고, 2-3개월 이상의 기대수명, 전신항암치료에 반응하지 않는 악성흉수, 치료적 흉강천자 후 폐 확장 확인된 환자에서 시행한다[9].
흉막유착술에 사용되는 약제인 경화제는 흉관 카테터 또는 흉강경 등을 이용하여 주입할 수 있으며, 경화제에 따라서 매우 다양한 치료 효율을 보인다(Table 4) [9]. 경화제의 안전성과 효과에 대한 연구들이 시행되었으나, 아직까지 적절하게 비교된 데이터가 부족하여 가장 이상적인 약제의 선택이라는 측면에서 논쟁의 소지가 있지만 talc가 악성흉수를 방지하는 데 가장 효과적인 약제로 알려져 있다[25,26].
일반적으로 talc 사용에 따른 부작용은 호흡곤란, 열, 흉통, 폐렴, 부정맥, 무기폐, 급성호흡부전 등이 알려져 있으며, 가장 치명적인 급성호흡부전의 발생률은 약 1-9%로 보고된다[19,27]. 이런 급성호흡부전의 합병증은 talc 입자의 크기가 클수록 드물게 발생하는 것으로 알려져 있다[27]. 따라서, talc 흉막유착술에 의한 저산소증 등의 합병증을 줄이기 위해서 입자의 크기가 큰 것을 사용하도록 추천하고 있다[4]. 일부 세균의 생산물과 사이토카인 등의 치료 성적이 보고되고 있으나, 아직까지는 널리 사용되기에는 제한적이다(Table 4) [2,9,20].
흉막유착술 시행 시 영국흉부학회(British Thoracic Society)에서는 다음과 같은 권고를 하고 있다[4]. 첫째, 악성흉수를 배액 또는 흉막유착술을 위하여 소구경(10-14Fr) 카테터를 사용 한다. 둘째, 리도카인(3 mg/kg; 최대용량 250 mg)은 경화제 주입 전에만 사용한다. 셋째, 시술 전 투약은 흉막유착술과 관련된 통증과 불안을 완화하기 위해서 고려한다. 넷째, 흉막유착술 약제 주입 후 환자를 여러 방향으로 회전 시킬 필요는 없다. 다섯째, 흉막유착술 약제 주입 후 1시간 동안 카테터를 잠근다. 여섯째, 흉막유착술 약재 주입 후 하루에 250 mL 이상의 배액이 없다면 24-48시간 내에 카테터를 제거한다.
결 론
악성흉수는 거의 모든 악성종양에서 발생할 수 있는 흔히 접하는 임상적 문제이다. 새로운 영상의학적 기법의 소개로 진단의 정확도가 향상되었으나, 확진을 위해서는 악성세포를 세포학적, 조직학적 검사를 통하여 확인하는 것이 필요하다. 환자의 전신상태와 원인 질환에 대한 평가 후 악성흉수에 대한 적절한 치료 방법을 선택하는 것이 중요하겠다(Table 3, Fig. 1). 최근 분자생물학의 발전과 조직학적 진단기술의 발전으로 기존 세포학적, 조직학적 검사의 진단율이 향상되고 있다. 향후 신속하고, 효과적인 진단 방법과 안전하고 효율적인 경화제의 개발이 필요할 것이다. 악성흉수 진단 후에는 보다 적극적인 치료적 중재를 통하여 환자 삶의 질을 향상시킬 수 있도록 노력하여야 하겠다.