이뇨제 사용의 원칙과 실제
Principles and Practice of Diuretic Therapy
Article information
Trans Abstract
Diuretic drugs are the most commonly used agents to control edema or volume overload. However, the clinical use of diuretics is not confined to edema control. Recently, diuretics have been revisited for the management of various diseases, including hypertension and congestive heart failure. Diuretics are classified mainly by their sites of action in the renal tubules, and have unique characteristics and adverse effects according to their mechanisms of action. To use diuretics adequately, it is very important to understand their characteristics. (Korean J Med 2011;80:8-14)
서 론
이뇨제는 임상에서 가장 흔히 처방되는 약제 중의 하나로 서 신장의 요세관에서 나트륨의 흡수를 저해함으로써 소변으로 수분 및 나트륨 배설을 촉진하는 약제이다. 그러나 이뇨제는 부종의 조절뿐 아니라 심부전, 간경변, 전해질 이상 및 고혈압 치료 등 다양한 질환에서 사용되고 있다. 또한, 이뇨제의 종류에 따른 작용기전과 부작용이 다르므로 이에 대한 정확한 이해를 바탕으로 한 적절한 사용은 효율적인 치료와 부작용의 최소화를 위하여 매우 중요하다. 본문에서는 신장의 나트륨 배설 조절 기전과 각 이뇨제의 작용기전을 바탕으로 한 선택적인 임상적 적용에 대하여 고찰하고자 한다.
신장 요세관에서의 나트륨 조절
체내 나트륨 균형에서 신장은 가장 중요한 역할을 담당하며, 사구체를 통하여 여과된 나트륨을 신장 요세관의 분절에 따라 특이적으로 분화되어 있는 물질전달체(transporter)를 통하여 재흡수함으로써 신체의 나트륨 배설을 조절한다. 성인은 일반적인 식사를 통하여 하루 150~300 mEq의 나트륨을 섭취하는데, 사구체 여과액이 하루 180 L임을 감안하면 여과된 나트륨의 99% 이상은 신장에서 재흡수되고 약 1%만이 소변을 통하여 배설된다[1]. 신장 요세관의 나트륨 재흡수는 근위세관(proximal tubules, PT), 굵은 오름 부분(thick ascending limb, TAL), 원위세관(distal tubules, DT) 그리고 집합관(collecting duct, CD)에서 일어나며, 각 부위는 고유한 기전에 의하여 나트륨 재흡수에 관여한다[1].
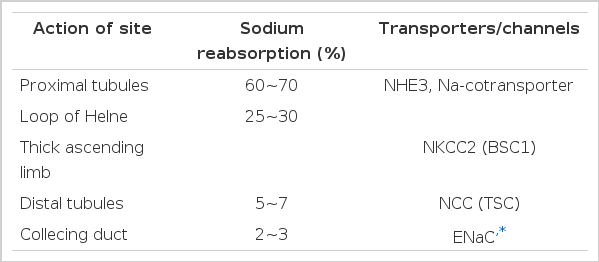
사구체로 여과된 나트륨의 약 60~70%는 근위세관에서 나트륨-수소이온(NHE3), 나트륨-포도당(Na-glucose cotransporter), 나트륨-인산 (NaPi-2) 등 다양한 나트륨-공동물질전달체를 통하여 등장성(isotonic)으로 재흡수된다. 굵은 오름 부분에서는 요세관 내강세포막(luminal membrane)에 존재하는 NKCC2(Na-K-2Cl cotransporter; bumetanide-sensitive sodium channel, BSC1)라는 물질전달체와 기저외막(basolateral membrane)에 존재하는 Na-K-ATPase를 통하여 여과된 나트륨의 약 25~30%가 체내로 재흡수된다. NKCC2는 가장 강력한 이뇨제인 고리 이뇨제(loop diuretics)의 작용 부위이다. 원위세관에서는 thiazide계 이뇨제가 작용하는 NCC (Na-Cl cotransporterl)를 통하여 5~7%의 나트륨 재흡수가 일어난다. 집합관의 주세포(principal cells)에서는 알도스테론에 의하여 조절되고 amiloride계통 이뇨제의 작용 부위인 ENaC (epithelial sodium channel)라는 물질전달체를 통하여 여과된 나트륨 2~3%의 재흡수가 일어난다(표 1)[2].
신장의 나트륨 배설은 신경계 및 여러 호르몬에 의하여 조절되는데 레닌-안지오텐신-알도스테론, 항이뇨호르몬, 인슐린, 베타 아드레날린 수용체 등은 나트륨 재흡수를 촉진시키는 한편, 알파 아드레날린 수용체, 도파민, PGE2, 심방나트륨이뇨인자(ANP) 등은 나트륨 배설을 촉진시킨다[2]. 따라서 이러한 호르몬 균형에 영향을 미치는 질환이나 약물 등은 나트륨 균형의 변화 및 이뇨제의 효과에 영향을 미칠 수 있다. 대표적인 예로 임상에서 많이 사용되는 비스테로이드성 진통제(NSAIDs)는 PGE2의 합성을 억제함으로써 나트륨 배설을 저해하여 부종을 유발할 수 있으며, 이뇨제와 병용하는 경우 이뇨 효과를 저해한다.
이뇨제의 종류 및 작용기전
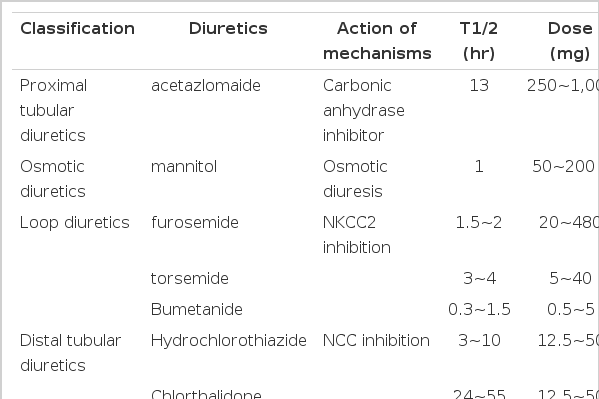
이뇨제는 신장에서 나트륨 재흡수를 막거나 배설을 촉진함으로써 요량을 증가시키는 약제로서 일반적으로 이뇨제가 작용하는 신장 부위에 따라 분류된다(그림 1). 각 약제의 종류에 따른 작용기전 및 주된 임상이용은 다음과 같으며, 각 이뇨제의 일반적인 약물학적 특성 및 투여법은 표 2에 정리되어 있다.
1. 근위세관 작용 이뇨제(Proximal tubular diuretics)
근위세관은 가장 많은 양의 나트륨 재흡수가 일어나는 부위이지만 세포횡단(transcellular)뿐 아니라 세포주위간(paracellular) 경로를 통하여 여러 종류의 물질전달체가 관여하며, 이 부위에서 나트륨 재흡수를 막아도 보다 원위부에서 나트륨 재흡수가 증가되기 때문에 근위세관에 작용하는 이뇨제의 이뇨효과는 미약하다. 근위세관에 작용하는 대표적인 이뇨제로는 탄산탈수효소 억제제(carbonic anhydrase inhibitor)인 acetazolamide가 있다. 탄산탈수효소는 사구체에서 여과된 중탄산염의 재흡수에서 중요한 역할을 하는데, 중탄산염의 재흡수와 동반되어 나트륨의 재흡수가 일어난다. 즉, acetazolamide는 중탄산염의 재흡수에 동반된 나트륨 재흡수를 저해하는데, 그 이뇨효과가 매우 미약하므로 체액과다나 부종 조절의 일차적 선택 약제로 사용되지는 않는다. Acetazolamide는 대사성 산증을 유발하므로 대사성 알칼리증의 치료 혹은 대사성 알칼리증이 호흡성 산증을 악화시킬 수 있는 만성폐쇄폐질환(COPD) 환자에 동반된 부종의 치료에 선택적으로 사용된다. 그 외에도 녹내장 환자에서 안압 감소 및 고산병의 예방의 목적으로 이용된다[3].
2. 삼투압 이뇨제(Osmotic diuretics)
삼투압 이뇨제는 일반적으로 사구체를 통하여 자유롭게 여과되지만 요세관에서 재흡수되지 않는 물질로서 이때 형성된 삼투압 농도를 이용하여 이뇨를 유발하는 약제이다. 가장 많이 사용되는 약제로 mannitol이 있다. Mannitol은 사구체를 통하여 자유롭게 여과되기 때문에 사구체여과율에 영향을 받으며 진행된 신부전에서는 반감기가 36시간까지 지연될 수 있으므로 사구체 여과율 감소에 따른 투여간격의 조정이 필요하다[3]. Mannitol은 임상에서 급성 콩팥병(acute kidney injury)의 예방 목적으로 사용되었으나 현재 이에 대한 임상적인 증거가 불충분하므로 추천되지 않는다. 그러나 급성 간질환에 동반된 뇌부종 및 급성 뇌압 상승의 조절에는 효과가 있으므로 이를 위한 목적으로 사용되고 있다[3,4]. 그러나 mannitol은 다뇨를 유발하여 다량의 수분손실을 유발하기 때문에 고나트륨혈증, 혈량저하증 및 전해질 이상을 흔히 동반하므로 적절한 수액대치 요법을 필요로 한다.
3. 고리 이뇨제(Loop diuretics)
굵은 오름 부분(thick ascending limb; TAL)에서는 여과된 나트륨의 25~30% 가량의 재흡수가 일어나기 때문에 고리 이뇨제는 가장 강력한 이뇨효과를 가지며, 임상에서 현재 가장 많이 사용되는 이뇨제이다. 고리 이뇨제는 NKCC2 (Na-K-2Cl cotransporter) 작용하여 나트륨 재흡수를 막는데, 종류로는 bumetanide, furosemide, torsemide, ethacrynic acid 등이 있으며, 이 중 furosemide와 torsemide가 가장 널리 사용되는 약제이다.
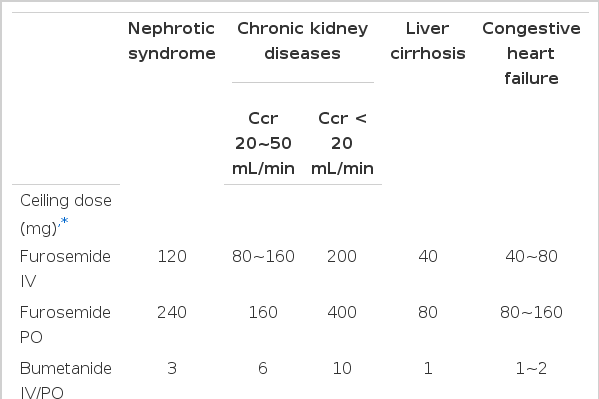
Furosemide는 혈장에서 90% 이상 단백과 결합된 상태로 존재하기 때문에 사구체를 통하여 여과되지 못하고 근위세관의 유기음이온 수용체(organic anion transporter, OAT)를 통하여 내강으로 분비된 후 free form 형태로서 고리관에서 작용한다. 신장에서 furosemide의 40~50%은 glucuronic acid와 결합하므로 50%만이 free form의 형태로 내강 내에 배설되는 한편, bumetanide나 torsemide는 주로 간에서 대사된다[5,6]. Furosemide는 생체이용률(bioavailability)이 40~50% 정도이므로 경구 투여할 때는 정주 투여 시에 비하여 2배의 용량이 필요하지만, torsemide나 bumetanide는 경구와 정주 투여량이 동일하다. Furosemide의 이뇨작용은 요세관 내강 내 free form에 의하여 일어나는데 내강 내 furosemide의 농도가 일정 수준에 도달하면 더 이상 이뇨효과가 강화되지 않는 역치에 도달하게 되며 이때 필요한 이뇨제의 용량을 최고용량(ceiling dose)이라고 한다(표 3)[1,7,8]. 특히 furosemide은 반감기가 1시간 정도로 짧기 때문에 반감기를 지나게 되면 이뇨효과가 감소한다. 따라서 원하는 이뇨 효과를 얻는 용량에 도달하게 되면, 일회 투여용량을 올리는 것보다 투여빈도를 늘리거나 지속적인 정주 요법을 사용하는 것이 보다 적은 투여용량으로 효율적인 치료가 가능하다. Furosemide는 대부분 하루 1회보다는 2회 이상 투여하는 것이 효율적이며, torsemide는 반감기가 3~4시간 정도 유지되기 때문에 하루 1회 투여가 가능하다[5,6]. 또한 이뇨제 투여시기는 1회 투여의 경우 아침에 투여하고, 2회 이상 투여하는 경우 저녁에 투여된 이뇨제로 인한 야간뇨가 수면을 방해할 수 있기 때문에 가능한 오후 4~5시 이후에는 투여하지 않는 것이 바람직하다.
고리 이뇨제는 가장 강력한 이뇨작용을 가지며, 신기능이 저하된 상태에서도 이뇨효과를 발휘하므로 만성콩팥병, 신증후군 등 대부분의 신장 질환과 사구체여과율이 50 mL/min 이하로 감소된 환자에서 선택적인 이뇨제로 사용된다. 고리 이뇨제는 사구체여과율의 감소되거나 신증후군 환자에서는 요세관 내강에 도달하는 양이 감소하고, 간경변이나 울혈성 심부전의 경우 이뇨제에 대한 요세관의 반응도가 감소하기 때문에 동일한 이뇨효과를 얻기 위해서는 정상 상태보다 고용량을 필요로 한다. 굵은 오름 부분은 Mg2+, Ca2+의 재흡수가 일어나는 부위이므로 고리 이뇨제는 대사성 알칼리증, 저칼륨혈증, 마그네슘 및 칼슘의 소실을 유발하여 이와 연관된 합병증을 유발할 수 있다. 이밖에 고리 이뇨제는 내이독성(ototoxicity)이 있으므로 aminoglycoside 같은 내이독성이 있는 약제와 함께 사용하는 경우 특히 주의를 요하며, 고용량을 bolus로 정주하는 경우 독성 위험도가 증가하기 때문에 160~200 mg을 투여하는 경우 20~30분 정도에 걸쳐서 서서히 주입하여야 한다[1,3,5].
고리 이뇨제는 소변 내 칼슘 배설을 증가시키기 때문에 악성종양의 뼈전이 등에 의한 고칼슘혈증의 치료제로 사용되며, 굵은 오름 부분에서 나트륨 재흡수 억제는 신장 수질부의 삼투질 물질의 축적을 막아서 요농축능의 저하를 유발하며 자유수분 배설률(free water clearance)을 증가시키기 때문에 SIADH (syndrome of inadequate ADH secretion)에 의한 저나트륨혈증에서 치료제로 사용될 수 있다[3].
4. 원위세관 이뇨제(Distal tubular diuretics)
원위세관에서는 NCC (Na-Cl-cotransporter)를 통하여 5~7%의 나트륨 재흡수가 일어나며, 이 부위에 작용하는 대표적인 이뇨제는 thiazide계열의 이뇨제이다. Thiazide 계열의 약제로는 hydrochlorothiazide가 가장 많이 사용되며 이외에도 indapamide, chlorothiazide, chlorothalidon 등이 있으며, 비 thiazide 계통으로는 metolazone이 있다. 원위세관 이뇨제는 중등도의 이뇨효과를 가지며 일반적으로 사구체여과율이 50 mL/min 이하인 경우 단독으로는 이뇨 효과를 가지지 못하지만, metolazone은 중등도의 신기능이 저하된 환자에서도 단독사용이 가능하다. Thiazide 계열의 이뇨제는 부종의 조절뿐 아니라 특발성 고혈압의 치료 및 울혈성 심부전 등 심혈관계 질환에서 널리 사용된다[9,10]. 원위세관 이뇨제의 부작용으로는 대사성 알칼리증, 저칼륨혈증 및 저나트륨혈증 등 전해질 이상 그리고 당불내성, 고지질혈증 등 대사성 이상을 들 수 있다. 한편, 원위세관 이뇨제는 칼슘 배설을 저하시키기 때문에 특발성 고칼슘뇨증이나 재발성 신결석의 치료 및 신성요붕증의 보조적인 치료제로 사용된다[3].
5. 원위부 칼륨보존 이뇨제(Distal potassium sparing diuretics)
집합관에 작용하는 이뇨제는 알도스테론 억제제인 spironolactone과 알도스테론에 의해 조절받는 나트륨 물질전달체인 ENaC (Epithelial sodim channel)에 작용하는 amiloride, triamterene 등이 있다. 이들 이뇨제는 알도스테론의 작용을 억제하므로 고리 이뇨제나 원위세관 이뇨제와는 달리 요 칼륨배설을 감소시키기 때문에 칼륨보존 이뇨제라고도 불린다. 집합관 이뇨제는 이 부위에서 여과된 나트륨의 2~3%만이 재흡수되기 때문에 이뇨 효과가 크지는 않으나, 알도스테론의 활성화가 부종이나 복수를 유발하는 간경변이나 ENaC의 비정상적인 활성화에 의한 Liddle 증후군의 치료에서 일차적 선택 약제로 사용된다[5].
집합관 이뇨제는 요 칼륨배설을 증가시키는 고리 이뇨제나 원위세관 이뇨제와 병용하는 경우 저칼륨혈증 위험을 감소시키는 반면, 요 칼륨배설을 감소시키는 안지오텐신 효소길항제, 베타 차단제 등과 함께 사용할 때는 고칼륨혈증의 발생 위험도를 증가시키므로 주의를 요한다[3]. 또한 알도스테론이 칼륨뿐 아니라 수소이온의 배설도 촉진시키기 때문에 이들 이뇨제는 대사성 산증을 유발할 수 있다.
각 질환에서 이뇨제 사용의 실제
이뇨제는 부종 조절을 위하여 가장 널리 사용되지만, 고혈압, 전해질 및 산염기 장애의 치료 등 다른 질환에서도 흔히 사용된다. 이뇨제의 선택과 투여방법은 원인 질환이나 신기능의 정도, 그 외 특수한 목적에 따라 선택적으로 이용되는데 신증후군이나 만성콩팥병, 핍뇨 등 대부분의 신질환에서는 고리 이뇨제가[5-7], 고혈압이나 울혈성 심부전에서는 thiazide 계열의 약제가 선택적으로 사용된다[9,10]. 각 질환에서 이뇨제 사용의 일반적인 원칙은 다음과 같다.
1. 신증후군(Nephrotic syndrome)
신증후군에서는 고리 이뇨제가 일차적 선택 약제로 사용된다. 그러나 가장 많이 사용되는 furosemide는 90% 이상이 알부민과 결합한 후 근위세관의 유기음이온수용체(organic anion transporter, OAT)를 통하여 요세관 내강으로 분비되므로, 신증후군에 동반되는 저알부민혈증은 근위세관으로의 효율적인 약물전달을 어렵게 하고, 단백뇨에 의하여 furosemide가 내강 내에서 알부민과 결합함으로써 free form이 감소하기 때문에 사구체여과율이 정상이라도 일반적인 경우보다 고용량을 필요로 한다[5-7]. 부종 조절을 위한 알부민 투여는 일반적으로 추천되지 않으나 고용량의 고리 이뇨제로도 적절한 이뇨효과를 얻지 못하거나 저알부민혈증에 의한 체액결핍이 동반되는 경우 알부민과 이뇨제를 동시에 투여하거나 알부민과 이뇨제를 1시간 정도 미리 혼합한 후 정주할 수 있다. 또한, 만성적으로 사용하여 초기 이뇨 효과가 지속되지 않는 경우는 thiazide 계열이나 amiloride 등 원위부에 작용하는 이뇨제와 병용 투여할 수 있다.
2. 만성콩팥병(Chronic kidney disease)
사구체여과율이 50 mL/min 이하로 감소하면 대부분의 이뇨제는 단독으로 충분한 이뇨효과를 나타내지 못하기 때문에 고리 이뇨제가 선택적으로 사용된다. 사구체여과율의 정도에 따라 투여용량의 조절이 필요하며 일반적으로 사구체여과율의 감소가 심할수록 고용량이 필요하다. 특히, furosemide의 경우 심한 신부전에서는 투여량의 10~15%만이 요세관 내강 내에 분비되므로 이뇨효과가 감소하지만, 혈장 농도는 상승하므로 ototoxicity 같은 부작용의 위험도는 증가하므로 이에 대한 주의를 요한다[3,6,7]. 만성콩팥병에서 고리 이뇨제는 체액과다에 동반된 고혈압의 치료, 고칼륨혈증이나 대사성 알칼리증의 교정을 위한 목적으로도 사용된다.
원위세관 이뇨제 중 metolazone은 중등도 신부전 환자에서도 단독으로 효과적인 이뇨효과를 가지므로 이들 환자에서 고리 이뇨제와 병용요법으로 사용하기에 적합하다.
3. 고혈압(Hypertension) 및 울혈성 심부전(Congestive heart failure)
특발성 고혈압에서 thiazide 계열의 이뇨제는 일차적 선택 약제로 오래 전부터 사용되어 왔다. Thiazide 이뇨제에 의한 혈압 강하효과는 수축성 혈압 10~15 mmHg, 확장기 혈압 5~10 mmHg 정도를 감소시켜서 보다 강력한 이뇨효과를 가지는 고리 이뇨제에 비하여 월등한 것으로 알려져 있다. 이들 이뇨제의 혈압강하 효과는 초기에는 세포외액의 감소를 통하여 일어나지만 지속적으로 사용하는 경우 세포외액은 정상으로 되는 반면 말초혈관 저항성을 감소시켜서 일어나는 것으로 알려져 있으며, hydrochlorothiazide의 경우 하루 12.5~25 mg을 하루 1회 투여한다[9]. 또한 안지오텐신 전환 효소 길항제나 안지오텐신 수용체 길항제와 병용하는 경우 이들 약제의 혈압강하효과를 증강하고 고칼륨혈증의 위험도를 감소시키므로 임상에서 흔히 이들 약제와 병용하여 사용되고 있다. 특히 2002년에 보고된 ALLHAT (Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial)연구에 의하면 thiazide 계열인 chlorothalidne이 다른 고혈압 약제에 비하여 울혈성 심부전의 위험도를 감소시킴이 보고되어서, 현재는 특이 질환이 없는 특발성 고혈압의 경우 이들 이뇨제가 일차적 선택제로 추천되고 있다[9,11].
그 외에 원인이 발견된 이차성 고혈압의 경우 이뇨제가 치료제로 사용될 수 있다. 사구체여과율 감소에 의한 체액과다가 고혈압을 유발한 경우 고리 이뇨제가, 일차성 알도스테론증이나 Liddle 증후군에서 spironolactone이나 amiloride 같은 집합관에 작용하는 약제가 선택적으로 사용된다[9].
울혈성 심부전에서는 신기능이 정상인 경우는 thiazide 계열의 이뇨제를 사구체여과율이 50 mL/min 이하로 감소된 중등도 이상의 신부전이 동반된 경우는 고리 이뇨제가 추천된다[3,5]. 심부전 환자에서 digoxin 약제를 함께 사용하는 경우 이뇨제에 의한 저칼륨혈증이 digoxin의 독성 위험을 증가시키므로 주의를 요한다.
4. 간경변(Liver cirrhosis)
진행된 간경변 환자에서 복수 혹은 말초부종은 혈관확장에 의한 이차성 알도스테론증이 주요 기전으로 작용하기 때문에 알도스테론 수용체 길항제인 spironolactone이 일차적 선택 약제로 사용된다. Spironolactone은 하루 50 mg 1회 투여로 시작하여 점차적으로 증량하여 하루 400 mg까지 증량할 수 있다[5]. 다만, spiromolactone은 약물 작용 시작 시간이 24~48시간이므로 급성 부종 조절에는 적합하지 않으며, 이뇨 효과의 판단여부는 약물투여 후 최소 1~2일을 기다려야 한다[3,5]. 고용량의 spironolactone 단독으로 충분한 이뇨효과를 얻을 수 없으면 thiazide를 추가하고, 필요 시 고리 이뇨제를 병용할 수 있다. Thiazide나 고리 이뇨제에 의한 대사성 알칼리증, 저칼륨혈증은 간경변 환자에서 간성혼수를 악화시킬 수 있으므로 주의를 요한다.
5. 기타 질환
고리 이뇨제는 칼슘배설을 증가시키므로 고칼슘혈증의 치료제로 사용되며, thiazide 계열의 약제는 반대로 요중 칼슘배설을 감소시키기 때문에 특발성 고칼슘혈뇨나 이로 인한 신결석 환자에서 치료제로 사용할 수 있다[3].
이뇨제 저항성 및 해결점
이뇨제를 사용할 때 최고 용량(ceiling dose)으로 투여하여도 이뇨효과가 충분하지 못하거나(이뇨제 저항성: diuretics resistance) 처음 이뇨제에 반응한 후에 점진적으로 이뇨효과가 감소(이뇨제 내성; diuretics tolerance)하는 현상을 흔히 접하게 된다.
이뇨제 관성은 이뇨제 사용에 따른 생리적인 적응현상에 의한 것으로, 이뇨제에 의하여 이뇨가 일어나면 체액감소와 원위부 요세관에 도달하는 나트륨 배설이 증가하므로 교감신경계와 레닌-안지오텐신-알도스테론 등 호르몬-신경계의 활성화가 일어나고, 장기적으로 투여하는 경우에는 원위세관이나 집합관 세포의 비대로 인하여 원위부 신장에서 다시 나트륨 재흡수가 증가함으로 인하여 발생한다. 이를 극복하기 위해서는 이뇨 후 나트륨 저류를 막기 위하여 저염식이를 지속적으로 유지하는 것과 고리 이뇨제 사용 시에 원위세관이나 집합관 이뇨제 등 원위부에 작용하는 이뇨제의 병용이 필요하다[3,5,7].
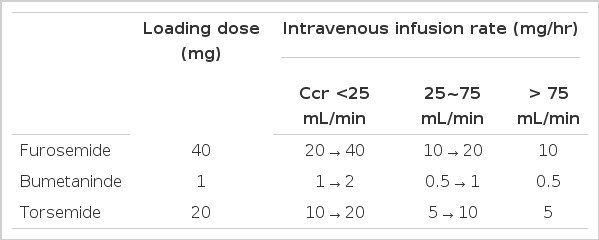
이뇨제 저항성은 최고 용량의 이뇨제를 사용하여도 원하는 이뇨효과를 얻지 못하는 경우로 부종의 오진, 과다한 나트륨 섭취, 환자의 비순응도(noncompliance), 부적절한 이뇨제 투여, 나트륨 배설을 저해하는 비스테로이드성 진통제 같은 약물 병용, 저알부민혈증, 다량의 단백뇨의 존재, 사구체여과율의 저하, 저혈압 등 여러 원인에 의하여 발생한다[3,5,7]. 이를 극복하기 위해서는 저염식 유지, 이뇨제 작용을 저해하는 약물 복용의 중지 등 원인적 접근이 필요하며, 고리 이뇨제의 경우 투여간격을 조절하거나 지속적인 정주 요법을 시도할 수 있으며, 작용기전이 다른 이뇨제와 병용요법을 시도할 수 있다. 고리 이뇨제의 정주 요법은 표 4와 같이 시행할 수 있다[7,12]. 고리 이뇨제를 thiazide와 병용하는 경우 thiazide의 약물작용시간이 고리 이뇨제보다 느리고 미리 원위부의 나트륨 재흡수를 막기 위하여 thiazide를 1시간 정도 먼저 복용하는 것이 효율적이다[12].
결 론
이뇨제는 임상에서 흔히 처방되는 약제로 부종의 조절을 위하여 가장 많이 사용되지만 그 외에도 다양한 목적으로 사용되고 있다. 이뇨제는 작용기전에 따라 다양한 종류가 있고, 이에 따라 선택적으로 적용되는 질환이나 부작용도 다르다. 따라서 적절한 이뇨제의 선택과 사용은 부작용을 줄이고 효율적인 치료를 위하여 매우 중요하다. 적절한 이뇨제 사용을 위해서는 이뇨제 치료를 시작하기 전에 환자의 전신상태를 정확히 파악하고, 각 환자에 따라 이뇨제 치료의 목적과 표적을 점검한 후에 개별적인 치료를 시행하는 한편, 치료에 따른 부작용을 감시하고, 원하는 치료반응을 저해하는 요소들을 제거하는 노력이 필요하겠다.