장질환 환자에서 놓치기 쉬운 미세영양소 결핍
Micronutrient Deficiencies That Should Be Considered in Intestinal Diseases
Article information
증 례
46세 남자가 약 3개월 이상 반복되는 소장 출혈과 설사로 거의 식사를 못하고 지속적인 총경정맥 영양공급을 받던 중에 전원되었다. 환자는 30대 중반에 크론병으로 진단되어 원위부 회장절제술을 받았고, 수년 후 소장 폐쇄와 유착으로 공장의 부분 절제를 받은 상태였다. 이후 생물학적 제제로 치료를 받아오던 중이었다. 흡연과 음주력은 없으며, 당뇨병, 심혈관질환의 병력도 없었다. 키 169 cm, 몸무게 48 kg이었고 눈 주변에 붉은 습진 병변, 입술 양쪽으로 헐어있는 소견, 움푹 패인 듯이 구부러진 손톱, 가늘고 곱슬거리며 들뜬 머리카락과 복부에는 수술 자국들이 확인되었다. 환자는 눈 앞이 뿌옇게 잘 안 보이고 기력이 없으며 가슴이 답답하고 숨이 차다고 호소하였다. 임상 소견에서 고열 등 바이러스 감염의 증거는 없었다.
검사 소견
- 흉부 X-선 촬영: 경미한 양측 흉수, 심비대
- 복부 X-선 촬영: 특이 소견 없음
- 심전도: 맥박수 96회/분, 좌전섬유속 차단(left anterior fascicular block)
- 혈액 검사: 혈색소 8.0 mg/dL, mean corpuscular volume (MCV)과 mean corpuscular hemoglobin (MCH) 감소, 정상 백혈구수, C반응단백질 10.8 mg/dL, 혈청 알부민 2.0 mg/dL, 정상 전해질 농도, 정상 갑상선 기능
진단의 일차 단계: 영양 스크리닝과 영양 평가
본 환자와 같이 만성 질환에 이환된 경우에는 질병 자체에 대한 평가와 함께 영양 평가가 이루어져야 한다. 환자는 nutritional risk screening (NRS) 2002 평가 척도를 사용하였을 때, 체질량지수 16.8인 점 만으로도 심각한 영양 결핍군에 속하였다. 3개월 이상 제대로 식이를 하지 못한 채 총경정맥 영양에 의존하고 있었으므로 에너지 요구량과 단백질 요구량에 맞게 영양 공급을 받고 있었는지 평가가 필요하였다. 일반적으로 심각한 영양 결핍으로 영양 치료가 필요한 환자에서는 미세 영양소 결핍이 함께 동반되어 있을 가능성이 높기 때문에 이에 대한 평가도 필요하였다. 더구나, 환자는 수 회의 장 절제 수술과 오랜 기간의 총경정맥 영양 공급을 받고 있는 상태였다. 진료 지침에 의하면 염증성장질환 환자가 임상 증상이 없는 관해기에 있더라도 정기적인 미세영양소를 평가하고 측정하도록 권고하고 있다[1].
환자의 낮은 체질량지수와 심각한 염증 상태를 고려하여 계산한 에너지 요구량은 1,440 kcal/일(= 48 kg × 25 kcal/kg BW/day × 1.2 [스트레스지수])이고, 단백질 요구량은 89 g/일(중등도 염증 상태의 단백질 요구지수 1.5 × 환자의 이상 체중 60 kg)이었는데, 문진과 처방받은 수액을 고려하면 에너지 요구량의 70%, 단백질 요구량의 60% 미만으로 공급받고 있었다. 혈중 비타민 B12, 셀레늄, 비타민 D 측정을 위한 25-OHD 검사를 시행하였고, 엽산, homocysteine, 구리 농도를 측정하였다. 심장초음파검사에서 좌심실이 늘어나고 심박출률은 30%였다. 수일 후 확인된 엽산, homocysteine, 구리는 정상 범주였으나, 혈중 25-OHD 및 비타민 B12 농도 저하, 셀레늄 혈중 농도는 2.0 μg/dL 미만으로 매우 감소되어 있었다. 골밀도 검사에서 골감소가 확인되었다.
최종 진단과 치료 경과
환자는 크론병 악화와 병합된 심각한 영양 결핍으로 진단되었으며, 비타민 B12 결핍, 골감소증의 원인이 된 비타민 D 결핍 그리고 심각한 수준의 셀레늄 결핍에 의한 심부전으로 진단되었다. 만성 출혈로 인한 철결핍성 빈혈이 동반되어 있었고, 피부 병변의 양상과 함께 만성 설사 증상을 고려할 때 임상적으로 아연 결핍도 의심되었다. 회장말단 절제 상태에서 비타민 B12 결핍이 확인되었으므로 지속적인 월 1회 비타민 B12 근주를 계획하였고, 아연 결핍에 대하여 아연 100 mg 10일간 투여한 후 복합 미량 원소(multi-trace elements)와 복합 비타민제(multivitamin)를 용법에 맞게 수액을 통하여 정맥 투여하였다. 철 결핍은 정맥 주사제로 보충하였다.
셀레늄 공급은 1일차에 셀레늄 100 μg을 수액에 추가 정주하고, 2일차에서 7일차에 200 μg을 투여한 후 경구 식이가 가능할 때까지 주 2회 200 μg을 투여하였다. 투여 후 서서히 증상과 심비대가 호전되었고, 1개월 후 추적 심장초음파에서 심박출률은 55%로 회복되었다. 크론병에 대해서는 생물학적 제제의 변경 후 임상적 호전을 보여 경장액과 연식을 유지 중에 퇴원하였다. 6개월 후 외래 내원 때에는 모발, 피부 병변과 손톱의 변화도 호전되었다. 이후 골감소증의 원인이 된 비타민 D 공급, 비타민 B12 월 1회 근육주사, 경구 철분제 투여와 함께 경구 복합 영양제를 투여받고 있다.
고 찰
미세영양소는 미량원소와 비타민을 지칭하며, 하루 필요량이 mg 또는 μg으로 소량이지만 여러 대사 과정이 잘 이루어지도록 도와 정상적인 신체 기능을 유지하는 중요한 영양소이다. 미량원소에는 아연, 셀레늄, 요오드, 구리, 크롬, 망간, 불소 등이 포함되며, 비타민은 종류가 많지만 대개 지용성인 비타민 A, D, E, K와 수용성인 비타민 B (B1, B6, B9, B12)와 비타민 C가 언급된다. 일반적으로 정상적인 식이 섭취로 충분히 보충이 되지만, 여러 질병, 특히 장질환이 심각하여 경구 섭취가 부족해질 경우에는 결핍이 심한 정도에 따라 치명적인 상황까지 겪게 될 수 있다. 장간막허혈(mesenteric vascular occlusion), 염증성장질환, 장루, 복부 수술의 합병증, 장루, 악성종양, 심한 운동기능 장애 등 장질환이 심각하거나, 경정맥 혹은 경장 영양에 의존하고 있는 경우, 결핍되기 쉬운 미세영양소를 예방적으로 투여하고 결핍 증상을 보일 경우에는 먼저 의심하고 적절한 진단을 조기에 내릴 수 있어야 한다. 미세영양소 결핍의 위험군에서 문진과 신체 진찰을 통하여 다양한 결핍의 증상과 징후를 찾아내고, 혈액 검사를 포함한 여러 검사를 이용하여 진단을 확진하며, 경우에 따라서는 환자의 임상 상태에 적합한 영양소를 경험적으로 투여하여 증상 호전을 확인하는 것이 본 내용의 주요 골자이다.
장질환 중 발생하는 미세영양소 결핍의 병태생리와 위험인자
장질환 환자에서 미세영양소 결핍이 발생할 수 있는 병태생리를 파악하고, 결핍의 위험인자들을 살피는 것이 중요하다. 첫째, 가장 흔하고 중요한 인자는 음식 섭취 불량이다. 복통, 설사, 식욕 저하 등의 증상으로 음식을 회피하게 되는 것이다[2]. 둘째, 미세영양소의 장분비 소실이 지속되는 상태 혹은 흡수 장애가 발생할 수 있는 경우에 결핍의 위험성이 증가한다. 장염증으로 만성 설사가 지속되는 경우는 아연, 칼슘, 칼륨이 소실되기 쉽고, 만성 출혈 환자에서는 철 결핍, 담즙 배액이 증가하면 구리 결핍이 가능하다. 흡수 장애는 염증 혹은 절제, 우회(bypass) 혹은 장루에 의하여 발생할 수 있다. 대부분의 미세영양소는 공장의 근위부 200 cm에서 주로 흡수되는데, 담즙산, 지방, 지용성 비타민, 비타민 B12는 회장 말단 100 cm 길이의 특정 부위에서만 흡수된다[3,4]. 따라서 절제 위치에 따라 영향을 받는 미세영양소 종류가 달라진다(Table 1). 회장의 상당 부분이 절제되면 흡수되지 못한 과량의 수분뿐 아니라 담즙산과 지방이 대장으로 넘어오게 되어 지방변 설사를 일으킬 수 있다. 장의 운동 기능 장애 역시 영양소 흡수에 영향을 줄 수 있다. 장 통과시간이 과도하게 빠른 경우에는 영양소가 장내 머무르는 시간이 짧아져서 흡수에 필요한 시간을 확보할 수 없고, 통과시간이 너무 느린 경우에는 장내 세균의 증식으로 오히려 영양소 흡수가 방해될 수 있다. 회맹판의 보존 유무 역시 중요한데, 회맹판은 영양소가 회장말단에 머무르는 시간을 적절히 길게 하여 흡수를 증가시키고, 대장으로부터 변이 역류되지 못하게 하여 담즙산 흡수에 영향을 끼칠 수 있는 장내세균의 증식을 막는 역할을 하기 때문이다. 셋째, 약물과의 상호작용으로 흡수가 방해되어 미세영양소 결핍을 일으킬 수 있다. Sulfasalazine과 methotrexate는 엽산의 흡수를 방해하고, 스테로이드는 칼슘, 아연, 인의 흡수 방해, 비타민 C의 대사와 비타민 D 저항성을 손상시킨다. Cholestyramine은 지방수용성 비타민, 비타민 B12와 철분의 흡수를 방해한다. 넷째, 장염이 심하여 이화작용(catabolism)이 증가하면 영양소의 하루 요구량이 증가하므로 미세영양소의 상대적 요구량도 증가할 수 있다. 다섯째, 오랜기간 경정맥 영양에 의존하는 경우, 총경정맥 영양액에 포함되어 있지 않은 미세영양소들의 결핍이 가능하다. 따라서, 투여 수액에 비타민 B1, 아연, 구리, 셀레늄, 크롬 등이 적정량으로 포함되어 있는지 확인해야 한다. 한편, 결핍보다는 드물지만, 경정맥 영양공급 중에 과다 투여로 미세영양소 독성이 가능할 수도 있으므로 적절한 모니터링이 필요하다[5].
장질환 환자에서 보이는 다양한 미세영양소 결핍의 임상적 고찰
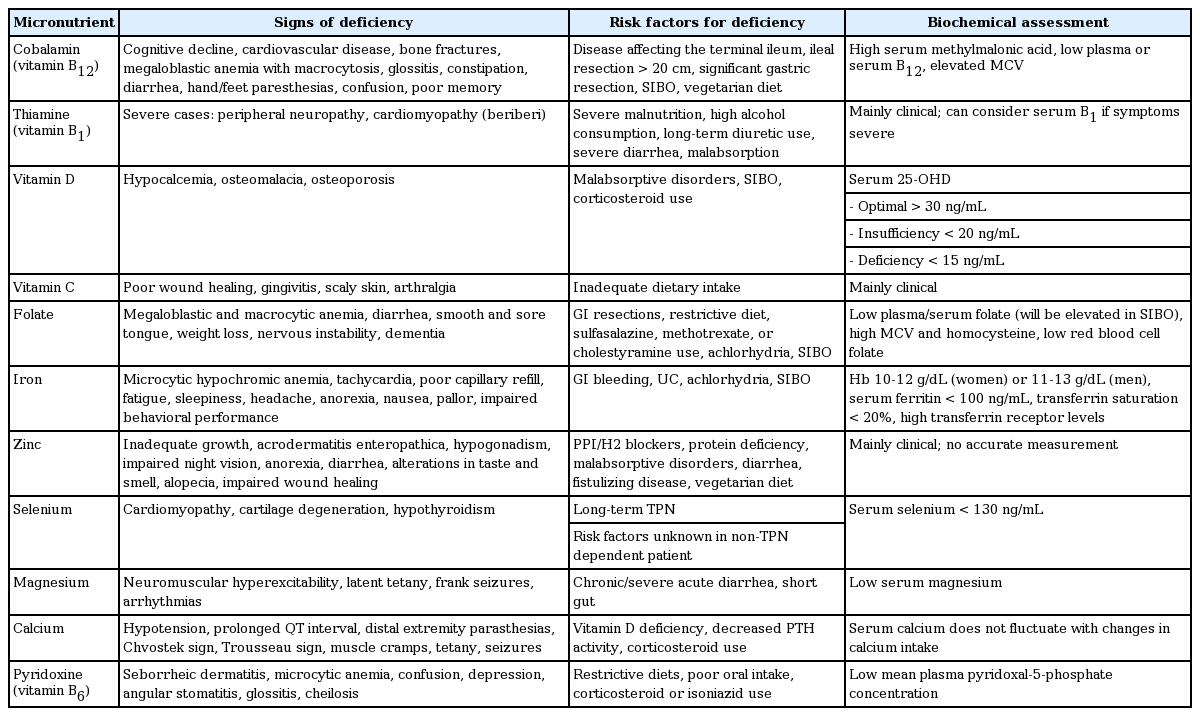
결핍되면 임상 예후에 의미 있는 영향을 끼칠 수 있으므로 결핍의 주요 증상과 징후를 숙지할 필요가 있다(Table 2) [1,2,6]. 비타민 B12은 조개, 고기, 생선, 조류, 달걀, 치즈 등의 동물성 식품에 포함되어 있다. 주요 흡수 부위는 회장 말단이므로 이 부위의 염증이 심하거나 절제된 경우(특히 20 cm 이상 절제된 경우)에는 결핍이 발생한다. 장내세균 과증식을 포함한 흡수 장애, 위축성 위염, 위절제 후 등에서 흡수 저하로 발생하거나, 또는 엄격한 채식주의자 등에서 섭취가 부족해도 결핍 증상이 발생한다. 비타민 B12는 purine 대사, 골수에서의 정상 적혈구 생성 그리고 신경 기능에도 관여하므로, 결핍되면 대구성(macrocytic) 빈혈, 사지의 감각 저하와 저림, 운동 장애, 치매와 기분 변화 등의 신경학적 증상이 발생할 수 있다. 혀의 통증, 식욕상실, 변비 등 위장 증상도 가능하다.
엽산은 주로 녹색 채소와 통곡물에 많이 함유되어 있다. 장질환에서의 엽산 결핍은 주로 sulfasalazine 같은 약제 사용 환자에서 발생한다. 엽산은 적혈구와 백혈구 생성에 관여하며 아미노산 대사에도 관여한다. 결핍이 되면 거대세포성빈혈(megaloblastic anemia) 또는 신경계 질환을 일으킬 수 있으며, 염증성장질환에서 엽산 결핍이 대장암 발생 위험을 증가시킨다.
비타민 D는 기름진 생선과 달걀에 많이 함유되어 있는데, 기본 기능은 칼슘과 인의 항상성을 적절히 유지하는 것으로 장에서 칼슘과 인의 흡수를 돕는다. 가장 활성화된 형태인 D-1, 25(OX)2D3이 칼슘 흡수에 영향을 끼친다. 비타민 D는 면역계도 자극하여 세포 분화와 T림프구의 기능에 중요한 역할을 하고 자가면역의 위험을 낮추며, 산-염기의 균형을 돕는다. 비타민 D는 햇빛 노출로 피부에서도 생성이 되는데, 피부에서는 독성을 일으킬 정도의 과량을 생성할 수는 없기 때문에 충분한 일광 노출은 비타민 D 보충에 큰 도움이 된다. 다만, 서구 지침에서는 강한 햇빛에 너무 오래 노출되면 피부암의 발병이 증가할 수 있다고 경고하고 있다. 칼슘은 뼈와 치아 건강에 꼭 필요하며 신경 전도와 근육의 수축에 중요한 역할을 한다. 따라서, 일광 노출이 매우 부족하거나 지방흡수장애증후군이 있거나 염증성장질환, 신부전이 있는 경우에 비타민 D 결핍이 쉽고, 항경련제를 먹는 간질 환자에서는 비타민 D의 간 대사가 영향을 받을 수 있다. 비타민 D가 장에서 흡수될 때에는 담즙이 필요하다. 비타민 D가 부족하면 칼슘의 흡수가 저하되고 결과적으로 골밀도 감소 및 골절 가능성이 증가하는데, 특히 스테로이드 복용력이 있는 환자에서 위험성이 증가한다.
비타민 B1은 체내에서 thiamine pyrophosphate의 형태로 탄수화물과 분지사슬아미노산(branched chain amino acid)의 대사에 관여한다. 주로 공장에서 흡수가 되고 적혈구와 혈장으로 운반된다. 만성 영양 결핍, 알코올 중독자, 편식, 장기간 이뇨제 투여, 투석, 심한 설사, 흡수 장애 등에서 비타민 B1이 부족해지기 쉽다. 비타민 B1이 결핍되면 식욕부진, 체중 감소, 의식 변화와 근력 저하가 가능하며, 심해지면 고심박출 심부전, 전신 부종의 증상을 보이는 wet beriberi, 다발성 신경병증의 Wernike 증후군 혹은 dry beriberi가 단독 혹은 혼합형으로 나타나기도 한다. 드물지만 전격성 심부전과 심한 젖산증(lactic acidosis)으로 집중 치료가 필요한 상태가 발생할 수 있다(shoshin beriberi). 비타민 B1 결핍에 의한 심부전의 경우 심전도만으로는 대부분 특이한 변화를 발견할 수 없다. 알코올 중독자 등의 고위험군에서 젖산혈증 외 원인이 뚜렷하지 않은 급성심부전이 있으면 우선 의심할 수 있으며, 생화학적인 검사로 확진한다. Wernike 증후군은 수일에서 수주에 걸쳐 진행하여 오심, 안진, 안구의 운동 장애, 보행 실조, 하지의 전진과 발열, 의식의 저하를 일으킬 수 있으며, 치료가 지연되면 기면, 혼수, 사망에 이르게 된다. 감각의 둔화, 전신 쇠약, 빈맥, 기립성 저혈압 같은 자율신경계 증상이 가능하다.
철은 산소 운반이 주요 기능이다. 세포 호흡과 적혈구, 백혈구, 간 내의 이화제(catalase) 활성을 조절하는 산화제(oxidase) 생성에 필수적이다. 십이지장과 근위부 소장에서 흡수되므로 이 부위에 광범위한 질병이 있거나, 식이 섭취 저하, 장출혈, 흡수 장애로 인하여 결핍이 발생할 수 있다. 결핍으로 빈혈이 발생하면 피부 창백, 피로감, 집중력 저하, 면역계 약화가 발생한다. 비타민 C 혹은 이를 다량 함유한 오렌지 주스와 함께 복용함으로써 흡수율을 높이는 반면, 차와 커피는 흡수를 방해할 수 있다.
아연은 면역 기능에 중요하여 자연 살해 세포(natural killer cell, NK cell) 및 대식구(macrophage)의 탐식 기능(phagocytic activity)에 영향을 끼치고 단백질 합성에 관여한다. 결핍되면 모발의 색조 변화, 탈모, 입맛의 변화(impaired taste), 면역 장애, 야맹증, 상처 치유력의 손상, 정자 수의 감소, 피부 병변이 발생할 수 있고 어린이에서 성장 지연이 발생할 수 있다. 피부 병변으로는 사지와 신체의 개구부, 즉 입, 눈, 귀, 생식기 및 항문 주변에 발적을 동반한 수포성 농포성 병변이 발생할 수 있다. 심한 설사나 누공, 장루, 장액의 소실이 심한 경우뿐 아니라 심한 화상과 같이 체액의 소실이 심한 경우에도 아연 결핍이 발생하기 쉬운데, 상태가 심하면 필요 공급량이 증가한다. 과량 투여하면 오히려 림프구 활성이 악영향을 받으므로 주의해야 한다.
셀레늄은 고기, 곡물, 생선에 자연적으로 함유되어 있고, 다양한 생물학적 대사에서 중요 역할을 하는데, 항산화성 glutathione peroxidase 성분 중 하나이며, 갑상선 호르몬 생성에도 필요하다. 지속적으로 결핍되면 거대 적혈구증(erythrocyte macrocytosis), 근육 이상(muscle dysfunction), 심근증(cardiomyopathy) 그리고 뇌염(encephalitis)이 발생할 수 있다. 셀레늄 결핍은 흔하지 않고, 환경과 토양에 따라 발생률이 달라질 수 있다. 예를 들면, 중국의 한 내륙 지방에서는 토양과 식이에서 셀레늄이 매우 부족하다고 한다. 오랜기간 총경정맥 영양 요법을 하는 환자의 경우 셀레늄 결핍이 발생한 증례는 많이 보고되어 왔으며, 놓치지 않도록 주의해야 한다[7]. 정맥 주사로 투여되는 영양제에는 약제안정성 문제로 셀레늄 성분이 포함되어 있지 않기 때문이다. 대략 4주 이상의 총경정맥 영양을 받는 환자에서 셀레늄 결핍이 발생할 가능성이 높다고 알려져 있다. 우리나라는 셀레늄 부족 지역이 아니므로 자연적인 식이 섭취를 하는 경우에는 문제가 없을 것으로 보이나, 경구식이가 가능하더라도 경장 영양액에 의존하는 경우에는 경장액 제품의 성분에 셀레늄이 제외되지는 않았는지 살펴보아야 한다. 최근의 한 보고에 의하면 활동성 크론병 환자가 오랜 기간 셀레늄이 함유되지 않은 성분 경장액(elemental diet)으로만 영양 공급을 받던 중 모발과 손톱의 변화, 사지 감각 이상, 시력 이상의 셀레늄 결핍 증상을 보였다[8]. 경구 복합영양제를 복용해 온 경우라도 제품에 따라서는 셀레늄이 함유되지 않기도 하므로 약제의 성분과 함량을 확인해야 한다.
미세영양소의 측정
환자의 기저 질병 상태와 임상 증상, 환자의 전반적인 영양 상태, 정맥 영양만 혹은 경장 영양만 하는지에 따라 측정할 미세영양소를 결정한다. 예를 들면, 칼륨, 칼슘, 인, 마그네슘은 설사가 만성적으로 지속되거나, 소장의 활동성 염증이 있거나 심한 영양 결핍으로 재급식증후군(refeeding syndrome)이 있을 때 측정하고 모니터링할 것을 권한다. 프로트롬빈 시간과 아연도 소장의 염증성 질환이 있을 때 질병이 가볍지 않다면 측정이 권유된다. 설사 증상이 심각하고 심한 영양 결핍의 징후를 보이거나, 정맥 영양 혹은 경장 영양 공급으로부터 보충 부족이 예상되는 등의 위험인자를 가진 것이 아니라면 셀레늄이나 구리를 우선적으로 측정할 필요는 없다. 소장의 활동성 염증이 심한 크론병의 경우 비타민 D (25-hydroxyvitamin D, OHD), 비타민 B12의 측정이 필요하며 철결핍성 빈혈의 유무도 확인해야 한다.
일반적으로, 염증성장질환 환자가 관해기에 있고 뚜렷한 결핍 증상이 없더라도 1-2년에 1회씩 주요 미세영양소인 비타민 D, 엽산, 철, 비타민 B12를 정기적으로 측정할 것을 권고하고 있다[9]. 골질환 발생이 의심되거나, OHD 혈중 농도가 낮은 환자에서는 부갑상선호르몬의 측정이 도움이 된다.
미세영양소 측정의 문제점은 미세영양소는 미량이므로 오염의 가능성도 높고 측정의 오류가 발생하기 쉬우며, 비용이 고가라는 것이다. 또한, 종류에 따라서는 혈중 농도 측정으로 조직에서의 미량 원소 농도를 예측하기도 쉽지 않다. 구리의 경우 심하게 결핍되면 혈청의 구리 혹은 ceruloplasmin으로 진단이 가능하지만, 결핍이 경미하거나 전신 염증 상태 등에서는 검사 해석에 주의를 요한다. 비타민 E는 고지혈증에 의하여 조직내 농도가 낮게 측정되므로 혈중 지질에 대한 보정이 이루어져야 한다. 환자가 심각한 염증 상태에 있다면, 아연, 철분, 셀레늄의 혈중 농도는 낮게, 구리는 높게 측정될 수 있어 주의해야 한다.
때로는 혈중 농도를 측정하는 것보다 결핍이 의심되는 영양소를 투여하였을 때 증상 혹은 혈액 검사 지표가 호전되는지를 확인하는 것이 더 유용할 수 있다. 예를 들어, 혈청 아연 농도는 심한 결핍 상태에서만 유용하므로 대개 임상 증상이 뚜렷하다면 우선 투여 후 증상의 호전을 지켜보는 경우가 흔하다. 단, 안전을 위해서는 신장과 간기능이 양호한 환자에게 시행하는 것이 좋다. 비타민 B1 역시 임상적 의심 하에 투여하는 경우가 대부분이다. 크롬은 매우 미량이고 오염이 잘 되어 측정하기 어려우므로 투여 후 포도당 불내성 호전을 확인함으로써 적정 투여를 모니터링하기도 한다.
치료의 원칙
미세영양소의 결핍이 심각해져서 뚜렷한 임상 증상으로 나타나기 전까지, 혈액 검사 등으로 초기의 결핍을 확인하기는 쉽지 않다. 따라서 영양 공급의 단계에서부터 임상 상황에 따른 하루 섭취 요구량(recommended daily intake)을 공급할 수 있도록 노력하는 것이 권장된다. 설사 등으로 장 소실이 지속되는 상황이거나, 심한 질병 염증 반응, 감염, 산화스트레스 상태 등의 임상 상태에서는 미세원소의 대사 요구량이 증가하여 권장 투여량도 증가함을 알아야 한다. 임상 상황에 따른 경험적 투여와 결핍 상황의 치료 원칙을 표 3에 정리하였다.
결 론
미세영양소 결핍은 결핍이 예상되는 질병 상황에서 임상의가 의심하는 것이 가장 중요하다. 따라서 미세영양소 결핍이 발생하기 쉬운 임상 상황 혹은 위험군을 파악하고, 미리 예방적으로 보충을 하거나, 각 영양소가 결핍되었을 때 나타나는 증상들을 숙지하여 조기에 치료하는 것이 불필요한 치료 기간을 늘리지 않도록 하는 최선의 방법이라 생각된다. 미세영양소의 결핍은 혈액 검사를 통하여 진단할 수도 있으나 전신 염증 상태 등에 따라 검사 결과 해석이 달라지기도 하므로 주의가 필요하다. 때로는 임상 증상과 징후만으로 치료를 시도하여 임상적 호전 여부를 보는 것으로 진단하기도 한다. 치료는 결핍 진단 후 권고 지침에 따르는 것이 일반적이지만, 특수한 상황에서는 경험적으로 미세영양소를 투여한다.