감염 동맥류로 인한 척추 골수염으로 오인한 베체트병 1예
A Case of Behçet’s Disease Mimicking Vertebral Invasion of a Mycotic Aneurysm
Article information
Abstract
감염 동맥류의 이차적인 척추 침범 또는 척추골수염으로 인한 척추 주변 조직의 염증성 변화의 가능성을 의심하였으나, 임상 경과 및 증상, 병리 조직을 토대로 최종적으로 베체트병에 의한 복부대동맥류 및 척추체의 손상으로 진단한 증례를 경험하여 보고한다.
Trans Abstract
Behçet’s disease is a systemic vasculitis of unknown etiology characterized by recurrent oral and genital ulcers and uveitis. The vascular involvement of Behçet’s disease affects arteries, veins, and blood vessels of all sizes, and it can include venous or arterial thrombosis and arterial aneurysms. There are only a few reports of an aortic aneurysm invading a vertebral body in a patient with Behçet’s disease. Here, we report the case of a 45-year-old man who was initially diagnosed with vertebral invasion of a mycotic aneurysm. He underwent vascular surgery and received empirical antibiotics, but all cultures were negative. However, he had persistent, recurrent deep vein thrombosis and elevated inflammatory markers. After reviewing the pathology, a final diagnosis of Behçet’s disease was made. He was successfully treated with corticosteroids. This report presents a rare case of Behçet’s disease mimicking vertebral invasion of a mycotic aneurysm.
서 론
베체트병(Behçet’s disease)은 재발성 구강 아프타성 궤양, 성기 궤양, 피부 병변, 안구 침범, 위장관계 및 혈관계 침범 등의 다양한 증상 및 징후를 특징으로 하는 원인 불명의 전신 염증성 혈관염이다. 베체트병의 주요 혈관 침범은 동맥류, 심부정맥혈전증, 혈전정맥염 등의 다양한 크기의 정맥 및 동맥 침범으로 나타나며, 전체 베체트병 환자 중 28% 정도에서 동반된다[1]. 베체트병이 종종 혈관염이나 혈전증으로만 발현되어 베체트병의 초기 진단이 어려운 경우가 있다[2]. 저자들은 감염 동맥류(mycotic aneurysm)의 이차적인 척추 침범 또는 척추 골수염에서 시작된 이차적 감염 동맥류를 의심하고 복부 대동맥류 절제 및 Y자 혈관 이식편을 삽입 후 항균제 및 항결핵제 치료 중 최종적으로 베체트병에 의한 척추 침범으로 진단된 증례를 경험하였기에 이를 보고한다.
증 례
환자: 45세 남자
주소: 오른쪽 종아리 통증
현병력: 5년 전부터 허리 통증이 있었으나 경과 관찰하였고, 1년 전부터 오전에 6시간 이상씩 앉은 자세를 유지하였다고 하였으며, 3개월 전부터 오른쪽 종아리가 붓고 통증이 발생하였다. 근육통으로 생각하여 물리 치료 후 통증은 완화되었으나, 부종은 지속되었다. 내원 3일 전 오른쪽 슬와에 압통이 발생하여, 내원 1일 전 연고지 흉부외과를 방문하였고 초음파에서 혈전으로 인한 오금정맥 폐쇄가 의심되어 응급실로 내원하였다.
과거력: 특이 사항은 없었다.
이학적 소견: 활력 징후는 혈압 132/87 mmHg, 맥박 90회/분, 호흡수 20회/분, 체온 36.7℃였고 의식은 명료하였다. 신체 검사에서 흉부 청진에서 호흡은 깨끗하였고 심잡음은 들리지 않았다. 복부 검진에서 특이 소견은 보이지 않았다. 늑골척추각 압통은 없었다. 양측 슬관절에 압통을 동반한 열감, 발적, 부종이 관찰되었으며, 오른쪽 발등동맥의 맥박은 촉지되지 않았다.
혈액 검사 소견: 말초혈액 검사에서 백혈구 수치가 7,000/mm3, 혈색소 14.0 g/dL, 혈소판 322,000/mm3였다. 생화학 검사에서 D-이합체(D-dimer)는 1.45 mcg/mL로 상승되어 있었고, C-반응성단백질(C-reactive protein)이 5.28 mg/dL로 상승되어 있었으며, 알부민 3.2 g/dL로 감소되어 있었고, 이외 혈청 생화학 검사 및 혈액 응고 검사는 모두 정상 범위였다.
방사선학적 소견: 흉부 단순 촬영 검사에서 이상 소견을 없었으며, 하지 정맥 전산화단층촬영(computed tomography [CT] venography)에서 중간부터 먼 쪽 오른 두렁정맥과 오금정맥, 앞정강정맥, 뒤정강정맥 그리고 종아리정맥에 심부정맥혈전증이 확인되었고, 저명한 혈관 주위 침윤을 동반하고 있어 화농 혈전정맥염(suppurative thrombophlebitis)의 가능성이 있었다. 또한 3번 요추 근처 신하대동맥(infrarenal aorta) 주변 공간에 3.4 cm의 가장자리가 조영 증강되는 액체저류가 있었으며, 인접한 3번 요추 척추체에 골파괴 소견이 확인되었다(Fig. 1). 이에 척추 주변 농양과 대동맥 주위 조직의 염증을 동반한 척추 골수염을 의심하여 허리 자기공명영상(magnetic resonance image, MRI) 검사를 시행하였고, T1 및 T2 강조영상(T1, T2 weighted sequence)에서 불균일한 신호로 보이는 4.3 cm의 연조직 병변이 척추 주변 조직과 대동정맥 공간(aorto-caval space)에 있었다. 요추 3번 척추체에 미란이 있었으며, 요추 4번 척추의 위쪽 종말판에도 골수 신호변화가 있었다(Fig. 2). 일주일 후 대동맥 CT를 촬영하였고, 콩팥 아래 복부 대동맥에 1.6 cm의 빠르게 커지고 있는 가성대동맥류가 있었다(Fig. 3). 이에 CT 및 MRI 결과를 종합하여 볼 때 감염 동맥류의 이차적인 척추 침범 또는 척추 골수염으로 인한 척추 주변 조직의 염증성 변화의 가능성이 높다고 생각하였다.
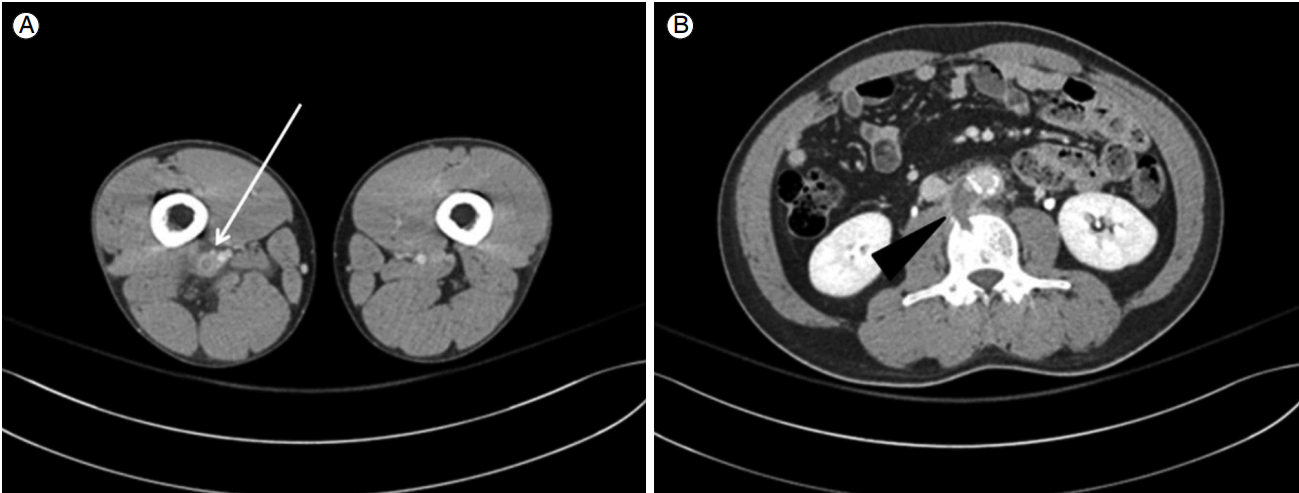
(A) Computed tomography venography at the initial presentation shows deep venous thrombosis in the mid to distal right superficial saphenous vein (arrow). (B) There is fluid collection in the para-aortic space and adjacent bone destruction of the L3 vertebral body (arrowhead).
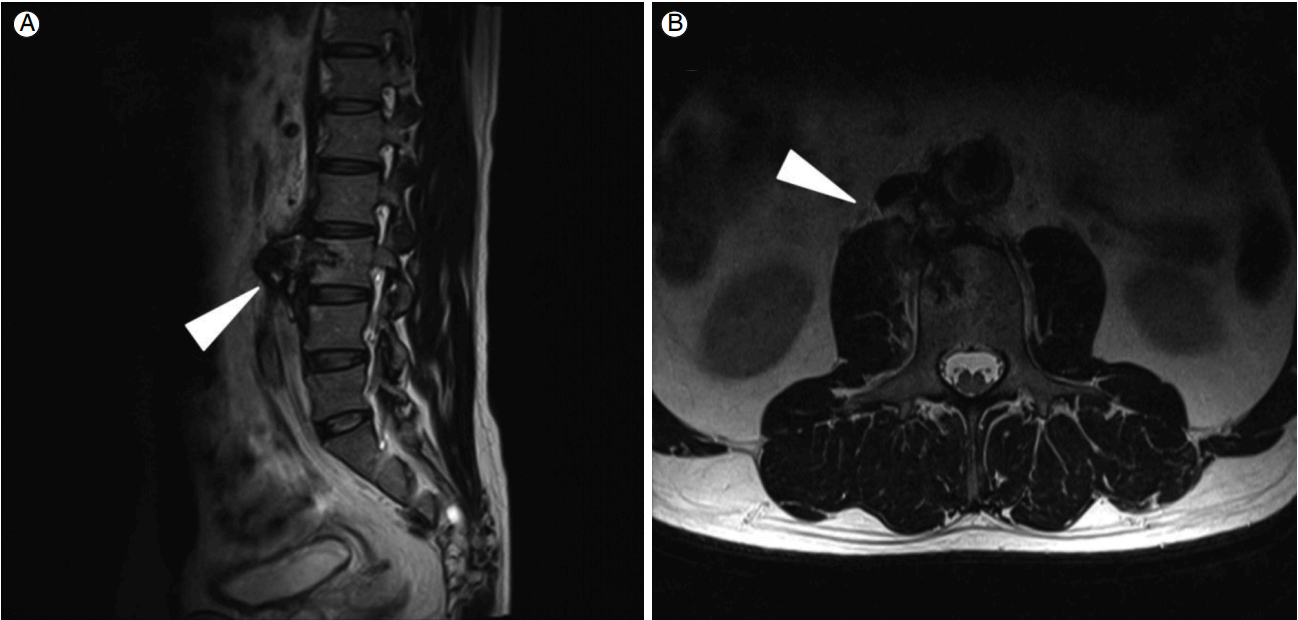
T2-weighted magnetic resonance images of the spine at presentation. The (A) sagittal and (B) transverse views of the spine show erosion of the L3 vertebra and a well-defined soft tissue lesion (aneurysm) in the prevertebral space and aortocaval space (arrowhead).
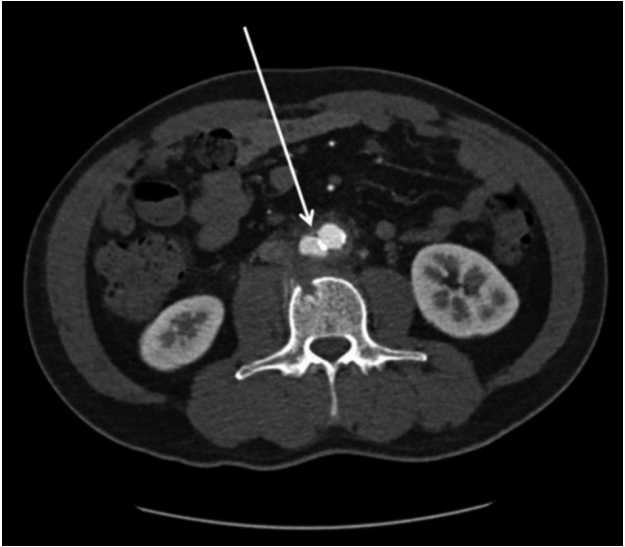
Aortic computed tomography images 1 week later. The infra-renal abdominal aorta shows a rapidly growing 1.6 cm pseudoaneurysm at the L3 level (arrow).
심전도 소견: 분당 74회로 정상 동율동이 확인되었다.
치료 및 경과: 내원 당일 2쌍의 혈액배양 검사 후에 경험적 항생제로 ceftriaxone과 vancomycin을 투약하였다. 입원 7일째 혈관외과에서 복부대동맥류 절제 및 Y자 이식편 삽입(resection and Y-graft interposition of abdominal aortic aneurysm)을 시행하였다. 신장동맥 아래쪽에 있는 대동맥 및 온엉덩동맥을 제거하고 그물막(omentum)을 결장 후방으로 위치시켜 폴리테트라플루오로에틸렌(polytetrafluoroethylene) 이식편을 덮었다. 수술 소견에서 농양은 저명하지 않았고, 대동맥에 염증이 있으면서 주위 조직이 육아조직화(granulation change)되어 있었다. 절제된 조직에서 균 배양 검사와 16S rRNA gene sequencing 검사를 시행하였으나 원인 미생물이 진단되지 않았다. 대동맥 수술 검체의 병리 결과는 만성 대동맥염으로 확인되었다. 병리 검체에서 그람 염색, acid fast bacilli 염색 및 Periodic Acid Schiff’s (PAS) 염색, 결핵 polymerase chain reaction을 시행하였으나 특이 소견은 없었다. 입원 19일째 원인이 밝혀지지 않은 감염증으로 결핵 인터페론감마검사 양성인 점을 고려할 때, 세균 및 결핵 감염을 모두 고려하여, isoniazid 300 mg, rifampin 600 mg, pyrazinamide 1,500 mg, levofloxacin 750 mg을 하루 1회 투여하기로 하였고, 정맥혈전증에 대해서는 저분자량 헤파린(low molecular heparin)을 투약하다가, 직접 트롬빈 억제제(direct thrombin inhibitor)로 변경하여 퇴원하였다.
퇴원 후 4주간 항생제 투약에 의한 전신 상태 저하 및 답답한 느낌을 호소하며 항균제 및 항결핵제 중단과 투약을 반복하였다. 퇴원 8주 후 추적 MRI를 시행하였고 척추 골수염의 범위는 어느 정도 감소하고 있으나, 하대정맥, 양쪽 근위온엉덩정맥에서 염증성 혈전을 동반한 혈관염의 소견을 보였다. 재입원하여 CT venography를 촬영하였고 하대정맥부터 양쪽 속엉덩정맥, 바깥 엉덩정맥까지 광범위하게 혈전이 있었다. 이전 수술시 대동맥 검체 병리 슬라이드를 재검토하였고, 만성 대동맥염으로 대동맥은 호중구, 림프계 세포, 조직구, 형질세포 등의 대부분의 염증세포 침윤이 있었다. 죽상동맥경화가 동반되어 있었으며, 거대세포의 침윤은 없었다(Fig. 4). 이상의 병리 결과는 혼합 염증성 패턴으로 베체트병의 가능성을 시사하는 소견이었다. 환자는 평소 자주 반복되는 구강 궤양이 있었으며 성기 궤양 및 포도막염의 과거력은 없었으나 시행한 패설지 반응(pathergy test) 결과 양성을 보였다. 그간의 임상 경과 및 검사 결과를 토대로 결핵을 비롯한 다양한 감염성 질환에 대한 증거가 뚜렷하지 않음을 고려할 때 환자는 International Criteria for Behçet's Disease 진단 기준을 충족시키는 베체트병 및 이로 인한 광범위한 혈전과 혈관염으로 판단하였다. 이후 메틸프레드니솔론 1 mg/kg을 투약하였으며, 오른쪽 종아리 통증과 부종 등 증상은 모두 호전되었다. 외래에서 추적 관찰하며 스테로이드 감량하며 유지 중이다.
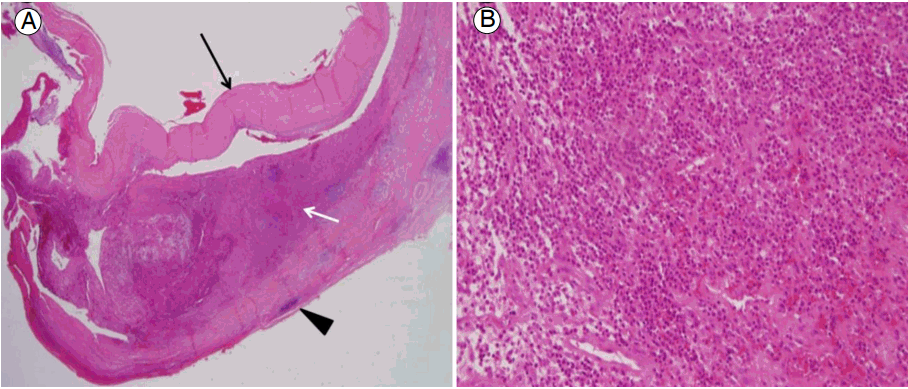
(A) Histologically, the abdominal aorta shows a mixed inflammatory pattern with severe inflammatory infiltration and atherosclerosis. There is fibrotic degeneration of the aortic wall (black arrow), a severe mixed inflammatory infiltrate in the adventitia (white arrow), and lymphoid aggregates (arrowhead). There is no evidence of multinuclear giant cell infiltration (hematoxylin and eosin [H&E] stain, ×40). (B) The mixed infiltrate consists of neutrophils, lymphohistiocytes, and plasma cells (H&E stain, ×200).
고 찰
본 증례는 감염 동맥류의 이차적인 척추 침범 또는 척추골수염으로 인한 척추 주변 조직의 염증성 변화의 가능성을 의심하여 수술 및 항생제, 항결핵제를 투약하였으나 적절한 치료 반응을 보이지 않았고 최종적으로 베체트병에 의한 복부 대동맥류 및 척추체의 손상으로 진단한 증례이다. 환자는 과거부터 사용되던 International Study Group (ISG)의 베체트병 진단기준은 만족하지 못하나 신경 및 혈관 침범 등의 다양한 임상 양상을 고려하여 최근 제시된 International Criteria for Behçet's Disease의 진단기준으로는 구강궤양, 패설지 반응 양성 및 혈관 침범을 만족하므로 베체트병 진단이 가능하였다[3]. 특히 대동맥 병리 소견은 베체트병을 시사하는 소견이었으며 심부정맥혈전증, 동맥류 등 베체트병에서 발생하는 혈관 이상을 동반하고 있었다[4]. 이전 보고에 따르면 ISG의 베체트병 진단기준을 만족시키지는 못하지만, 주요 혈관염 증상이 먼저 나타나는 경우가 드물게 있다고 알려져 있다[2].
베체트병의 근골격계 침범은 비교적 흔하며, 관절염이나 관절통이 그중 가장 많다. 드물지만 골괴사, 근육통, 섬유근육통이 보고되었다[5]. 그러나 일차적으로 뼈를 직접 침범하여 척추 골수염 양상으로 발생한 베체트병의 증례보고는 없다. 본 증례 역시 베체트병이 근골격계를 직접 침범한 것이 아니라, 혈관염으로 동맥류가 선행하고 이차적으로 척추체에 미란을 일으켜 척추 골수염으로 오인되었다. CT와 MRI 소견을 종합하여 볼 때 척추체 내부 병변의 경계가 명확하고, 대동맥류를 중심으로 척추체까지 침범하는 쐐기 모양을 하고 있어 동맥류가 척추 병변에 선행하였다는 것을 뒷받침한다. 본 증례처럼 감염이 동반되지 않은 박동성 동맥류에 의한 척추의 손상은 감염성 척추 골수염과 같은 감염 상황에서의 골용해성 병변과 비교하여 경계가 규칙적이고 분명하다고 알려져 있다[6]. 동맥류가 척추체를 침범하는 기전은 잘 알려져 있지 않다. 동맥류의 간헐적 박동이 척추체를 압박하여 척추체에 허혈성 손상을 일으키거나, 동맥류 주위 염증을 일으켜서 이러한 골병변이 발생할 수 있겠다[7].
베체트병에 의한 동맥류의 영상 소견은 조영이 잘 되는 주머니모양 동맥류이며 20% 정도에서 다른 다발성 가성 동맥류를 형성한다[8]. 이에 비하여 감염성 대동맥류는 분엽성의 불규칙한 윤곽과 주변에 지방 조직의 침윤 및 액체저류가 동반된다[9]. 감염성 동맥류는 빠르게 진행하며 이 두 종류를 구분하는 것은 감염된 동맥류 환자에게 염증성 동맥류로 오인하여 면역 억제제를 투약할 수 있어 중요하다[9]. 베체트혈관염의 병리 소견은 혼합 염증성 패턴(mixed inflammatory pattern)이며, 호중구, 림프구, 조직구, 형질세포, 대식세포, 호산구, 비만세포 등 대부분의 염증세포가 관찰된다. 괴사 조직은 있을 수 있으나 저명한 육아종성 염증 패턴은 보이지 않는다. 이러한 혼합 염증성 패턴은 혈관염의 병리 소견에서 상대적으로 드물게 보이는 종류로 베체트병, 코간증후군, 재발성 다발 연골염과 관련이 있다[4]. 본 환자에서도 대부분의 염증세포 침윤이 관찰되는 혼합 염증성 패턴을 보였다.
베체트병에서 발생하는 동맥류는 드물지만 파열을 일으킬 수 있어 주요 사망 원인이 된다. 대동맥과 주요 혈관 분지의 진성 혹은 가성 동맥류로 혈관 중간층이 두꺼워지며, 탄력섬유의 분리가 일어나서 혈전과 혈관 확장, 동맥벽의 파열을 일으킨다[10]. 치료는 파열의 가능성이 있으면 가능하면 수술적 치료를 하고 수술 후 재발을 막기 위하여 스테로이드가 권장된다.
문헌 검색시 베체트병에 의한 대동맥류와 이로 인한 척추체의 손상은 본 증례를 제외하고 여섯 개의 증례만이 보고되었다. 기존 증례들은 대부분 이미 베체트병을 진단받은 환자에게서 대동맥류와 척추 병변이 발견되었다. 본 증례의 경우는 대동맥류의 진단 및 치료 과정에서 베체트병이 진단되었다는 점에서 차이가 있으며 비슷한 환자를 진단하는데 교훈을 주는 바가 있다. 결론적으로 본 환자의 증례는 정맥 혈전증과 대동맥 주변 침윤을 동반한 대동맥류가 발생한 환자에서 비감염성 원인으로 베체트병을 감별진단으로 고려하는 것이 필요함을 시사한다.