최신 담도내시경 검사기법
Recent Advances of Peroral Cholangioscopy
Article information
서 론
담도내시경 검사(cholangioscopy)는 담관 내부의 내시경적 검사를 통해 치료가 어려운 담관 결석의 안전한 쇄석술, 일반적인 영상 검사나 내시경역행담췌관조영술(endoscopic retrograde cholangiopancreatography, ERCP)을 통해 정확한 진단이 어려운 담관 협착이나 담관내 미세한 병변에 대한 내시경적 검사, 또는 특정 담관 질환에 대하여 병변의 경계 확인 등의 보다 정밀한 검사 등을 시행할 수 있는 유용한 검사 방법이다. 하지만 담관의 해부학적 구조 등 근본적으로 담관 내부로의 내시경적 접근에 제한이 있어 일부 제한된 기관에서, 선택적으로 시행되어 왔다. 담도내시경 검사는 경피적(percutaneous) 또는 경구적(peroral) 접근이 가능하고, 경피적 담도내시경 검사는 경피경간(percutaneous transhepatic) 경로를 형성하는데 2-3주 정도 기간이 필요하고 검사를 모두 마칠 때까지 경피적 배액관을 유지해야 하는 불편함이 있다. 최근 10여 년간 담도내시경 분야, 특히 경구적 담도내시경 검사(peroral cholangioscopy, POC)의 방법에서 획기적인 발전이 있어 왔으며, 그 임상적 유용성이 확대되고 있다. 본고에서는 경구적 담도내시경 검사에 있어서 최근까지 진보된 검사 방법들에 대하여 알아보고자 한다.
본 론
경구적 담도내시경(POC)의 세 가지 검사 방법
현재 시행되고 있는 경구적 담도내시경 검사 방법은 크게 세 가지로 나누어 볼 수 있다. 1975년[1] 경구적 담도내시경 검사가 처음 소개된 이후 현재까지 이어져온 1) 모자내시경 시스템(mother-baby endoscope system), 2) 2007년 처음 소개된 SpyGlass 시스템(SpyGlass Direct Visualization System, Boston Scientific Corp., Marlborough, MA, USA) [2,3] 3) 2006년부터 시작된 극세경 내시경(ultra-slim endoscope)을 이용한 직접 경구적 담도내시경(direct POC) 방법이 있다[4-7]. 담관 내로 내시경을 삽입하는 방법에 따라 나누면 모자내시경 시스템과 SpyGlass 시스템은 ERCP를 시행하는 십이지장경(duodenoscope)의 부속기구 채널을 통해 십이지장경의 지지하에 작은 직경의 담관내시경(choledochoscope)을 ERCP의 기구와 같이 담관 내로 삽입하는 방법이고, 직접 경구적 담도내시경 검사는 십이지장경과 같은 다른 내시경의 도움 없이 작은 직경의 내시경을 구강, 식도 및 위를 지나 십이지장 유두부 입구를 통하여 담관 내로 직접 삽입하는 방법이다. 시술에 필요한 내시경의사에 따라 나누면, 모자내시경 시스템은 모내시경과 자내시경을 두 명의 내시경 의사가 각각 조작하여 서로 긴밀한 협력이 필요하며, 최근 도입된 SpyGlass 시스템과 직접 경구적 담도내시경 방법은 한 명의 내시경 의사가 시술을 시행할 수 있다(single-operator cholangioscopy).
모자내시경 시스템(mother-baby endoscope system)
모자내시경 시스템은 십이지장경이 ‘모내시경’이 되고 십이지장경의 부속기구 채널을 통해 삽입되는 담관내시경이 ‘자내시경’이 되어 경구적 담도내시경 검사를 시행하여 ‘모자내시경’이라 이름하게 되었다[8]. 경구적 담도내시경 검사를 시행하기에 앞서 일반적으로 내시경 유두괄약근절개술(endoscopic sphincterotomy, EST)이 시행되어 십이지장 유두부 입구가 확장된 상태에서 검사를 시행하게 되며, 자내시경인 담관내시경을 십이지장경의 부속기구 채널을 통해 삽입하고 십이지장경을 조작하는 내시경 의사와 담관내시경을 조작하는 내시경 의사 간에 긴밀한 협조 하에 담관내시경을 유두부 입구를 통하여 담관 내로 삽입하게 된다(Fig. 1) [8,9]. 담관내시경의 외경은 3.0-4.1 mm 정도이고, 담관내시경의 부속기구 채널의 직경은 1.15-1.7 mm이다(Table 1). 내시경의 기술적인 발전이 계속되면서 담관내시경 영상의 해상도가 매우 향상되었고, 이전에 광섬유 방식에서 최근에는 디지털영상장치를 도입함으로써 더욱 향상된 해상도의 영상을 얻을 수 있으며, 협대역영상(narrow band imaging, NBI)과 같은 영상증강 내시경 검사(image enhanced endoscopy)를 통한 담관내 병변의 내시경적 검사가 가능하다[10-12].

Mother-baby endoscope system. Two endoscopists who are experts for ERCP is handling each other endoscopes in close cooperation. ERCP, endoscopic retrograde cholangiopancreatography.

Brief specifications of choledochoscopes in “Mother-baby” endoscope system for peroral cholangioscopy
최근 도입된 SpyGlass 시스템이나 직접 경구적 담도내시경 검사가 소개되기 전까지 모자내시경 시스템이 경구적 담도내시경 검사의 주요한 방법이었지만 여러 가지 제한점으로 인해 널리 시행되지 못하였다. 먼저 두 개의 별개 내시경 시스템이 사용되고 각각의 내시경을 ERCP에 익숙한 두 명의 전문 내시경 의사가 협력하면서 시술을 시행해야 하고 실제로 검사를 시행하면서 내시경 조작에 어려움이 있다. 또한 자내시경인 담관내시경은 미세한 장비들과 기술들이 집약된 기기로서 비교적 고가이면서 또한 내구성이 약한 단점이 있어 조작에 매우 주의가 필요하다. 그리고 담관내시경의 부속기구 채널의 직경이 작아 여러 가지 부속기구 사용에 제한이 있고 내시경적 관찰 후 확진을 위해 조직 생검을 시행할 수 있지만 충분한 양의 검체를 획득하기 어려운 단점이 있다[4,13].
SpyGlass 시스템(spyglass direct visualization system)
SpyGlass 시스템은 한 명의 내시경 의사가 시행할 수 있는 경구적 담도내시경 검사로서 2007년 처음 소개되었는데, 올림푸스사의 모자내시경 시스템과 유사한 방식이지만 그 단점들을 극복할 수 있는 새로운 담도내시경 시스템으로서 미국 보스턴사에서 개발되었다[2,3]. 모자내시경 시스템의 자내시경, 즉 담관내시경 역할을 하는 0.9 mm 직경의 광학탐침(SpyGlass, Boston scientific Corp.)을 10 Fr 직경의 카테터(SpyScope, Boston scientific Corp.)에 장착하여 다른 ERCP 부속기구와 같이 담관 내로 삽입하며, SpyScope의 조작부를 십이지장경 조작부 아래에 장착함으로 한 명의 ERCP 내시경 의사가 담도내시경 검사를 시행할 수 있도록 하였다. 이 SpyScope은 선단부가 상, 하, 좌, 우의 네 방향으로 굴곡이 가능하고 SpyGlass 광학탐침이 통과되는 채널 외에 조직 검사를 위한 조직생검 겸자(SpyBite, Boston scientific Corp.)나 쇄석술을 위한 레이저 또는 전기수압 탐침을 삽입할 수 있는 1.2 mm의 부속기구 채널과 물을 주입할 수 있는 채널이 독립적으로 존재한다. 이러한 SpyGlass 시스템이 소개되면서 그동안 제한된 기관에서 제한적으로 시행되어오던 경구적 담도내시경 분야에 새로운 장이 마련되게 되었다[14,15].
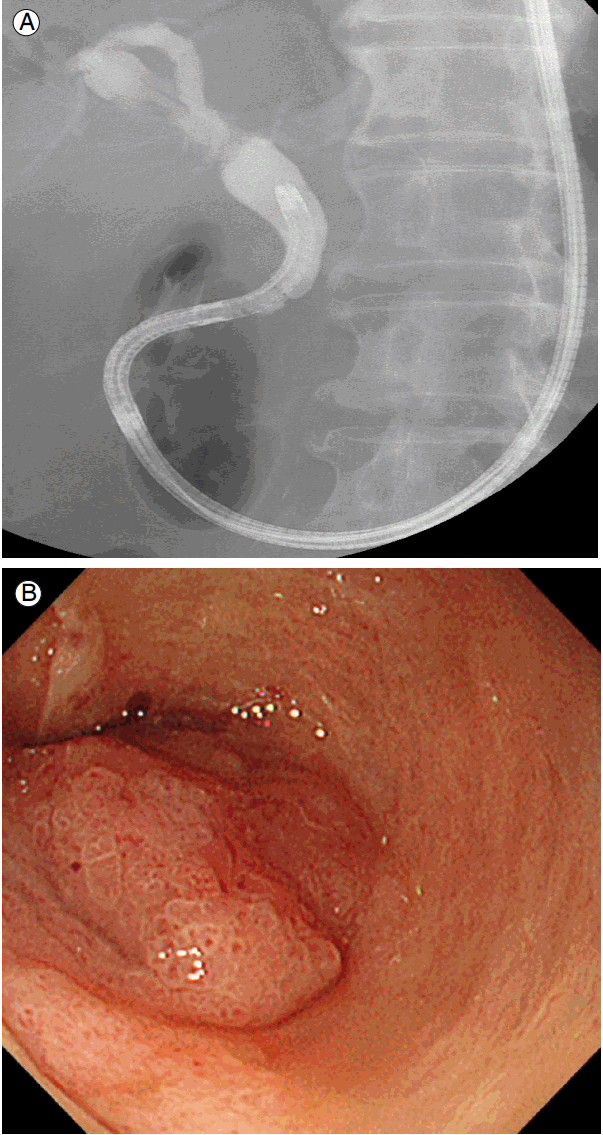
초기 모델의 만족스럽지 못한 영상 해상도(6,000픽셀)나 조작의 불편함 등을 향상시킨 새로운 모델의 SpyGlass 시스템(SpyGlass DS Direct Visualization System [DS: “digital and simple”], Boston scientific Corp.)이 최근 개발되었는데, SpyGlass 광학탐침과 SpyScope을 일체화시켜 사용이 편리하고 초기 모델보다 4배 향상된 해상도의 디지털 영상을 제공하며 내시경 시야각도 약 60% 정도 향상되었다(Figs. 2 and 3) [16,17]. 이러한 SpyGlass 시스템의 개발은 여러 가지 담췌관 질환의 진단 및 치료에 있어서 담도내시경 검사의 접근성을 보다 쉽게 하였고, 어려운 담석의 쇄석술이나 진단이 어려운 담관협착에 대한 내시경적 검사 및 조직생검 등 다양한 담췌관 질환에 대하여 임상적으로 사용되고 있다[18-20]. 하지만 비교적 고가의 SpyScope은 일회용 내시경 기기이며, 아직까지 국내에서 상용화하기 위해서는 경구적 담도내시경 검사에 대한 급여정책 등의 문제가 해결되어야 한다.

Peroral cholangioscopy by using SpyGlass DS system (Boston Scientific Corp., Marlborough, MA, USA). (A) A SpyScope attached to a duodenoscope. (B) A fluoroscopic image of the SpyScope in the bile duct.
직접 경구적 담도내시경 검사(direct peroral cholangioscopy)
1977년 Urakami 등[21]은 모자내시경 방식에서와 같은 십이지장경의 도움 없이 일반 상부위장관 내시경을 십이지장 유두부 입구를 통하여 직접 담관 내로 삽입하여 담도내시경 검사를 시행하여 보고하였고, 1978년 Rösch와 Koch [22]는 담관-십이지장 문합술(choledochoduodenostomy)이 시행된 환자에서 소아용 상부위장관 내시경을 이용하여 직접 경구적 담도내시경 검사를 시행하여 보고하였다[21,22]. 이와 같이 모자내시경 방식과 달리 하나의 내시경을 담관 내로 직접 삽입하여 담도내시경 검사를 시행하는 것을 직접 경구적 담도내시경 검사라고 한다. 하지만 이러한 검사 방법은 1977년 처음 소개된 이후 더 이상의 연구나 보고가 없다가 2006년, 2009년에 미국과 국내에서 내시경을 직접 담관 내로 삽입하기 위해 보조기구의 도움을 사용하는 연구들이 보고되면서 발전하게 되었다[5-7].
담관이 매우 확장되어 있고, 십이지장 유두부 입구가 넓게 확장되어 있는 경우에는 일반 상부위장관 내시경을 이용한 직접 경구적 담도내시경 검사가 가능할 수 있지만, 일반적인 담관 질환에서 담관 직경 및 유두부 입구의 확장 정도를 고려하여 소아 상부위장관 내시경 검사나 경비내시경 검사에 사용되는 극세경 내시경(ultra-slim endoscope)이 사용된다(Table 2). 십이지장과 담관이 일반적으로 급격한 각도로 서로 만나기 때문에 내시경의 담관내 삽입을 돕기 위한 보조기구를 사용하게 된다. Larghi와 Waxman [5]은 ERCP를 통해 유두철선을 미리 담관 내에 삽입한 후, 십이지장경을 제거하고 삽입되어 있는 유도철선을 극세경 내시경의 부속기구 채널을 통해 역으로 삽입하면서 유두철선을 따라 내시경을 담관 내로 삽입하는 방법을 보고하였지만 시술 도중 유도철선이 쉽게 담관에서 이탈하여 담도내시경의 성공률이 높지 못하였다. 이후 여러 가지 보조기구를 사용한 직접 경구적 담도내시경 방법이 보고되었지만, 국내에서 연구하여 보고된 풍선도관을 이용한 방법이 높은 성공률을 보였고 현재까지 가장 널리 이용되고 있다[5,7]. 먼저 ERCP를 시행하여 유도철선을 간내담관이나 협착 상부의 담관에 삽입한 후, 십이지장경을 제거하고 유도철선을 따라 극세경 내시경을 십이지장 유두부 입구까지 삽입한다. 이 때 극세경 내시경의 부속기구 채널에 5 Fr 두께의 풍선도관(ERCP를 통한 담석제거술에 사용되는 풍선도관)을 삽입하고 풍선도관을 통하여 유도철선을 따라 내시경을 삽입하게 된다. 십이지장 유두부 입구에서 유도철선을 따라 풍선도관을 상부 담관으로 삽입하고 풍선을 통해 고정한 후, 고정된 풍선도관을 지지대로 삼아 내시경이 담관 내로 삽입될 수 있다. 환자에 따라서는 ERCP를 통해 유도철선을 삽입하는 과정 없이 극세경 내시경을 직접 십이지장 유두부 입구까지 삽입하고, 직접 유도철선과 풍선도관을 담관 내로 삽입한 후 담도내시경 검사를 시행할 수 있다[23].
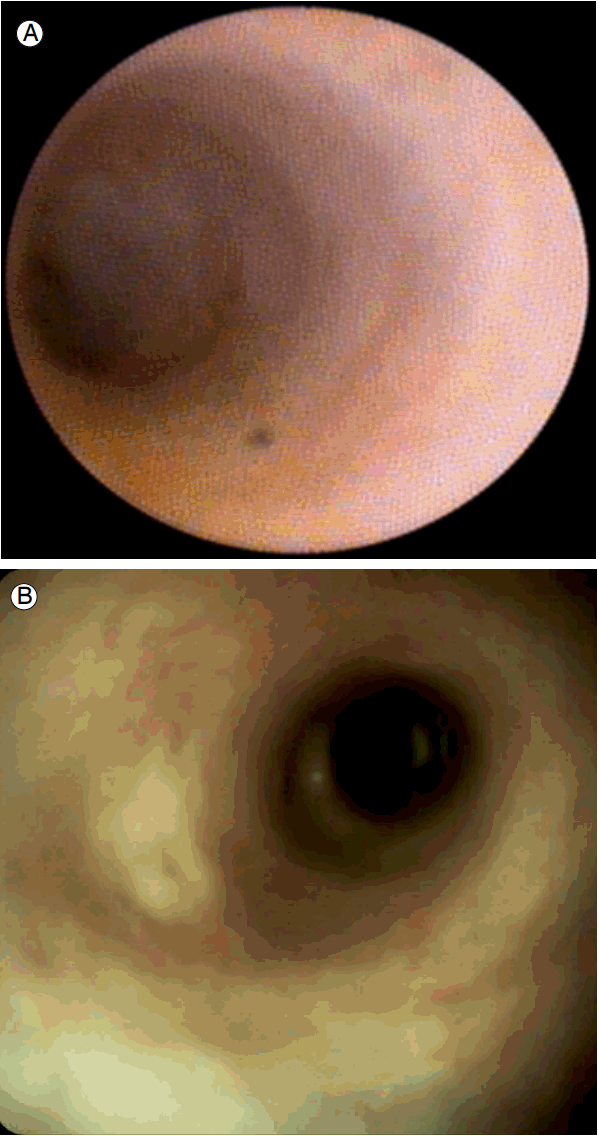
극세경 상부위장관 내시경을 이용한 직접 경구적 담도내시경 검사는 일반적인 상부위장관 내시경 영상과 같은 매우 우수한 내시경 영상을 얻을 수 있고 내시경의 종류에 따라 NBI, i-scan 등과 같은 영상증강 내시경 검사 또한 가능하다(Fig. 4) [4,24,25]. 또한 2.0 mm 크기의 부속기구 채널을 통해 충분한 양의 조직검체 획득이 가능하고 조직 검사 외에 5 Fr 두께의 다양한 부속기구들을 사용한 담관내 내시경 시술이 가능하다. 또한 담도내시경 검사를 위한 추가적인 장비가 필요하지 않고 일반적으로 사용되고 있는 내시경 시스템과 극세경 내시경을 사용하여 검사를 시행하기 때문에 현재로서 가장 경제적인 경구적 담도내시경 검사 방법이다[26]. 하지만 총담관이 8-10 mm 이상으로 확장된 환자에서 시행되고, 풍선도관의 지지를 통해 내시경이 담관 내에 삽입되었다가 담관내 시술을 위해서 풍선도관을 제거하게 될 때 내시경이 담관에서 이탈되는 내시경 위치의 불안정성이 환자에 따라 나타날 수 있다.
Direct peroral cholangioscopy by using an ultra-slim endoscope. (A) An ultra-slim upper endoscope was advanced into the bile duct. (B) Endoscopic image of bile duct mass on direct peroral cholangioscopy.
최근에는 풍선도관의 조작부를 잘라도 풍선이 유지되는 풍선도관이 개발되어 ERCP를 통해 풍선도관을 간내담관이나 협착 상부에 위치시켜 고정한 후, 풍선도관 조작부를 절단하고 십이지장경을 제거한 다음, 고정된 풍선도관을 따라 극세경 내시경을 삽입하여 담도내시경 검사를 시행할 수 있다. 극세경 내시경을 삽입하는 도중 지지하는 풍선도관이 담관에서 이탈될 위험이 적어 쉽고 안전하게 담도내시경 검사를 시행할 수 있다[27]. 또한 풍선도관과 같은 보조기구의 도움 없이 직접 내시경을 담관 내로 삽입하기 위해 내시경 선단에 이중 굴곡 기능을 갖는 극세경 내시경이 직접 경구적 담도내시경 검사를 위해 개발되고 있다[28,29].
결 론
상부위장관 조영술과 대장조영술 대신 위내시경 검사와 대장내시경 검사가 보편화되면서 위장관 질환의 진단 및 치료에 있어서 많은 진보가 있었던 것과 같이, 담도내시경 검사는 ERCP의 한계를 넘어서는 진단 및 치료적 발전을 가져올 수 있다. 현재까지도 ERCP가 담도 질환에 대한 진단 및 치료적 내시경 검사의 기본적이고 주요한 방법이지만, 경구적 담도내시경 검사는 진단이 어려운 담관 협착의 진단과 치료가 어려운 담관 결석의 치료에 매우 유용한 방법으로 자리잡고 있으며, 일반적인 영상 검사와 ERCP를 통해 진단이 어려운 미세한 담관병변이나 조기 담관암 등이 담도내시경 검사를 통해 진단될 수 있다. 과거 일부 기관에서 제한적으로 시행되어 오던 경구적 담도내시경 검사는 최근까지의 발전을 통해 그 접근성이 매우 확대되어 왔으며, 향후 그 추이를 주목할 만 하다.