로마 기준 IV 이해하기: 로마 기준 IV 개정의 배경
Understanding the Rome IV: Background to the Rome IV Revision
Article information
Trans Abstract
Functional gastrointestinal disorders (FGIDs) are common and may be serious. As such disorders are identified principally on the basis of their symptoms, symptom-based classifications assume great importance. The Rome diagnostic criteria for FGIDs are widely used in both research and practice. Over time, the criteria have been revised as new data accumulate; the Rome IV criteria were recently released. The changes from the Rome III criteria principally reflect the data of literature reports and committee recommendations based on all available evidence. Here, we offer a historical perspective and discuss the Rome IV changes.
서 론
소화기 질환은 기질적 질환(organic disorder), 운동 질환(motility disorder), 기능성 질환(functional disorder)으로 분류할 수 있다[1]. 기능성 위장관 질환(functional gastrointestinal disorder)의 증상에 따른 분류는 연구 및 진료를 위하여 증상을 근간으로 하는 표준화된 진단기준(symptom-based criteria)이 필요하여 로마 위원회(The Rome committee)에서 만들기 시작하였다. 소화기 증상으로 내원하는 환자들은 혈액 검사, 영상, 내시경 및 조직검사 등의 결과를 토대로 진단하고 설명하는 과정을 가진다. 실제 임상에서 다양한 검사 방법들을 이용해도 구조적 원인을 찾을 수 없거나 원인을 찾아도 환자의 증상을 설명하기 어려운 경우를 빈번히 경험한다. 이와 같이 만성 재발성 위장관 증상이 있지만 다양한 검사를 이용한 진단 과정의 노력에도 증상을 설명하지 못하는 경우를 기능성 위장관 질환으로 정의한다.
기능성 위장관 질환은 1980년대 후반까지도 병태생리, 분류, 환자 치료 및 연구를 위한 가이드라인이 존재하지 않았지만 과민성 장증후군의 진단을 위한 위원회가 만들어져[2] 로마 기준(Rome criteria)을 만드는 시작점이 되었다. 이후 식도, 위 및 십이지장, 장, 담도, 항문 및 직장의 해부학적 구조를 근간으로 기능성 위장관 질환의 진단기준이 처음으로 만들어진[3] 후 2006년에 새로운 과학적 근거를 중심으로 한 로마 기준 III이 만들어졌다[4]. 이러한 과학적 분류는 약제 및 임상 연구의 적용에 표준화된 진단기준으로 널리 이용되었다. 이후에도 꾸준한 제약회사의 재정적 도움, 미국 식품의약국에서 약제 연구를 위한 과학적인 진단기준의 필요성 제안, 새로운 연구 방법의 발전에 따라 최신지견이 포함된 로마 기준 IV가 델파이 방법(Delphi method)에 의해서 10년 만에 발표되었다[5]. 이는 환자의 질병을 생의학(biomedical) 관점과 임상 관찰 사이의 차이점을 설명하고 생의학과 정신 사회적 인자 사이의 관계 융합 및 추후 생물정신사회적 모델(biopsychosocial model)에 의한 평가를 포함한 다양한 연구 방법을 하나로 묶어 다중 접근할 수 있는 구조를 제시해 주고 있다. 본고에서는 로마 기준 IV 개정의 배경과 변경된 내용의 흐름에 대하여 기술하고자 한다.
생물정신사회적 모델과 로마 기준 IV
기능성 위장관 질환에 대한 인식과 연구의 발전은 자연과학 및 질병(disease) 설명 모델의 변화와 연관되어 있다. 1637년 Descartes가 제안한 이원론(dualism), 즉, 몸과 마음이 분리될 수 있다는 개념이 발표된 이후 신체와 정신을 구분하는 철학적 접근과 동시에 의학 분야에서도 신체와 정신을 구분하여 접근하게 되었다. 이는 이후의 과학적 사고 방법의 변화와 질병의 이해에 많은 영향을 주었고 행동 및 정신 질환 연구의 시발점이 되었다. 1800년대 초 의학에서 정신과의 분리, Pasteur의 미생물의 발견과 Koch의 질환의 germ theory가 발표된 후 의학이 생물학적 관점으로 이동되었지만, 19세기에 질환(illness)과 질병의 설명을 위한 새로운 모델을 제시하려는 시도가 있었다. 20세기 초에서 중반까지 스트레스를 받으면 장의 운동에 문제가 생기고 화가 나면 위 발적 및 운동과 분비기능 항진, 두려움 및 우울할 때 점막이 창백해지고 분비 및 운동 기능의 감소가 일어난다는 동물과 인체 대상 연구가 시작되어 감정과 환경의 자극에 위장관의 반응이 일어남에 대한 과학적 근거를 제시해 주었다. 의학기술이 발전되면서 1960년대에는 질병 설명의 모델이 생의학적 관점에서 많은 연구가 이루어지게 되었고 1970년대 초에 장관의 전기생리학 검사가 가능해져 식도 운동 질환(아칼라시아, 공피증), 과민성 장증후군에서 통증과 장관 기능 이상의 기전, 즉 스트레스, 호르몬, 지방 식이가 장관 운동을 증가시키고 증상 유발과 연관성이 있다는 가설이 제시되었다. 1970년대 후반에 구체적인 장관 운동 관련 생물 표지자(biomarker)를 제시하였지만 이는 후속 연구들에서 증상과의 연관성이 높지 않음을 보고하여, 생의학적 관점의 기관, 세포, 호르몬 등의 세부적인 변화에 대한 연구 결과가 기능성 질환의 증상을 모두 설명할 수 없으며 장관의 기질적 이상 외에 다른 인자가 관여함을 시사하였다[1]. 즉 1960-70년대에는 기능성 위장관 질환의 병인을 생물학적 원인(biological causes)에서 찾았지만 환자의 증상을 설명하는 데 한계가 있었고, 1980년대 초 질환의 정신 사회적 이해가 발전하면서 1977년 정신과 및 내과의사인 Engel에 의해 생물정신사회적 모델이 제시되었다[6-8].
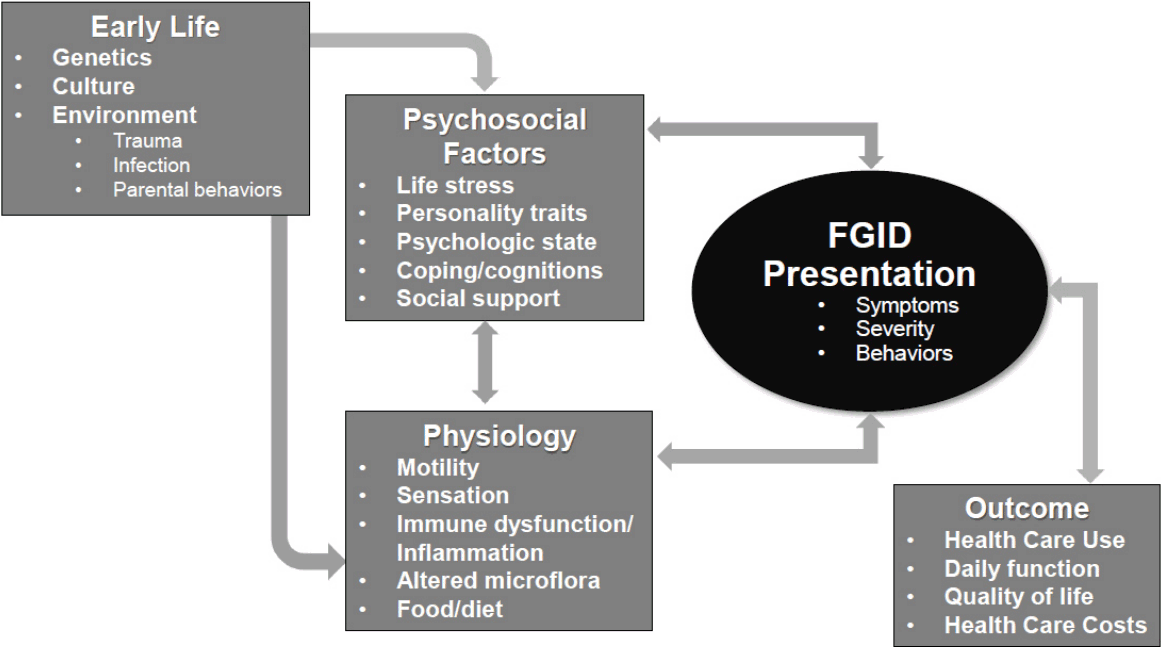
1980년대부터 기능성 위장관 질환에 대한 의사들의 인식이 확대되고 생의학적 모델로 설명되지 않고 증상으로 진단이 가능한 기능성 질환에 대한 정의와 진단 분류 체계에 대한 합의가 필요하였다. 미주 및 유럽의 전문가들이 1987년 조직을 결성하고 1988년 로마에서 처음 진단기준을 논의하였으며, 초기에는 매우 적은 수의 연구 결과만으로는 진단기준을 개발하기 어려워 델파이 방법으로 전문가들의 합의 과정을 기초로 기능성 위장관 질환에 대한 진단기준을 정하였으며[3,9], 이를 보완하여 1994년 로마 기준 I을 출판하였다[10]. 이후 과학기술의 발전에 따라 장관의 구심성 신호의 측정, 신경자극 및 기록, 통증 인지 평가, 신경세포와 면역 기능의 연관 관계 평가가 가능해졌다. 또한 뇌 기능 평가가 가능해져 뇌-장 축(brain-gut axis)의 연관성을 객관적으로 평가할 수 있게 되었고, 1999년에 로마 기준 II에서 신경소화기학(neurogastroenterology)이란 용어가 사용되었다[11,12]. 이는 기능성 위장관 질환에 대한 생물정신사회적 모델의 구조적, 생리적 연관성의 연구에 많은 영향을 주었다. 최근 개정된 로마 기준 IV에서 제시한 기능성 위장관 질환의 생물정신사회적 모델은 그림 1과 같다[1]. 이는 로마 기준 III의 근간을 유지하면서 생애 초기의 문화와 외상, 감염, 부모의 행동 등의 환경 요인을 포함하였다. 정신사회적 인자는 성격 특성 및 인지가 추가되었고, 생리학적 인자는 면역 이상과 음식이 추가되었다. 기능성 위장관 질환의 표현은 증상이 발생하면 의사를 방문한다는 항목 대신 건강관리 이용(health care use)으로 변경하였고 건강관리 비용(health care cost) 측면을 추가하여 근거가 확립된 새로운 내용을 보강하였다.
로마 기준 IV 분류 및 변경 내용
분류의 근간은 로마 기준 III와 마찬가지로 생리학적 현상보다는 주로 증상을 기준으로 만들어졌고, 해부학적 분류에 의해 식도에서 항문 및 직장까지 성인 33개, 소아 20개의 영역으로 나누었다(Table 1) [1].
위장관 질환에서는 narcotic bowel syndrome (opioid-induced gastrointestinal hyperalgesia) 및 opioid-induced constipation, 위-십이지장 질환에 cannabinoid hyperemesis syndrome의 진단기준이 새로 추가되었다. 본 질환들은 기존의 기능성 위장관 질환과는 다르고 원인 인자가 확실하기에 진정한 기능성 질환은 아니지만 증상의 발현이 장-뇌 상호작용에 의해서 발생하기 때문에 추가한 것으로 설명하고 있다.
기능 즉 functional이라는 문구를 제거하려는 노력을 하였고 기능성 위장관 질환에 장-뇌 상호 연관 질환(disorders of gut–brain interaction)이라는 부제를 추가하였다. 예를 들어 식도의 경우 functional esophageal disorder를 esophageal disorder로 functional abdominal pain syndrome를 centrally mediated abdominal pain syndrome으로 변경하였다. 하지만 기능성 설사(functional diarrhea)와 기능성 가슴쓰림(functional heartburn)의 경우는 구조적 문제에 의한 질환과 증상이 비슷하고 감별하기 위해 그대로 두었다.
새로운 연구 분야의 결과에 관한 논문을 새로 포함하였다. 장내 미생물, 음식, 영양과 위장관 기능에 관련된 내용, 약제에 대해서는 유전학적인 내용, 나이, 성, 여성의 건강, 문화적 내용을 두 개의 논문으로 나누었다. 정신 사회학적 내용은 생물정신사회학적인 내용으로 변경하였고 기능성 복통 증후군을 centrally mediated abdominal pain syndrome으로 변경하였다.
진단을 위한 증상 설문지의 역치 및 증상 횟수의 변화를 주었다.
위식도역류 연관 근거, 즉 내시경, 24시간 보행성 식도 산도 검사, 증상과의 연관성, 양성자펌프억제제 검사에서 음성인 경우를 기능성 가슴쓰림으로 로마 기준 III에서 분류를 하였지만, 임상적으로 생리학적 역류를 보이는 경우에서도 감각이 예민하여 가슴쓰림을 유발할 수 있는 reflux hypersensitivity를 새로 추가하였다.
과민성 장증후군의 경우 1개월에 3일에서 평균적으로 최소 주 1회로 횟수의 변화가 있고 복통 및 복부 불편감에서 복부 불편감을 삭제하고 복통이 있는 경우로 변경하였다. 또한 배변으로 상기 증상이 호전된(improvement) 경우에서 연관된(related) 경우로 변경되었고, 증상과 함께(onset) 배변 횟수와 형태의 변화와 관련된 경우에서 증상과 함께라는 문구를 삭제를 하였다. 또한 기능성 위장관 질환은 임상적으로 증상이 스펙트럼으로 존재할 수 있음을 인정하였다. 즉 변비와 변비형 과민성 장증후군 간에는 시간이 지남에 따라 서로 변화될 수 있다. 하지만 임상적 상황과는 다르게 약제의 연구 및 효능을 확인하기 위해서는 명확한 진단기준이 필요하기에 특정한 증상을 중심으로 한 기준을 제시하였다.
증상의 아형 분류 체계는 Bristol Stool Form Scale을 이용하여 나누는 4가지 아형은 그대로 유지하였지만 변비형과 설사형의 경우 전체 배변 중 25% 이상에서 형태의 변화가 있는 경우에서 증상이 있는 배변과 관련된 변의 형태가 25% 이상으로 변경하여 미분류 과민성 장증후군의 아형이 현저히 줄었다. 임상 약제의 연구를 할 때에는 매일 배변일지를 작성하여 25%의 기준을 가지고 최소 2주간의 배변 형태를 평가해야 한다.
기존의 chronic idiopathic nausea와 functional vomiting을 하나로 묶어서 chronic nausea and vomiting syndrome으로 새로운 진단을 만들었다.
결 론
최근 개정된 로마 기준 IV는 기존 로마 기준 III의 전반적인 근간을 유지하면서 기존의 진단기준에 비해서 새롭게 밝혀진 근거를 추가하여 개정되었다.
소화기 증상은 기질적, 운동 및 기능성 질환 사이에 서로 중복될 수 있고, 기능성 질환 간에도 중복 증상이 나타날 수 있는 등 다양한 형태로 발현되기 때문에 임상에서 본 기준을 이용하여 진단 및 치료를 적용할 경우에는 제한점이 있다. 하지만 표준화된 내용을 중심으로 연구가 이루어져야 결과 해석 및 병태 생리를 이해할 때 지침이 될 수 있고, 새로운 신약 개발의 효과 판정에 가이드를 제시하여 환자의 치료에 도움을 줄 수 있다.