흉통을 호소하는 환자에 대한 접근법
Diagnostic Approach to Chest Pain
Article information
Abstract
흉통은 다양한 장기의 다양한 병리적 변화로 유발되는 증상으로서 흉통에 대해 접근할 때 많은 질환들에 대한 고려가 요구된다. 가장 큰 문제점은 진단이 지연되면 위중해질 수 있는 치명적인 질환들이 포함되어 있는 증상군이므로 먼저 중증응급 질환 여부를 신속하고 확실하게 밝혀낸다는 자세로 진료에 임해야 한다. 흉부-복부 CT 촬영이 가능한 환경에서는 감별진단에 많은 도움을 받을 수 있으며, 중증응급 질환이 확인되거나 진단이 모호한 경우에는 신속히 상급기관으로 이송하여 적절한 처치를 받도록 해야 한다.
임상 증례
65세 남자가 약 2주 전부터 시작된 앞가슴의 통증으로 심장내과 외래를 방문하였다. 평소 다니던 집 앞의 100미터 정도의 언덕길을 걸어 올라가다가 가슴이 아프고 숨이 차는 일을 겪기 시작하였으며, 과거력으로는 5년 전부터 고혈압, 고지혈증과 당뇨병으로 약물 치료 중이었다. 혈압, 맥박, 호흡수는 모두 정상이었으며, 이상 심음이나 호흡음은 청진되지 않았고 흉곽의 압통은 관찰되지 않았다.
진단의 단계
흉통은 의사를 방문하는 환자들이 흔하게 호소하는 증상으로서 통증으로 내원하는 환자들 중 복통(40.9%) 다음으로 흔한(15.6%) 것으로 보고된 바 있다[1]. 흉곽의 내외부와 인근에는 심장, 대동맥, 폐, 식도, 위, 간담도계, 피부, 골격계, 근육, 신경, 유방 등의 많은 장기 및 조직이 존재한다. 이러한 장기나 조직의 세포가 허혈이나 외상, 감염, 염증, 유전적 이상 등에 의한 손상을 받으면 질환이 발생하고 그 증상으로 흉통이 나타날 수 있다[2]. 특히 순환과 호흡을 직접적으로 담당하는 장기들이 모여 있는 흉곽의 특성 때문에 흉통의 유발 원인 중에는 생명을 위협하는 매우 위험한 질환들이 포함된다. 이 중에는 급성 관상동맥증후군(급성 심근경색증, 불안정협심증), 대동맥 질환, 폐동맥색전증, 심장눌림증, 긴장기흉, 급성 종격동염과 같이 진단과 치료에 소요되는 ‘시간’이 환자의 예후에 중대한 영향을 미치는 질환들이 있으므로, 흉통을 호소하는 환자를 만났을 경우에는 이러한 중증응급질환의 가능성을 반드시 염두에 두고 신속히 평가하고 대처해야 한다[3].
응급 질환과 비응급 질환의 감별
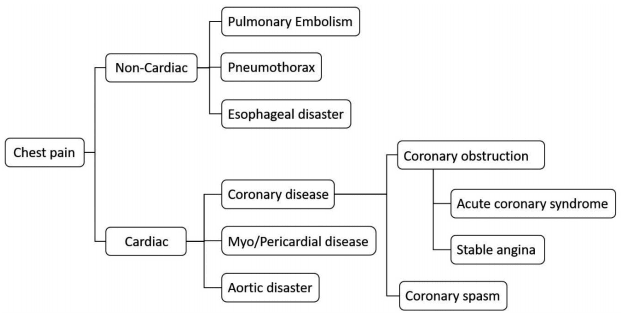
실제로 중증응급 질환에 의한 흉통 환자들이 ‘담결림’, ‘배탈’ 등으로 간과하여 의사를 찾기까지의 시간을 지체하거나, 첫 의료 접촉시 진단에 실패하여 안 좋은 예후를 초래하게 되는 증례들이 드물지 않게 발생한다[4,5]. 이러한 응급질환이 배제된 이후에는 사망이나 장애 발생의 위험이 적으므로 시간을 가지고 진단과 치료에 임할 수 있다. 따라서, 흉통을 호소하는 환자에 대해 초기 접근할 때는 중증응급 질환을 감별하는데 우선적으로 집중해야 한다(Fig. 1).
진단의 일차 단계
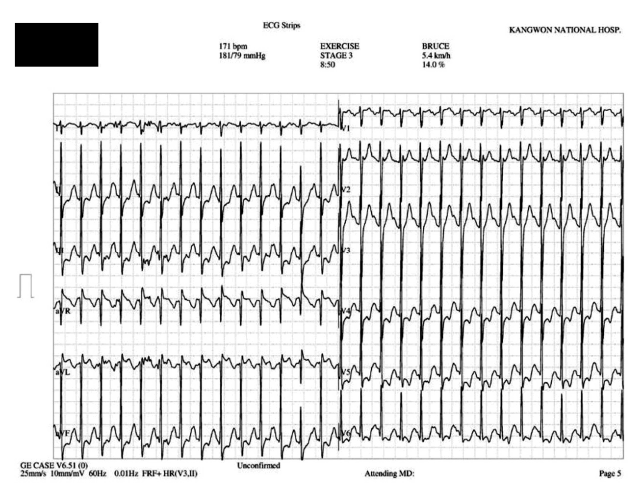
이 환자는 급성 관상동맥증후군의 가능성이 의심되어 입원 조치하였다. 흉부 X선 촬영과 심전도에서는 이상 소견이 관찰되지 않았다. 운동할 때 흉통과 호흡곤란을 호소하기에 허혈심장병을 의심하여 시행한 심근효소 검사 수치는 troponin-I가 0.1 ng/mL (정상범위 0-0.1), CK-MB가 2.4 ng/mL (정상범위 0-5)로서 상승 소견은 관찰되지 않았다. 심장초음파검사에서도 국소적 벽운동 이상, 좌심실 기능 이상이나 판막의 이상은 관찰되지 않았다. 부하 검사로 시행한 답차 검사(treadmill test) 중에는 3단계에서 흉부 불편감을 호소하였으며 심전도의 lead II, III, aVF와 V4-6에서 유의미한 ST분절하강 소견이 관찰되어 검사를 중단하였다(Fig. 2). 상부위장관 내시경 검사에서는 만성 표재성 위염이 관찰되었다.
최종진단과 치료 경과
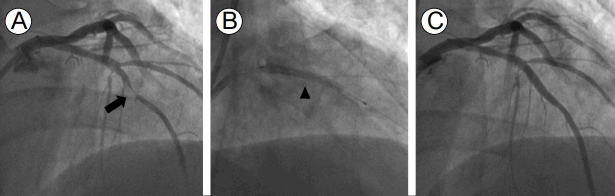
관상동맥협착증에 의한 불안정협심증이 강력히 의심되어 관상동맥조영술을 시행하였고, 좌전하행동맥(left anterior descending artery) 중위부의 심한 협착이 확인되어 약물용출성 스텐트를 사용한 경피적 관상동맥성형술(percutaneous coronary intervention, PCI)을 시행하였다(Fig. 3). PCI 이후 흉통은 소실되었으며 고혈압, 고지혈증과 당뇨병에 대한 약물 치료에 더해 aspirin과 clopidogrel을 병행한 이중 항혈소판 치료(dual antiplatelet therapy)를 유지하였고, 1년이 경과 후 clopidogrel만 중단하고 나머지 약물 치료를 유지 중이다.
고 찰
본 증례와 같은 급성 관상동맥증후군(급성 심근경색증, 불안정협심증)에 더하여 대동맥박리증, 폐동맥색전증, 심장눌림증, 긴장기흉, 급성 종격동염 등은 치명적 예후를 초래할 수 있는 대표적인 흉통 유발 질환이다. 이 중 ST분절 상승형 급성 심근경색증, 심장눌림증, 기흉, 급성 종격동염은 일차 진료에서 대부분 적용 가능한 심전도 검사와 X선 촬영만으로도 진단이 가능하지만 대동맥 질환이나 폐동맥색전증은 심전도나 X선 사진에서는 이상 소견을 보이지 않는 경우가 빈번하다. 또한, 이 질환의 환자들이 항상 전형적인 증상만을 보이지는 않는다는 점도 진단에 어려움을 초래한다[4]. 이러한 흉통 유발성 중증응급 질환 각각에 대한 진단적 접근은 다음과 같다.
급성 관상동맥증후군(acute coronary syndrome, ACS)
허혈심장병의 특징적인 증상은 운동으로 유발되거나 악화되는 흉골하부의 조이거나 누르는 듯한 흉통으로서 목, 아래턱이나 왼팔로 뻗치는 방사통이 동반되기도 한다. 이 중 ACS는 급사 및 심부전증 등의 후유 장애를 유발할 수 있어 신속한 진단과 치료가 요구된다. 관상동맥이 완전 폐색되어 발생하는 ST분절 상승형 심근경색증(ST-segment elevation myocardial infarction, STEMI)은 휴식으로도 흉통이 완화되지 않고 20분 이상 지속되는 경우 의심해야 한다. 관상동맥이 불완전 폐색되어 혈류가 부분적으로 유지되는 경우에는 ST분절 비상승형 급성 관상동맥증후군(non ST-segment elevation acute coronary syndrome)으로 발현하게 되며 이에는 ST분절 비상승형 심근경색증(non ST-segment elevation myocardial infarction)이나 불안정협심증(unstable angina, UA)이 포함된다. UA는 휴식 중에 흉통을 겪거나 흉통을 겪기 시작한 기간이 2주 이하이거나 증상이 점차 심해지는 양상을 보이는 특징으로써 안정협심증(stable angina)과 구분되며 급성심근경색증의 발생이 임박하였다는 경고이므로 즉각적인 진단과 치료를 요한다[6]. ACS가 의심되는 환자들에게는 반드시 심전도 검사를 시행해야 하며, 특히 고령자의 흉부 불편감이나 복부 불편감 등을 ‘소화불량’등으로 간과해서는 안된다. STEMI의 경우에는 심전도에서 특징적인 ST분절 상승 소견이 관찰되므로 진단이 어렵지 않지만 후벽경색의 경우에는 ST분절 상승 대신 V1-2 유도에서 ST분절 하강과 QRS복합(complex)의 R/S파 비율 반전이 나타나며, 기존에 좌각차단이 있던 환자이거나, 전벽경색이 심해서 심실중격의 전도계가 손상되어 좌각차단이 발생한 경우에는 ST분절이 왜곡되어 상승이 나타나지 않기도 한다[7]. 이러한 경우는 진단이 늦어져서 예후가 악화되므로, 흉통이나 호흡곤란을 호소하는 환자의 심전도를 평가할 때는 각별한 주의가 필요하다. 또한, ACS의 증상으로 전형적인 흉통 대신 호흡곤란, 구역질, 구토, 발한, 실신 등만 나타나는 경우도 있어 진단에 혼선을 빚게 되며, 이러한 현상은 주로 노인에서 빈발한다[8]. UA의 경우 휴식기에는 신체 검사, 심전도, 심초음파 검사 소견, 심근효소수치의 이상이 관찰되지 않아 병력청취만으로 판단해야 하는 경우가 많다. 이렇듯 ACS의 진단에 혼란을 주는 여러 변수들이 있으므로 특히 호흡곤란이 동반된 흉통 환자는 관상동맥질환 처치가 가능한 전문기관으로 의뢰하는 것이 안전하다.
대동맥박리(aortic dissection, AD)
AD는 적절한 진단과 치료에 실패할 경우 대동맥파열이나 주요혈관 폐색으로 인해 사망이나 후유 장애의 발생위험이 매우 높은 질환이다. 상행대동맥이나 하행대동맥 중 침범되는 부위와, 영향을 받는 분지혈관의 위치에 따라 증상과 신체 검사 소견이 달리 나타난다. 흉통은 90% 이상의 급성 AD 환자가 호소하는 주요 증상으로 가슴과 등에 갑자기 찢어지는 듯한 심한 통증이 시작되는 것이 특징이다[9]. 박리가 중단되면 통증도 잦아들며 박리가 다시 진행되면 통증도 다시 시작된다. 흉통에 더해 구역질, 구토, 실신, 발한도 나타날 수 있으며 주요혈관의 침범으로 인해 급성 뇌졸중의 증상이 발생하기도 한다. 척수동맥이나 하지동맥의 침범 시에는 하지마비나 약화가 관찰된다. 신체 검사에서는 특이 소견이 나타나지 않는 경우도 많지만 혈압상승이 흔하게 나타나며, 특히 양측 팔이나 양측 하지 간의 맥박이나 혈압이 차이가 나는 경우에는 강력히 의심해 볼 수 있다[10]. 반면, 심장눌림증이나 흉강내 대동맥파열 시에는 저혈압이나 쇼크가 관찰된다. 근위부 박리 시에는 대동맥판막 지지구조의 붕괴로 인한 대동맥판부전증이 발생하여 이완기 심잡음이 청진될 수 있다. 무명동맥이나 경동맥의 침범 시에는 마비, 약화, 의식저하 등의 신경학적 이상 소견이 나타난다. X선 촬영에서는 종격동 비대 소견이 나타나기도 한다. 컴퓨터단층촬영(computed tomography, CT)의 보급이 보편화되어 있는 우리나라의 상황에서는 AD가 의심되는 상황이라면 진단은 어렵지 않다. CT촬영으로 AD 진단의 민감도와 특이도가 거의 100%에 달하기 때문이다[11]. 그 외 혈관조영술, 경식도 심초음파 검사 등도 사용이 된다. AD 역시 의증으로 떠올리면 진단이 어렵지 않은 질환이므로 급성 흉통 환자에서 반드시 염두에 두어야 하고 의심이 되거나 확인 후에는 진단과 치료가 가능한 기관으로 즉시 이송이 필요하다.
폐동맥색전증(pulmonary embolism, PE)
PE 역시 치명적이어서 치료를 안 할 경우 18% 정도가 사망하며 이는 치료가 시행된 환자의 7배에 달하는 사망률로 보고된 바 있다[12]. 주로 급성으로 나타나는 흉막성 흉통을 비롯하여 호흡곤란, 두근거림, 어지러움, 실신 등이 증상으로 나타나지만 비특이적이다. 신체 검사 소견도 활력 징후의 변화, 빈맥, 빈호흡, 흉막마찰음이나 수포음 등이 관찰될 수 있지만 진단율은 낮다[13]. 특히 기저 질환으로서 만성 폐색성 폐질환, 폐렴, 울혈성 심부전 등이 있는 경우에는 진단이 더욱 어려워진다. 위험 인자는 혈전성향(thrombophilia), 고령, 항인지질항체 증후군(anti-phospholipid syndrome), PE의 병력, 거동 장애, 악성 종양, 심부전, 비만, 신증후군, 흡연, 하지정맥류, 중심정맥관 거치, 인공박동조율기 삽입, 호르몬 치료, 장거리여행, 경구피임약복용, 임신, 수술, 외상 등으로 다양하며 이러한 위험 인자가 많은 환자가 호흡곤란 및 흉통을 나타낼 때에는 PE의 가능성을 반드시 염두에 두어야 한다. Wells criteria나 revised Geneva score 등이 PE의 가능성을 임상적으로 예측하는 모델로 사용되고 있으나 정확도는 여전히 제한적이다[14,15]. PE에서는 혈전의 생성과 제거의 과정이 체내에서 진행되므로 섬유소의 분해물질인 D-dimer의 혈중농도 상승이 특징적으로 나타나며 음성예측도(negative predictive value)가 거의 100%로 탁월하여 낮은 D-dimer 수치로 PE의 배제가 가능한 수준이다. 다만 특이도는 낮아서 감염이나 염증, 악성 종양, 수술, 외상, 화상, 멍, 허혈심장병, 뇌졸중, 말초동맥 질환, 대동맥 질환 등에서도 상승할 수 있다[16]. 흉부 CT는 PE의 진단에도 매우 유용하며 성능이 지속적으로 개선되고 있어 D-dimer 측정과 병용하면 진단율을 더욱 높일 수 있다[17]. PE는 심부정맥혈전증(deep vein thrombosis)과 합병되는 경우가 많으므로 하지부종이 동반된 호흡곤란이나 흉통 호소 환자에서는 반드시 고려해야 할 질환이고 흉부 CT 촬영시 하지정맥조영 CT도 같이 진행할 필요가 있다. PE는 흉통 유발 질환들 중에서도 진단이 쉽지 않지만 임상적 예측모델과 D-dimer 측정, CT 촬영을 병행하면 성공적인 진단이 가능하다.
심장눌림증(cardiac tamponade), 기흉(pneumothorax), 종격동염(mediastinitis)
심장눌림증, 기흉, 종격동염 등도 치명적인 질환이지만 간단한 흉부 X선 촬영만으로도 진단이 용이하다. 심낭삼출액의 축적에 의해 심장의 이완과 충만이 방해를 받는 심장눌림증은 X선 사진에서 공모양의 둥글고 확장된 심장 음영(globular heart)이 특징이다. 기흉은 폐혈관음영이 존재하는 폐부와 혈관음영이 없는 흉강의 경계선이 관찰되며 긴장기흉의 경우에는 심장음영의 편향이 보이기도 한다. Boerhaave’s syndrome 등 식도천공으로 발생하는 급성 종격동염의 경우에는 종격동기종(pneumomediastinum)이 관찰될 수 있으나 이환 초기에 촬영된 경우에는 15-25% 정도에서 정상 소견을 보이므로 유의해야 한다[18]. 이들 질환에서도 진단이 모호할 경우에는 역시 CT 촬영이 큰 도움이 된다.
기타 흉통 유발 질환들
위에 설명한 치명적인 응급 질환들 외에도 흉통을 유발하는 질환으로는 심장막염을 비롯해 비대심근병, 역류성 식도염, 흉막염, 소화성 궤양 질환, 공황 장애, 간담도 질환, 췌장 질환, 경추간판 탈출증, 신경성 통증, 신체화 장애, 심리적 통증 장애 등의 다양한 질환이 있다[3]. 이 질환들도 악화되면 잠재적 위험을 가질 수 있으나 응급 질환은 아니므로 해부학적 구조와 장기별로 발생 가능한 병리현상의 조합을 생각해 접근할 수 있다.