비후성 심근병증 환자에 동반한 완전 폐색을 보이는 심근교에 대한 스텐트 삽입술 후 10년간의 임상 경과
A Totally Occluded Long Segment Myocardial Bridge: 10-year Follow-up after Percutaneous Coronary Intervention in a Patient with Hypertrophic Cardiomyopathy
Article information
Abstract
본 증례는 갑자기 악화된 흉통으로 내원한 환자에서 시행한 초음파에서 비후성 심근병증이 발견되어 이에 대한 약물 치료를 하였으나 증상이 완화되지 않았고, 심근허혈이 의심되어 시행한 관상동맥조영술에서 긴 길이의 완전 폐색을 동반한 심근교가 관찰되어 혈관내 초음파 유도하 중재술을 시행하였던 예이다. 시술 후 증상은 호전되었고, 약물 치료하면서 10년간 좋은 임상 경과를 보여 보고하는 바이다.
Trans Abstract
Intracoronary stent implantation can improve coronary hemodynamics and myocardial ischemia in patients with symptomatic bridging. However, percutaneous coronary intervention for this lesion is limited due to the high prevalence of restenosis and risk of complications. We present a case of a totally occluded long-segment myocardial bridge in a patient with hypertrophic cardiomyopathy who was successfully implanted with a bare metal stent under intravascular ultrasound guidance without complications. The patient has been free of ischemic symptoms with stent patency for 10 years.
서 론
심근교는 관상동맥이 근육 안으로 지나가는 행로를 보이는 것을 말한다. 관상동맥은 심실 수축기에 주로 눌리게 되고 이완기에 풀리게 된다. 심장 관류의 3분의 2가 이완기에 나타나기 때문에 심근교는 대개 큰 문제를 일으키지 않는다. 하지만 2 cm 이상 긴 심근교는 심근의 허혈 및 관상동맥의 혈전, 혹은 돌연 심장사를 유발할 가능성이 있다[1].
본 저자들은 비후성 심근병증 환자에 동반한 완전 폐색을 보이는 3 cm 정도의 매우 긴 심근교 환자에서 약물에 반응하지 않은 지속적인 흉통이 있어, 혈관내 초음파를 이용하여 성공적으로 스텐트 삽입술을 시행하여 흉통이 호전되고 10년간 좋은 임상 경과를 보인 예를 경험하였기에 보고하는 바이다.
증 례
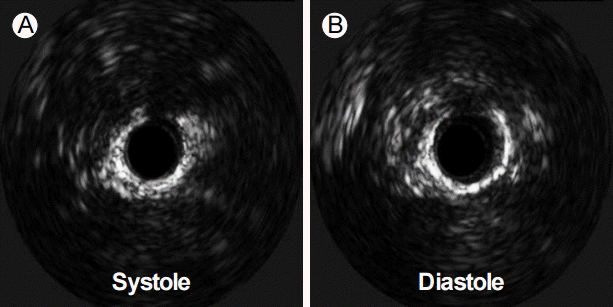
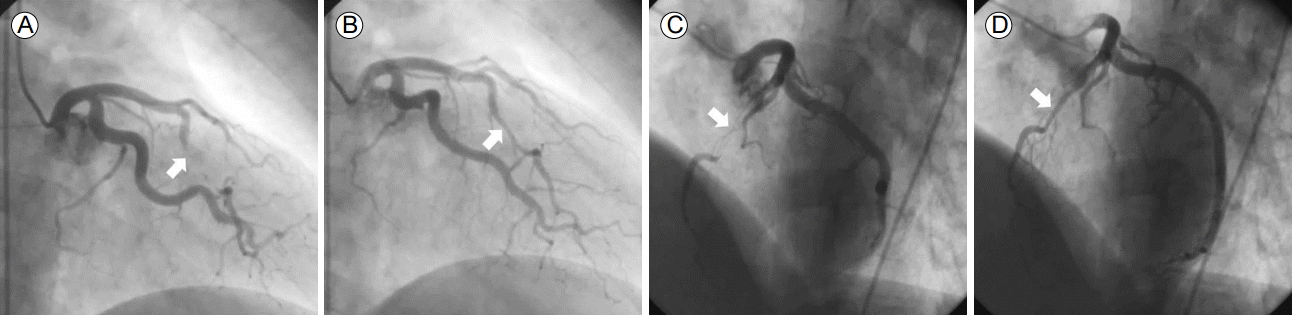
40세 남자가 휴식 상태에 발현한(Canadian Cardiovascular Society class III-IV) 식은땀과 함께 쥐어짜는 양상의 전흉부 통증을 주소로 내원하였다. 3개월 전에는 보다 약한 강도의 통증이 악화와 호전을 반복하였으나 내원 1시간 전부터는 호전이 되지 않고 지속적으로 통증이 발생하였다. 내원시 혈압은 110/60 mmHg였고 심박수는 120회였으며 심음은 규칙적이었으며 심잡음은 들리지 않았다. 특이 병력은 없었으며 20갑년의 흡연력이 있었다. 심전도는 동성빈맥을 보였으며 ST-T파의 변화 소견은 없었다. 단순 흉부 사진과 혈액 검사에서 특이 소견은 없었다. 심초음파에서 심실 중격이 17 mm 정도로 두꺼워져 있었으며, 좌심실 유출로의 폐쇄가 관찰되었고 최대 속도는 3.5 m/sec 정도였다. 입원하여 3일간 베타-1 선택적인 베타차단제인 atenolol을 점차 증량하며 관찰하였으나, 증상은 호전되지 않았고 운동 부하 심전도에서 1 mm 정도의 ST 분절 하강이 V4-6에서 관찰되어 관상동맥조영술을 시행하기로 하였다. 관상동맥조영술에서 3 cm 이상의 좌 전하행지 중위부 혈관 분절이 수축기에 완전히 폐색되고 이완기에 50% 정도의 협착을 보이는 심근교가 관찰되었다(Fig. 1). 혈관내 초음파를 시행하였을 때 수축기에는 초음파 도자를 완전히 감쌀 정도의 심한 압박이 관찰되었고, 이완기에는 완화가 지연됨을 관찰할 수 있었다(Fig. 2). 초음파를 이용하여 병변의 길이와 혈관의 직경을 구한 후, 3.5 × 20 mm의 풍선을 이용하여 넓히고 3.5 × 32 mm의 일반 금속 스텐트를 삽입하였다(Express®, Boston Scientific Corp, Natick, MA, USA) (Fig. 3A). 스텐트 삽입 후 시행한 혈관내 초음파에서 스텐트의 적절한 혈관내 안착과 팽창을 확인하였고, 스텐트 경계면에 박리 등의 합병증이 없음을 확인하였다(Fig. 3B). 시술 후 시행한 좌심실조영술에서 심실 중앙부의 폐색 및 좌심실 유출로와 좌심실 간의 압력 차가 40 mmHg에 달함을 확인하였다(Fig. 3C and 3D). 시술 후 흉통은 완화되었고, 아스피린, 클로피도그렐 및 베타차단제를 처방하여 퇴원하였다.
Coronary angiogram showing long-segment systolic total occlusion in the mid-left anterior descending artery with 50% stenosis during diastole.

(A) Percutaneous coronary intervention was performed using a 3.5 × 32 mm bare metal stent (Express®; Boston Scientific Corp., Natick, MA, USA). (B) Intravascular ultrasound showing the well-expanded stent with good apposition. (C, D) A left ventricular angiogram showing mid-ventricular obstruction with a pressure gradient between the left ventricle and left ventricular outflow track (40 mmHg).
1년 후 추적 관상동맥조영술(2005년 8월 11일)에서 경미한 협착 소견만 관찰되었다. 추적 운동 부하 검사에서 예전에 관찰되었던 ST 분절 하강은 관찰되지 않았으며, 운동 능력 장애는 보이지 않았다. 약물 치료를 지속하면서 1년에 한 번씩 심초음파를 시행하면서 꾸준히 외래 추적 관찰을 시행하였다.
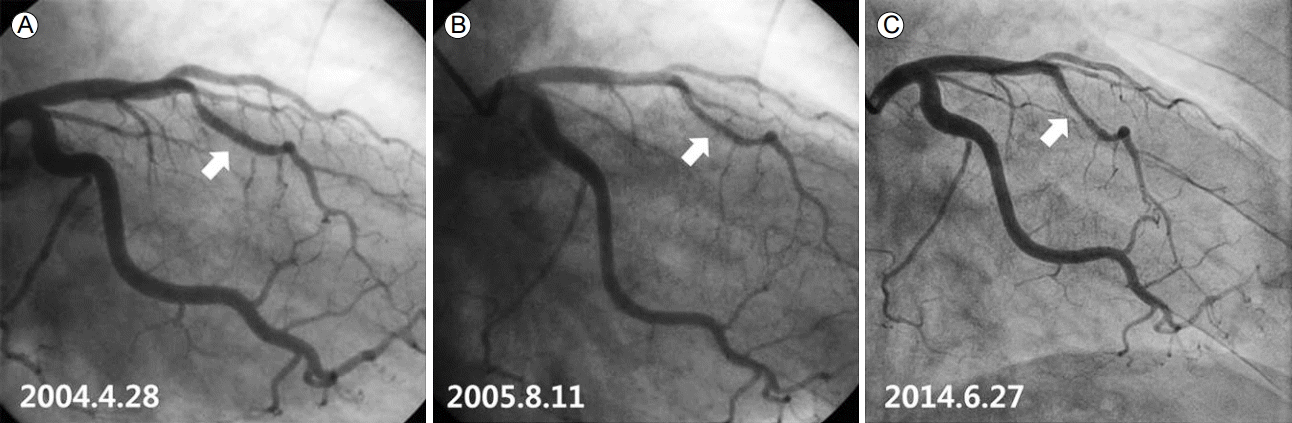
10년째 되는 해에 추적 관상동맥조영술을 시행하기 위해 내원하였다. 추적 검사(2014년 6월 27일)에도 경미한 협착만 보였고, 2005년에 시행한 영상과 비교하였을 때 저명한 변화는 관찰되지 않았다(Fig. 4). 이후 지속적인 외래 추적 관찰 중이다.
고 찰
심근교는 비후성 심근병증의 15-40% 정도의 환자에서 관찰되며, 비후성 심근병증 환자에서 심근교와 돌연사의 관계는 명확하지 않다[2,3]. 하지만 이러한 보고가 있다고 하더라도, 본 증례와 같이 3 cm 정도의 긴 병변에 나타나고 완전 폐색이 될 정도로 심한 협착으로 있다면 심장허혈 및 돌연사의 가능성을 배제할 수는 없다. 증상이 심한 심근교 환자에서 스텐트 삽입술을 하면 관상동맥의 혈역학 및 심근허혈을 호전시킬 수 있다는 보고들이 있지만[4,5], 여전히 이러한 시술은 선호되는 방법은 아니다. 그 이유는 심근교 환자에서 스텐트 삽입술 후 재협착과 합병증의 빈도가 비교적 높기 때문이다[6,7].
심근교에 대한 스텐트 시술 후 장기 임상 경과를 관찰한 대표적인 연구는 다음 두 가지가 있다[7,8]. 하나는 일반 금속 스텐트로 시술 후 2년간 경과 관찰을 하였다[7]. 36% 정도의 재협착을 보였지만 증상 완화를 관찰하였고 사망을 비롯한 심혈관 사건은 발생하지 않았다. 비교적 최근에 발표한 연구는 약물 용출 스텐트로 시술 후 5년간 관찰을 하였다[8]. 재협착은 일반 금속 스텐트를 사용한 경우와 비교하여 감소한 18.7%를 보였다. 1명에서 스텐트 삽입술시 관상동맥 파열로 인한 합병증을 경험하였으며 즉각적인 스텐트 삽입술을 통하여 회복하였다. 이 연구에서도 마찬가지로 5년간 증상 완화에 효과를 보였으며 재협착 이외의 사망, 심근경색증 등의 심장 사건은 관찰되지 않았다. 본 증례에서는 일반 금속 스텐트 삽입 후 10년간 유의한 재협착을 보이지 않았으며, 증상 완화를 보였고 다른 심장 사건 또한 보이지 않았다. 다만 본 증례의 시술 당시에는 약물 용출 스텐트가 도입되기 전이었기 때문에 일반 금속 스텐트의 재협착을 줄이기 위하여 혈관내 초음파를 유도 하에 시술을 진행하였으며, 이는 또한 시술 중 합병증을 예방하는 효과도 있다. 그 기전으로는 먼저, 병변의 길이와 혈관의 크기를 정확하게 측정하여 적절한 크기와 길이의 스텐트를 선택할 수 있어 혈관 파열을 예방할 수 있고, 병변을 정확하게 치료할 수 있다. 또한 시술 후 스텐트의 적절한 안착과 팽창 정도를 평가하여, 부족하다면 non-compliant 풍선 도자를 이용한 고압력의 추가 시술로 재협착과 스텐트 혈전증을 줄일 수 있다. 마지막으로, 시술 후 스텐트 전후방의 박리 등의 합병증을 조기 발견하여 치료할 수 있다[9,10].
본 증례와 같이 수축기에 완전 폐색되는 긴 길이의 심근교와 비후성 심근병증이 합병될 경우 이완기 장애를 초래할 수 있고 또한 심근 산소 요구량을 증가시킬 수 있다. 본 증례와 같이 이완기 초기에도 지속적으로 50% 이상의 협착을 보이는 경우에는 그 정도가 심할 수 있다(spill over phenomenon). 본 증례의 경우 심근효소가 증가하거나 심초음파에서 국소벽 운동 장애는 보이지 않았지만, 3일간의 약물 치료에도 반응하지 않았고 운동 부하 검사에서 심근허혈이 의심되었기 때문에 관상동맥조영술을 시행하였고, 긴 길이의 심근교를 발견하였다. 또한 심근교를 시술시 일반 금속 스텐트 삽입술의 합병증과 재협착을 줄이기 위해 혈관내 초음파 유도 하에 시술을 진행하였고, 시술 후 환자의 증상이 호전되었음은 물론 10년간 큰 문제없이 성공적으로 추적 관찰하였기에 보고하는 바이다.