대동맥박리에서 가강에 의해 장골동맥 폐색시 좌측 상완동맥을 통한 스텐트 시술
Type B Aortic Dissection with Malperfusion of Both Common Iliac Arteries That Underwent Stent Placement Using the Left Brachial Approach
Article information
Abstract
관류 장애를 동반한 하행대동맥박리의 경우 수술적인 치료 시에 높은 사망률을 보인다. 혈관내 시술은 수술의 대안으로 하지혈관폐색이 동반된 하행대동맥박리에서 좋은 임상 결과를 보여주었다. 이 증례는 가강에 의하여 진강이 눌려서 하지혈관폐색이 동반된 하행대동맥박리에서 양쪽의 대퇴동맥이 가강에서 기시하여서 스텐트 이식편 시술이 불가능하여서 좌측 상완동맥을 통하여 선택적인 스텐트 삽입술을 시행하여 하행대동맥과 양측 장골동맥의 혈류를 복원하였고 36개월 동안 경과 관찰시에 이상 소견 없이 유지되었다. 저자들은 하행대동맥박리에 동반된 하지혈관의 관류 장애 시에 좌측 상완동맥을 통한 선택적 스텐트 삽입술 치료로 효과적이고 안전하게 치료된 증례 1예를 경험하였기에 보고한다.
Trans Abstract
Malperfusion syndrome is a complication of acute descending aortic dissection (DAD) and it is associated with a poor clinical outcome. Surgical treatment for it has a high rate of mortality. Thoracic endovascular aortic repair (TEVAR) for DAD with malperfusion syndrome has resulted in good clinical outcomes. However, when both common iliac arteries are compromised by a false lumen, it is impossible to conduct TEVAR because there is no accessible artery. We successfully treated a case of DAD with malperfusion syndrome in which both common iliac arteries were compromised by placing stents in both arteries using the left brachial approach.
서 론
합병증을 동반한 급성 하행대동맥박리(acute complicated descending aortic dissection)는 치료하지 않을 경우 초기 사망률이 매우 높은 질환이다[1]. 특히 가강(false lumen)에 의해 진강(true lumen)이 눌려 상장간막동맥(superior mesenteric artery), 복강동맥(celiac trunk), 신장동맥(renal artery), 하지로 가는 동맥이 눌려져서 장, 신장, 간, 하지에 허혈(ischemia)이 발생하는 관류 장애(malperfusion)를 동반하는 하행대동맥박리(descending aortic dissection)의 경우 종종 생명을 위협하는데 관류 장애는 하행대동맥박리의 21%에서 나타나며, 관류 장애가 동반된 하행대동맥박리의 병원내 사망률은 46%까지 보고되고 있다[2].
합병증이 동반된 하행대동맥박리 환자에서 수술적 치료는 혈관내 시술(endovascular aortic repair)에 비해 나쁜 생존율을 보였고(사망률: 수술 33.9 % vs. 혈관내 시술 10.6 %) [1,2], 다른 연구에서도 약물 치료, 수술, 혈관내 시술로 치료한 환자의 사망률은 각각 9.6%, 32.1%, 6.5%로 혈관내 시술 성적이 수술보다 좋은 성적을 보였다[2].
합병증을 동반한 하행대동맥박리의 수술적 치료에 대한 대안으로 혈관내 시술이 소개되었으며, 3가지 정도의 방법이 치료를 위해 많이 사용된다. 스텐트 이식편(stent-graft) 삽입술, 분지혈관에 스텐트 삽입술(selective stenting in the compromised artery), 창냄술(fenestration)을 이용하여 목표 장기의 혈류를 회복시키는 시키는 치료가 시도되었다[1]. 3가지 방법 중에서 대동맥박리의 내막 파열(intimal tear) 부위를 찾아서 스텐트 이식편으로 진강에서 가강으로 가는 혈류를 차단하여 분지혈관으로의 혈류를 복원시키고 대동맥박리의 재형성(remodeling)을 유도하는 방법이 이상적이다. 그러나 스텐트 이식편을 시술하기 위해서는 적어도 하나의 대퇴동맥(femoral artery)과 장골동맥(iliac artery)이 진강에서 기시해야 한다. 양쪽 대퇴동맥과 장골동맥이 가강에서 기시한다면 스텐트 이식편을 시술할 수 있는 접근 혈관을 찾을 수가 없다. 이러한 경우에 좌측 상완동맥(left brachial artery)을 통하여 유도철선을 가강에 의하여 눌린 양쪽 장골동맥, 대퇴동맥의 진강으로 보낸 후에 스텐트 시술을 시행하면 성공적으로 혈류를 복원할 수 있다.
저자들은 급성 하행대동맥박리시 양쪽 장골동맥과 대퇴동맥이 가강에 의하여 눌려서 심한 하지허혈을 호소하는 환자에서 좌측 상완동맥을 통하여 성공적으로 양쪽 장골동맥에 스텐트 시술을 시행해 혈류를 복원하고 하지허혈을 개선한 뒤 36개월간의 추적 관찰 기간에서 잘 유지된 예를 보고한다.
증 례
환 자:35세 남자
주 소: 2시간 전 시작된 가슴 및 등 통증 이후 발생한 좌측 하지의 감각 저하, 색조 변화 및 통증
현병력: 5년 전부터 혈압이 높았으나 투약하지 않고 지내던 자로 2시간 전 시작된 가슴 및 등 통증 이후 발생한 좌측 하지의 감각 저하, 색조 변화 및 통증으로 타 병원에서 흉부 컴퓨터단층촬영(computerized tomography, CT)을 시행하였고 하행대동맥박리 소견을 보여 본원으로 전원되었다.
과거력: 5년 전 고혈압 진단 이후 투약은 하지 않았다.
가족력 및 사회력: 5갑년의 흡연력이 있는 흡연자이며 음주력은 없고 특이 가족력도 없었다. 평소 운동은 하지 않았으며 특별히 가리는 음식 없이 규칙적인 식습관을 가지고 있었다.
이학적 검사: 내원시 활력 징후는 혈압 170/100 mmHg, 맥박수 75회/분, 호흡수 20회/분, 체온 36.4도였다. 흉부진찰에서 심잡음은 들리지 않았고 정상 폐음 소견이었다. 복부 및 사지 진찰에서 양측 대퇴동맥은 잘 촉지되지 않았고 좌측 하지의 피부는 차가웠으며 청색으로 변해있었고, 심한 통증과 저린감을 호소하였다. Fontaine class III의 하지 통증을 호소하였다.
검사실 소견: 내원 당시 일반 혈액 검사 및 일반 화학 검사, 전해질 검사, C-반응단백질(C-reactive protein), 심근효소 검사에서 특이 소견이 관찰되지 않았다. 심전도에서 좌심실비대 소견 외 특이 소견은 보이지 않았고 흉부 X-ray에서 종격동 확장 소견이 관찰되었다(Fig. 1A).
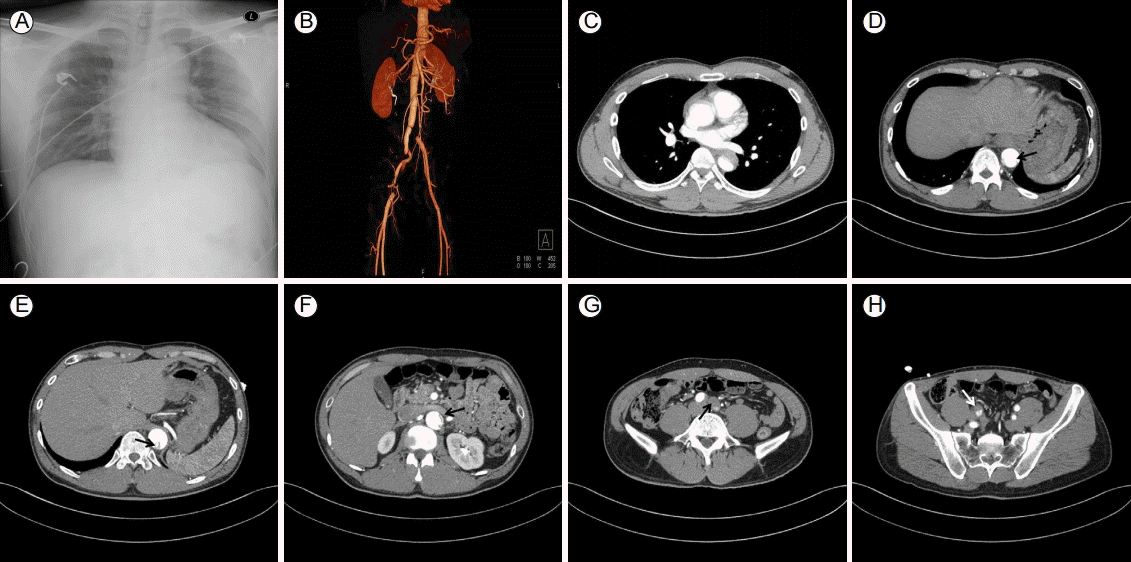
Baseline CT. (A) A chest X-ray shows mediastinal widening. (B) A 3D reconstruction image shows occlusion of the left common iliac artery and right external iliac artery. (C) Findings of intramural hematoma of the ascending aorta are observed. (D) The intimal tear site (black arrow) is located at the mid-thoracic aorta. (E) The true lumen (black arrow) of the descending thoracic aorta is severely compressed by the false lumen. (F) The true lumen (black arrow) of the abdominal aorta was collapsed by the false lumen. (G, H) Blood flow in the right external iliac artery (white arrow) and left common iliac artery (black arrow) was compromised and arose from the false lumen. CT, computerized tomography.
방사선 소견: 내원시 시행한 컴퓨터단층촬영에서 상행대동맥의 벽내 혈종(intramural hematoma) 소견(Fig. 1C) 및 흉부대동맥(thoracic aorta) 중간 정도 부위에서 기시한 내막판(intimal flap in the mid-thoracic aorta)이 가강을 형성하여(Fig. 1D) 원위부 대동맥 분지부(distal aortic bifurcation)까지 대동맥박리가 관찰되며 하행 흉부대동맥이 가강에 의하여 진강이 심하게 눌려있는 모습을 보이고 있고(Fig. 1E) 상장간맥동맥은 진강에서 기시하였으며 혈류는 원활하게 유지되었다. 가강에 의한 진강이 거의 다 눌려진 폐쇄 소견이 복부대동맥(abdominal aorta)에서 관찰되었고(Fig. 1F), 좌측 신장동맥은 진강, 우측 신장동맥은 가강에서 혈류가 기시함이 관찰되었다. 우측 외장골동맥(external iliac artery) 및 좌측 총장골동맥(commoniliac artery)은 진강이 가강에 의해 완전히 눌려서 양측 하지로 가는 혈류가 완전히 차단된 것을 관찰할 수 있었다(Fig. 1B, 1G, and 1H).
치료 및 경과: 혈압조절 및 맥박조절을 통한 약물 치료로 안정화시키면서 양 하지 통증이 심하게 악화되고 양측 발등동맥이 촉지되지 않으며 청색증(cyanosis)이 나타나서 응급으로 혈관내 시술을 시행하였다. 환자는 양쪽의 장골동맥과 대퇴동맥이 가강에 의하여 거의 다 눌려있었지만 일단은 대퇴동맥으로 진강이 천자가 된다면 스텐트 이식편을 사용하여 내막 파열을 막아서 진강의 혈류를 복원하고 하지의 혈류를 복원시키고 대동맥 재형성(aortic remodeling)에도 좋은 영향을 줄 수 있어 스텐트 이식편 시술을 먼저 계획하였다.
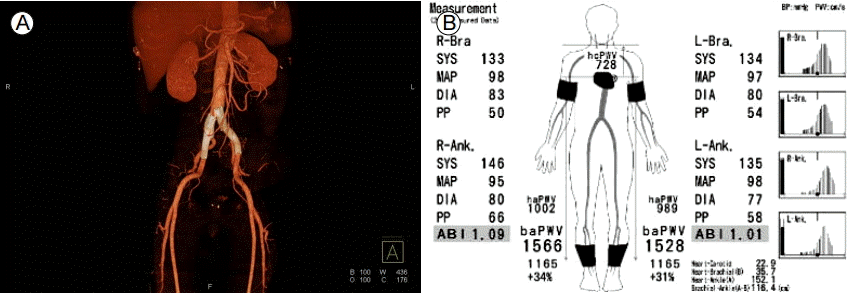
양측 대퇴동맥을 천자하여 7 french 유도초(sheath)를 삽입하였다. 우측 대퇴동맥 유도초를 통하여 0.035 inch Terumo 유도철선(Terumo, Tokyo, Japan)을 완전 협착된 우측 총장골동맥 및 복부대동맥으로 조심스럽게 진행시켰고 유도철선은 흉부 하행대동맥 부위에서 가강으로 들어갔고 상행대동맥까지 진행이 되지 않았다. 좌측 대퇴동맥을 천자하여서 유도철선을 진행시켰으나 가강으로 진행이 되어서 더 이상 시술이 어려웠다(Fig. 2A and 2B). 오른쪽 장골동맥은 진강과 가강을 가로질러서 유도철사가 놓여서 일단 진강과 가강 사이에 개창을 하여 혈류를 복원시키고자 풍선확장술(6 mm × 40 mm, Powerflex, Cordis, NJ, USA) 후에 자가팽창형 스텐트 삽입술(self expandable stent, 14 × 80 mm, S.M.A.R.T., Cordis, NJ, USA)을 우측 장골동맥에 시행하였다. 그러나 우측 장골동맥의 혈류는 회복이 되지 않았다(Fig. 2C and 2D). 유도철사가 진강과 가강을 가로지르는 것으로 생각되었으나 스텐트는 가강에만 설치되어서 우측 장골동맥의 혈류는 회복되지 않는 원치 않는 결과를 얻었다. 양쪽 대퇴동맥을 통한 진강으로의 접근이 되지 않아서 스텐트 이식편 시술은 불가능한 것으로 판단하고 좌측 상완동맥을 천자하여서 진강으로 유도철선을 보내어 양쪽 장골동맥, 대퇴동맥의 진강으로 진행시킨 후 양쪽 장골동맥에 스텐트 시술하기로 계획을 변경하였다. 먼저 좌측 상완 동맥을 천자하고 6 french 유도초를 삽입 후 0.035 inch 유도철선을 상행대동맥으로 진행시킨 후 표식자 돼지꼬리형 카테터(marked pigtail catheter)로 대동맥조영술(aortography)을 시행하였다. 가강에 의하여 진강이 완전히 눌려서 원위부 대동맥에서 양쪽 장골동맥으로 가는 혈류는 없었다. 7 french Shuttle sheath (Cook Medical, Bloomington, IN, USA)로 바꾸어서 하행흉부대동맥까지 보낸 후에 0.035 inch Terumo 유도철선을 5 french 다용도 카테터(multipurpose catheter)와 함께 조심스럽게 진행시켜서 하행흉부대동맥의 내막판 파열 부위를 통하여 가강으로 유도철선이 진행하지 않도록 대동맥조영술을 시행하면서 진강으로 계속 진행시켰다. 먼저 가강에 의하여 눌린 우측 장골동맥으로 유도철선과 카테터를 진행시켰고 이전에 넣은 스텐트는 가강에 위치하고 있었다(Fig. 2D). 유도철선을 우측 표재대퇴동맥(superficial femoral artery)으로 진행시켰고 카테터를 통하여 조영술을 시행해 우측 표재대퇴동맥 진강을 확인하였다. 스텐트 시술을 위해 카테터를 통하여 유도철선을 0.035 inch Amplatz Extra Stiff 유도철선(Cook Inc., Bloomington, IN, USA)으로 바꾸었다. 먼저 8 mm × 60 mm 풍선도자(Powerflex Extreme, Cordis, NJ, USA)를 우측 총장골동맥에 위치시키고 확장시킨 후 기존에 가강에 들어가 있는 자가팽창형 스텐트를 누르기 위하여 14 mm × 60 mm 풍선확장형 스텐트(Express, Boston Scientific, Natick, MA)를 우측 장골동맥에 삽입하였다(Fig. 2E). 진강에 삽입한 풍선확장형 스텐트에 의하여 가강의 자가팽창형 스텐트는 눌려졌고 우측 장골동맥과 대퇴동맥의 진강 혈류는 회복되었다(Fig. 2F). 좌측 장골동맥의 혈류를 회복하기 위하여 같은 방법으로 유도철선과 카테터를 조심스럽게 좌측 장골동맥으로 진행시켰고(Fig. 2G) 카테터를 통하여 좌측 표재대퇴동맥의 진강을 확인한 후에 풍선확장술을 시행한 후 10 mm × 80 mm 자가팽창형 스텐트(S.M.A.R.T., Cordis, NJ, USA)를 좌측 총장골동맥 기시부부터 삽입하였다. 그 후 양쪽 장골동맥과 대퇴동맥의 혈류는 회복되었고 하행대동맥과 양쪽 대퇴동맥 사이의 압력 차는 관찰되지 않아 시술을 마쳤다(Fig. 2H). 시술 다음 날 serum creatinine level이 1.07 mg/dL에서 2.44 mg/dL로 상승하는 소견이 관찰되었는데 조영제에 의한 신장병증으로 생각되어 수분 공급하며 경과 관찰하였으며 이후 회복되었다. 시술 5일째 시행한 상완발목지수(ankle brachial index)에서 우측 1.05, 좌측 1.07로 성공적인 혈류 재개통이 이루어졌음을 확인하였다. 시술 후 환자의 하지 통증은 시술 전 fontaine class III에서 IIa로 많이 호전되었다. 시술 9일째 시행한 컴퓨터단층촬영에서 양측 총장골동맥의 혈류 회복이 관찰되었다(Fig. 3A). 환자는 다른 합병증 없이 혈압조절 이후 퇴원하였다. Aspirin과 clopidogrel, statin 및 혈압약(beta blocker, angiotensin receptor blocker, calcium channel blocker)을 사용하였다. 퇴원 후 36개월 동안 특별한 증상이나 하지의 파행(claudication)은 없었고 시행한 상완발목지수에서 우측이 1.09, 좌측 1.01로 이상이 없었다(Fig. 3B). 그리고 시술 12, 24, 36개월에 시행한 컴퓨터단층촬영에서 하행대동맥 및 양측 총장골동맥의 혈류가 원활하게 유지됨을 확인하였다.

Endovascular procedure. (A) A guide wire inserted through the right femoral artery was advanced in the false lumen and did not proceed to the ascending aorta. (B) A guide wire inserted through both femoral arteries was advanced in the false lumen. (C) To restore blood flow, we conducted balloon dilation for the right iliac artery. (D) The restoration of blood flow was not achieved in the right iliac artery after treatment with a self-expandable balloon stent (white arrow). (E) We inserted the stent in the true lumen of the right iliac artery using the left brachial approach. (F) The stent was well positioned in the true lumen, and complete restoration of blood flow was achieved in the right iliac and femoral arteries. (G) We advanced a guide wire in the left iliac artery using the left brachial approach and confirmed the left iliac artery. (H) Restoration of blood flow in the true lumen of both the common iliac and femoral arteries after stent insertion.
고 찰
하행대동맥박리의 치료법 선택은 전통적으로 합병증 동반 여부에 따라 결정되는데, 합병증이 동반된 B형 대동맥박리의 치료는 수술적 치료와 혈관내 시술이 있다.
혈관내 시술의 임상 결과에 관한 메타분석을 보면, 급성기의 경우에는 초기 사망률 10.2%, 뇌졸중 및 척수허혈은 각각 4.9%, 4.2%였고, 급성기 이후(> 2주)에는 초기 사망률 6.6%, 뇌졸중 및 척수허혈은 각각 1.9%, 1.5%로 보고되었다[1]. 급성기에 혈관내 시술은 급성기가 지난 2 주 이후에 시행한 경우보다 높은 빈도의 사건 발생을 보인다. 그러므로 가능하다면 최소 2주 이상 급성기를 지난 후 혈관내 시술을 하는 것이 좋은 결과를 기대할 수 있다[3]. 상기 환자에서도 혈관내 시술을 가능하면 급성기를 지난 2주 이후에 시행하려고 했으나, 양 하지 통증이 심하게 악화되고 양측 발등 동맥이 촉지되지 않으며 청색증이 나타나서 응급으로 혈관내 시술을 시행하였다. 환자는 양쪽의 장골동맥과 대퇴동맥이 가강에 의하여 거의 다 눌려있어서 2주까지 기다리는 것은 환자의 하지 손상 위험이 있어 급성기에 응급 혈관내 시술을 시행하였다.
임상적으로 가강에 의하여 진강이 눌려서 생기는 관류 장애의 경우에는 수술적 치료가 해부학적으로 어렵고 사망률이 매우 높은 것(25-50%)으로 보고되고 있다[4]. 관류 장애를 동반한 하행대동맥박리 환자에서 수술적인 치료를 시행하는 경우에는 대동맥을 인조 혈관으로 치환한 후에 복강동맥, 상장간막동맥, 신장동맥을 수술한 대동맥에 이식해야 하므로 기술적으로도 어렵고 수술 시간도 오래 걸리는 단점이 있다. 그러므로 관류 장애를 가진 하행대동맥박리 환자의 경우 수술적인 치료의 성적이 좋지 않다. 그리하여 하행대동맥박리에 동반된 관류 장애에 대한 혈관내 시술이 수술에 대한 대안으로 소개되었다. 혈관내 시술은 하지나 상지혈관을 통하여 분지혈관의 혈류를 회복시키므로 시술이 비교적 간단하고 시술 시간이 짧게 걸리는 장점이 있다. 혈관내 시술의 방법은 다양한데 크게 3가지 방법으로 나누어진다[4].
첫째는 스텐트 이식편을 내막 파열 부위에 삽입하여 가강으로 가는 혈류를 차단하여 진강을 회복시켜서 혈류를 회복시키는 방법으로 가장 보편적으로 이루어지고 있고 좋은 성적을 보이고 있다. Nienaber 등[5]이 조사한 메타 연구에 따르면 합병증이 동반된 하행대동맥박리에서 혈관내 스텐트 이식편 시술시 혈류회복에 성공하는 것은 95%이고 1년 그리고 2년 생존율은 80% 이상으로 보고하였다. 두 번째는 가강에 의하여 혈류가 차단된 주요한 혈관, 신장혈관, 경동맥, 상장간막동맥, 하지혈관 등에 스텐트 시술을 하여 혈류를 회복시키는 선택적인 스텐트 삽입술(selective stenting), 세 번째는 가강과 진강을 큰 풍선카테터(balloon catheter)를 통하여 창냄술(fenestration)을 하여 가강과 진강 사이에 혈류를 통하게 만드는 방법이다. Patel 등[6]이 보고한 자료에 따르면, 창냄술과 선택적인 스텐트 삽입술은 수술과 비교하여 초기 사망률은 유의하게 줄여 주었으나 장기간의 경과 관찰시 창냄술은 하행대동맥 파열(descending aortic rupture)이 발생하는 경우가 많이 보고되었다. 그러므로 가능하다면 스텐트 이식편을 삽입하여 가강으로 가는 혈류를 차단하여 진강을 회복시켜서 대동맥 재형성을 시키는 것이 장기적으로는 바람직한 방법이다. 그러나 스텐트 이식편을 시술하기 위하여서는 스텐트 이식편이 접근하기 위한 한 쪽 이상의 장골동맥, 대퇴동맥이 진강에서 기시하여야 시술이 가능하다. 대동맥과 장골동맥이 일부 가강에 의하여 눌려지더라도 대퇴동맥이 진강에서 기시하는 경우는 스텐트 이식편을 진행시키면 눌려진 진강으로의 진행이 가능하다. 그러나 상기 증례에서는 복강동맥 근처에서 내막 파열이 발생하였고 가강을 통한 혈류가 증가하면서 진강이 아래쪽으로 심하게 눌려 우측 외장골동맥 및 좌측 총장골동맥의 진강이 완전폐색이 되어서 하지에 허혈을 유발하고 있었다. 이 증례처럼 양쪽 대퇴동맥과 장골동맥이 가강에서 기시하는 경우에는 유도철선이 대동맥과 장골동맥의 가강 내에 위치하게 되어서 스텐트 이식편 시술이 불가능하다. 이러한 경우에는 왼쪽 상완동맥을 천자하여서 하행대동맥에서 장골동맥, 대퇴동맥으로 선행적으로(antegrade) 유도철선을 진행시키면 하지동맥까지 진강으로 쉽게 진행시킬 수 있다. 그 후 스텐트 시술을 시행하면 가강에 의하여 눌린 진강의 혈류를 회복시킬 수 있다. 스텐트 이식편 시술이 가능하다면 먼저 시행하는 것이 바람직하다. 그러나 상기 증례에서는 내막 파열 부위가 복강동맥에서 직상방에 크게 있어서 스텐트 이식편을 시행하는 경우에는 스텐트 이식편의 안착점(landing zone)이 없어서 복강동맥의 혈류를 차단하게 되므로 시행할 수 없었고, 왼쪽 상완동맥을 통한 접근 시에도 내막 파열 부위가 커서 진강과 가강을 오가면서 유도철사가 놓이게 될 가능성이 많았고 이 경우에 스텐트 이식편의 시술은 위험하였다. 그래서 장골동맥의 혈류의 복원을 위해 각각의 장골동맥에 스텐트를 시술하였다.
복강동맥의 경우 대동맥 파열과 같은 다른 시술 방법으로는 치료가 불가능한 응급 환자의 경우에는 스텐트 이식편으로 막을 수 있는 것으로 알려져 있다. 그러나 복강동맥을 스텐트 이식편으로 막는 경우에는 90% 정도는 상장간막동맥에서 우회로가 형성되어서 간의 기능이 보존되지만 10% 정도는 우회로가 형성되지 않아서 간이 괴사되어 치명적인 결과를 초래하게 된다. 그러므로 복강동맥을 막는 경우에는 풍선으로 먼저 복강동맥을 막은 후에 상장간막동맥을 통하여 조영제를 주입해 복강동맥으로 가는 우회로가 형성되는지 확인한 후에 복강동맥을 스텐트 이식편으로 막을 수 있다[7]. 상기 환자의 경우에는 각각의 장골동맥에 스텐트를 시술하면 복강동맥을 막지 않아도 되는 다른 시술 방법이 있어서 스텐트 이식편을 시행하지 않았다.
선택적인 스텐트 시술 방법들을 통하여 하행대동맥박리에 따른 관류장애증후군(malperfusion syndrome) 환자에 대해 혈관내 시술 시에 수술에 비하여 생존율 및 합병증에서 뛰어난 성적이 증명되었으나 장기 예후에 대한 자료는 아직 부족한 실정이다.
본 증례는 급성 하행대동맥박리에서 가강에 의하여 진강이 눌려서 양쪽의 장골동맥 및 대퇴동맥이 막혀서 하지허혈이 유발된 경우로 스텐트 이식편 시술이 불가능해서 좌측 상완동맥 접근을 통해 양쪽 장골동맥에 선택적인 스텐트 삽입술을 통하여 진강의 혈류를 회복시켜 효과적으로 치료하였고 36개월 동안 잘 유지된 증례로 문헌고찰과 함께 보고한다.