신장암 환자에서 Pazopanib을 사용한 후 발생한 심부전 1예
Heart Failure Secondary to Pazopanib for Treatment of Metastatic Renal Cell Carcinoma
Article information
Abstract
신장암 환자에서 VEGFR-TKIs과 관련된 심부전은 드무나 생명을 위협할 수 있는 위험한 부작용으로 pazopanib으로 인한 심각한 심부전은 거의 없는 것으로 알려져 있다. 국내에서 pazopanib으로 인한 심각한 심부전에 대하여서는 보고된 바가 없다. 이에 저자들은 pazopanib 투여한 이후 발생한 심각한 심부전 1예를 경험하였으며 pazopanib 투여시 주기적인 심장기능 평가 필요성 및 증상 발현 시에 약물 중단을 통하여 증상 호전을 기대할 수 있어 이에 대하여 증례보고한다.
Trans Abstract
A 78-year-old man was diagnosed with renal cell carcinoma, and left nephrectomy was performed. He started pazopanib. One month later, he visited our hospital because of general weakness and dyspnea. His oxygen saturation was low. A chest X-ray showed pulmonary edema and bilateral pleural effusion. An echocardiogram showed a larger left ventricle and lower ejection fraction than observed at the previous examination. The patient discontinued pazopanib and started diuretics and digoxin. His symptoms improved and a follow-up X-ray showed improvement in the pulmonary edema with bilateral pleural effusion.
서 론
신세포암은 신장암중에서 가장 흔한 종류의 암으로 진단 당시 25-30%의 환자에서 전이성 병변을 가지고 있다[1]. 전이성 신세포암에서 vascular endothelial growth factor receptor (VEGFR) antagonists는 널리 사용되어 오고 있다. 보트리엔트(VotrientTM, Pazopanib)는 VEGFR, platelet-derived growth factor receptors, c-Kit를 표적으로 하는 경구 섭취로 복용할 수 있는 표적 치료제이다[2].
Pazopanib의 알려진 심혈관계 부작용으로는 고혈압, 좌심실 수축성 기능장애, 심부전, 혈전증, 심근허혈 및 심근경색이 알려져 있다[3]. 이 중에서 pazopanib으로 인한 심각한 심부전은 매우 드무나 위험한 부작용으로 현재까지 pazopnib과 연관되어 발생한 심각한 심부전은 국내에서 보고된 바가 없으며 해외에서 몇 개의 증례가 보고된 바 있다[4-6]. 저자들은 신세포암으로 좌측 근치적 신절제술을 시행하고 pazopanib을 사용한 이후 발생한 심각한 심부전 1예를 경험하였기에 문헌고찰과 함께 보고한다.
증 례
환 자: 78세 남자
주 소: 전신기력저하 및 호흡곤란
현병력: 3일 전부터 시작된 전신기력저하 및 점점 악화되는 호흡곤란으로 내원하였다.
과거력: 3개월 전 본원에서 신세포암으로 좌측 근치적 신전제술을 시행하였으며, 폐전이 및 간전이로 인하여 1개월 전부터 pazopanib을 복용하였다. 신부전 및 고혈압으로 약물 투여 중이었다.
가족력 및 사회력: 특이사항은 없었다.
진찰 소견: 내원시 혈압 120/70 mmHg, 맥박수 95회/min, 호흡수 20회/min, 체온은 36.5℃였다. 의식은 명료하였다. 흉부 진찰에서 호흡음은 미약한 기관지 호흡음이 들렸으며 저명한 심잡음은 들리지 않았다. 하지에 말초 부종은 경미하게 존재하였다.
검사 소견: 말초혈액 검사에서 백혈구는 10,460/mm3, 혈색소 9.6 g/dL, 혈소판 241,000/mm3로 빈혈 소견을 보였다. 전해질 검사에서 Na 142 mEq/L, K 7.0 mEq/L로 고칼륨혈증을 보이고 있었으며 blood urea nitrogen (BUN) 77.7 mg/dL, creatinine 3.01 mg/dL였다. Brain natriuretic peptide (BNP) 수치는 1,805.2 pg/mL로 상승한 소견을 보였다.
심전도에서 천막 모양의 T파나 느린 맥은 보이지 않았으며 흉부 단순촬영은 이전과 비교하여 저명한 폐부종 소견은 보이지 않았다.
치료 및 경과: 고칼륨혈증 소견을 보여 수액 치료 및 이뇨제 사용을 통하여 고칼륨혈증을 교정하였으며 다시 시행한 검사에서 K은 5.3 mEq/L 소견을 보였다. 입원 12일째 호흡곤란이 악화되었고 환자 산소포화도 82%로 확인되었다. 이에 흉부 단순촬영을 시행하였으며 폐부종 및 양측 흉수 소견을 보여(Fig. 1A) 산소 공급 및 심초음파를 시행하였다. 환자의 이전 심초음파는 박출률(ejection fraction) 64.68%로 정상 소견을 보이고 있었으나(Fig. 2) 증상 발생 이후 시행한 심초음파에서 박출률 31.40%로 감소하였고, 좌심방 및 좌심실비대, 좌심실의 전반적인 운동저하 소견이 관찰되었다(Fig. 3). Pazopanib 복용을 중단하고 digoxin 및 이뇨제를 투여하기 시작하였으며 1주일 후 증상은 호전되었다. 증상 호전 이후 시행한 흉부 단순촬영에서 환자 폐부종 및 양측 흉수 소견은 호전되었다(Fig. 1B).
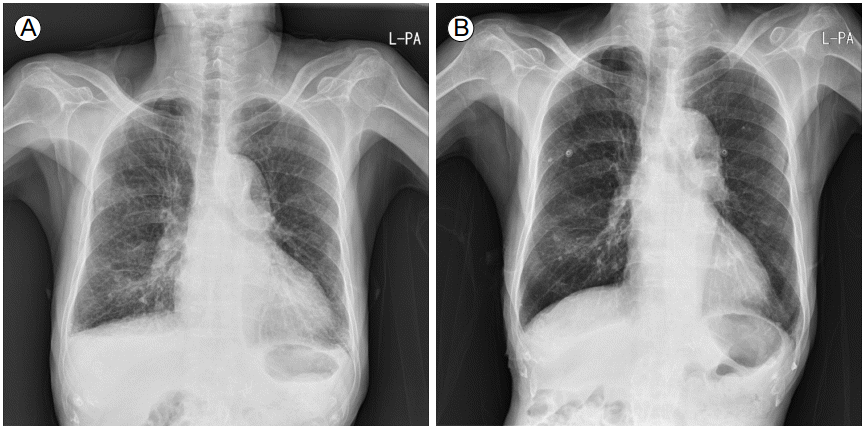
(A) The initial chest X-ray showed pulmonary edema and bilateral pleural effusion. (B) The follow-up X-ray showed improvement in the pulmonary edema and pleural effusion.
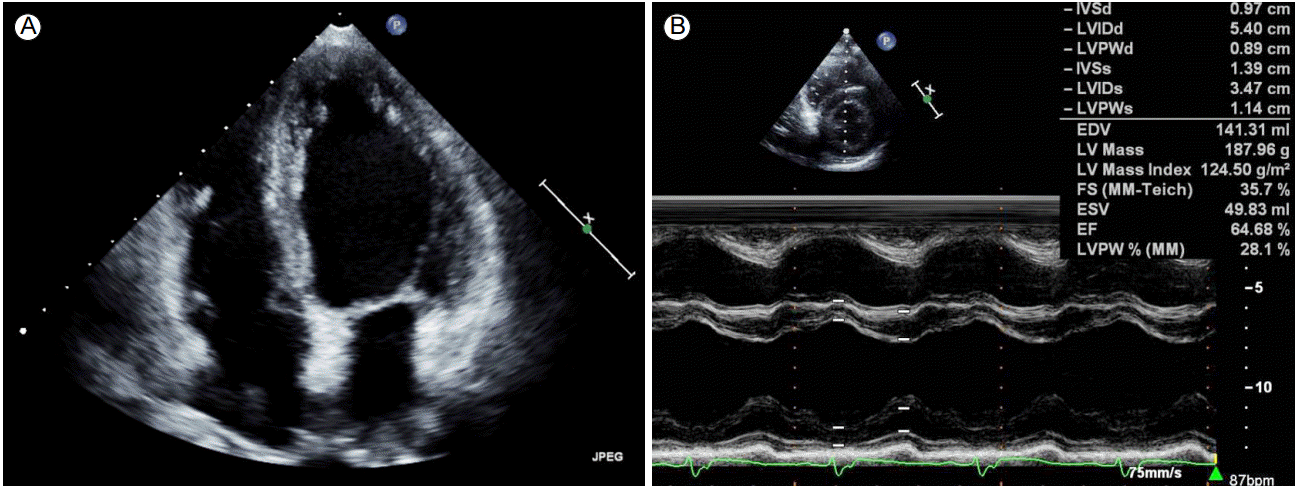
The patient’s previous echocardiogram showed (A) a normally sized left ventricle and (B) a normal ejection fraction of 64.68%. IVSd, interventricular diastolic septal thickness; LVIDd, left ventricular internal dimension during diastole; LVPWd, left ventricular diastolic posterior wall thickness; IVSs, interventricular systolic septal thickness; LVIDs, left ventricular internal dimension during systole; LVPWs, left ventricular systolic posterior wall thickness; EDV, end diastolic volume; LV, left ventricle; FS, fractional shortening; MM, Morton M.; ESV, end-systolic volume; EF, ejection fraction.

The echocardiogram showed (A) left ventricular enlargement, moderate to severe global hypokinesia, and (B) a low ejection fraction (31.40%). IVSd, interventricular diastolic septal thickness; LVIDd, left ventricular internal dimension during diastole; LVPWd, left ventricular diastolic posterior wall thickness; IVSs, interventricular systolic septal thickness; LVIDs, left ventricular internal dimension during systole; LVPWs, left ventricular systolic posterior wall thickness; EDV, end diastolic volume; LV, left ventricle; FS, fractional shortening; MM, Morton M.; ESV, end-systolic volume; EF, ejection fraction.
고 찰
신세포암은 신피질에서 발생하는 암으로 신장암의 80-85%를 차지하고 있으며 전체 암의 2% 정도를 차지하고 있다. 조직학적으로 투명세포암가 제일 흔한 형태이다. 신세포암은 주로 옆구리 통증, 혈뇨, 배에서 만져지는 종괴 또는 전이된 병변으로 인한 증상 등이 나타날 수 있으며 복부 영상 검사에서 우연히 발견되는 경우도 있다[2].
Pazopanib은 VEGFR-1, -2, and -3; PDGFR-a and -b; and c-KIT에 작용하는 multi-tyrosine kinase inhibitor로 신생혈관 생성 억제를 통하여 항암 효과를 보이는 것으로 알려져 있다. Pazopanib은 주로 간을 통하여 대사되며 대변으로 배설되며, 4% 미만이 소변으로 배출된다. 따라서 신장기능 저하가 임상적으로 pazopanib의 약동학에 상대적으로 영향이 낮다는 것을 시사한다[2].
Pazopanib은 임상시험 2상과 3상에서 무진행 생존기간(progression free survival)과 치료반응 비율에 효과가 있음을 입증하였으며 기존에 사용하던 sunitinib에 비하여도 비열등한 치료 효과를 나타내었다[1,7,8].
부작용은 고혈압, 설사, 털 색상 변화, 식욕 부진 및 메스꺼움이 발생할 수 있으며 혈액 검사 이상소견으로는 고혈당, 간기능 수치 이상이 가장 흔하게 나타난다[9].
심혈관 관련 부작용으로는 서맥, 심장기능 저하, 심근경색 및 허혈이 pazopanib을 사용한 신장암 환자에서 드물게 나타나고 있으며(< 1%) 치료와 관련된 심부전과 좌심실 박출률 저하는 3상 시험에서 거의 없는 것으로 알려져 있다[7-9]. 하지만 최근 발표되는 논문들에서 pazopanib과 연관되어 심부전 발생 위험도가 상승하거나 박출률이 감소할 수 있다고 보고되고 있다[3,10].
심부전은 VEGF 억제제 사용에서 매우 드무나 생명을 위협할 수 있는 부작용이다[10]. 심부전과 관련된 신생혈관 생성 억제 약물의 발병 기전은 현재 잘 알려져 있지 않지만, 여러 가지 기전들이 연관되어 있을 것으로 추측되고 있다[10]. Sorafenib, sunitinib, vandetanib, pazopanib, axitinib, regorafenib (VEGFR-TKIs)은 고혈압의 위험을 높이는 것으로 알려져 있으며 고혈압은 잘 알려진 심부전 발생 위험인자 중의 하나이다. 다른 기전으로는 VEGF 신호전달 과정 억제를 통한 심근 독성 발생 가능성 및 심첨부 풍선확장증후군(apical ballooning syndrome)을 생각해 볼 수 있다[5,6,10].
본 증례에서는 pazopanib을 사용하기 이전의 심초음파 검사에서는 정상적인 박출률을 보였으나 pazopanib을 사용한 이후 호흡곤란 및 BNP 상승 등의 소견이 보여 시행한 심초음파에서 저명한 박출률 감소 소견이 보였으며(64.68% to 31.40%) 좌심실 운동저하 소견이 보였다. 수액 치료 및 이뇨제 사용에도 환자 C-reatinine 수치는 상승하지 않았으며 내원 이전의 C-reatinine 검사에도 2.0 mg/dL 이상의 수치를 보인 적이 있기에 만성 신부전에 동반된 급성 신부전으로 인한 일시적인 심부전 가능성이 낮을 것으로 보여 pazopanib으로 인한 심부전 발생으로 진단하였다. 환자 약물 치료 및 pazopanib 중단을 통하여 증상 호전 및 흉부 단순촬영 검사에서 호전된 소견을 보였으며 언급된 것 이외의 다른 심부전을 일으킬 수 있는 요소는 발견되지 않았다. 이전에 보고된 증례에서도 약 중단 및 보존적인 심부전 치료로 증상 및 검사 결과가 호전되었다[4-6].
따라서 신장암 환자에서 pazopanib으로 치료를 받는 경우에 드물지만 심부전이 발생할 수 있다는 것을 염두에 두어야 하며 주기적인 심장기능 평가 및 증상 발현 시에 약물 중단을 고려해야 한다.