관상동맥 스텐트의 최근 현황
Current Status of Coronary Stent
Article information
Trans Abstract
Coronary artery disease is one of the principal causes of mortality worldwide. Andreas Grüntzig initially developed balloon angioplasty to treat the condition. Coronary stenting was first used in the mid-1980s to prevent abrupt vessel closure and restenosis. Stent material and design have received a great deal of attention over the past 30 years. Modern polymer stents feature antiproliferative coatings. Recently, a bioresorbable stent scaffold was introduced. This article focuses on the current status of coronary stents, especially with respect to certain aspects of clinical practice.
서 론
1978년 Grüntzig[1]는 관상동맥의 협착 병변에 풍선 확장술(plain old balloon angioplasty)을 최초로 시행하였다. 1980년대 중반에 이르러서는 풍선 확장술 이후 발생하는 급성 혈관 폐쇄를 예방하고[2] 재협착을 막기 위한 목적[3]으로 관상동맥 스텐트(coronary stent)가 개발되었고, 스텐트의 사용은 급성 합병증을 예방하고 임상 결과를 개선할 수 있었기에[4] 빠르게 보편화되었다. 지난 30여 년간 스텐트의 재료 및 디자인, 항증식성 약물의 종류, 약물을 코팅하는 폴리머에 따라 수많은 관상동맥용 스텐트가 개발되었고, 관상동맥 중재시술영역에서 스텐트의 적용 범위 및 선택의 폭이 넓어졌다. 최근에는 생체융해성 스캐폴드의 임상 연구가 활발하여 곧 국내에도 도입될 예정이다. 임상에서 사용되는 관상동맥 스텐트 및 생체융해성 스캐폴드에 대해 논의하고자 한다.
본 론
금속 그물망(bare-metal stent)
금속 그물망은 풍선 확장술 이후 발생하는 급성 혈관 폐쇄를 예방하여 응급 관상동맥 우회술(emergent coronary artery bypass surgery)을 줄였다. 그러나 시술 2주 이내에 발생하는 혈전성 폐색이 18%에 달해 항혈소판제나 항혈전제의 필요성이 대두되었고 이로 인하여 스텐트 시술과 출혈 위험은 필연성을 갖게 되었다[5]. 스텐트 시술은 풍선 확장술만 시행하는데 비해 재협착에 의한 재시술을 줄여 주요 심혈관 사건의 감소 효과를 입증하였다[6]. 이에 따라 임상에서 폭넓게 금속 그물망 시술이 이루어졌으며 2중 항혈소판제를 사용하는 것이 항혈전제 사용보다 유용하다는 것도 밝혀졌다[7]. 하지만 혈관 손상 이후에 발생하는 혈관 평활근 세포(vascular smooth muscle cell)의 이주, 증식에 의한 금속 그물망내 신생내막의 과증식(neointimal hyperplasia)과 내경이 감소한다는 새로운 문제점이 제기되었고 재협착률이 20-30%에 달하였다[8,9]. 따라서 관상동맥 스텐트가 갖는 물리적 장점에 더해 재협착을 억제할 수 있는 추가적인 방법이 연구되기 시작했다.
1세대 약물 방출 스텐트(first generation drug-eluting stent)
약물 방출 스텐트는 금속 그물망에 비해 재협착을 현저히 줄였으며[10,11] 복합 병변이나 좌주간지 협착[12]의 표준 치료였던 관상동맥 우회술에 비해 사망, 심근경색, 뇌졸중 등 임상 사건의 발생 측면에서 별다른 차이를 보이지 않는 것으로 밝혀졌다. 이런 결과에 힘입어 약물 방출 스텐트를 시술하게 되면서 관상동맥 질환의 치료에 있어 중재시술의 영역이 더 넓어지게 되었다. 1세대 약물 방출 스텐트는 sirolimus 방출 스텐트(Cypher, Cordis, Warren, NJ, USA)와 paclitaxel 방출 스텐트(Taxus, Boston Scientific, Natick, Massachusetts, USA)가 있다. Cypher는 스테인레스 스틸 재질로 스트럿(strut)의 두께가 140 mm로 비교적 두껍고 sirolimus가 140 m/cm2 농도로 폴리머를 통해 코팅되어 있어 28일 이내 80%가 방출된다. 1999년 최초 임상 연구에서 신생내막 증식을 억제하는 효과를 입증한 뒤[13], 무작위 배정 임상 연구인 RAVEL연구에서 비교적 단순 병변을 가진 238명의 환자를 대상으로 시술했을 때 1년 이후 금속 그물망의 재협착률이 26.6%에 비해 0%라는 결과를 보여 주었다[14]. 이런 결과는 대규모 복합 병변을 대상으로 한 SIRIUS 연구를 통해 재시술을 포함한 주요 심혈관 사건을 유의하게 줄이는 것으로 확인되면서[15] 당뇨, ST 상승 심근경색, 만성폐색 병변, 복합 병변 등 다양한 임상 질환군에 대한 적용으로 이어졌다. 메타분석을 통해 장기적 예후를 비교해볼 때 Cypher는 금속 그물망에 비해 재시술을 줄이는 효과가 있고, 사망 및 심근경색의 발생은 비슷하다[10,11]. Taxus는 스테인레스 스틸 재질로 microtubule을 억제하고, G0/G1 및 G2/M 시기의 세포 주기를 정지시키는 paclitaxel이 100 m/cm2 농도로 폴리머를 통해 코팅되어 있다. 비교적 서서히 약물이 방출되어 28일 이내 10% 미만이 방출되며 스트럿(strut)의 두께는 원래 132 mm (Taxus Express)였으나 97 mm (Taxus Liberté)로 얇게 개선되었다. Cypher에 비해 구조상 열린 구조(open cell)라 복합 병변에서 유리하며 무작위 배정 임상 연구인 TAXUS I에서 6개월째 재협착의 발생이 없었으며[16], ST상승 심근경색[17] 및 좌주간지 시술[18]에서 금속 그물망보다 재시술의 발생이 적었다. 장기 추적 관찰한 메타분석 결과를 보면, 금속 그물망에 비해 재시술이 유의하게 적은 장점이 있다(Table 1).
Cypher와 Taxus스텐트를 단기간 추적, 비교한 임상연구에서 Cypher가 Taxus에 비해 내경의 감소 및 재협착의 발생 측면에서 더 우수하다고 보고하였다[19,20]. 16개의 임상연구를 메타 분석하여 2년간의 임상 결과를 비교해보면 Cypher가 병변의 재시술(위험도: 0.74, 95% 신뢰구간 0.63-0.87, p < 0.001) 및 스텐트 혈전증(위험도: 0.66, 95% 신뢰구간 0.46-0.94, p = 0.02)의 위험도를 낮추나 사망(위험도: 0.92, 95% 신뢰구간 0.74-1.13, p = 0.43) 및 심근경색(위험도: 0.84, 95% 신뢰구간 0.69-1.03, p = 0.10)의 발생에서는 차이가 없었다[21].
약물 방출 스텐트(drug-eluting stent)의 장단점
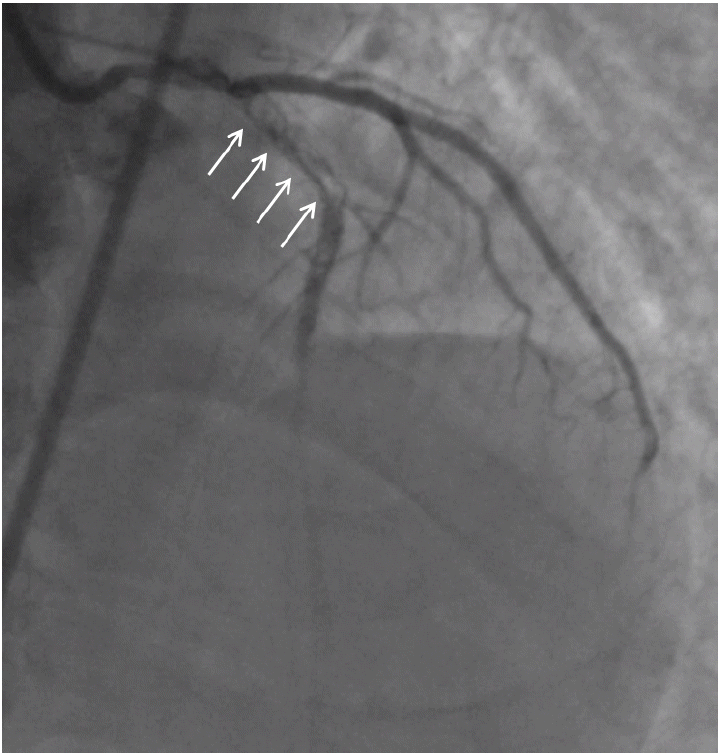
약물 방출 스텐트의 가장 중요한 장점은 재협착에 의한 재시술을 감소시킨다는 것이다. 38개의 임상연구에 대한 메타분석[22]에서 4년간 추적 관찰했을 때 약물 방출 스텐트는 금속 그물망보다는 Cypher의 경우 70%, Taxus의 경우 58% 재협착에 의한 재시술을 감소시켰고 34개의 관찰 연구를 메타분석하여 실제 임상에서 사용된 병변을 대상으로 하더라도 금속 그물망에 비해 재시술(위험도: 0.54, 95% 신뢰구간 0.48-0.61) 감소를 입증하였다[23]. 하지만 약물 방출 스텐트의 임상 경험이 쌓이면서 2006년 BASKET-LATE 연구[24]와 SCAAR 등록 연구[25]에서 10-30%의 치사율을 보이는 스텐트 혈전증의 문제가 제기되었다(Fig. 1). 시술 1개월 이내 발생하는 조기 스텐트 혈전증(early stent thrombosis)이나 1개월에서 1년 사이 발생하는 후기 스텐트 혈전증(late stent thrombosis)은 2중 항혈소판제의 조기 중단이나 작은 사이즈의 스텐트 시술, 병변 길이가 28 mm 이상인 경우, 여러 스텐트 시술, 석화화 및 작은 혈관의 시술과 관련이 있는 것으로 보고되며[24], 금속 그물망과 약물 방출 스텐트의 발생률 차이는 없었다. 하지만 약물 방출 스텐트의 경우 지속적으로 스텐트 혈전증이 발생하여(0.5-0.6%/년) 1년 이후 발생하는 스텐트 혈전증(very late stent thrombosis)은 금속 그물망보다 유의하게 발생률이 높았다[22,25,26]. 이는 항증식약물 및 폴리머에 의해 스텐트 부위가 혈관 내피세포로 덮이는 과정이 지연되고(delayed endothelization) [27,28] 과민 반응(hypersensitivity reaction) [29]이 발생하기 때문으로 여겨져, 혈관 재생을 개선한 약물 방출 스텐트를 고안하는 계기가 되었다.
2세대 약물 방출 스텐트(second generation drug-eluting stent)
기존 스텐트의 재료 물질인 스테인레스 스틸을 대체하여 방사상 강도(radial strength)가 크고 방사선 비투과성인 코발트 크롬(cobalt chromium)이 이용되면서 스트럿이 더 얇아지고, limus 계통의 항증식약물을 사용하며, 생체 적합성이 개선된 폴리머를 사용한 것이 특징이다. 대표적으로 zotarolimus 방출 Endeavor (Medtronic Cardiovascular, Santa Rosa, CA, USA) 및 Resolute (Medtronic Cardiovascular, Santa Rosa, CA, USA) 스텐트와 everolimus 방출 Xience (Abbott Vascular, Santa Clara, CA, USA) 스텐트가 있으며, 현재 중재 시술 분야에서 주로 사용된다. Endeavor는 세포막 성분인 포스포콜린 폴리머를 이용, 시술 14일 이내에 95% 이상의 zotarolimus가 방출되어 염증 반응이 Cypher보다 덜하다[28]. Endeavor와 금속 그물망을 비교한 ENDEAVOR II 연구[30]에서 스텐트 내 내경 감소 및 재협착 발생 측면에서 우수한 결과를 보였으며 5년간 추적관찰에서 재시술률이 더 낮았고, 사망, 심근경색 및 스텐트 혈전증은 유사하였다[31]. Endeavor는 1세대 약물 방출 스텐트인 Cypher/Taxus와 비교할 때 12개월째 내경 감소측면에서 불리한 결과를 보이나[32,33], 재시술 측면에서 격차는 5년 째 감소하여 후기 따라잡이(late-catch) 현상이 없는 것을 알 수 있다. 우리나라의 단일 기관에서 시행된 Endeavor, Cypher, Taxus 무작위 배정, 비교 연구, ZEST [34]에서는 12개월째 사망, 심근경색, 허혈로 인한 재시술을 포함한 복합 임상 사건의 발생이 10.2%로 Cypher 8.3%, Taxus 14.1%로 Cypher 보다는 비열등하고(p = 0.01), Taxus보다 우수한(p = 0.01) 결과를 보였다. ZEST 연구에서 12개월째 스텐트 혈전증의 발생은 0.7%로, Cypher 0%, Taxus 0.8%와 유사하였으나 드물게 발생하는 스텐트 혈전증의 차이를 알기에는 대상 환자의 수가 부족하고, 2세대 약물 방출 스텐트를 고안하게 된 계기가 된 1년 이후의 스텐트 혈전증(very late stent thrombosis)의 발생을 비교하기에는 제한적이다. 모든 시술환자(all-comer), 8,800명을 대상으로 Endeavor와 Cypher를 무작위 배정하는 임상연구, PROTECT가 진행되었으나[35] 2012년 유럽 심장학회에서 1년 이후 발생하는 스텐트 혈전증(very late stent thrombosis)의 발생에 별다른 차이가 없다고 발표된 후 출간되지는 않았다. Xience는 100 mg/cm2의 everolimus가 6-8 mm 두께의 생체 적합성 폴리머에서 30일 내에 80%까지 방출된다. Xience 스텐트는 1세대 약물 방출 스텐트인 Taxus와 비교한 SPIRIT II/III 연구에서 6-12개월째 내경의 감소가 덜하고[36,37], 1년 간 추적관찰했을 때, 재시술의 감소에 따른 복합임상 사건의 발생이 유의하게 적은 것으로 보고되었다[38]. 고무적인 것은 COMPARE 연구[39]에서 12개월째 스텐트 혈전증의 발생이 Xience 치료군에서 0.7%로 Taxus 치료군의 2.6%보다 유의하게 낮다는 점이다.
생융해성 폴리머 약물 방출 스텐트
시술 후 6-9개월째 융해되는 생융해성 폴리머를 이용한 biolimus 방출 스텐트로 Biomatrix (Biosenors, Morges, Swizerland)와 Nobori (Terumo, Tokyo, Japan)가 있다. Biomatrix는 LEADERS 연구에서 9개월째 심장관련 사망, 심근 경색 및 목표 혈관 재시술 등 복합 임상 사건의 발생에 있어 Cypher에 비해 비열등하였고[40], 4년째 비슷한 결과를 보여주었다[41]. 특히, 주목할 것은 1년 이후 발생하는 스텐트 혈전증의 발생률이 1%로 Cypher의 2%에 비해 유의하게(p = 0.005) 낮다는 점이다.
생체융해성 스캐폴드(bioresorbable scaffold)
생체융해성 스캐폴드는 풍선 확장술 후 발생하는 내막 손상 및 박리로 인한 급성 폐색을 스캐폴드를 이용하여 방지, 3-6개월의 일정 기간 동안 혈관 내경을 유지하여 수축 재형성(negative remodeling)을 막고[42], 항 증식 약물의 방출로 내막의 과증식을 방지하여 재협착을 예방한다[43]. 기존 스텐트의 재료인 금속과 다른 재료로 만들어져 혈관의 고유한 특성을 유지하고, 후기 혈전증(late thrombosis)의 위험성을 낮추고자 개발되었다[44]. 생체 내 융해 과정을 통해 혈관 내피세포로 시술 병변이 덮이는 과정을 통해 후기 혈전증의 위험성이 낮아지고, 젋은 연령의 환자에서 향후 추가적인 관상동맥 중재시술이나 관상동맥 우회술이 용이하다. 특히 재료가 금속이 아니기 때문에 인공 음영(artifact) 없이 컴퓨터 단층 촬영(computed tomography)이나 자기 공명 영상(magnetic resonance imaging)으로 추적 검사가 가능하며, 혈관 확장 및 연축 기능을 유지(vasomotion)함으로써 박동성 혈류(pulsatile flow) 및 전단 스트레스(shear stress)에 반응하여 혈관의 확장성 재형성(positive remodeling)이 가능하다. 그 밖에도 금속 그물망 시술 이후 지속적인 염증 반응은 신생 죽종(neo-atheroma) 발생과 후기 따라잡이 현상(late catch)의 원인으로 지목되기 때문에[45] 염증 반응이 적은 것 또한 생체융해성 스캐폴드의 장점이 된다[46]. 아직까지 임상 연구 결과가 제한적으로 Communaut' Europeen 인증 및 임상에서 사용 가능한 것은 Absorb (Abbott Vascular, Santa Clara, CA, USA)와 DESolve (Elixir Medical Corporation, Sunnyvale, CA, USA)가 있으며, 안정성과 유효성 측면에서 추가적인 연구가 필요한 상황이다.
Magnesium stent
마그네슘은 큰 방사상 강도(radial strength)로 시술 후 반동(recoil)이 적고 추가 확장(post-dilatation)을 하더라도 골절이 잘 생기지 않는 금속성 성질을 띄고 있어 생체융해성 스캐폴드의 재료로 일찍부터 주목을 받아 연구가 진행되었다(Fig. 2). 융해 반응 시 표면이 미란되어 점차 얇아지므로 일정 기간 동안 충분히 수축 재형성(negative remodeling)에 저항하기 어렵다는 문제점이 있으며 인간 대상 최초 연구(PROGRESS-AMS trial) [45]는 AMS-1 (Biotronik, Berlin, Germany)로 진행되었는데 마그네슘 스캐폴드가 빠른 속도로 융해되어 4개월째 재협착률이 50%에 달하고, 1년째 재시술률이 45%로 결과가 좋지 않았다. 따라서 융해 속도를 지연시키기 위해 지르코늄 및 이트륨을 마그네슘에 첨가하였고, paclitaxel을 3개월에 걸쳐 방출하도록 1 μm 두께로 polylactic-co-glycolic acid 폴리머를 이용하여 코팅한 AMS-3가 개발되었다. AMS-3를 이용한 전향적, 인간 대상 연구는 BIOSOLVE-1 연구(Biotroniks Safety and Clinical Performance of the First Drug- Eluting Generation Absorbable Metal Stent in Patients with de Novo Lesions in Native Coronary Arteries) [47]로 46명 환자의 단순 병변에서 시술되어 6개월째 2명(4.3%)의 재시술 외에 사망이나 혈전증은 발생하지 않았다. 6개월째와 12개월째 후기 내강 소실(late lumen loss)은 0.65 ± 0.5 mm, 0.39 ± 0.33 mm의 결과를 보였다.

Absorbable magnesium stents (AMSs). (A) AMS-1; The first-generation magnesium stent featured sinusoidal hoops; adjacent hoops were linked by three straight bridges. (B) AMS-3; The next-generation magnesium stent was modified by the addition of zirconium and yttrium, and was drug-eluting (the drug was paclitaxel).
ABSORB everolimus-eluting bioresorbable vascular scaffold
Absorb BRS (Abbott Vascular, Santa Clara, CA, USA)는 poly-L-lactic acid를 주재료로 하여 이용하고, 항 증식약물인 everolimus를 poly-D, L-lactide로 코팅하여 방출하도록 개발되었다. poly-L-lactic acid는 lactide로 가수분해되었다가 Krebs cycle을 통해 이산화탄소 및 물로 대사되며 2 μm보다 작은 입자는 대식구에 의해 탐식된다. 스캐폴드의 구조는 3차례 변경되었으며(Fig. 3) 급성 반동(acute recoil)은 Xience 스텐트와 유사하다[48].
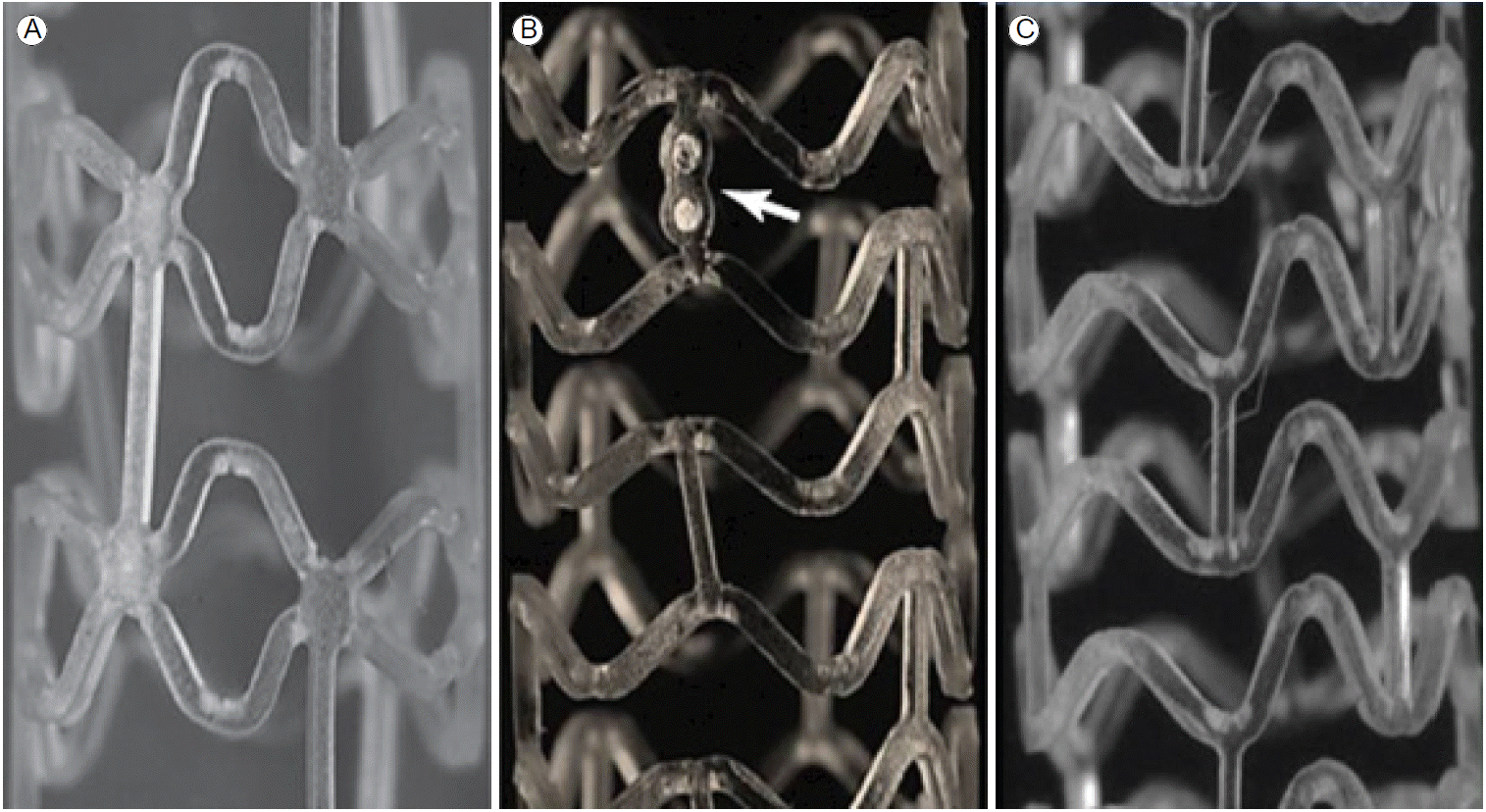
The ABSORB everolimus-eluting bioresorbable vascular scaffold. (A) The first-generation bioresorbable vascular scaffold features paired out-of-phase sinusoidal hoops directly linked at each peak and valley. Each pair is in turn linked using three straight connectors. This design was used in Cohort A of the ABSORB trial. (B) The second-generation Absorb scaffold, tested in Cohort B of the ABSORB trial, features in-phase sinusoidal hoops linked at the peaks and valleys by three straight connectors. All three Absorb scaffolds carry radiopaque platinum markers at either end (arrow). (C) The third-generation stent (the commercialized version) features small changes to the shape of the bends in the hoops and to the strut thickness and width. Also, certain changes in the manufacturing process facilitate later post-dilation to a larger diameter without tissue damage. Strut thickness is increased from 150 to 155 μm and strut width from 163 to 188 μm in the 2.5- and 3.0-mm-diameter third-generation Absorb devices, respectively; the 3.5-mm-diameter third-generation device has a strut thickness of 155 μm and a strut width of 213 μm. The 3.0-mm-diameter third-generation scaffold can be safely post-dilated to 3.5 mm, and the 3.5-mm-diameter device to 4.0 mm.
1세대 Absorb를 이용하여 단순 병변을 가진 30명의 환자를 대상으로 5년간 추적관찰한 Cohort A 연구[49]에서 주요 임상사건의 발생은 단 1명이었다. 혈관 내 초음파(intravascular ultrasound, IVUS)에서 6개월째 스캐폴드의 쭈그러듦(shrinkage) 소견에도 불구하고 후기 내강 소실(late lumen loss) 0.44 mm로 확인되었으며, 6개월에서 2년 사이 스캐폴드 크기의 변화가 없었음에도 내강이 커진 것으로 혈관내 초음파(IVUS) 및 광 간섭성 단층 촬영(optical coherence tomography)을 통해 관찰되었다[43]. 특히 혈관의 생리적인 기능이 회복되어 질산염 투여 시 혈관이 확장하고 에르고노빈(ergonovine) 투여 시 혈관이 수축하는 반응이 확인되었다. 2세대 Absorb는 가수분해의 속도를 늦추도록 고안되어 101명의 환자를 대상으로 Cohort B 연구[50]에서 적용되었다. 2년째 주요 임상사건의 발생은 6.8%였고, 후기 내강 소실은 0.27 mm로 Xience 스텐트와 유사한 결과를 보여주었다. 혈관 내 초음파 및 광 간섭성 단층 촬영에서 6개월에서 2년 사이 혈관의 양성 재형성(positive remodeling) 및 스캐폴드의 크기가 증가되면서 신생 내막의 증가를 감쇄하여 실제 내강의 감소는 거의 없는 것으로 확인되었다[51]. 단순 병변에서 2세대 약물 방출 스텐트인 Xience와 Absorb를 무작위 배정하여 2년째 혈관 확장 및 연축 기능의 유지(vasomotion) 및 최소 내강 직경(minimum luminal diameter)을 비교하는 ABSORB II 연구(clinicaltrials.gov identifier, NCT01425281)가 진행 중이며 1년째 중간 분석에서 임상 사건 발생이 3% 대 5%로 유사한 것으로 발표되었다[52]. 미국 식약청(U.S. Food and Drug Administration)의 허가를 위해 대규모 무작위 배정, 임상연구인 ABSORB III 연구(clinicaltrials. gov identifier, NCT01751906)와 다 기관 등록 연구로 ABSORB Extend 연구(clinicaltrials.gov identifier, NCT01023789)가 진행되어 결과를 기다리고 있다.
REVA bioabsorbable stent
1세대 REVA (Reva Medical, San Diego, CA, USA) BRS는 약물을 방출하지 않는 형태로 27명의 환자를 대상으로 RESORB 연구에서 적용되었으나 스캐폴드의 문제로 인해 4-6개월째 재시술이 많았다. 이를 개선하고자 스캐폴드 디자인(slide-lock, ratchet) 및 중합체(tyrosine-derived polycarbonate polymer)의 가공 공정의 개선, sirolimus 방출하도록 하여 ReZolve BRS가 개발되었다(Fig. 4). 아직 최초 임상 시험의 결과가 보고되지 않았으나 50명의 환자를 대상으로 RESTORE 연구(clinical trials.gov identifier, NCT01262703)가 진행 중이다.
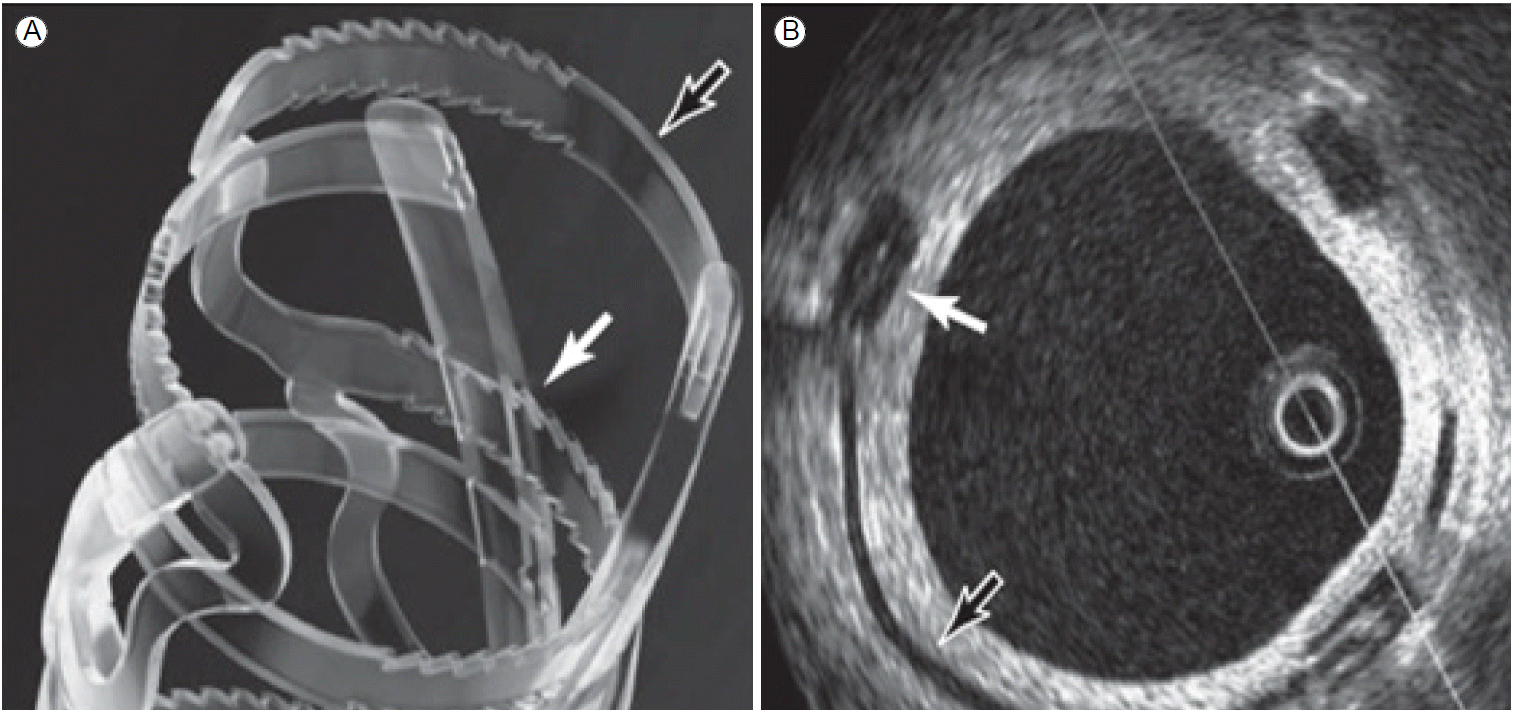
The REVA bioabsorbable stent. (A) The REVA bioresorbable scaffold features a unique slide-and-lock mechanism (black and white arrows) that permits the lumen of the scaffold to be enlarged without concentrating strain on the hinge points (unlike standard polymeric scaffolds). After expansion of the ReZolve scaffold, the locking mechanism maintains the expansion and affords radial strength. (B) An optical coherence tomography image. The strut (thickness, 120 μm) is indicated by the black arrow; the white arrow indicates the ratchet (strut thickness, 250 μm).
DESolve bioresorbable scaffold
DESolve (Elixir Medical Corporation, Sunnyvale, CA, USA) 스캐폴드는 poly-L-lactic acid 중합체로 구성되며 구조는 그림 5와 같다. 3 mm 두께로 poly-D, L-lactide가 코팅되어 sirolimus의 대사물인 myolimus (Novartis, Basel, Switzerland) 또는 novolimus (Elixir Medical, Sunnyvale, CA, USA)를 방출한다. DESolve First-in-Man 연구[53]는 myolimus 방출 스캐폴드를 단순 병변을 가진 16명의 환자에 적용하여 6개월째 조영술에서 비교적 좋은 후기 내강 소실, 0.19 mm를 보여 주었고, 1명의 환자에서 재시술이 발생하였다. 현재는 120명의 환자를 대상으로 novolimus를 방출하는 스캐폴드를 이용한 무작위 배정 임상 연구가 진행 중이다.

The DESolve stent (Elixir Medical Corporation, Sunnyvale, CA, USA). (A) The balloon-mounted scaffold (black arrow); radiopaque markers (white double arrow). A gap is evident gap between the balloon marker (M) and the scaffold. (B) The scaffold features in-phase sinusoidal hoops linked by three straight connectors. (C) A scaffold post-dilated to a diameter of 4.75 mm without strut fracture.
결 론
1980년대부터 30여 년간 관상동맥 스텐트의 변천사를 살펴보면 기존의 스텐트가 갖는 문제점을 찾아내고 개선하여 더 나은 임상 결과를 얻고자 했던 노력을 엿볼 수 있다. 흥미로운 점은 오래전 개발된 금속 그물망은 임상 상황에 따라 여전히 시술되고 있는 데 반해, 1세대 약물 방출 스텐트인 Cypher와 Taxus는 강력한 신생내막 증식 억제효과로 각광을 받았음에도 스텐트 혈전증과 같은 안전성의 문제로 더 이상 시술되지 않는다는 점이다. 현재 우리나라에서는 2세대 약물 방출 스텐트가 주로 사용되지만 생융해성 폴리머를 갖는 약물방출 스텐트가 좋은 임상 결과를 보여주고 있으며, 국내에 곧 도입될 생체융해성 스캐폴드의 비중도 늘어날 전망이다. 생체융해성 스캐폴드의 경우 아직까지 시술 경험이 없고, 분지부나 만성 폐색 및 좌주간지 등의 복합 병변에 대한 임상 결과가 부족하다. 하지만 스텐트 시술 이후의 장기적인 안전성을 고려하고 생체융해성 스캐폴드 시술 후 혈관 고유의 기능을 유지하여 예후를 개선하는 결과와 이어진다면 관상동맥 스텐트의 변천사에 큰 갈림길이 될 것이다.