내장 유충 이행증과 안구 유충 이행증이 동시에 발현된 개회충증 1예
A Case of Toxocariasis with Visceral Larva Migrans Combined with Ocular Larva Migrans
Article information
Abstract
저자들은 수년 전부터 정기적으로 다량의 소의 육회, 간, 천엽을 생식하는 51세 여자 환자에서 내장 유충 이행증과 안구 유충 이행증이 병발하여 알벤다졸과 스테로이드 치료로 후유증 없이 호전된 1예를 경험하였기에 문헌고찰과 함께 보고하는 바이다.
Trans Abstract
Toxocariasis is an infection in a human host caused by Toxocara canis or Toxocara cati larvae. Clinical manifestations are classified according to the organs affected, such as visceral larva migrans (VLM) and ocular larva migrans (OLM). Epidemiological evidence suggests that OLM tends to occur in the absence of systemic involvement and vice versa, which has led to two manifestations of this infection being reclassified as VLM and OLM. No case of a patient with VLM combined with OLM has been reported in Korea. Here, we report a case of VLM combined with OLM in a 51-year-old female caused by massive ingestion of raw cow meat, manyplies, and liver. (Korean J Med 2012;83:543-549)
서 론
개회충증(Toxocariasis)은 개나 고양이를 숙주로 하는 개회충(Toxocara canis)과 고양이회충(Toxocara catis)에 의한 인간 감염이다. 감염은 충란에 오염된 흙 또는 채소를 섭취하거나 유충을 가지고 있는 감염된 연장숙주(paratenic host)를 생식함으로써 일어난다.
임상적으로 대부분의 환자가 무증상이나, 유충이 소장벽으로 침투한 후 간문맥을 침범하여 간, 폐, 안구, 뇌, 심장 등 다양한 장기로 이동하면서 출혈, 괴사, 호산구성 염증을 일으키며 증상을 발현할 수 있다. 개회충중은 주요 침범 장기에 따라 내장 유충 이행증(visceral larva migrans)과 안구 유충 이행증(ocular larva migrans)으로 분류되기도 하는데 이는 안구 유충 이행증은 안구 및 시신경 외에 다른 장기를 침범하지 않고 내장 유충 이행증 또한 안구 및 시신경을 침범하지 않는 경향이 있기 때문이다[1]. 폴란드 시골 지역에 매일 가축과 접촉하는 학동기 아동에게서 내장 유충 이행증과 안구 유충 이행증이 병발한 예가 보고되었으며[2] 아직까지 국내에서 보고된 사례는 드물다. 이에 저자들은 내장 유충 이행증과 안구 유충 이행증이 병발한 1예를 경험하였기에 문헌고찰과 함께 보고하는 바이다.
증 례
51세 여자 환자가 내원 1주일 전부터 발생한 상복부통증으로 응급실에 내원하였다. 계통적 문진상 두통, 어지러움, 졸음, 시야결손을 호소하였다.
환자는 내원 일주일 전 건강 검진에서 당뇨병을 진단받았으나 치료받지 않았고 수년 전부터 정기적으로 1년에 2회 500 g 정도되는 소의 육회, 간, 천엽을 생식한 기왕력이 있었으며 가족력상 특이사항은 없었다.
내원 당시 활력 징후는 혈압 130/90 mmHg, 맥박 분당 80회, 호흡수 분당 20회, 체온 36.0℃였다. 신체검진에서 경부에 특이소견 및 임파선 촉지는 없었고, 흉부에 호흡음 및 심음에 이상은 없었다. 복부 촉진에서 간비대 소견을 보였으며 압통과 반발압통은 없었고 신경학적 검사에서 의식은 기면 상태였고 정상 뇌신경기능을 보였으며 운동능력은 우측 상지가 Grade III, 우측 하지가 Grade IV였고 그 외에 이상소견은 없었다. 혈액검사에서 백혈구 19,300/mm3 (중성구 분율 35%, 호산구 분율 34%), 혈색소 13.4 g/dL, 혈소판 162,000/mm3였고 말초혈액 호산구 수는 6,562/m3 (정상치 < 500/mm3), 총 IgE는 610 IU/mL (정상치 0.10-200.0 IU/mL)로 증가되어 있었으며 말초혈액 도말 검사는 심한 호산구 증가 외 다른 이상 소견은 없었다.
혈청 생화학 검사상 AST 66 IU/L, ALT 36 IU/L, 총 빌리루빈 0.79 mg/dL, C-반응성 단백질 1.62 mg/dL이었으며 뇌척수액검사상 백혈구 2/μL, 포도당 113 mg/dL, 단백질 81 mg/dL로 수막염 소견은 없었다. 개회충 유충의 분비 배설항원(Toxocara excretory secretary antigen, TES-Ag)에 대한 IgG 항체를 검출하는 ELISA kit 결과는 0.302 (양성 표준혈청역가 > 0.250)로 의미 있게 증가되어 양성이었다. 대변 충란 검사는 음성이었으며 간흡충, 폐흡충, 유구낭충, 스파르가눔 항원에 대한 혈청 특이 IgG 항체 검사결과는 모두 음성이었다.
흉부 전산화 단층 촬영에서 양측 폐야를 침범하는 경계가 불분명한 다발성 결절성 병변들이 관찰되었고(Fig. 1A), 복부 전산화 단층 촬영에서 간 양엽에 1 cm 미만의 다발성 저음영 병변들이 관찰되었다(Fig. 2A). 뇌 자기공명영상에서는 양측 전두엽, 후두엽과 소뇌에서 다발성 뇌경색을 보였다 (Fig. 3A). 안저검사에서 좌안 시신경의 이측 하방에서 황반부에 근접해 있는 경계가 분명한 염증성 부종으로 둘러싸인 황백색의 융기된 육아종성 단일 병변이 관찰되었고(Fig. 4A)우안은 특이사항이 없었다.
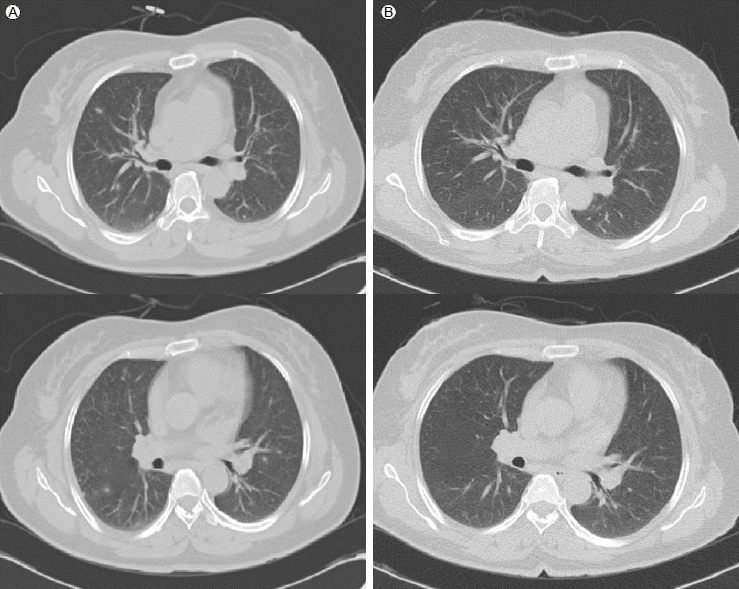
Chest computed-tomography (CT) findings. (A) CT scan shows multifocal, ill-defined, nodular ground-glass opacity in both lungs. (B) The CT scan shows improvement of the lesions 5 months after albendazole treatment.
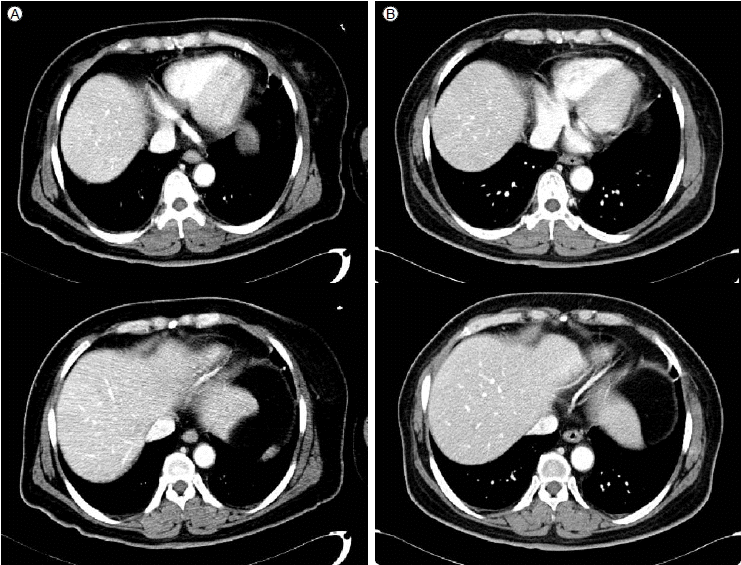
Abdominal computed-tomography (CT) findings. (A) CT scan shows multiple subcentimeter-sized low-attenuated lesions in the liver. (B) CT scan shows improvement of the lesions 10 weeks after albendazole treatment.
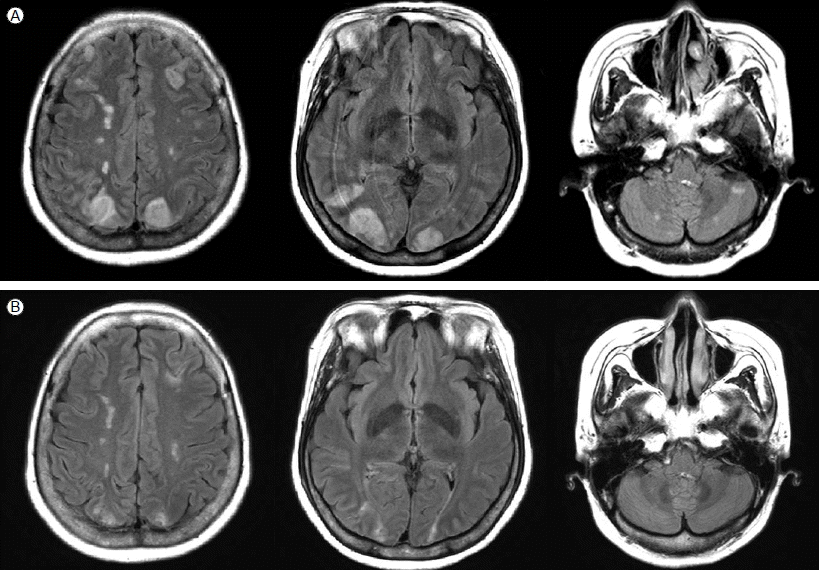
Brain magnetic resonance imaging (MRI) findings. (A) Axial fluid attenuated inversion recovery MRI shows multiple hyperintense lesions in both frontal lobes, occipital lobes, and the cerebellum. (B) MRI scan shows improvement of the lesions 2 weeks after albendazole treatment.

Fundoscopic findings. (A) A round, yellow-white elevated granulomatous lesion and macular edema are seen in the macula of the left eye. (B) The lesion disappeared 6 months after albendazole treatment.
상기 병력 및 검사결과를 토대로 소의 육회, 간, 천엽 생식 후 개회충 감염에 의한 간, 폐, 중추신경계, 안구를 침범한 개회충증으로 진단하고 알벤다졸(albendazole) 400 mg을 하루 2회씩 2주 동안 투여하였고, 프레드니솔론(prednisolone) 30 mg을 하루 2회씩 5일간 투여 후 점차로 감량하여 치료 후 시야결손 및 두통이 소실되고 의식이 명료해졌으며 우측편 마비 증세 호전을 보이고 알벤다졸 투약 2주 후 뇌 자기공명영상에서 양측 전두엽, 후두엽과 소뇌에서 관찰되던 병변(Fig. 3B)과 안저검사에서 관찰되던 병변이 호전되어 퇴원약으로 프레드니솔론 5 mg을 처방하고 입원 54병일째 퇴원하였다. 알벤다졸 투약 10주 후 호산구는 1,917/mm3로 감소하였고 복부전산화 단층촬영에서 저음영 병변들의 개수는 감소하였으며(Fig. 2B) 투약 12주 후 프레드니솔론 중단하였고 투약 5개월 후 흉부 전산화 단층 촬영에서는 대부분의 결절이 소실되었으며(Fig. 1B) 투약 6개월 후 안저검사에서 병변은 소실되었다(Fig. 4B). 알벤다졸 투약 8개월 후 호산구는 1,260/mm3로 감소하였고 복부전산화 단층촬영에서 이전에 보였던 간농양이 완전히 소실되었으며 현재 특별한 증상 없이 추적관찰 중이다.
고 찰
개회충증은 세계 대부분의 지역에서 각기 다른 유병률로 보고되고 있으며[3] 서구의 연구에 따르면 유아나 학동기 아동에서 오염된 토양 및 감염된 강아지와 접촉이 많으므로 발생 위험률이 높다고 알려졌으나[4] 서구의 연구 결과와는 다르게 생야채, 익히지 않은 고기 및 동물의 내장을 먹는 식습관을 가진 우리나라에서는 충란에 오염된 야채나 유충이 포함된 초식 동물의 간과 근육을 생식하는 성인에서 발생 위험률이 높은 것으로 보고되고 있다[5].
개회충증의 임상양상은 이동한 유충이 인간의 장기에 직접 기계적 손상을 일으키거나 유충이 분비배설 항원을 통해 IgE 매개 독성을 일으키는 면역병리학적인 기전에 의한 것으로 알려져 있다[6]. 개회충증 환자의 대부분은 무증상이나 발생 가능한 임상적 특징으로는 백혈구 및 호산구의 증가, 만성피로 그리고 발열과 전신 무력감 등의 전신증상과 함께[3,4] 침범되는 장기에 따라 간과 폐를 침범하여 간비대나 천식을 일으키거나 드물게 안구에 침범하여 포도막염이나 망막병변을 일으키며 중주신경계를 침범하여 간질, 행동 장애, 뇌경색 등을 일으킨다[1,5].
개회충증은 임상양상에 따라 세 가지로 분류되는데 부화된 유충이 소장 벽을 뚫고 혈류를 통하여 간, 폐, 뇌 등의 신체 각 장기에 유충이 이행함으로써 나타나는 내장 유충 이행증, 3기 유충에 의해 안구 및 시신경이 손상받는 안구 유충 이행증[1], 내장 유충 이행증과 안구 유충 이행증의 범주에 속하지 않으며 간비대, 기침, 불면증, 복부 통증과 같은 비특이적인 증상을 발현하는 숨은형 개회충증(covert toxocariasis)으로 나눌 수 있다[4,5]. 내장 유충 이행증과 안구 유충 이행증의 임상양상의 차이는 섭취한 충란과 유충의 수, 재감염의 빈도, 유충 이행 경로 및 숙주 면역 반응 등에 의해 결정된다[7]. 안구 유충 이행증은 이전에 개회충 종에 감작되지 않은 사람에게 보통 한 개의 3기 유충이 눈에 집락화한 결과로[4] 전신적인 면역반응이 일어나도록 자극되지 못하고 안구에만 국한적으로 유발되어 혈청 검사에서 TES‐Ag에 대한 IgG가 검출되지 않고 호산구증가증이 나타나지 않는 경우가 많다. 반면에 내장 유충 이행증은 다량의 충란이나 유충을 섭취하여 유충이 장기를 이행하면서 면역반응을 일으켜 증상이 나타나고 호산구증가증, IgE 증가소견이 관찰된다. 개회충의 균주에 따라 특정한 장기에 대한 친화성이 있어 침범하는 장기가 다르다는 의견도 있다[1]. 내장 유충이행증과 안구 유충 이행증은 이와 같은 임상적인 차이로 다르게 분류되었고 우리나라에서 두 임상상이 병발하는 경우는 보고된 바가 드물다. 이러한 증례가 드문 이유로는 안구 유충 이행증에서 내장 유충 이행증이 병발할 가능성이 낮은 것으로 알려져 있어서 안구 유충 이행증에 이환된 경우에 내장 유충 이행증에 대한 검사가 적절히 이루어지지 않아서 간과된 경우도 있을 수 있다.
국내에서 발표된 안구 유충 이행증 증례에서도 다른 전신 증상 및 이상소견은 없었고 생고기 및 간 등 생식을 한 기왕력은 82%로 보고되었다[8]. 본 증례에서는 환자가 수년간 매년 2회씩 다량의 소의 육회, 간, 천엽을 생식하여 많은 수의 개회충 유충을 섭취하였을 것으로 의심되며 다양한 개회충의 균주가 섭취되어 각각 친화성이 있는 장기로 이행되어 내장 유충 이행증과 안구 유충 이행증이 병발했을 가능성이 있으며, 수년간 정기적으로 생식을 하였기 때문에 이미 내장 유충 이행증에 이환되었으나 무증상으로 지내다가 안구 유충 이행증이 새롭게 이환되었을 가능성도 있다.
임상적으로 대부분의 개회충증 환자가 무증상이어서 주로 호산구증가증을 평가하는 과정에서 진단되며, 확진은 이환된 장기의 조직검사로 유충의 여부를 확인하는 것이나 침습적이고 진단율이 높지 않아 최근에는 혈청학적 검사로 진단을 하는 경우가 많다[1]. 혈청학적 검사로 가장 흔하게 사용되는 진단 방법은 개회충의 2기 유충의 분비배설 항원이나 추출항원을 이용한 TES‐ELISA 검사이며 다른 기생충 감염과의 교차반응을 일으킬 수 있고 과거 감염에서도 TESELISA검사가 양성으로 나올 수 있으므로 혈청 IgE 증가, 호산구증가증이 동반되고 애완동물을 기르거나 소, 닭 등의 고기, 내장을 생식하여 개회충에 노출된 병력 및 임상소견을 종합하여 현성 감염으로 진단한다[3,6]. 혈청 외에도 안구 유충 이행증의 경우 방수(aqueous humor)로, 중추신경계를 침범한 경우 뇌척수액으로 TES‐ELISA 검사를 하는 것이 진단에 도움을 줄 수 있다[3]. 본 증례에서는 방수 및 뇌척수액으로 TES‐ELISA 검사를 시행하지 않았지만 소의 간, 육회, 천엽을 생식한 기왕력이 있고 혈청 TES‐ELISA 검사가 양성이며 안저검사 결과 전형적인 육아종성 단일 병변이 관찰되었고 항구충제와 전신스테로이드 치료 후 시야결손이 호전되고 안저검사상 병변이 사라졌으며 신경학적 결손 및 뇌 자기공명영상에서 관찰되었던 다발성 병변이 호전되어 안구 유충 이행증과 중추신경계를 침범한 내장 유충 이행증으로 진단할 수 있었다.
개회충증의 장기 침범 여부 및 정도를 진단하기 위해서는 영상학적 검사가 필요하다. 간 병변은 복부전산화 단층촬영에서 다발성의 저음영 종양으로 나타나는 경우가 많고[4] 흉부전산화 단층촬영에서 가장 흔하게 관찰되는 폐 침윤소견은 한쪽 혹은 양쪽 폐야를 침범하는 무작위로 분포된 젖빛유리혼탁이며 이동성을 특징으로 한다[9]. 중추신경계를 침범한 경우 뇌 전산화 단층촬영 및 뇌 자기공명영상에서 비특이적으로 다양하게 나타나며 본 증례에서와 같이 T2-강조 자기공명영상에서 고강도로 나타나는 다발성의 국한된 병변으로 보고된다[4,7].
호산구증가증만을 동반한 무증상의 감염은 저절로 치유되므로 치료를 요하지 않지만 증상을 동반하거나 내장 유충이행증 및 안구 유충 이행증에 이환된 환자는 치료의 적응 증이 된다. 표준화된 치료법은 없으며 현재는 알벤다졸 400 mg을 하루 2회 5일간 복용하는 방법이 추천되나[1] 5일간 치료 후 호전되지 않거나 재발하는 경우도 보고되므로 치료 기간이 경과에 따라 10일에서 1개월까지 연장될 수 있으며[2,10] 적절한 치료 기간에 대한 연구는 더 필요하다.
구충제로 죽은 유충이 심한 과민반응을 일으킬 수 있기 때문에 전신스테로이드가 급성 염증 반응 및 면역학적 반응을 감소시키기 위하여 사용되며, 특히 전신증상이 심하거나 안구 및 중추신경계, 심근을 침범하였을 경우에 구충제에 추가되어 사용된다[4,5].
결론적으로 생식 문화가 있는 우리나라에서는 성인 환자가 다량의 개회충 유충을 섭취할 수 있으므로 개회충증이 호발하는 연령 및 발현되는 임상증상이 기존의 서구에서 연구된 결과와 다르게 나타날 수 있다. 현재까지 서구의 연구에 의하면 내장 유충 이행증과 안구 유충 이행증은 병발하는 경우가 드물며 이환되는 기전 및 임상소견이 다르게 분류되었다. 내장 유충 이행증과 안구 유충 이행증이 병발하여 임상적으로 발현하는 것은 드문 증례임을 보고하며 생식을 많이 한 기왕력이 있어 개회충의 유충을 다량으로 섭취하였을 것이 의심되는 내장 유충 이행증 환자가 시야결손을 호소할 때 안구 유충 이행증이 병발할 수 있는 가능성을 고려하여야 하겠다.