중증난치천식과 유전학
Severe Refractory Asthma and Genetics
Article information
Trans Abstract
Asthma is multifactorial complex disorder originated from genetic and environmental factors. Some genetic variants or alleles have been known to be associated with the presence or development of asthma. Gene polymorphisms may be associated with declined lung function and severe exacerbations in asthma, indicating the contribution of genetic variants to the development of severe refractory asthma. Severe refractory asthma is heterogeneous disease and may be classified into various phenotypes and endotypes. Each endotype might be characterized by the presence of gene polymorphisms, which might be useful to determine an endotype. In addition, patients with severe refractory asthma have been known to respond differently to asthma medications, which may be explained by pharmacogenetics. Polymorphisms in the genes related to the pathway or receptors for drugs may determine the good or poor responses to the medication. The pharmacogenetic studies may allow patients with severe asthma to take the most effective personalized medicine, which may control severe refractory asthma well. Collectively, genetic testing for the presence of severe asthma and pharmacogenetics for asthma medications may be useful for the diagnosis and management of severe refractory asthma. (Korean J Med 2012;83:430-437)
서 론
천식은 기도의 만성염증성 질환으로 유전자와 환경인자가 다양하게 복합적으로 작용하여 발생되는 다인자복합질환 (multifactorial complex disease)이다. 유전적 소인을 가진 환자가 환경인자와 결합하면 기도에 알레르기염증이 생기고 천식이 발생한다. 유전적 요인은 약 36-79% 정도 천식 발생에 영향을 미치는 것으로 알려져 있다[1-3]. 부모 중 한 사람이 천식을 가지고 있으면, 자녀는 2배 정도 천식에 걸릴 가능성이 높아지고, 쌍둥이 연구에서 천식발생 일치율은 일란성에서 19%, 이란성에서 4.8%로 일란성에서 이란성에 비해 4배 정도 높다[4].
대부분 경증 및 중등도 천식은 흡입스테로이드 등의 천식약물에 잘 반응하여 큰 문제없이 잘 조절되지만, 중증난치천식(이하 중증천식)은 천식약물에 대한 반응이 좋지 않아 치료하기가 매우 어렵다. 중증천식 환자는 전체 천식의 10%정도이지만, 중증천식으로 인한 사회경제적 비용은 천식으로 인한 전체 비용의 많은 부분을 차지하고 있다[5]. 향후 중증천식에 대한 병인기전 연구와 효과적인 치료제 개발이 필요하다.
2000년도 미국 NIH의 National Heart, Lung, and Blood Institute에서 중증천식에 대한 모임을 만들어 2001년 8개의 대학 또는 병원이 참여하는 Severe Asthma Research Program (SARP)이 시작되었고[6], 2000년도 American Thoracic Society (ATS)에서 중증천식에 대한 정의 및 기준을 발표하였다[7]. 유럽에서는 European Network for Understanding Mechanisms of Severe Asthma (ENFUMOSA)를 만들어 중증천식을 연구하고 있었다[8]. SARP는 ATS의 중증천식의 기준을 이용하여 중증천식 환자를 모집하여, 임상적, 생리학적, 유전학적,방사선학적 특징을 평가하여 중증천식을 분석하였다[9]. 중증천식이 단일 질환이 아닌 이질적 질환으로 다양한 표현형을 가지고 있는 것으로 알려지게 되었고, 최근 SARP에서는 중증천식 환자를 5개의 클러스터로 분류하기도 하였다[10]. 가장 최근에는 기능적 또는 병태생리학적 기전을 중심으로 중증천식의 endotype을 분류하려는 시도를 하고 있으며, 자연경과, 임상적 소견, 병태생물학적 소견, 생물표지자, 치료에 대한 반응을 중심으로 분류하며, 유전학적 소견도 포함되어 있다[11].
중증천식은 최소한 6개월 이상 충분히 치료를 잘 하더라도 조절이 되지 않는 경우를 주로 말하는 것으로 알려져 있기 때문에[12], 천식약물 치료에 대한 반응이 부족하거나 없는 경우도 중증천식에 포함될 수 있다. 또한 천식 환자는 동일한 약물에 대한 치료 반응이 매우 다를 수 있다. 이러한 현상은 약리유전학(pharmacogenetics), 즉 약물의 수용체 및 대사 경로에 관련된 유전자의 변이에 따른 차이로 설명할 수 있다.
저자는 ① 천식의 발생에 관련되는 유전자 변이, ② 천식의 중증도에 관련되는 유전자 변이, ③ 천식약물과 관련된 약리유전학 등과 관련된 최근 지식을 정리하여, 중중천식에서 유전학의 역할을 기술하고자 한다.
실제로 환자진료에서 유전자 검사를 진단 및 치료에 이용하고 있다. 예를 들면 과다호산구증후군 환자에서 FIP1L1/PDGFRA (F/P) 유전자 변이를 검사하여 양성이면 F/P-positive myeloproliferative variant를 진단하고, 효과적인 약물로 imatinib를 사용한다. 향후 천식 및 알레르기분야에서도 유전자 변이를 검사하여 중증천식의 진단, endotype의 결정, 효과적인 천식약물의 선택 등의 환자 진료에 중요한 정보를 제공할 수 있을 것으로 기대해 본다.
천식의 발생에 관련되는 유전자
천식은 유전적 질환으로 특정한 유전자 변이를 가진 사람에서 천식이 잘 발생할 수 있다. 유전자 변이는 candidate gene approach, linkage study, genom-wide association study (GWAS) 등의 방법을 통해 확인 한다. Candidate gene approach 및 linkage studies 검사를 통해 현재까지 알려진 중요한 천식발생에 관련되는 천식유전자를 표 1에 정리하였다. 천식유전자는 천식의 중간표현형, 예를 들면 총 IgE 증가, 피부단 자시험 양성, 기도과민성 존재, 호산구 증가 등과 관련성을 나타낼 수 있기 때문에 천식유전자와 각 중간표현형과의 관련성도 기술하였다. 이들 중에서 disintegrin and metalloprotease 33 (ADAM33) 20p13 [13], dipeptidylpeptidase 10 (DPP10) 2q14.1 [14], plant homeodomain zinc finger protein 11 (PHF11) 13q14.2 [15], G protein-coupled receptor for asthma susceptibility (GPR) 7p15-p14 [16], and prostaglandin D2 receptor (PTGDR) 14q24 [17] 천식유전자는 천식 발생과 비교적 강하게 관련되는 것으로 알려져 있다.
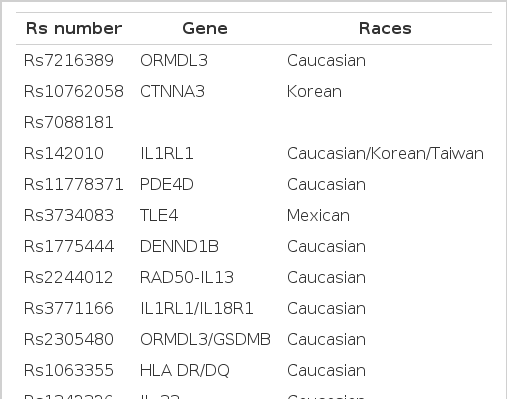
GWAS 연구를 통해 알려진 중요한 천식유전자는 표 2에 정리하였다. 이들 유전자들 중 반복연구 또는 메타분석을 통해 일관성 있게 천식발생과 연관이 있는 것으로 확인된 유전자는 ORM1-like 3 and gasdermin B (ORMDL3-GSDMB), IL-33, IL-1 receptor-like 1 (IL-1RL1), RAD50 homolog and IL-13 (RAD50-IL13), major histocompatibility complex class II DR/DQ (HLA-DR/DQ) 등으로 알려져 있다.
많은 유전자들이 천식의 발생과 관련되는 것으로 알려져 있지만, 사실 각 유전자의 천식발생에 기여하는 위험율 (attributable risk fraction)은 3.9-24% 정도로 낮은 편이다[18]. 즉, 천식의 발생에 영향력이 강한 미지의 천식유전자가 존재할 것으로 생각되며, 더 많은 연구를 통해 천식유전자를 발견해야 될 것이다.
중증천식과 관련되는 유전자
유전적 요인이 천식의 중증도에 영향을 주어 중증천식의 발생에 관련할 수 있다. 중증천식이 아프리카계 미국흑인에서 많이 발생하는 현상은 유전적 요인이 중증천식의 발생에 관련될 가능성을 시사한다. 천식의 발생에 관여하는 천식유전자가 천식의 중증도 또는 중증천식의 발생에 모두 관련되지 않을 것이며, 천식의 발생과 관련이 없는 유전자가 중증천식의 발생에 관여할 수 있을 것이다. 천식의 중증도 및 중증천식의 발생과 관련된 유전자 변이를 소개하면 다음과 같다.
RAD50/IL13 및 HLA DR/DQ
중증천식 환자를 대상으로 GWAS를 분석한 결과, 염색체 5q31.1에 있는 RAD50-IL13 유전자 변이가 중증천식의 발생과 관련성이 있으며, 염색체 6p21.3에 위치해 있는 HLA-DR/DQ 유전자 변이도 중증천식의 발생과 관련되는 것으로 보고되었다[19].
ADAM33
ADAM33 유전자 변이는 천식의 발생 유전자로 언급하였다. 그러나 200명의 천식 환자를 대상으로 20년 이상 종적으로 관찰하였을 때, ADAM33 유전자 변이를 가진 천식 환자에서 더 심한 FEV1의 점진적 감소를 보였다. 이는 오랜 천식에서 발생하는 기도폐쇄의 비가역적 변화를 의미하며, 기도개형으로 설명한다[20]. 일반인을 대상으로 한 연구에서도 ADAM33 유전자 변이는 폐기능의 점진적 감소와 관련되었고, 만성폐쇄성폐질환 환자에서 ADAM33 변이의 빈도가 증가됨이 보고되었다[21]. 흡연 환자에서 ADAM33 유전자 변이는 만성폐쇄성폐질환의 발생 및 폐기능 감소와 관련되었다[22]. 따라서 천식에서 ADAM33 유전자 변이는 천식의 발생에도 관여하지만, 폐기능의 점진적 감소와 관련된 기도개형 및 중증천식의 발생에도 관여될 것으로 보인다.
Hedgehog interacting protein (HHIP)
2009년 Framingham 심장 연구에 참여한 일반인을 대상으로 GWAS 분석하여 염색체 4번에 존재하는 HHIP 유전자 변이가 FEV1/FVC의 감소와 관련되는 것으로 보고되었고[23], 일반인을 대상으로 한 2010년 CHARGE Consortium 연구[24]와 SpiroMeta consortium 연구[25]에서도 HHIP 유전자 변이가 FEV1/FVC 감소와 관련되는 것이 재현되었다. 일반인에서 얻은 상기 HHIP 유전자 변이와 폐기능 감소의 관련성을 중증천식 환자들을 대상으로 관련성 분석을 시행하였다. HHIP 유전자 변이는 FEV1 및 FVC 감소와 관련되었고, 기도폐쇄의 가역성과도 관련되었다. 폐기능과 관련성 있는 것으로 알려진 다른 유전자 patched homolog 1 (PTCH1) 및 family with sequence similarity 13, member A (FAM13A)를 포함하여 joint analysis를 시행하였을 때, 유전자 개수가 증가할수록 FEV1, FVC, FEV1/FVC이 더 심하게 감소되었다. 폐기능과 관련된 2개의 다른 유전자 phosphotyrosine interaction domain containing 1 (PID1)과 notch 4 (NOTCH4)를 추가하여 총 5개의 유전자를 가지고 분석하였을 때도 유전자 개수가 증가할수록 FEV1은 더 감소되었고, ATS 기준에 의한 천식의 중증도 또는 SARP 연구에서 분류된 천식중증도 클러스터에서도 중증 천식 또는 클러스터를 가진 환자 수가 증가되었다. 그러나 이 연구에서 HHIP 유전자 변이와 천식의 발생과는 관련성이 없었다[26]. 따라서 HHIP 유전자 변이는 천식의 발생에는 관여하지 않지만, 천식의 중증도 및 중증천식의 발생에 강하게 관련되는 것으로 보인다.
IL-1RL1
천식은 호산구 기도염증을 특징으로 하며, 호산구 염증이 증가되면 천식의 중증도가 심해질 수 있다. 2번 염색체에 있는 IL-1RL1 유전자 변이가 천식의 발생과 호산구 증가와 관련되는 것으로 알려져, IL-1RL1 유전자 변이가 중증천식의 발생에 관여할 수 있을 것이다. 호산구 및 천식과 관련되는 다른 유전자로는 WD repeat domain 36 (WDR36), IL-33 유전자 등도 있다[27].
IL4 receptor, alpha (IL-4RA)
IL-4RA R576 유전자 변이는 천식의 발생뿐만 아니라, 폐기능 감소 및 천식의 중증도와 관련되는 것으로 보고되었다 [28]. SARP 환자를 포함하는 중증천식 환자에서 IL-4RA 유전자 변이, 특히 E375A와 Q551R 변이는 천식의 중증 악화 즉, 중환자실 입원 또는 생명 위협 천식악화 발생과 관련되었다. 기관시내시경 조직검사를 통해 IL-4RA 유전자 변이와 조직의 알레르기염증과의 관련성을 최초로 분석하였으며, E375A 유전자 변이가 있는 경우에 조직 내 비만세포의 수가 증가되고 비만세포 표면의 IgE 양이 증가되었다. 이러한 소견은 중증천식에서 잘 나타나기 때문에 IL-4RA 유전자 변이는 천식의 중증 악화와 관련된다고 볼 수 있다[29].
천식에서 약리유전학
천식약물에 대한 치료반응은 환자에 따라 다르다. 동일한 약물을 사용하더라도 환자에 따라 치료효과가 좋은 경우가 있고 그렇지 않는 환자가 존재한다. 이러한 반응 차이는 약물에 대한 반응 유전자의 변이가 원인일 수 있다. 중증천식은 약물치료에 대한 반응이 매우 좋지 않는 경우를 포함하기 때문에[12], 약물치료에 효과가 없는 유전자 변이를 가지고 있는 천식 환자는 중증천식 환자일 수 있다. 또한 약물유전자 변이를 검사하여 중증천식 환자에게 효과적인 천식약물을 처방한다면 천식조절이 매우 잘 될 수 있을 것이다.
베타2항진제
1997년 천식 환자에서 속효성베타2항진제를 흡입한 후 FEV1 증가 여부를 관찰하는 연구를 시행하여, ADRB2 유전자 16번 codon에 arginine 동형접합체 유전자가 있는 경우에 glycine 동형접합체를 가진 경우에 비해 5.3배 반응이 좋은것으로 보고되었다[32]. 그러나 2000년 천식 환자에게 속효성베타2항진제를 지속적으로 투여하면서 반응을 관찰하였고, arginine 동형접합체 유전자를 가진 환자에서는 천식악화의 빈도가 높은 것으로 보고되었다[33]. 2004년 arginine 동형접합체를 가진 천식 환자에게 지속적으로 속효성베타2항진제를 투여하였을 때 폐기능이 감소되고 증상의 악화가 발생되었다[34].
지속성베타2항진제에 대한 반응은 다를지도 모른다. 속효성베타2항진제 경우와 마찬가지로, 2006년 지속성베타2항진제를 지속적으로 사용하는 arginine 동형접합체를 가진 환자에서 폐기능이 감소되고 증상 조절이 잘 되지 않음이 보고되었다[35]. 그러나 2009년[36]과 2010년[37] 지속성베타2항진제에 대한 치료반응은 ADRB2 유전자 변이와 관련성이 없는 것으로 보고되었다. 국내보고에서는 43명의 천식 환자를 대상으로 ADRB2 유전자를 분석한 결과, arginine 동형접합체를 가진 경우에 외국보고와는 달리 지속성베타2항진제에 대한 반응이 오히려 좋아서 폐기능이 증가되고 천식조절이 더 잘 되는 것으로 보고되었다[38]. 인종에 따른 약리유전학의 차이도 고려할 필요가 있을 것이다.
최근 베타2항진제에 대한 치료반응과 관련된 것으로 알려진 다른 유전자로는 arginase 1과 arginase 2 유전자, S-nitrosoglutathione reductase (GSNOR) 유전자가 있다.
흡입스테로이드
중증천식 환자는 스테로이드 저항이 잘 발생하며 고용량 흡입스테로이드 또는 전신스테로이드를 사용해야 되는 경우들이 많고, 중증천식에서 스테로이드 무감응(insensitivity)의 기전은 보고되고 있다[39]. 스테로이드 수용체 유전자로 nuclear receptor subfamily 3, group C, member 1 (NR3C1)이 있으며, NR3C1 유전자 변이가 있는 경우 스테로이드에 대한 치료 반응이 좋은 것으로 보고되었다[40]. 다른 유전자로는 stressinduced-phosphoprotein 1 (STIP1) 유전자가 있으며, 이는 스테로이드 수용체를 활성화하는 단백질을 담당하는 유전자이다. STIP1 유전자 변이도 흡입스테로이드에 대한 FEV1 증가와 관련되었다[41]. Corticotropin releasing hormone receptor 1 (CRHR1) 유전자 변이도 스테로이드에 대한 반응이 좋은 것으로 보고되었다[42]. T-bet 전사인자를 담당하는 T-box 21 (TBX21) 유전자 변이는 흡입스테로이드에 대한 기도과민성의 호전과 관련되는 것으로 보고되었다[43]. 반대로 glucocorticoidinduced transcript 1 (GLCCI1) 유전자 변이는 흡입스테로이드에 대한 반응 감소와 관련되었다[44]. 저친화성 IgE 수용체인 Fc fragment of IgE, low affinity II, receptor for CD23 (FCER2) 유전자 변이는 흡입스테로이드를 사용하고 있는 천식 환자에서 악화에 의한 입원율 증가, 증상악화, 스테로이드 용량이 증가 등의 지표와 관련되었다[45].
류코트리엔 조절제
류코트리엔 생성에 관여하는 경로 또는 수용체에 관여하는 유전자의 변이는 류코트리엔 조절제의 치료반응에 영향을 줄 수 있다. 류코트리엔 생성에 관여하는 arachidonate 5-lipoxygenase (ALOX5)의 유전자 변이는 류코트리엔 조절제의 치료 효과에 영향을 줄 수 있다. ALOX5 promoter에서 tandem repeat polymorphism을 분석하였으며, 5/5 또는 4/5 repeat를 가진 환자에서 몬테루카스트 치료 후에 천식악화 빈도의 감소, FEV1 증가, 속효성베타2항진제 사용량 감소 등이 관찰되었다[46]. ALOX5 유전자 변이 중 하나인 rs2115819의 GG 동형접합체를 가진 환자는 6개월간의 몬테루카스트 치료 후 FEV1이 증가되었다[47]. 일본 연구에서는 천식 환자를 대상으로 leukotriene C4 synthase (LTC4S) 유전자 변이를 분석하여 프란루카스트에 대한 반응을 분석하였고, C (-444) 대립유전자를 가진 경우에 A (-444) 대립유전자에 비해 약물에 대한 효과가 좋아, FEV1이 증가된다고 하였다[48]. 류코트리엔 조절제 약물의 운반 단백질을 담당하는 유전자의 변이도 약물의 반응에 영향을 미칠 수 있다. 운반 단백질 유전자 solute carrier organic anion transporter family, member 2B1 (SLCO2B1) G 대립유전자 동형접합체를 가진 천식 환자에서 몬테루카스트의 혈청 약물 농도가 더 높았다[49].
중증천식의 분류에서 유전자 역할
중증천식은 단일 질환이 아닌 이질적 질환으로, 다양한 종류의 표현형 또는 endotype으로 분류될 수 있다. 이러한 분류는 각 종류에 맞는 치료제 개발을 가능하게 할 수 있다. 중증천식의 분류에 임상적 및 생물학적 특징뿐만 아니라, 유전자 변이도 도움이 될 수 있다. Wenzel [11]은 중증천식의 endotype을 early onset allergic, persistent eosinophilia, allergic bronchopulmonary mycoses, obese-female, neutrophilic 다섯 가지로 분류하였고, early onset allergic 형태에서는 17q12-21 Th2 pathway 유전자가 관여하고, persistent eosinophilia에서는 류코트리엔 경로에 관여하는 유전자가 관여될 수 있다고 하였다. 각 endotype에 특이한 유전자 변이가 있을 수 있고, 유전자검사를 통해 endotype의 결정에 도움이 될 수 있고, 이는 효과적인 치료제의 선택으로 이어질 수 있다.
중증천식에서 후성학(epigenetics)의 역할
유전자 연구의 결과는 연구하는 지역과 대상에 따라 그 결과가 상이할 수 있다. 이러한 현상은 천식의 병인기전에 다른 요인이 작용할 수 있다는 의미이고, 그중에 한 가지가 후성학이 될 수 있다. 후성학은 DNA 자체의 순서에 변이가 생긴 것이 아니라, DNA와 histone 단백질의 유전자부호해독 후 수정(post-translational modification) 과정에서 발생한다. Histone deacetylase (HDAC) 효소는 염증성 유전자 발현을 억제 또는 조절하는 역할을 한다. 최근 HDAC2가 스테로이드 수용체의 보조인자(cofactor)로 알려져 있으며, 스테로이드 작용에 필수분자로 알려져 있다. 중증천식에서는 HDAC 활성도가 감소되어 있고 스테로이드에 대한 반응 감소와 관련되어 있는 것으로 보고되어 있다[50]. 흡연 등의 산화스트레스도 HDAC 활성도를 감소시킬 수 있다. 환경적 요인에 의한 DNA methylation 등도 후성학 기전의 한 가지가 될 수 있고, 다른 기전으로는 microRNA (mRNA)에 의한 기전도 생각해 볼 수 있다. mRNA의 발현은 천식의 발생과 중증도에 영향을 미칠 수 있는 것으로 생각하고 있다[51].
결 론
천식에서 유전자 변이는 중증천식의 발생과 중증천식의 다양한 표현형 또는 endotype의 분류에 관련될 수 있다. 중증천식 환자들의 약물에 대한 반응은 서로 다르며, 이는 약리유전학에 의해 일부 설명이 가능하다. 중증천식의 발생과 약리유전학에 관련된 유전자 검사를 통해 중증천식의 진단, endotype의 분류, 효과적 약물 선택 등이 가능할 것으로 생각된다. 중증천식 환자에서 약물치료에 효과적인 반응을 담당하는 유전자 변이를 검사하여 개개인에게 효과적인 천식약물을 처방한다면, 개인적 맞춤치료가 가능하고, 매우 효과적으로 중증천식을 관리할 수 있을 것이다.
인종에 따라 유전자 변이가 중증천식 및 약리유전학에 대하여 미치는 영향이 달라질 수 있기 때문에 미국이나 유럽에서 시행된 유전자 연구 결과를 그대로 국내 중증천식 환자들에게 적용하는 것은 적절하지 않을 수 있다. 향후 국내의 중증천식 환자들을 대상으로 지속적으로 중증천식 관련 유전자 및 약리유전학에 대한 신빙성 있는 데이터를 만들어 나가야 할 것이다. 기능적 또는 임상적 연구를 시행하여 중증천식과 약리유전학에서 담당 유전자 변이의 정확한 역할을 규명해야 할 것이다.