4회의 면역 억제제 펄스 치료로 생존한 치명적 농도의 파라캇 중독 1예
Successful Management of Fatal Paraquat Poisoning with Four Courses of Steroid and Cyclophosphamide Pulse
Article information
Abstract
저자들은 치명적인 혈중 파라캇 농도(10.4 μg/mL)를 보여주면서 다발성장기부전 및 폐 섬유화에 의한 저산소증이 병발하여 생존 가능성이 극히 희박했던 중증 파라캇 중독 환자에서 골수기능억제가 나타날 정도까지 선제적이고 적극적으로 4차례의 스테로이드와 시클로포스파미드 펄스 면역 억제치료를 반복하였고, 치료 경과 중 면역 억제제로 인한 심각한 골수기능억제와 감염 등의 합병증이 발생하였으나 포기하지 않고 적극적인 치료를 시행하여 환자를 생존시켰기에 문헌고찰과 함께 보고하는 바이다.
Trans Abstract
Although severe paraquat poisoning is fatal, intensive immunosuppression can be successful in selected patients. We report the case of a 33-yr-old patient who was poisoned by paraquat and developed multi-organ failure, progressive hypoxemia, and pulmonary fibrosis. The patient was successfully treated with four courses of immunosuppressive pulse therapy. The patient presented to the hospital 2.5 hours after ingesting 2 mouthfuls of paraquat. The serum level of paraquat was 10.40 μg/mL at 3 hours and 3.36 μg/mL at 10 hours after ingestion, which is predictive of a fatal outcome. The first course of steroid and cyclophosphamide pulse therapy was initiated after hemoperfusion. During the hospital course, the patient showed progressive hypoxemia with pulmonary fibrosis. Accordingly, three additional courses of immunosuppressive pulse therapy were administered to prevent pulmonary injury. This treatment inevitably led to bone marrow suppression, which was recovered with supportive care. The patient fully recovered after repeated immunosuppressive pulse therapy without residual hypoxemia and was successfully discharged from the hospital. (Korean J Med 2012;83:373-377)
서 론
Bipyridyl 화합물계 제초제인 파라캇(Paraquat, 1,1’-demethyl-4, 4’-bipyridyl)의 음독은 심장혈관허탈 및 다발성장기부전 그리고 진행성 폐섬유화로 인해 높은 사망률을 보인다. 특히 음독량이 많을 경우 높은 혈청 파라캇 농도를 보이면서 거의 모든 환자가 사망하는 것으로 알려져 있고 따라서 적극적인 치료를 포기하는 경우가 많다. 저자들은 다발성장기부전과 함께 심한 저산소증이 발생한, 기존의 연구들에서 치명적인 혈중 파라캇 농도(음독 후 3시간, 10.40 μg/mL; 음독 후 10시간, 3.36 μg/mL)를 보인 중증 파라캇 중독 환자를 혈액관류 치료 및 4차례의 면역 억제제 펄스 치료를 통해 성공적으로 생존시켰기에 문헌고찰과 함께 보고하고자 한다.
증 례
환 자: 민○○, 여자 33세
주 소: 오심, 구토, 구강 내 작열통
현병력: 내원 2시간 30분 전 자살 목적으로 24.5%로 희석된 농사용 파라캇 용액 두 모금을 음독하였다. 음독 직후 수차례 구토했으며 30분 뒤 인근 지역병원으로 이송되어 15,000 cc 위세척 후 한림대 춘천성심병원 응급실로 내원하였다.
과거력: 10년 전부터 편집성 정신분열병(paranoid schizophrenia)으로 진단되어 본원 정신과에서 외래치료를 받고 있었다.
가족력 및 사회력: 특이 소견 없음.
진찰 소견: 혈압 100/60 mmHg, 맥박수 64회/분, 호흡수 20 회/분, 체온 36℃였다. 의식은 명료하였고 정신운동활동(psychomotor activity)이 항진되어 있었다. 구강 내 점막이 대부분 엷은 녹색으로 착색되었고 강한 휘발성 향을 확인할 수 있었다. 흉 복부 및 사지 신체 검사에서 이상 소견은 없었다.
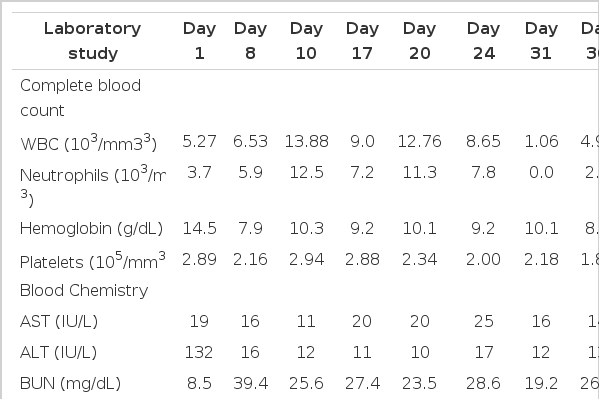
초기 검사 소견: 내원 시 시행한 혈액 및 소변 검사 결과는 Table 1과 같다. 혈액 응고 기능 검사는 정상이었고 혈중 요소 질소 8.5 mg/dL, 크레아티닌 0.7 mg/dL, AST 13 IU/L, ALT 19 IU/L, LDH 132 IU/L, 총 빌리루빈 0.78 mg/dL이었다. 동맥혈가스검사에서는 pH 7.4, PaCO2 21 mmHg, PaO2 65 mmHg, HCO3 13 mEq/L, O2 saturation 92%이었다. 소변 검사는 미세혈뇨(RBC 25-50/HFP) 외에는 정상이었다. Sodium dithionite를 이용한 파라캇 정성 검사 결과 혈청 1+, 소변 1+로 관찰되었으며 음독 3시간째 크로마토그래피법을 이용하여 측정한 혈청 파라캇 농도는 10.4 μg/mL이었다. 내원 시 응급실에서 시행한 단순흉부촬영에서는 이상 소견이 관찰되지 않았다.
치료 및 임상경과: 병력 청취와 약물 보관용기 확인을 통해 파라캇 음독으로 진단하였고 즉시 치료를 시작하였다. 환자 안정을 위해 먼저 페티딘(pethidine) 25 mg을 정맥 주사하였고 흡착제인 Fuller's earth와 만니톨(mannitol)을 섞어 비위관을 통해 4시간 간격으로 투여하였다. 흡수된 파라캇의 신장으로의 배설을 높이기 위해 등장성 생리식염수와 퓨로세마이드(furosemide)를 정맥 주사하였다. 폐섬유화를 방지하기 위한 항염증 치료로 시클로포스파미드(cyclophosphamide 1 g/day IV for 2 days)와 스테로이드(methylprednisolone, 1 g/day IV for 3 days then maintenance dexamethasone IV 10-20 mg/day)로 구성된 면역 억제제 펄스 치료를 한차례 시행하였고 추가적인 폐섬유화 방지와 항산화 치료를 위해 페니실라민(penicillamine)과 콜히친, 비타민 C, 레바미피드(Rebamipide)를 지속적으로 투여하였다. 파라캇을 효과적으로 제거하기 위해서 내원 직후부터 혈액 관류(hemoperfusion)를 6시간씩 2차례 시행하였다. 첫번째 혈액 관류 후 혈청 dithionite 검사결과는 약 양성(trace), 소변 dithionite 검사는 음성이었으며 두 번째 혈액 관류 후 모두 음성으로 전환되었다.
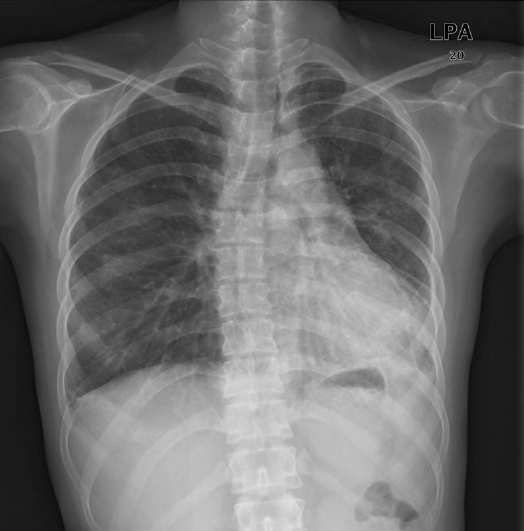
입원 5일째 단순흉부촬영에서 좌폐하엽의 불규칙한 음영이 악화되었고(Fig. 1) 이후 점차 진행되는 양상을 보여 입원 6일째 두 번째 면역 억제제 펄스치료를 시행하였다. 그러나 입원 10일째 산소포화도가 87%로 감소하면서 호흡 곤란을 호소하여 세 번째 면역 억제제 펄스치료를 다시 실시하였으며 입원 17일째 증상 및 동맥혈가스검사 결과가 다시 악화되어 입원 20일째 네 번째 면역 억제제 펄스치료를 시행하였고, 이후 경구 프레드니솔론으로 변경하여 감량하였다.
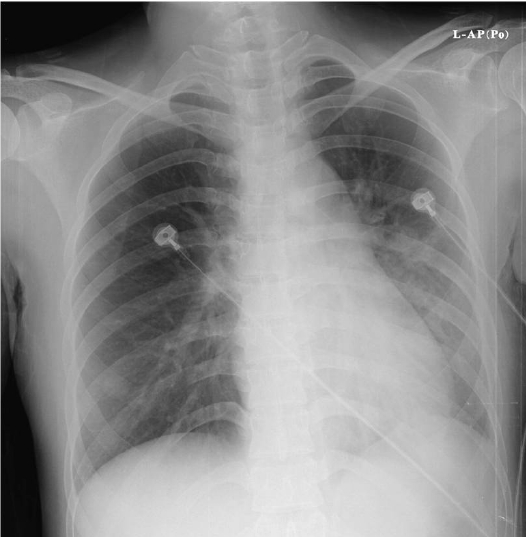
Anterior-posterior chest X-ray view shows both pleural effusion and increased haziness in the left retrocardiac area and ill-defined haziness in the paracardiac left lower lung field on hospital day 5.
내원 45일째 시행한 흉부 고해상도 전산화 단층촬영검사에서 양측폐 주변으로 불규칙한 반점형 경화(patch consolidation)와 젖빛 유리모양 혼탁(ground-glass opacity) 및 폐실질 변형(parenchymal distortion)이 관찰되어 파라캇에 의한 폐섬유화가 있음을 확인할 수 있었다(Fig. 2).
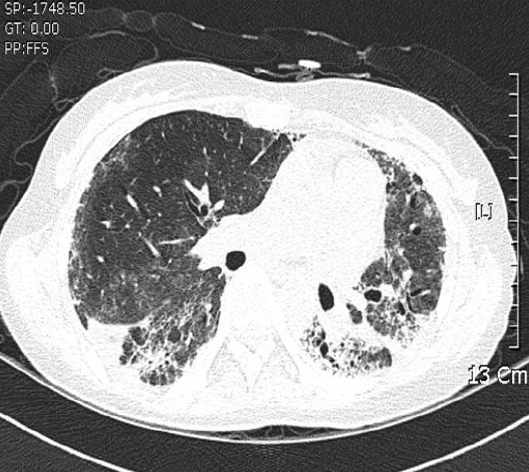
Chest high-resolution computed tomography scan reveals patchy ground glass opacity and consolidation with parenchymal bands, reticulation, and traction bronchiectasis in the periphery of the right and left upper lung 6 weeks after paraquat ingestion.
내원 26일째 발열(39.7℃)과 함께 백혈구 증가증(13,700/uL) 발생하여 불명열 진단하에 경험적 항생제인 레보플록사신 (levofloxacin)과 타조박탐(tazolactam)을 사용하였다. 항생제 사용 후 발열은 호전되었으나 발열 원인 및 원인 균주가 확인되지 않던 중, 입원 31일째 심한 호중구 감소증(absolute neutrophil count 0/uL)이 발생하여 6일간 격리 치료 및 과립구 집락자극 인자를 사용하였고 경구 프레드니솔론을 하루 15 mg으로 감량하였다. 항생제는 추가적인 배양 검사 후 세페핌(cefepim)과 이세파신(isepamicin)으로 변경하였고 항진균제인 암포테리신(amphotericin)을 추가하였다. 이후 증상 호전되면서 단계적으로 프레드니솔론을 감량하였고 내원 42일째 프레드니솔론을 투여 중지한 후 단순 흉부촬영에서도 폐 음영과 반점형 경화가 호전되어(Fig. 3) 입원 56일째 퇴원하였다. 이후 현재까지 12개월간의 외래 추적관찰 기간 동안 환자 상태는 양호하게 유지되었으며 특별한 내과적 치료없이 경과관찰 중이다.
고 찰
파라캇은 국내에서 흔히 사용되는 제초제로, 연속적인 산화환원 반응에 의한 제초 효과가 뛰어나며 토양과 접촉 시 분해되어 농작물 내 잔류가 적다는 장점이 있다. 하지만 약물 오용 등에 의한 급성 중독 발생 시 높은 사망률이 보고되며 실제 국내에서 매년 수백 명 이상이 이로 인해 사망하는 것으로 보고되고 있다[1]. 사람에서 반치사량(LD50)은 35 mg/kg으로 24.5%로 희석된 파라캇으로 환산하면 8-12 mL에 해당한다[1]. 파라캇의 음독량에 따라 사망의 원인과 생존 기간에 차이가 있는데 다량 음독의 경우 1일에서 5일 사이에 심장혈관허탈 및 다발성장기부전으로 사망하며 중등도 정도의 음독일 경우 급성 신손상, 간염, 폐 섬유화 등이 순차적으로 발생하면서 대개 2-3주 후에 폐 섬유화에 의한 가스교환장애로, 저산소증에 빠져 사망하는 것으로 알려져 있다[2].
파라캇 중독 시 손상되는 대표적인 장기는 폐인데 주로 음독 후 3일에서 14일 사이에 폐부종, 폐출혈, 급성 호흡곤란증후군(ARDS), 폐섬유화 등과 같은 변화가 나타난다[3]. 파라캇은 산화환원 반응을 통해 과산화기(superoxide radical, O2-) 및 수산기(hydroxyl radical, OH-)와 같은 활성산소(free radical)를 생성하여 직, 간접적으로 세포막 파괴, 세포의 기능저하 및 손상을 초래하고[2] 호중구 매개 염증반응을 유발하여 다발성장기부전 및 최종적으로 폐섬유화를 진행시킨다. 산소 분압이 높고 활성산소 제거 효소가 적은 제2형 폐포 섬유(type 2 pneumocyte)의 특성 때문에 폐에 대한 독성은 초기부터 치명적으로 나타나며 산소 투여로 손상이 가속화 될 수 있다[1].
혈청 파라캇 농도는 급성중독의 중증도를 평가하고 예후를 예측하여 치료 방침을 결정하는 데 가장 중요하다. 음독 후 2시간 이내에 혈중 최고 농도에 이르고 이후 급격히 감소하는 파라캇의 약동학적 특성 때문에 음독 후 채혈 시점을 반드시 같이 고려해야 한다. 혈청 파라캇 농도에 따른 치사율의 예측 연구로 가장 잘 알려진 것이 Proudfoot's curve이다[4]. 이들 연구에 따르면 음독 후 1, 4, 6, 10, 16, 24시간에 시행한 혈중 파라캇 농도가 2.0, 0.6, 0.3, 0.16, 0.1 μg/mL을 초과한 경우 대부분 사망하였으며, 특히 24시간 내 측정한 혈중 파라캇 농도에 따른 환자 생존율 예측에 있어 다른 연구보다 정확도가 높다고 보고된 바 있다[5]. 음독 3시간째 시행한 증례 환자의 혈청 파라캇 농도는 10.4 μg/mL로 Proudfoot's curve에 적용 시 생존이 극히 어려울 것으로 예상되었으며, Jones 등[6]의 연구에 적용 시 예상 생존율은 1.74%이었다. 저자들의 문헌고찰에 의하면 국내에서 보고된 파라캇 중독 생존자의 최대 혈중 농도는 Gil 등[3]의 연구에서 음독 3시간째 2.64 μg/mL, Hong 등[7]의 연구에서는 2.5시간째 5 μg/mL로 보고되었으며 증례 환자의 경우 이를 2배 이상 상회하는 농도였다. 또한 음독 10시간 후 혈액 관류 치료 중 재 측정한 혈청 파라캇 농도도 3.36 μg/mL로서 Koo 등[8] 및 Lheureux 등[9]의 기존의 여러 연구에서 음독 10시간 후 혈청 농도가 2 μg/mL을 초과 시 모두 사망하였음을 고려해 볼 때 역시 치명적인 농도로 생각된다.
파라캇 중독 시 특별한 해독제는 없으며 파라캇의 체내 흡수를 억제하고 흡수된 파라캇의 제거를 촉진하면서 조직에 대한 손상을 줄이기 위해 아래와 같은 치료가 권장되고 있다. 첫째 위장관에서의 흡수 방지를 위해 위세척, 구토 유발제, Fuller's earth와 같은 흡착제를 투여한다. 둘째 이미 흡수된 혈중 파라캇의 배설을 증가시키기 위해 이뇨제와 함께 다량의 등장성 수액을 투여하여 강제 이뇨를 유발하거나 혈액관류, 혈액투석, 지속적 혈액여과(continuous venovenous hemofiltration) 등을 시행한다. 셋째 이미 흡수된 파라캇의 조직에 대한 손상을 줄이기 위해 고용량의 스테로이드 및 시클로포스파미드와 같은 면역 억제제를 투여하거나 비타민 C, 비타민 E, 글루타티온, 아세틸시스테인과 같은 항산화제[2] 등을 사용한다. 고용량의 스테로이드는 대식세포와 중성구에서 과산화기의 생성을 억제하고, 시클로포스파미드는 세포 및 체액 면역 반응을 억제하여 염증 반응을 감소시킴으로써 효과를 나타낼 수 있는 것으로 알려져 있다. 이외에도 콜라겐 합성을 억제하고 폐 섬유화를 감소시키기 위해서 페니실라민과, 콜히친 등을 투여하기도 하며 파라캇의 폐 축적을 방지하기 위해 D-propranolol을 사용하기도 한다[2].
저자들은 과거의 연구[10]에서 다량의 파라캇 음독 시 조기에 발생하는 심장혈관허탈 및 다발성장기부전은 적극적인 혈액여과 요법 등을 통해서 어느 정도 치료할 수 있었으나 결국 폐섬유화에 의한 저산소증으로 대부분이 사망하였음을 보고한 바 있다. 이번 증례의 경우도 높은 혈중 파라캇 농도로 인해 사망이 필연적으로 예상되었으나 생존할 수 있었던 것은 음독 후 조기에 1차 면역 억제제 펄스치료를 시행한 후, 폐 손상의 징후 및 저산소증의 발생에 따라 선제적이고 적극적으로 3차례 추가 반복하였기에 가능했던 것으로 추정된다.
이렇게 고용량의 면역억제제를 반복적으로 사용할 경우 가장 문제가 되는 것이 감염과 골수기능억제와 같은 합병증 발생이다. 특히 증례 환자의 경우 총 4 g의 시클로포스파미드가 사용되면서 심각한 호중구 감소증이 동반되어 면역 억제에 의한 기회 감염의 위험성이 증가하였으나 무균적 조작 및 광범위 항생제 사용과 같은 적절한 치료를 시행하여 곧정상으로 회복할 수 있었다. 따라서 감염과 골수기능억제에 대한 적절한 치료가 가능하다면, 치명적인 예후를 보이는 중증 파라캇 중독, 특히 폐섬유증을 동반한 경우에서 면역억제 펄스치료를 골수기능억제가 나타나는 수준까지 선제적 및 반복적으로 시행하고 이후 보존적 치료를 통해 폐섬유화와 골수기능억제 동시 회복을 기대하는 치료법도 적극적으로 고려해 볼 수 있을 것으로 사료된다.