파국 항인지질 증후군 의증 환자의 파종혈관내응고 관련 급성 신손상 1예
Acute Kidney Injury Associated with Disseminated Intravascular Coagulation that Developed after a Hysterectomy in a Patient with Probable Catastrophic Antiphospholipid Syndrome
Article information
Abstract
본 증례의 환자는 수술 전 응고 검사 결과가 정상이었으나 수술 후 파종혈관내응고와 응고 인자 결핍이 발생하였고 그 결과 급성 신손상이 발생한 경우로 명확하지는 않으나 파국 항인지질 증후군이 선행되었을 것으로 생각된다. 본 증례와 같이 수술 등의 선행 요소 후에 파종혈관내응고가 발생하고 빠른 속도로 다발성 장기 부전이 발생하는 환자들에서 파국 항인지질 증후군을 감별해야 할 것으로 생각된다.또한 선행 요인 후 발생한 파종혈관내응고와 관련된 급성 신손상인 경우, 감염에 의한 파종혈관내응고가 아니라면 스테로이드 치료가 신장기능 및 파종혈관내응고 호전에 도움이 될 것으로 생각된다.
Trans Abstract
Acute kidney injury associated with disseminated intravascular coagulation (DIC) and a coagulation factor defect may develop with infection, malignancy, severe trauma, or obstetric complications. However, a gynecological etiology, such as hysterectomy, in a patient with adenomyosis has rarely been reported. We describe a case of a 42-year-old women who presented with DIC and acute kidney injury after a total hysterectomy. We thought that the cause for the acute kidney injury might be small vascular thrombosis and acute tubulointerstital nephritis due to probable catastrophic antiphospholipid syndrome with DIC. The patient was successfully treated with steroid therapy. (Korean J Med 2012;82:739-743)
서 론
파종혈관내응고(disseminated intravascular coagulation, DIC)는 기저질환에 의해 이차적으로 발생하는 증후군으로, 혈액 응고가 광범위하게 활성화되어 장기로 가는 산소의 공급을 막아 다발성 장기 손상을 초래할 수 있다. 파국 항인지질 증후군(catastrophic antiphospholipid syndrome, CAPS)은 항인지질 증후군이 빠르게 진행된 형태로, 다수의 작은 혈관들이 막힘으로써 다발성 장기 부전을 초래한다. 파국 항인지질 증후군 환자의 19-28%에서 파종혈관내응고의 특징을 갖는 것으로 보이며 파국 항인지질 증후군이 파종혈관내응고의 원인이 될 것으로 생각된다[1].
파종혈관내응고와 관련된 급성 신손상은 수술 후 나타날 수 있는 합병증 중의 하나이다. 그러나 전자궁적출술 등 부인과적 수술 후 발생하는 파종혈관내응고와 관련한 급성 신손상은 그 알려진 예가 드물다. 저자들은 자궁선근증 치료를 위한 전자궁적출술 후 파국 항인지질 증후군이 의심되는 환자에게서 파종혈관내응고 관련 급성 신손상을 경험하였기에 이를 보고하는 바이다.
증 례
환 자: 42세, 여자
주 소: 불규칙 과다월경
현병력: 2003년 자궁선근증을 진단 받았으나 특별한 처치없이 경과관찰하며 지내던 중 2007년 10월경부터 불규칙 과다월경이 심해져 2009년 3월 산부인과 외래 내원하였고 전자궁절제술을 위하여 산부인과에 입원하였다.
과거력: 4회의 자연 유산 과거력이 있었고, 2003년 자궁각 임신(cornual pregnancy)으로 복강경 자궁각절제술(laparoscopic cornual resection) 및 복강경 근종적출술(laparoscopic myomectomy)을 시행하였다. 음주력 및 흡연력은 없었다.
진찰 소견: 입원 당시 환자의 활력징후는 혈압 100/60 mmHg, 맥박수 72회/분, 호흡수 18회/분, 체온은 37℃이었다. 흉부청진상 호흡음은 정상이었고 심음은 규칙적이었으며 다른 이학적 검사에서도 특이소견은 없었다.
검사실 소견: 입원 5일 전 외래에서 시행한 혈액검사에서 백혈구 5,080/μL, 혈색소 12.7 g/dL, 혈소판 351,000/μL, 혈액요소질소 13.9 mg/dL, 혈청 크레아티닌 0.9 mg/dL로 정상이었고, 혈액 응고검사에서 프로트롬빈 시간(PT) 11.7 sec, 활성화부분트롬보플라스틴 시간(aPTT) 32.7 sec, 출혈시간(BT) 1.30 min으로 정상이었다. 소변검사에서 pH 5.5, 단백뇨(-), 혈뇨 1-4/HPF, 백혈구뇨 1-4/HPF이었다.
방사선 검사: 입원 5일 전 외래에서 시행한 단순흉부방사선 사진에서 심비대 및 활동성 폐 병변은 관찰되지 않았다(Fig. 1A).

(A) Chest X-ray before surgery shows no active disease. (B) Chest X-ray on postoperative day 1 shows increased pulmonary vascular markings and bilateral pleural effusion.
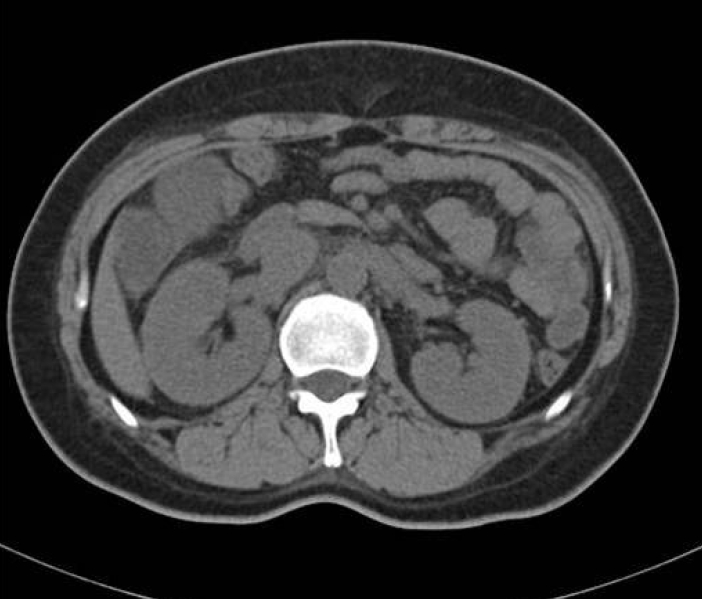
경과 및 치료: 환자는 입원 다음 날 복식 전자궁절제술을 시행 받았다. 수술 동안 혈역학적으로 안정되었고 수술 직후 특이 합병증은 발생하지 않았다. 수술 후 1일째 육안적 혈뇨 및 핍뇨 소견 보이면서 환자는 갑작스러운 흉부 불편감 및 호흡곤란, 수술 부위 통증을 호소하였고 하지에서 함요부종이 관찰되었다. 이에 급성 신손상 및 폐부종, 출혈성 질환이 의심되어 혈액검사 및 방사선 검사를 시행하였다. 혈액검사에서 요소질소 35.0 mg/dL, 크레아티닌 5.2 mg/dL로 증가하였고 proBNP는 5,385 pg/mL로 측정되었다. 혈색소 8.8 g/dL, 혈소판 123,000/µL로 감소하였고 PT는 12.0 sec으로 정상이었으나 aPTT는 84.1 sec으로 증가하였다. 단순흉부방사선 사진에서는 경도의 폐부종과 양측 흉막삼출 및 무기폐 소견 보여(Fig. 1B) 심기능 저하 및 폐질환이 의심되었다. 수술 후 2일째, 고용량의 주사 이뇨제 사용하였으나 1일 소변량은 500 cc/day 미만이었고, 혈청 크레아티닌이 6.6 mg/dL로 증가하였다. 콩팥 후 요로폐색을 감별진단하기 위하여 시행한 비조영증강 복부전산화단층 촬영에서 요로 폐쇄소견은 보이지 않았다(Fig. 2). 수술 후 3일째 소변량은 100 cc/day 미만, 혈중요소질소는 50.7 mg/dL, 크레아티닌은 8.4 mg/dL로 증가하였고 환자는 호흡곤란, 식욕부진, 구역 및 구토를 호소하여 우측 내경정맥에 영구적 도관(permanent catheter) 삽입 후 혈액 투석을 시작하였다. 혈액응고검사상 aPTT가 93.2 sec로 계속 증가되어 있었고, D-dimer 3519.77 ng/mL, FDP 40 µg/mL, 피브리노겐 < 70 mg/dL, 안티트롬빈 III 64%로 측정되어 파종혈관내응고를 의심하였다. 육안적 혈뇨 이외에 명확한 출혈 부위는 없었으나 혈색소 8.3 g/dL, 혈소판 107,000/µL로 감소하여 출혈 합병증 예방을 위해 신선동결혈장 3pint를 한차례 수혈하였고, 더 이상의 수혈은 하지 않았다. 37.6℃의 미열과 C-반응성 단백질(CRP)이 8.17 mg/dL로 증가하여 수술 후 복강내 감염에 의한 패혈증을 배제할 수 없어 혈액, 소변 및 객담에서 미생물 배양 검사 후 경험적 항생제를 투여하였다. 수술 후 6일째, 혈액 투석을 지속하며 보존적 치료에도 환자의 1일 소변량은 300 cc 미만이었다. 혈소판 수는 정상으로 회복되었고, 출혈 증상은 없었으나 aPTT는 지속적으로 연장되어 있었고 혼합검사(mixing test)에서 교정되지 않아 응고 인자 검사를 시행하였다. 그 결과 제8인자(Factor VIII)가 47%, 제9인자(Factor IX)는 34%, 제11인자(Factor XI)는 20%, 제12인자(Factor XII)는 58%로 모두 감소되어 있었고 제8인자 억제인자(Factor VIII inhibitor)가 0.26 BU 검출되었다. 환자가 자연 유산 4회의 과거력이 있었기 때문에 항인지질 증후군이 의심되었으나 루푸스 항응고인자 음성, 항카디오리핀항체(IgM, IgG) 음성, ß2GP1 항체(IgM, IgG) 음성 소견을 보였다. 자가면역질환에 대한 혈액검사상 ANA (-), ANCA (-), haptoglobin 51.6 mg/dL, ADAMTS 13 activity 63% (참고치: 44-121%)로 특이소견 없었으며, 대변검사에서 E. coli O157 검사는 음성이었다. 초기 혈액, 객담 및 소변 배양 검사에서 동정된 균은 없었고, 그 외 Korea Ab (-), Leptospira Ab (-), Murine typhus (-), Scrup thypus (-), HCV (-), HBs Ag (-), HBs Ab (-)로 특이소견은 없었다.
비록 조직 검사는 출혈의 위험성이 있어 시행하지 못하였으나 이상의 임상 증상 및 검사소견으로 볼 때 파종혈관내응고 및 응고 인자 결핍에 의한 신실질 소혈관 혈전증 및 미만성 미세혈관 폐 혈전증, 급성 세뇨관 간질 신염 추정 진단 하에 수술 후 8일째부터 Prednisolone 30 mg/day (0.5 mg/kg/day)을 투여하였다. Prednisolone 투여 7일째 환자의 1일 소변량은 2,000 cc 이상 유지되고 크레아티닌은 4.5 mg/dL로 감소하였다. Prednisolone 투여 10일째 혈액투석을 중단하였음에도 혈청 크레아티닌 점차 감소하여 혈액투석 도관을 제거하였다. 이후 환자는 특이 증상호소 없고 전신상태 호전되어 prednisolone 투여 20일째 prednisolone 20 mg/day로 감량하여 수술 후 25일째 퇴원하였다. 퇴원 당시 혈청 크레아티닌 1.4 mg/dL로 감소하였고, D-Dimer 576.08 ng/dL, FDP 음성, 피브리노겐 338 mg/dL, 안티트롬빈 III 94%로 파종혈관내응고에서도 호전된 소견 보였다. aPTT는 50.0 sec로 감소하였고, 혼합검사 후 교정되었으며 제8인자는 79%, 제9인자는 81%로 증가하였다. 환자는 신장내과 외래에서 prednisolone 20 mg/day 복용 총 한 달 유지 후 혈청 크레아티닌 1.0 mg/dL로 정상 소견 보여 중단하였다. 환자 prednisolone 복용 중단 두 달 후 시행한 검사에서도 정상 신기능과 정상 혈액 응고검사를 보이고 있었다.
고 찰
본 증례는 평상시에 출혈 소견을 보이지 않았고 수술 전 정상 응고 검사 결과를 보였던 환자가 자궁선근증 치료를 위한 전자궁적출술 후 파종혈관내응고 및 응고 인자 결핍, 급성 신손상이 발생한 경우이며 기저질환으로 파국 항인지질 증후군이 의심된다. 산과적 질환에 의한 파종혈관내응고는 일반적으로 잘 알려져 있고, 부인과적 수술과 관련하여서는 자궁근종 수술 후 파종혈관내응고가 발생한 경우는 보고된 바 있으나[2], 자궁선근증 치료를 위한 전자궁적출술 후 발생한 파종혈관내응고와 그로 인한 급성 신손상은 알려진 예가 드물다.
파종혈관내응고에서 급성 신손상은 사구체 미세 혈전과 관계가 있다. 염증이 발생하면 단핵구와 대식세포가 사구체로 이동하여 조직 인자 생산 및 전응고 활동을 하여 섬유소 침착을 일으키는 것으로 알려져 있고[3], Wiggins 등[4]에 의하면 혈관사이세포(mesangial cell)도 섬유소 침착에 관여하는 것으로 생각된다[4]. 또한, Aihara 등[5]은 패혈증과 파종혈관내응고가 동반된 급성 신부전 환자에서 신조직 검사 결과 세뇨관간질 신염의 소견을 보여 급성 신부전의 호전이 늦는 경우 세뇨관 간질 신염을 고려해야 한다고 주장하였다[5].
본 증례의 환자는 항인지질 항체 음성 결과를 보여 항인지질 증후군을 확진할 수는 없으나 IgA 형태의 항체와 항프로트롬빈 항체 검사는 하지 않아서 항인지질 증후군을 완전히 배제할 수는 없다. 또한, 제8인자 감소와 제8인자 억제인자 검출로 후천성 혈우병도 생각해 볼 수 있으나 인자의 활성도가 47%로 비특이적으로 낮게 나왔고 억제인자도 낮은 수치가 측정되었다. 그리고 제9, 11, 12 인자가 모두 감소하였기 때문에 후천성 혈우병보다는 파종혈관내응고로 인한 응고 인자 결핍과 생성 장애로 인한 것으로 보이며 수술 후에 악화된 파국 항인지질 증후군이 원인일 것으로 생각된다.
대부분의 파국 항인지질 증후군은 감염, 수술, 외상, 종양, 항응고제 중단/낮은 INR, 산과적 합병증, 루프스 플레어 등의 선행요인에 의해 유발된다. 임상양상은 주로 소혈관 혈전 및 폐쇄에 의한 다발성 장기부전으로 나타나며 본 증례의 환자와 같이 신장 침범이 가장 많아(73%) 급성 신부전, 혈전성 미세혈관병증, 신경색 등이 발생할 수 있다. 그리고 급성 호흡곤란 증후군, 폐동맥 혈전증, 폐포 출혈 등의 폐 침범(68%), 허혈성 뇌졸중이나 뇌병증 등의 대뇌 침범(63%), 그물울혈반, 괴사, 자반성 병변 등의 피부 침범(58%), 심부전, 심근경색, 판막 이상 등의 심장 침범(51%), 간(34%), 위장관(24%), 비장(18%), 부신(14%) 등의 순으로 장기의 침범을 보인다[6].
파국 항인지질 증후군에서 ‘definite CAPS’의 진단은 (a) 3개 이상의 장기 침범, (b) 1주일 이내의 기간 동안 동시에 발현, (c) 1개 이상의 장기 또는 조직의 소혈관에서 조직병리학적 확진, (d) 항인지질 항체 양성의 네 가지 기준을 모두 만족시켜야 한다[7]. 하지만 CAPS를 감별 진단해야 하는 실제 상황에서는 여러 가지 요소들이 빠른 진단을 어렵게 만든다. 항인지질 항체는 감염이 있거나 항응고제를 사용하였을 때에 일시적으로 양성으로 나올 수 있으며 이런 경우에는 항인지질 항체 양성이 혈전에 기여하는 요인이라고 볼 수 없다. 또한 파국 항인지질 증후군 환자에서 광범위한 혈전증이 발생하고 있는 동안에는 항인지질 항체 음성을 보일 수 있는데 이것은 항인지질 항체의 소모 때문인 것으로 생각된다[8,9]. 본 환자는 항인지질 항체를 시간이 지난 후 재검하지 않은 아쉬움이 있지만 ‘seronegative APS’의 가능성도 있을 것으로 생각된다. 또한 상기 환자처럼 수술 직후 출혈의 위험성이 있는 환자에서는 조직검사를 시행하는 것이 위험할 수 있어 ‘definite CAPS’의 진단을 더욱 어렵게 만든다.
파국 항인지질 증후군의 치료는 적절한 항응고제를 사용하거나 스테로이드로 치료하며, 이러한 치료에 반응이 없는 경우 혈장 여과술을 시행하여 볼 수 있다[10]. 본 환자는 스테로이드로 치료 후 호흡곤란 및 급성 신손상이 호전되었으며 전자궁적출술 후 파국 항인지질 증후군에 의한 파종혈관내응고가 발생하여 신장, 폐 및 심장이 침범되었을 가능성이 높을 것으로 생각된다.