소화기계 및 호흡기계에 발생한 이시성 4중복암
Quadruple Mtachronous Primary Neoplasms in the Aerodigestive Tract
Article information
Abstract
한 사람에서 다발성으로 악성종양이 발생하는 다발 원발암은 1889년 Billroth에 의해 처음 발표되었다. 최근 들어 악성종양에 대한 점진적인 진단 및 치료기술의 발달로 다발 원발암의 발생률은 증가되는 추세이다. 국내에서도 3중복암에 대한 몇몇 증례 보고가 있었으나 4중복암에 대한 발표는 드물다. 최근 저자들은 69세 남자에게서 발생한 이시성 4중복암-폐, 식도, 성문, 하인두-을 경험하였기에 문헌고찰과 함께 보고하는 바이다.
Trans Abstract
Multiple primary neoplasms, defined as the occurrence of multiple malignant neoplasms in the same individual, were first reported by Billroth in 1889. With gradual improvements in diagnostics, and the early detection and effective treatment of malignant neoplasms, the prevalence of multiple primary neoplasms seems to be increasing. Although there have been several reports of triple primary neoplasms in Korea, cases of quadruple neoplasms are rare. Recently, we diagnosed a 69-year-old male with primary neoplasms in the lung, esophagus, vocal cords, and hypopharynx. The authors report this rare case of four metachronous primary neoplasms and provide a review of the literature. (Korean J Med 2012;82:110-114)
서 론
악성 종양 환자에게서의 또 다른 악성 종양 발생률은 그렇지 않은 환자의 경우와 비교할 때 높으며, 이는 고령으로 갈수록 증가한다. 1889년 Billroth가 다발 원발암 발생에 대해 처음 보고한 뒤, 발암 성향을 가져오는 특정 인자가 있는 것인지 또는 우연의 일치인지에 대해 연구가 계속되고 있다. 진단에는 일반적으로 각 병변이 조직 병리학적으로 상이하고 악성이며, 또한 전이성 병변이 아니어야 한다는 1932년 Warren과 Gates의 정의가 사용된다. 우리나라에서도 3중복암을 포함하여 다발 원발암에 대한 보고가 수 차례 있었지만, 4중복암까지 보고된 예는 많지 않다. Billroth의 연구 당시와 마찬가지로, 현재도 상기도 및 소화관에서의 다발 악성 종양 발생률이 저자에 따라 7-20%로 보고될 정도로 높다. 이 중 하인두에서 발생하는 악성종양이 다발 원발암과 가장 밀접하게 연관된 것으로 나타나고 있다[1]. 저자들은 비소세포 폐암, 식도암 및 성문암, 그리고 설암까지 이시적 4중복암으로 진단받은 69세 남자 환자를 경험하여 보고하는 바이다.
증 례
2010년 7월 23일 69세 남자 환자가 타 병원에서 성문암(조직 검사결과: 분화도가 좋은 편평상피세포암종)을 진단받고, 방사선 치료를 받던 중 기기 고장으로 본원으로 전원되었다. 환자는 30년간 매주 소주 1-2병의 음주, 5년 전 금연하였으나 40년간 하루 1.5갑의 기왕 흡연력이 있는 농부로, 과거력상 다른 병원에서 중복 원발성 비소세포 폐암으로 2007년 4월 4일부터 25일까지 선행 방사선 치료 시행 후 2007년 5월 29일 및 6월 14일에 각각 우폐중엽 절제술(T1NOMO)과 좌폐하엽 절제술(T2N1MO)을 받았고, 2007년 7월 24일부터 9월 28일까지 보조화학요법을 받았다. 이후 2008년 6월 16일 식도암으로 Ivor lewis 수술 및 복강경 위 고정술(T1NOMO) 후 2009년 8월 11일부터 10월 1일까지 종격동 임파선 재발로 방사선 치료를 받고 지내던 중, 2010년 2월경부터 목쉰소리와 연하통에 대해 검사한 결과 성문암으로 진단되어 2010년 7월 1부터 방사선 치료를 시작하였다. 기기고장으로 본원 치료방사선학과에서 남은 방사선 조사를 실시하고, 2010년 8월 26일 총 66 Gy/33 fractions의 경부 방사선 치료를 종료하였다.
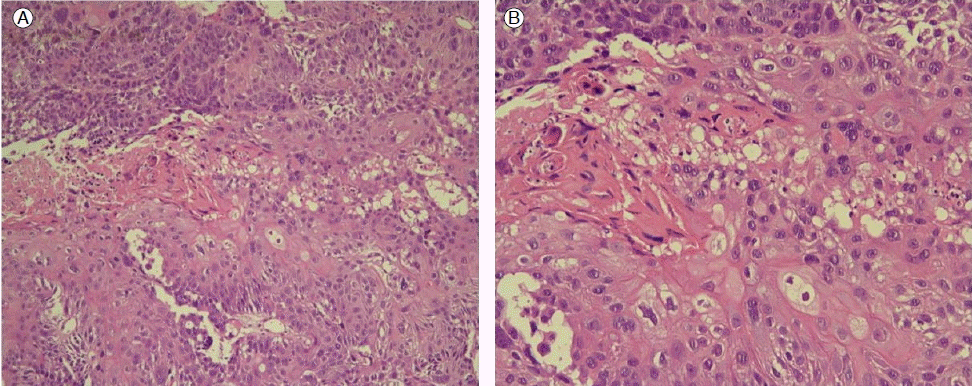
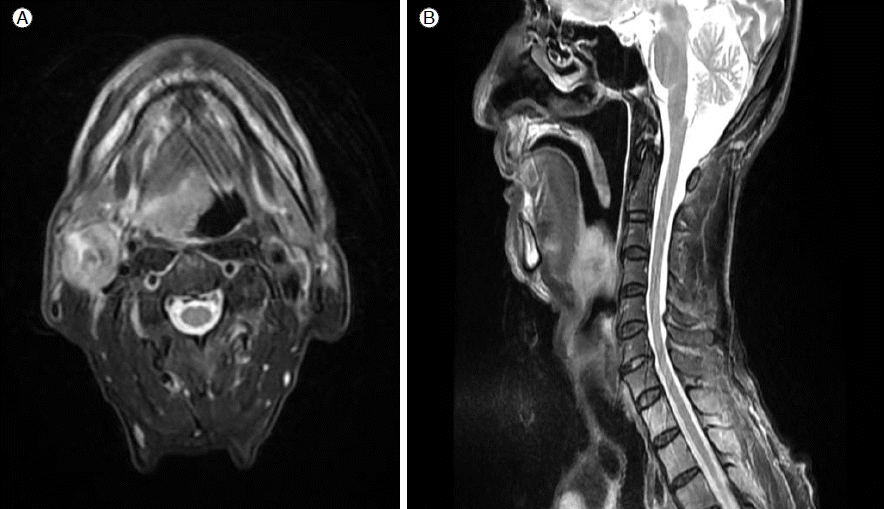
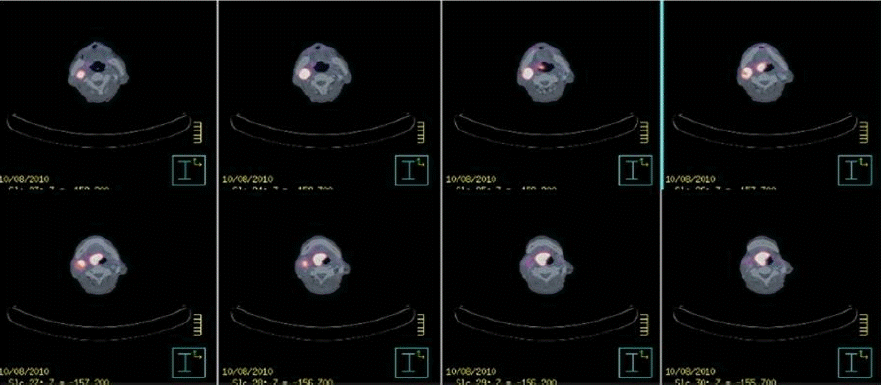
마지막 방사선 치료 후 40일 후인 2010년 10월 6일, 환자는 2주 전부터 발생한 목의 이물감 및 연하통을 주소로 본원 이비인후과 외래를 방문하였다. 활력징후는 정상이었으며, 이학적 검사상 우측 neck level II의 2 cm 임파선의 종대가 관찰되었고, 후두경 검사상 우설기저부에 ulcerofungating 양상의 종양 발견되어 이 병변에 대한 조직 검사를 실시하여 조직 검사 결과 편평세포암종이 확인되었다(Fig. 1). 구강인두 MRI 검사에서는 우설 기저부에서부터 하인두에 이르는 3.1 × 2.8 × 3.7 cm 소엽상의 경계를 보이는 종괴 및 우측 neck level Ⅱ의 2.6 × 2.4 × 3.2 cm 임파선 전이(T4N2) 소견이 보였다(Fig. 2). 또한 PET CT 검사에서는 우측 구강인두에서 후두개에 이르는 소엽상의 과대사병변(SUVmax 15.7)과 우측 neck level Ⅱ와 좌측 level Ⅲ에 각각 SUVmax 12.0 및 3.7의 과대사 병변이 관찰되었다(Fig. 3). 이로써 환자는 연속적으로 발생한 네 번째 악성종양을 진단받게 되었고, 고식적 항암화학요법을 위하여 혈액종양내과로 전과되었다. 전과 당시 환자의 키와 몸무게는 각각 171 cm, 50.1 kg이었으며, 혈액 검사 결과 hemoglobin 10.1 g/dL, hematocrit 31%, leukocyte count 7,830/μL with normal differentiation, platelet 279,000/μL, total protein 6.4 g/dL; serum sodium 138 mEq/L, serum potassium 4.5 mEq/L, serum chloride 104 mEq/L, serum BUN/Cr 16.8/0.68 mg/dL, serum CK/LDH 34/257 U/L, serum CRP 1.44 mg/dL, serum uric acid 3.9 mg/dL를 보였다. 2010년 10월 18일부터 고식적 화학요법으로 docetaxel/cisplantin을 시작하여 5차까지 마치고 실시한 구강인두 MRI에서는 우측 neck level Ⅱ임파선 전이 병변의 크기는 3.5 × 3.1 × 2.9 cm으로 큰 변화 없었으나 조영 증강되는 고형부분의 크기는 증가하여 질병진행으로 판단하고, TS-1/CDDP로 약제 변경하여 현재 2차까지 진행하고 외래 경과관찰 중에 있다.
고 찰
6개월의 발생 간격을 두고 동시성 또는 이시성으로 분류되는 다발 원발암은 1889년 Billroth에 의해 처음으로 보고되었다. 이후 1932년 다발 원발암의 진단에 대해 Warren과 Gate가 좀더 보편적으로 받아들일 수 있는 기준을 마련하였다[2]. 이는 각각의 종양이 조직병리학적으로 서로 다른 악성 병변임이 증명되어야 하고, 또한 각 병변이 전이에 의해 발생한 것이 아니어야 한다는 것이다. 2004년 2월 제정된 IACR (International Association of Cancer Registries) ICD-O 3판에서는 종양 발생 부위를 그룹화하고, 전신암에 대해서는 림프종, 백혈병, 카포시 육종, 중피종의 네 가지 조직군으로 분류를 한정함으로써 다발 원발암의 경계를 보다 명확히 규정하였다. 그러나 이들 다발 원발암의 원인, 발병률, 임상양상, 치료 및 예후에 대해서는 아직까지 명확하게 정립된 것이 없다.
10년간 조직병리학적 악성으로 진단된 9,870명의 환자를 대상으로 한 Cheng 등[3]의 보고를 보면, 246명(2.5%)에서 다발 원발암이 확인되었다. 이 중 절반 이상인 129명에서 소화기계 악성 종양이 동반된 것으로 나타났는데 2중복암과 3중복암이 각각 120명(93.02%), 9명(6.98%)이었고 4중복암은 없었다. 또한 소화기계 악성종양이 동반되지 않은 다발암의 빈도는 부인과(자궁경부, 자궁내막, 난소)암이 40명(45.97%), 비뇨기계(신장, 방광, 전립선) 10명(11.49%), 그리고 폐 및 유방암이 10명의 순서였다. 우리나라에서도 드물지만 3중복암의 보고가 있었으며, 더 드문 4중복암으로는 Hong 등[4]에 의해 직장, 결장, 위장, 갑상선의 이시 원발암, Son 등[5]에 의해 직장, 위장, 간내 담관, 담낭의 동시 원발암, 그리고 Bae 등[6]에 의해 직장, 결장, 위, 바터 팽대부의 이시 원발암이 보고되었다.
다발 원발암 발생의 원인 규명을 위한 시도는 질환에 대한 Billroth의 첫 보고 이후부터 지속적으로 있어 왔고, 면역학적 이상, 인종, 술이나 담배 등의 암 발생 인자에 대한 노출, 방사선 조사의 과거력 등이 거론되어 왔다. 실제로 9,233명의 유방암 환자를 대상으로 한 Stefano 등[7]의 연구에서 이전 국소 방사선 조사의 과거력이 있는 환자군에서 두 번째 암의 발생률이 유의하게 높은 것으로 나타났다. 2007년 발표된 다발 원발암에 대한 보고를 보면, 방광암 환자에서 다발암 발생률이 가장 높은 것으로 확인되었으며(16%), 그 다음이 구강 인두암(15%), 자궁암(11%)의 순으로 나타났다[8]. 이러한 소화기 및 호흡기 그리고 비뇨기에서 발생하는 다발 원발암에 대해 Slaughter 등[9]은 술, 담배와 같은 발암물질에 반복적으로 노출되는 호흡기 및 소화기의 상피세포 전체가 이미 각각 독립적으로 암세포 전단계 혹은 암세포의 단계에 있다가 이시적 악성종양으로 발현한다는 field cancerization의 과정을 처음으로 제시하였다. 최근에는 Boudewijn 등[10]에 의해 TP53 돌연변이 및 유전적으로 변형된 주변 조직이 다발 원발암 발생에 기여한다는 field cancerization에 대한 분자 생물학적인 제안도 있었으나 아직은 연구가 부족한 실정이다. 본 증례의 환자에서는 아쉽게도 분자 생물학적인 검사를 실시하지 못하였다.
평균 수명이 늘어남에 따라 암 발생률 또한 증가하여 2007년 미국의 암 통계 자료를 보면 일생동안 대략 남자는 두 명 중에 한 명, 여자는 세 명 중에 한 명에서 암이 발생하는 것으로 나타났으며, 국내 통계도 이와 비슷한 수준이다. 이와 같은 폭발적인 악성종양의 발생률 증가에도 불구하고, 현재까지 수술적 절제 이외에는 암에 대한 근치적 치료방법이 없다. 또한 많은 연구 결과가 보여주듯이, 암 발생 환자에게서 다른 암 발생률은 일반인의 암 발생률에 비해 높고, 후속암의 발생률과 생존율 사이에 음의 상관관계가 있는 것으로 밝혀져 있다. 이시성 다발 원발암은 선행암의 근치적 치료가 있었다면 발생하는 각 악성종양에 대해서도 수술적으로 절제하는 것이 원칙이다. Cheng 등[3]의 보고를 보면, 두 번째 발생하는 원발암에 대한 진단이 빠를수록 환자의 생존율이 증가하는 추세가 확인된다. 평균수명의 증가와 이에 비례하는 암 발생률의 증가로 현재 암의 조기 진단 및 암환자의 장기 생존율을 향상시킬 수 있는, 보다 정확하고 안전한 암 진단 및 치료법에 대한 지속적인 연구가 이루어지고 있다. 실제로 최근 두경부 다발성 종양 발생의 위험성과 DNA repair gene의 유전적 다형성간의 관련성을 연구한 한 논문에서 후두암의 경우 특정 haplotype에서 다발 원발암의 발생률이 증가하는 것으로 나타났다. 하지만 현재까지의 보고에서 주된 것으로 밝혀진 다발 원발암의 위험인자는 흡연과 가족력뿐이고, 많은 연구에도 불구하고 명확히 규명된 특정 유발인자는 없어 이에 대한 추가적인 연구가 필요할 것으로 보인다.
저자들은 최근 국내에서 거의 보고된 적이 없는 이시 4중복암을 경험하였기에 문헌고찰과 함께 보고하는 바이다.