폐외 결핵 진단에서 2개의 전혈 인터페론 감마 측정법의 유용성 비교
Comparison of the Diagnostic Usefulness of Two Whole-Blood Interferon-Gamma Assays for Extrapulmonary Tuberculosis
Article information
Abstract
목적:
QuantiFERON-TB GOLD (QFT-G)와 QuantiFERON-TB GOLD in tube (QFT-IT) 검사는 주로 활동성 폐결핵 또는 잠복결핵의 진단과 관련되어 연구되어져 왔으나, 폐외 결핵의 진단과 유용성은 아직 잘 밝혀지지 않은 상태이다. 본 연구는 폐외 결핵 환자에서 QFT-G와 QFT-IT의 진단적 유용성에 대해 비교 분석하였다.
방법:
2007년 6월부터 2010년 8월까지 임상적으로 폐외 결핵이 의심되어 QFT-G, QFT-IT 검사를 한 환자 각각 56명과 48명을 대상으로 하였다. QFT-G와 QFT-IT의 민감도, 특이도, 양성예측도, 음성예측도와 QFT-IT의 cut-off value를 통하여 진단적 유용성을 분석하였다.
결과:
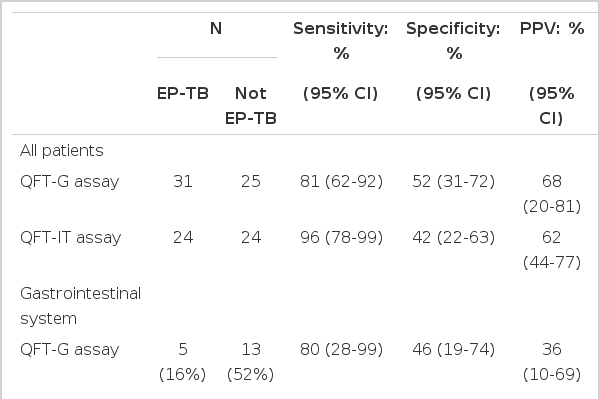
폐외 결핵으로 진단된 환자는 55명(53%)이었고 QFT-IT의 민감도, 특이도, 양성예측도, 음성예측도는 96%, 42%, 62%, 91%이었으며, QFT-G는 81%, 52%, 68%, 68%이었다. 감염 부위에 따른 검사 결과 또한 민감도, 음성예측도에서 QFT-IT가 QFT-G보다 더 높은 결과를 보였다. 본 연구에서 cut-off value는 기존에 권고하고 있는 cut-off value의 범위 안에 포함되었다(0.30-0.45 IU/mL, sensitivity 95.8%, specificity 41.7%).
결론:
QFT-IT는 M.tuberculosis 감염의 진단에 있어서 QFT-G보다 높은 민감도와 음성예측도를 보이며, 특이도에 있어서는 유사한 결과를 보여 새로운 IGRA방법으로서 폐외결핵의 진단을 더 강화시킬 수 있는 가능성을 보여주었다.
Trans Abstract
Background/Aims:
The QuantiFERON-TB Gold (QFT-G) and QuantiFERON-TB Gold in tube (QFT-IT) assays have been studied primarily for the use of diagnosing active pulmonary tuberculosis (TB) or latent TB. The clinical usefulness of these assays for the detection of active extrapulmonary (EP) TB has not been fully defined. The aim of this study was to compare the diagnostic value of these two interferon-gamma assays for EP-TB.
Methods:
From June 2007 to August 2010, we evaluated the usefulness of QFT-G (n = 56) and QFT-IT (n = 48) in patients (n = 104) with suspected EP-TB. The diagnostic sensitivity, specificity, postive predictive value (PPV), and negative predictive value (NPV) of QFT-G and QFT-IT, and the cut-off value of QFT-IT were analyzed.
Results:
EP-TB was diagnosed in 55 (53%) patients. The overall sensitivity, specificity, PPV, and NPV of the QFT-IT assay were 96%, 42%, 62%, and 91%, respectively, and those of the QFT-G test were 81%, 52%, 68%, and 68%, respectively. In subgroup analyses according to infection site, the sensitivity and NPV of QFT-IT were higher than those of QFT-G. Analysis confirmed that the manufacturer's recommended test cut-off value fell within our cut-off value range (0.30-0.45 IU/mL; 95.8% sensitivity, 41.7% specificity).
Conclusions:
The QFT-IT assay showed superior sensitivity and NPV, and equivalent specificity, as comparison with the QFT-G test for the detection of Mycobacterium tuberculosis infection. The logistic benefits of the QFT-IT test format should facilitate the diagnosis of EP-TB. (Korean J Med 2011;81:478-486)
서 론
폐외 결핵(extrapulmonary tuberculosis, ET-TB)은 폐 이외의 모든 장기에 침범한 결핵으로 우리나라의 폐외 결핵 신고 신환자수 추이를 보면 연간 2007년에는 5,005명이고, 2009년에는 6,923명으로 점점 증가하는 추세이다[1]. 노령화에 따른 기저질환 증가, human immunodeficiency virus (HIV) 감염환자나 tumor necrosis factor-alpha antagonist (TNF-alpha) 치료를 받은 면역억제 환자들이 증가하면서 폐외 결핵은 점점 증가하는 추세다. 그러나 폐외 결핵의 미생물학적, 병리학적 진단을 위해서는 침습적인 방법들이 요구되므로 폐결핵(pulmonary tuberculosis)보다 진단이 어렵다. 비록 tuberculin skin test (TST)가 결핵의 임상적 진단에 유용하다고 입증되었으나 우리나라처럼 bacillus calmette guerin (BCG) 예방접종을 필수적으로 하는 경우 TST의 특이도는 제한점이 있으며, 폐외 결핵을 가지는 면역억제 환자에서는 낮은 반응성을 나타내어 정확성과 신뢰성에 한계를 보여준다[2,3].
최근에는 전혈 인터페론 감마 측정법(interferon-gamma releasing assay, IGRA)이 결핵을 진단하는 데 사용되고 있다[4,5]. 대표적인 것으로 ESAT-6 (early secretory antigenic target-6)와 CFP-10 (culture filtrate protein-6)의 합성 펩타이드를 이용한 QuantiFERON- TB Gold (QFT-G)가 있다. 그러나 QFT-G 검사의 경우 전혈 채취 12시간 내에 결핵 특이 항원으로 검사해야 하는 제한점이 있다. QuantiFERON-TB Gold in tube (QFT-IT)는 이러한 단점을 보완하기 위해 개발된 방법으로 채취 혈액을 특이단백 항원(ESAT-6, CFP-10, TB 7.7)이 포함된 용기에서 직접 백혈구를 자극하여 interferon-gamma (INF-r) 양을 효소 면역법(enzyme-linked immunosurbent assay, ELISA)으로 측정하는 검사법이다.
QFT-G 검사는 주로 활동성 폐결핵 또는 잠복결핵의 진단과 관련되어 연구되었지만 최근 폐외 결핵의 진단과 유용성에 대해 몇몇 보고가 있었다[6,7].
그러나 폐외 결핵에 대한 QFT-IT 검사의 유용성에 대한 연구는 보고된 적이 없다. 이에 본 연구를 통해 다양한 형태의 폐외 결핵이 의심되는 환자에서 QFT-G와 QFT-IT의 진단적 유용성과 검사의 정확성에 대해 비교하고자 하였다.
대상 및 방법
대상 환자
2007년 6월부터 2010년 8월까지 39개월간 동아대학교병원에서 임상적으로 폐외 결핵이 의심되어 QFT-G를 시행한 56명과 QFT-IT 검사를 시행한 환자 48명을 대상으로 하였다. 조직학적 검사를 시행하지 않은 환자와 폐결핵 환자는 대상에서 제외하였다. 폐외 결핵은 감염 부위에 따라 위장관결핵, 림프절결핵, 골관절결핵, 비뇨생식기결핵, 복막결핵 및 기타결핵으로 나누었으며 각각 폐외 결핵으로 의심되는 환자는 다음과 같이 분류하여 정의하였다. 1) 위장관결핵은 발열, 복통, 설사, 식욕부진 등의 증상이 있고 대장내시경에서 회맹부에 궤양과 점막비후가 있는 경우 의심하였으며, 2) 림프절결핵은 림프절의 무통성 비대가 있는 경우 의심하였고, 3) 골관절결핵은 요통, 감각장애, 보행장애 등의 임상증상과 엑스선이나 전산화 단층 촬영, 자기 의심하였으며, 2) 림프절결핵은 림프절의 무통성 비대가 있는 경우 의심하였고, 3) 골관절결핵은 요통, 감각장애, 보행장애 등의 임상증상과 엑스선이나 전산화 단층 촬영, 자기 공명 영상에서 결핵이 의심되는 환자를 대상으로 하였으며, 4) 비뇨생식기결핵은 배뇨곤란, 무통의 혈뇨, 측복부 통증 등의 증상이 있으며 컴퓨터 단층 촬영 같은 영상의학적 검사에서 결핵이 의심되는 경우로 하였고, 5) 복막결핵은 복수, 발열, 복통 등의 증상이 있으며 복수에서 ADA (adenosine deaminase) 50 IU/L 이상 증가하였거나, 전산화 단층 촬영에서 고음영의 복수와 중심부 괴사가 있는 림프절 비대가 있는 경우 복막결핵을 의심하였다.
폐외 결핵의 진단은 감염부위의 조직에서 생검을 통해 건락육아종이 확인된 경우거나, 조직배양에서 결핵균이 증명된 경우일 때 진단하였다. 대상 환자들의 의무기록을 조사하여 기저질환(당뇨병, 악성종양, 만성신부전, 간경화, 면역억제제를 최근 3개월 이내 복용한 경우, HIV 감염) 여부를 분석하였다.
QFT-G 검사
QFT-G 검사는 헤파린 처리된 용기에 전혈을 채취하여, 자극 항원으로 ESAT-6와 CFP-10을 사용하고, 양성 대조 항원(mitogen) 및 음성 대조 항원(nil)을 16-24시간 배양한 후 분비된 INF-γ를 ELISA법으로 측정하여 판독하였다. INF-γ의 농도가 ESAT-6 또는 CFP-10에서 0.35 IU/mL 이상일 경우 양성으로 판정하고, 0.35 IU/mL 미만이거나 Nil 값의 25% 이하일 때는 음성으로 판정하였다. 양성 대조 항원이 0.5 IU/mL 이하인 경우에는 미정(indeterminate)으로 하였고 연구대상에서 제외하였다.
QFT-IT 검사
QFT-IT (Cellestis, Carnegie, Astralia) 검사는 QFT-G 검사와 원리상 큰 차이는 없으나 여기서는 같은 튜브에다 ESAT-6, CFP-10 외에 TB 7.7이 추가되어 동시에 검사하게 된다. 검체 채취 시 일반 헤파린 튜브가 아니라 항원 및 대조군 전용 용기에 직접 혈액을 채취하도록 하여 검체 채취 12시간 이내에 검사를 해야하는 QFT-G의 단점을 보완한다. 종전에는 항원별로 결과가 보고되었으나 이 방법에서는 세가지 항원이 같은 튜브에 들어 있어 항원별 결과는 보고되지 않고, INF-γ의 농도가 ESAT-6 또는 CFP-10에서 0.35 IU/mL 이상일 경우 양성으로 판정하고, 0.35 IU/mL 미만이거나 Nil 값의 25% 이하일 때는 음성으로 판정하였다. 양성 대조 항원이 0.5 IU/mL 이하인 경우에는 미정으로 하였고 연구대상에서 제외하였다.
통계
QFT-G와 QFT-IT의 진단적 유용성은 민감도, 특이도, 양성예측도, 음성예측도를 통하여 분석하였다. 폐외 결핵인 환자와 폐외 결핵이 아닌 환자 간의 비교는 연속변수의 경우 Mann-Whitney U-test, 범주형 변수의 경우 Fisher's exact test를 시행하였다. QFT-G와 QFT-IT의 각각의 receiver-operating characteristics (ROC) 분석을 시행하여 cutoff value를 알아보았다. p 값이 0.05 미만일 때 통계적으로 유의하다고 판정하였다. 통계분석은 PASW Statistics 18 (SPSS Inc., Chicago, IL, USA) 프로그램을 이용하였다.
결 과
대상 환자의 특성
폐외 결핵이 의심된 104명의 환자 중 폐외 결핵 환자는 55명 (53%), 폐외 결핵이 아닌 환자는 49명(47%)이었다. 환자의 연령 분포는 11세에서 86세이었으며, 중앙 연령 값은 52세였다. 폐외 결핵 환자와 폐외 결핵이 아닌 환자 사이의 나이, 성별, 면역 억제 질환의 동반 여부에는 유의한 차이가 없었다. 폐외 결핵으로 진단된 55명의 감염부위별 빈도는 위장관결핵(gastrointestinal tract, GIT), 림프절결핵(lymph node, LN), 골관절결핵(bone/joint), 복막결핵(peritoneum), 기타결핵(other), 비뇨생식결핵(GUS) 순서였다. 폐외 결핵이 아닌 49명의 감염부위별 질환은 위장관질환, 림프절질환, 골관절질환, 기타질환, 복막질환, 비뇨생식기질환 순서였다. 기타 결핵에는 피부결핵 3명, 흉막결핵 2명, 안결핵 1명, 근막결핵 1명이 포함되었다. 폐외 결핵이 아닌 49명의 감염부위별 질환은 장질환 29명(만성장염 15명, 궤양 9명, 선종 3명, 아밀로이드증 2명), 림프절질환 6명(키쿠치씨병 4명, 림프종 2명), 골관절질환 6명(골수염 1명, 골관절염 5명), 흉막 섬유화증 5명, 전이성 복막질환 2명, 급성 간질성 신염 1명이었다(Table 1).
QFT-G와 QFT-IT의 진단적 유용성
QFT-G를 시행한 56명 중에서 양성인 환자는 37명(66%)이었고, 그중 폐외 결핵으로 진단된 환자는 25명(67.6%)이었으며 QFT-G 음성인 환자 19명(33.9%) 중 폐외 결핵은 6명(31.6%)이었다.
QFT-IT를 시행한 48명 중에서 양성인 환자는 37명(77%)이었고, 그중 폐외 결핵으로 진단된 환자는 23명(62.2%)이었으며 QFT-IT 음성인 환자 11명(22.9%) 중 폐외 결핵은 1명(9.1%)이었다.
감염부위별 QFT-G와 QFT-IT의 진단적 유용성
위장관결핵으로 의심된 18명 중 11명(61%)에서 QFT-G 양성이었으며 그중 4명이 폐외 결핵으로 진단되었다. QFT-G 검사가 음성이었던 7명(39%)의 환자 중 폐외 결핵은 1명이었으며 림프절결핵으로 의심된 10명 중 7명(70%)이 QFT-G 양성이었고, 그중 6명이 림프절결핵으로 진단되었다. QFT-G 음성인 3명(30%) 중 폐외 결핵은 1명이었으며 골관절결핵으로 의심된 환자는 9명 중 5명(56%)이 QFT-G 양성이었으며, 그중 3명이 골관절결핵으로 진단되었다. QFT-G 음성인 4명(44%) 중 폐외 결핵은 3명이었으며, 비뇨생식결핵이 의심된 환자는 4명 중 3명(75%)이 QFT-G 양성이었으며 그중 3명 모두 비뇨생식결핵으로 진단되었다. QFT-G 음성인 1명(25%) 중 폐외 결핵은 없었으며 복막결핵이 의심된 환자는 7명으로 그중 5명(71%)이 QFT-G 양성이었고, 그중 5명 모두 복막결핵으로 진단되었다. QFT-G 음성인 2명(29%) 중 폐외 결핵은 1명이었으며 기타 폐외 결핵 질환으로 의심된 경우는 8명으로 그중 6명(75%)이 QFT-G 양성이었고, 그중 4명이 결핵으로 진단되었다. QFT-G 음성인 2명(25%) 중 폐외 결핵은 발견되지 않았다.
위장관결핵으로 의심된 22명 중 17명(77%)에서 QFT-IT 양성이었으며 그중 6명이 폐외 결핵으로 진단되었고, QFT-IT 검사가 음성이었던 5명(23%)의 환자 중 폐외 결핵은 없었다. 림프절결핵으로 의심된 12명 중 10명(83%)이 QFT-IT 양성이었으며 그중 9명이 림프절결핵으로 진단되었으며, QFT-IT 음성인 2명(17%) 중 폐외 결핵은 발견되지 않았다. 골관절결핵으로 의심된 환자는 6명 중 5명(83%)이 QFT-IT 양성이었으며 그중 3명이 골관절결핵으로 진단되었다. QFT-IT 음성인 1명(17%) 중 폐외 결핵은 없었고, 비뇨생식결핵이 의심된 환자는 2명으로 모두 QFT-IT 양성이었으며 모두 결핵으로 진단되었다. 복막결핵이 의심된 환자는 1명으로 QFT-IT 양성이었으며 결핵으로 진단되었다. 기타 폐외 결핵 질환으로 의심된 경우는 5명으로 그중 2명(40%)이 QFT-IT 양성이었고, 그중 2명이 결핵으로 진단되었다. QFT-IT 음성인 3명(60%) 중 폐외 결핵은 1명이었다(Table 2).
IGRA (QFT-G, QFT-IT) 양성과 위음성의 비교
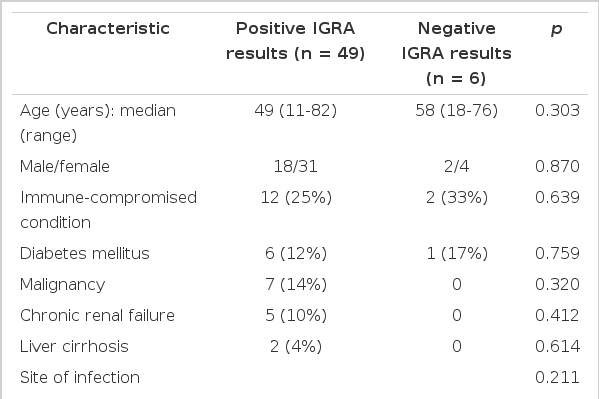
폐외 결핵으로 진단된 55명 중 6명(11%)이 위음성을 보였다. IGRA 양성인 환자와 IGRA 위음성인 환자에서 나이, 성별, 면역 억제 질환의 빈도, 폐외 결핵의 감염부위는 통계적으로 유의한 차이를 보이지 않았다(Table 3).
Cut-off value
QFT-IT에서는 IFN-γ cuff-off value를 0.365 IU/mL로 하였을 때 민감도 95.83%, 특이도 41.67%, 양성가능도비 1.610, 음성가능도비 0.121로, QFT-G에서는 IFN-γ cuff-off value를 0.520 IU/mL로 하였을 때 민감도 80.65%, 특이도 60%, 양성가능도비 2.016, 음성가능도비 0.322로 통계적으로 의미를 보였다(Table 4).
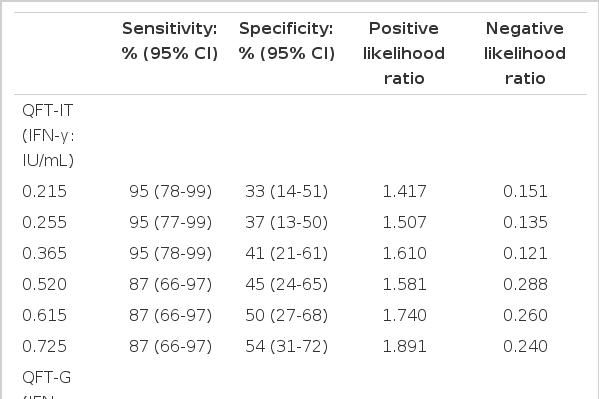
Test sensitivity, specificity, positive likelihood ratio, and negative likelihood ratio for the QuantiFERON-TB Gold (QFT-G) and QuantiFERON-TB Gold in tube (QFT-IT) assays at various cut-off values
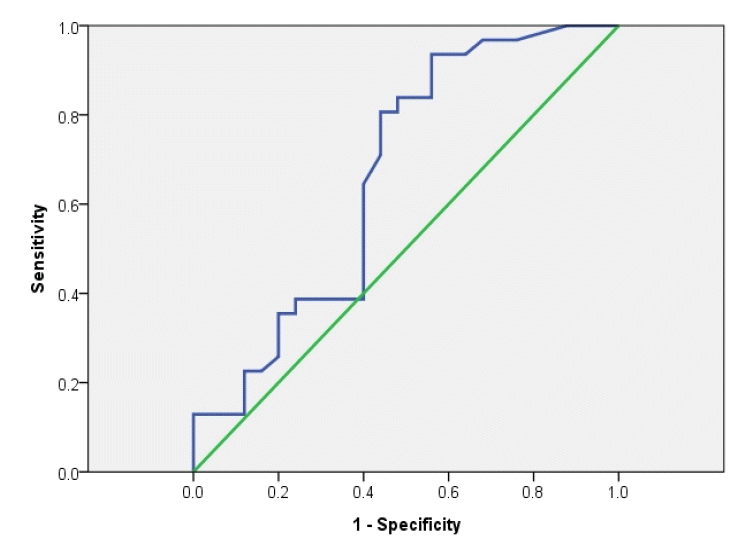
ROC curve로 분석하였을 때 QFT-IT의 area under curve (AUC)는 0.727 (95% confidence internal, 0.581 to 0.872), QFT-G의 AUC는 0.665 (95% confidence internal, 0.515 to 0.815)를 보였다(Figs. 1 and 2).

Characteristics of the receiver-operating curve for the QuantiFERON-TB Gold in tube assay were analyzed in the examination of its diagnostic usefulness for extrapulmonary tuberculosis.
고 찰
본 연구에서 폐외 결핵의 진단에 있어서 QFT-G는 민감도 81%, 음성 예측도 68%를 보이며 QFT-IT는 민감도 96%, 음성 예측도 91%로 QFT-IT가 QFT-G에 비해 민감도와 음성 예측도 면에서 높게 나왔다. 즉 IGRA가 잠복결핵과 현증결핵을 감별할 수 없다는 문제점을 감안할 때 QFT-IT가 QFT-G에 비해 폐외 결핵의 진단에 있어서 더 높은 정확성을 가질 수 있다는 것을 알 수 있다.
또한 본 연구에서는 폐외 결핵 환자의 QFT-IT에서 IFN-γ cuff-off value를 0.365 IU/mL로 하였을 때 민감도 95.83%, 특이도 41.67%로 가장 높은 결과를 보여 기존의 cut-off value가 유효함을 증명하였다.
결핵은 다른 감염성 질환과 달리 한번 감염이 되면 대부분 잠복감염 상태가 되고 적절한 치료를 받지 않으면 수십년 후에 발병하여 2차 전염원이 된다. 최근 면역억제 환자들이 증가하면서 폐외 결핵은 점점 증가하는 추세다. 그러나 폐외 결핵은 폐결핵보다 진단이 어렵다. 결핵이 쉽게 잠복감염 상태가 되고 진단이 늦어서 적절한 치료를 받지 않으면 또 다시 재발한다는 점을 고려할 때 결핵 의심 환자의 빠른 진단이 중요하다.
폐결핵과 폐외 결핵을 진단하는 데 여러 방법이 있다. Purified Protein Derivative (PPD)를 결핵균 항원으로 사용하는 IGRA는 BCG 접종의 영향을 받을 뿐만 아니라 결핵감염의 진단에 있어서 상대적으로 특이도가 낮아 방사선 검사나 객담 배양 검사 등 추가적 검사가 필요했다. QFT-G는 기존의 IGRA를 개선한 방법으로 잠복 결핵을 포함한 모든 결핵에서 사용되는 진단법이다.
QFT-G가 면역억제환자를 대상으로 한 경우에는 양성, 음성의 판정이 불가능한 불확정 결과가 많이 관찰됨을 보고하여 이 검사의 단점으로 지적되었고 검체 내 백혈구가 살아있는 동안 검사를 해야 하므로 검체 채취 12시간 이내에 시행되어야 한다는 단점이 있다[3]. 이를 보완하기 위해 나온 검사가 QFT-IT로 특이단백 ESAT-6, CFP-10, TB 7.7을 같은 튜브에 넣고 동시에 검사하는 방법이다. 그리고 QFT-IT 검사는 일반 heparin tube를 이용해 채취 후 12시간 이내 검사해야 했던 QFT-G 검사와 달리 전용 용기를 사용하여 더욱 편리해졌다.
IRGA의 폐외 결핵에 대한 보고는 하위 집단 분석을 통한 연구가 많았다[7,8]. 최근에 Song 등[9]은 폐외 결핵 환자만을 대상으로 한 연구에서 민감도와 특이도를 69%, 82%로 보고하였다. 그러나 음성예측도가 78%로 낮아 결과가 음성이라고 결핵을 배제하기가 어려웠고 폐외 결핵 중에서 림프절결핵과 척추결핵이 대부분이어서 모든 폐외 결핵에 적용하기에 어려움이 있었다. Lee 등[10]은 다양한 형태의 폐외 결핵에서 QFT-G의 정확성을 보고하였다. 이 연구에서 QFT-G의 민감도는 78%, 특이도는 79%였고 77%의 음성예측도를 보였고 폐외 결핵을 배제하는 데 제한점이 있음을 지적하였다. 이러한 일련의 폐외결핵에 대한 연구에서 IGRA 검사는 다양한 정확도를 보여 진단적 유용성에 있어 제한점이 있었다. Harada 등[11]은 결핵 진단에 있어서 새로운 QFT-IT와 QFT-G의 민감도와 특이도를 비교하여 보고하였다. 이 연구에서 QFT-G의 민감도와 특이도는 81.4%, 98.8%였고, QFT-IT의 민감도와 특이도는 92.6%, 98.8%으로 나와 QFT-IT가 결핵진단에 높은 특이도를 유지하면서 민감도가 더 높은 검사라고 보고하였다. 본 연구는 다양한 폐외 결핵의 진단에 있어서 보고된 적이 없는 QFT-IT의 진단적 유용성을 분석하여 QFT-G와 비교하였다. 본 연구의 결과를 살펴보면 폐외결핵 전체와 세부 장기 결핵 비교에서 QFT-IT가 민감도와 음성예측도가 높은 경향을 보여 결핵을 예측하거나 배제하는 데 있어 QFT-G에 비해 폐외 결핵의 진단적 유용성이 높을 수 있음을 알 수 있었다.
QFT-G 검사의 위음성은 면역억제 환자에서 흔하게 나타난다고 알려져 있다[12]. 본 연구에서 양성군과 위음성군을 기저질환에 따라 하위 집단 분석을 하였으나 두 군 간에 면역억제 환자를 포함하여 기저질환의 차이나 폐외 결핵의 감염부위 차이는 의미 있게 나오지 않았다. 기저질환의 유무, 폐외 결핵의 감염부위와 무관하게 검사결과가 음성이라도 폐외 결핵을 완전히 배제할 수 없음을 알 수 있다.
본 연구에서는 면역억제 환자에서 위음성이 더 흔히 나타나는 것이 아님을 알 수 있었고, 이전 연구들에서 QFT-G 검사 결과가 면역억제 환자에서 불확정으로 나오는 경우가 많아 단점으로 지적되었다. 본 연구에서 결과가 불확정으로 나온 경우는 대상에서 제외하였는데 불확정 결과가 면역저하로 IFN-γ가 적게 만들어질 수도 있으나, 면역상태와 관계없이 양성 대조군 tube의 잘못된 filling이나 mixing으로 같은 결과가 나올 수 있기 때문이다. 이번 연구에서 불확정이라고 나와 제외된 수는 총 6명이었고 모두 QFT-G 검사였으나 면역저하 환자는 아니었다. 비록 QFT-IT 검사에서 불확정이 나오지 않았지만 같은 원리의 검사임을 감안할 때, QFT-G 검사의 단점을 보완한 검사라고는 할 수 없을 것이다.
QFT-G보다 더 최근에 나온 QFT-IT의 cut-off value에 대한 연구는 있었지만 폐외 결핵만을 진단할 때 cut-off value에 대한 연구는 없었다[11]. QFT-IT에서는 IFN-γ cuff-off value를 0.365 IU/mL로 하였을 때 민감도 95.83%, 특이도 41.67%, QFT-G에서는 IFN-γ cuff-off value를 0.520 IU/mL로 하였을 때 민감도 80.65%, 특이도 60%로 나타났다. 하지만 폐외 결핵에서 QFT-IT 검사의 IFN-γ 수치가 0.30, 0.35, 0.40, 0.45 IU/mL에서 모두 같은 민감도 95.83%, 특이도 41.67%으로 보여 본 연구에서는 넓은 범위의 cut-off value가 나왔다. 더 많은 환자 대상수를 가지고 연구한다면 cut-off value의 범위가 좁아질 것으로 생각된다. QFT-IT 검사의 AUC는 0.727 (95% confidence internal, 0.581 to 0.872)으로 QFT-G의 0.665 (95% confidence internal, 0.515 to 0.815)보다 높게 나왔으나 환자군이 달라 직접적인 비교는 어려웠다.
우리 연구에는 한계점이 있다. 첫 번째, 본 연구는 후향적인 연구로 TST에 대한 비교 분석이 없다. 두 번째, IGRA 검사로 QFT-G와 QFT-IT를 같이 시행한 환자군이 없다. 그래서 시행한 검사군이 달라 비교 분석하는 데 비뚤림이 발생하였을 가능성이 있다. 세 번째, 폐외 결핵이 의심되는 환자에서 모두 IGRA 검사를 시행하지 않았고 IGRA 검사를 시행한 환자에서 모두 조직학적 검사나 배양검사를 시행하지 못했다. 따라서 후향적 연구에 따른 선택적 비뚤림이 발생하였을 가능성이 있다. 하지만 이러한 제한점에도 불구하고 본 연구는 다양한 폐외 결핵의 진단에 있어 IGRA test (QFT-G, QFT-IT)의 유용성을 비교한 논문으로 의미가 있다고 판단된다.
결론적으로 QFT-G와 QFT-IT 모두 중등도 이상의 정확성을 보였지만 QFT-IT의 민감도, 음성예측도가 QFT-G에 비해 높아 폐외 결핵을 진단하고 배제하는 데 더 유리할 것이라고 판단하였다. 두 군 간의 더 정확한 비교를 위해 향후 추가적인 전향적 임상 연구가 필요할 것으로 생각한다.