혈액투석 환자에서 중심동맥 경직도와 대동맥 석회화의 연관성
The Relationship between Central Arterial Stiffness and Aortic Calcification in a Cross-Sectional Study of Patients Undergoing Hemodialysis
Article information
Abstract
목적:
만성 신질환 환자에서 심혈관 질환은 주요 사망원인으로 전통적인 위험인자뿐만 아니라 비전통적인 위험인자인 대동맥 경화증, 혈관 석회화와도 연관되어 있을 것으로 생각된다. 그리고 이 위험인자는 측정방법에 따라 각 상관관계에 차이가 있었다. 혈액투석 환자군에서 맥파속도와 석회화 측정을 통해 각각의 상관관계 및 기여인자를 확인하고자 단면연구를 시행하였다.
방법:
2009년 1월부터 10월까지 관상동맥 조영술에서 협착이 관찰되지 않고 정상 크레아티닌 범위를 보이며 고혈압 치료 중인 환자를 고혈압군으로, 6개월 이상 유지 혈액투석 중인 자를 투석군으로 하였다. 각 군의 심혈관, 동반 질환 여부, 약제 복용력 등을 조사하였고 자동 파형 분석기를 통해 맥파속도를 투석 환자에서 non-contrast CT를 이용하여 혈관 석회화 여부를 측정하였다.
결과:
투석군에서 고혈압군에 비해 평균연령이 54.0 ± 13.7세로 낮았고 여성이 더 많았으며 흡연자가 27.9%로 적었음에도 동반 질환은 제 2형 당뇨병이 42.6%로 많고 수축기 혈압(145.3 ± 27.7 vs. 123.3 ± 17.5 mmHg, p< 0.05) 및 맥압(59.3 ± 19.4 vs. 50.7 ± 12.3 mmHg, p< 0.01)이 더 높았다. 투석군에서 hfPWV (11.3 ± 3.20 vs. 9.72 ± 2.16 m/s, p< 0.01), baPWV (17.76 ± 4.79 vs. 13.80 ± 2.95 m/s, p< 0.01)로 모두 증가되었다. 또한 투석군의 73.6%에서 석회화가 동반되었으며 최고 HU는 평균 387.4 ± 295.2 HU였고, 2.69 ± 2.43개의 석회화가 관찰되었다.
분절에 따른 동맥 경직도 및 혈관 석회화와 각 요인들간의 단변량 회귀분석에서 hf가 좋은 상관관계를 보였으며 연령(r = 0.613, p< 0.01), 맥압(r = 0.540, p< 0.01), 혈관 석회화의 HU 값(r = 0.483, p< 0.01), 성별(r = 0.354, p< 0.05), 당뇨 유무(r = 0.331, p< 0.05) 순으로 양의 상관관계를 보여주었다. 최고 HU 정도에 따른 혈관 석회화는 맥압(r = 0.483, p< 0.01), 연령(r = 0.392, p< 0.01) 이외에 투석기간(r = 0.389, p< 0.05)과도 상관관계가 있었으나 성별(r = 0.230, p= NS) 및 당뇨여부(r = -0.052, p= NS)에서는 관계를 보여주지 못했다. 맥파속도는 연령이 많고, 당뇨, 남성에서, 맥압이 높을수록(β = 0.454, p< 0.001, β = 0.250, p< 0.05, β = 0.239, p< 0.05, β = 0.217, p< 0.05) 혈관 석회화 정도는 맥압, 투석기간, 연령(β = 0.401, p< 0.001, β = 0.390, p< 0.05, β = 0.282, p< 0.05) 순으로 기여도가 높았다.
결론:
투석 환자에서 혈관경직도 증가의 위험인자로 고령, 당뇨, 남성 및 높은 맥압이 관여하며, 혈관 석회화의 위험인자는 고령, 투석기간 및 높은 맥압이 연관되어 있었다. 당뇨를 동반한 투석군에서 비당뇨군에 비교하여 혈관경직도가 증가되었다.
Trans Abstract
Background/Aims:
Cardiovascular (CV) disease is the leading cause of death in patients with chronic kidney disease. It may berelated to nontraditional risk factors such as arterial stiffness (AS) and vascular calcification (VC). AS, as evaluated by pulse wavevelocity (PWV), has been established to be an independent predictor of CV mortality. This study investigated the relationshipbetween AS and VC, and contributing risk factors in patients with hypertension undergoing hemodialysis (HD).
Methods:
Cross-sectional data are reported on 65 patients with hypertension and 61 patients undergoing HD. PWV, abdominalcomputed tomography (CT) scans, and serum markers of mineral metabolism were measured.
Results:
Mean heart-femoral (hf) PWV and brachial-ankle (ba) PWV were higher in the HD group than in the hypertensive group.In a univariate linear regression analysis, hfPWV was positively correlated with age (r = 0.613, p< 0.01), pulse pressure (r = 0.540,p< 0.01), highest aortic VC (HU) (r = 0.483, p< 0.01), gender (r = 0.354, p< 0.05), and diabetes (r = 0.331, p< 0.05). Aortic VCwas also positively correlated with pulse pressure (r = 0.483, p< 0.01), age (r = 0.392, p< 0.01), and dialysis duration (r = 0.389, p< 0.05). In a multivariate regression analysis, old age, diabetes, male gender, high pulse pressure, and dialysis duration weresignificantly associated with PWV in that order, whereas high pulse pressure, dialysis duration, and age were significant factors foraortic VC. Arterial stiffness was more prevalent and advanced in the diabetic HD group than that in the nondiabetic HD group.
Conclusions:
A high prevalence of arterial stiffness was noted in patients undergoing HD, which was closely related with old age,diabetes, male gender, and high pulse pressure. Patients with diabetes undergoing HD may be at risk for vascular stiffness. (Korean J Med 2011;81:215-222)
서 론
심혈관 질환은 만성 신질환 환자의 주요 사망 원인으로 투석 중인 환자에서 사망률의 절반 정도를 차지한다[1-3]. 이런 말기 신부전 환자에서 심혈관 질환의 발생원인을 고혈압, 당뇨, 고지혈증, 흡연 등의 전통적인 위험인자만으로는 충분히 설명하지 못하며 혈관 석회와와 동맥 경화증, 염증반응, 감염, 산화 스트레스 등 비전통적인 위험인자가 연관되어 있을 것으로 생각된다[4-6].
이 중에서 동맥 경직도와 혈관 석회화는 밀접하게 연관되어 있으며[7] 각 위험인자와 측정 방법에 따라 상관관계의 차이가 있었다. 하지만 우리나라에서 말기 신질환 환자의 동맥 경직도 및 석회화에 대한 연구는 미미한 실정이다[8]. 본 연구는 혈액투석 환자군에서 맥파속도와 석회화 측정을 통해 각각의 상관관계 및 기여인자를 확인하고자 단면연구를 시행하였다.
대상 및 방법
대상
2009년 1월부터 10월까지 본원에서 고혈압으로 치료 중으로 관상동맥 조영술에서 유의한 협착이 관찰되지 않고 정상범위의 혈중 크레아티닌을 보이는 성인을 고혈압군으로 하였다. 그리고 6개월 이상 안정적으로 유지 혈액투석 중인 외래 환자를 투석군으로 하였다. 대상자 중 악성 질환, 말초동맥 폐쇄질환이 동반된 환자들은 제외하였다.
방법
각 군에서 문진, 신체검사 및 의무기록지를 통해서 심혈관 질환, 동반 질환 여부, 흡연력, 약제 복용력 등을 조사하였다. 고혈압은 JNC VII guideline [9]에 의해 140/90 mmHg 이상이거나 고혈압 약제를 복용 중인 경력이 있는 것으로 정의하였다.
모든 환자에서 복용 중인 약제나 식이 조절은 하지 않았으며 투석 환자에서 인 결합제제는 calcium acetate, 비타민 D 유도체는 alfacalcitriol을 복용한 과거력이 있거나 복용 중인 자로 제한하였다.
맥파 속도(pulse wave velocity, PWV) 및 augmentation index (AI)
혈압과 맥파속도는 고혈압 약제의 복용을 금하지 않은 상태에서 누운 자세로 최소 5분 이상 안정 후에 자동 파형분석기(automatic wave-form analyzer: VP-2000, Colin Co, Komaki, Japan)를 사용하여 동일한 검사자가 측정하였다. 상완 및 발목의 혈압과 맥파는 양팔과 발목에 oscillometric sensor를 가진 cuff를 감아 기록하였다. 대퇴동맥의 맥파는 각각 우측 경동맥과 대퇴동맥에 tonometric sensor를 위치하여 기록하였다. 양쪽 손목에 심전도 유도를 부착하여 심전도를 감시하고, 흉골 좌연의 제2늑간에 심음도(microphone)를 두었다. 대퇴동맥의 맥파, 심전도 및 심음도의 기록이 안정 상태임을 확인한 후 모든 맥파를 동시에 기록하였다. 맥파속도를 결정하는 데 필요한 시간간격(∆T)과 측정 지점 간의 거리(L)는 모두 파형분석기에서 자동으로 계산되었다. 본 연구에서 혈압은 자동 파형분석기의 cuff로 측정한 상완 혈압이며, 높은 쪽의 혈압을 분석에 이용하였다. 맥파속도는 심장-대퇴동맥 맥파속도(heart-femoral pulse wave velocity, hfPWV)와 양측에서 평균 상완-발목동맥 맥파속도(brachial-ankle pulse wave velocity, baPWV)를 그리고 투석 환자에서는 동정맥루를 사용하지 않은 팔의 측정치를 분석에 이용하였다.
그리고 파동의 반향(wave reflection)과 동맥 경직도는 대동맥 맥박파의 형태를 결정하는 주요 인자로 중심 맥박파의 수축기를 분석함으로써 맥파속도와 좌심실 후부하의 박동성 인자에 대한 중요한 정보를 얻을 수 있는데, augmentation index (AI)가 그 중 하나이다. AI는 중심 대동맥의 압력파형곡선에서 반향파에 의해 증강된 대동맥의 수축기 압력의 두 번째 최고점에서 첫 번째 최고점의 차이를 맥박압으로 나눈 값을 백분위로 표시한 값으로 정의될 수 있다.
전산화 단층촬영(computed tomography, CT)
혈액투석 환자군에서만 non-contrast CT를 이용하여(120 kVp, 160 mAs) Toussaint [10,11] 등이 제시한 방법으로 복부 대동맥에서 석회화의 정도를 측정하였다. 주사범위는 1번에서 5번 요추까지였으며 3 mm 간격으로 측정하였고 1명의 영상의학과 의사가 석회화가 관찰된 부위의 최고 감쇄계수(Hounsfield unit, HU)와 각 개수를 기록하였다.
혈액 검사
혈액 채취는 8시간 이상 공복 후에 투석군에서는 투석 시작 전 시행하였다. 혈청 표지자는 일반 화학검사, 지질검사 및 칼슘, 인, calcium-phosphate (Ca × P) product, intact parathyroid hormone (iPTH) 등을 측정하였다. 그리고 총 혈청 칼슘은 corrected calcium = calcium + 0.8 × (4 - albumin)을 이용하여 보정하였다.
혈액투석 환자는 주 3회, 회당 4시간씩 high flux (FX60 또는 FX80)로 투석을 시행받았고, 환자의 혈청 칼슘농도에 따라 9.5 mg/dL 이상이면 칼슘농도 2.5 mEq/L로, 이하이면 3.5 mEq/L의 투석용액을 사용하였다. 투석 적절도는 Daugirdas 방법에 의한 가장 최근의 Kt/Vurea [12]로 나타냈다.
Kt/V = -Ln (R - 0.008 × t) + [(4 - 3.5 × R) × UF ÷ W]
Ln: natural logarithm
R: postdialysis BUN/predialysis BUN
t: dialysis session length in hours
UF: ultrafiltration volume in liters
W: patient’s postdialysis weight in kilograms
통계 분석
모든 측정값은 평균 ± 표준편차 또는 빈도로 표시하였다. 통계 분석은 윈도우용 SPSS 15.0을 이용하였다. 각 군간 대상자의 특성 비교는 Student t-검정, χ2-검정을 이용하였다. 각 맥파속도 측정값 및 혈관 석회화와 연령, 성별, 위험인자들 간의 상관관계는 단변량 회귀분석을 시행하였으며 의미가 있는 각 인자들은 맥파속도와 혈관 석회화에 대한 예측력을 다중 회귀분석으로 평가하였다. p 값이 0.05 미만이면 통계적으로 유의한 것으로 평가하였다.
결 과
임상적 특징
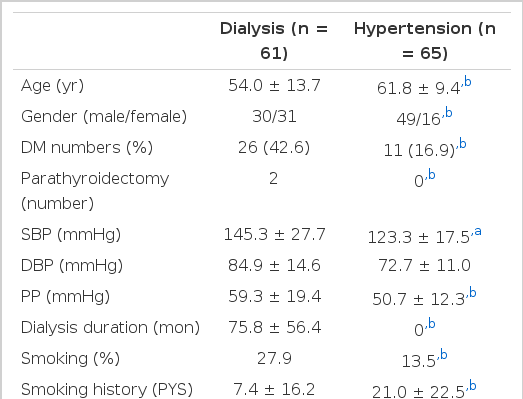
투석군에서 고혈압군에 비해 평균연령이 54.0 ± 13.7세로 낮았고 여성이 더 많았다(Table 1). 또한 투석 환자에서 고혈압이 80.7% 그리고 제 2형 당뇨병이 42.6%로 동반되었으며 안정 시 수축기 혈압(145.3 ± 27.7 vs. 123.3 ± 17.5 mmHg, p< 0.05) 및 맥압(59.3 ± 19.4 vs. 50.7 ± 12.3 mmHg, p< 0.01)이 더 높았다. 평균 투석기간은 75.8 ± 56.4개월이었으며 흡연자가 27.9%로 적었고 전체 흡연력은 7.4 ± 16.2년으로 고혈압 군보다 짧았다.
혈액 검사에서는 고지혈증 약제 복용의 유의한 차이(data not shown)는 없었지만 총 cholesterol이 유의(157.0 ± 31.4 vs. 174.0 ± 36.8 mg/dL, p< 0.01)하게 낮았고, 투석군의 평균 Kt/V는 1.69 ± 0.25이었다.
대동맥 경직도, 혈관 석회화 및 골대사 지표
각 군의 동맥경화 지표, 혈관 석회화 및 골대사의 혈청 표지자에 대해 비교하였다(Table 2). 투석군에서 hfPWV (11.3 ± 3.20 vs. 9.72 ± 2.16 m/s, p< 0.01), baPWV (17.76 ± 4.79 vs. 13.80 ± 2.95 m/s, p< 0.01)로 모두 증가되었으나 AI는 유의한 차이(26.2 ± 12.3 vs. 25.7 ± 13.1%, p= NS)를 보이지 않았다.
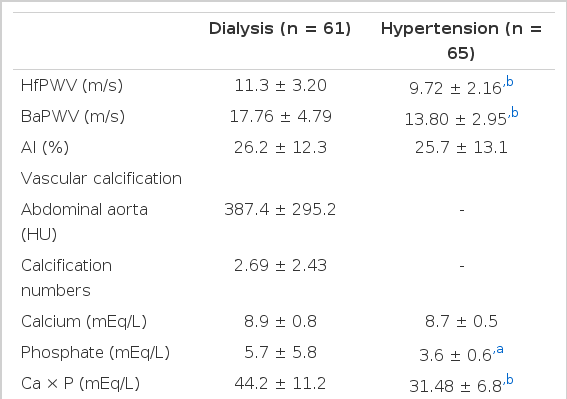
Arterial stiffness, vascular calcification, and serum markers of mineral bone metabolism in patients with hypertension undergoing dialysis
투석군의 73.6%에서 석회화가 관찰(data not shown)되었으며 대동맥 석회화의 최고 감쇄계수(highest HU)는 387.4 ± 295.2 HU (range 0-1,016)였고, 평균 2.69 ± 2.43개의 석회화가 관찰되었다. 골대사 표지자에서 칼슘(8.9 ± 0.8 vs. 8.7 ± 0.5 mg/dL, p= NS)은 차이를 보이지 않았으나, 인(5.7 ± 5.8 vs. 3.6 ± 0.6 mEq/L, p< 0.05), Ca × P (44.2 ± 11.2 vs. 31.48 ± 6.8 mEq/L, p< 0.01) 그리고 iPTH는 233.7 ± 391.1 pg/mL로 증가되었다. 칼슘 함유 인 결합제(calcium acetate 710 mg)는 89.8%에서 복용 중이었고, 누적 사용량은 3647.2 ± 3204.8정, 비타민 D 유도체(alfacalcitriol)는 212.9 ± 401.5정이었다. 분절에 따른 동맥 경직도 및 혈관 석회화와 각 요인들 간의 단변량 회귀분석에서 hfPWV가 baPWV보다 각 인자들과 더 좋은 상관관계를 보였으며, 연령(r = 0.613, p< 0.01), 맥압(r = 0.540, p< 0.01), 혈관 석회화의 HU 값(r = 0.483, p< 0.01), 성별(r = 0.354, p< 0.05), 당뇨 유무(r = 0.331, p< 0.05) 순으로 양의 상관관계를 보여주었다(Table 3).

Univariate regression analysis for the correlations between pulse wave velocity, vascular calcification, and other risk factors in patients undergoing dialysis
최고치 HU에 따른 혈관 석회화는 맥압(r = 0.483, p< 0.01), 연령(r = 0.392, p< 0.01) 이외에 투석기간(r = 0.389, p< 0.05)과도 상관관계가 있었으나 성별(r = 0.230, p= NS) 및 당뇨여부(r = -0.052, p= NS)와는 같은 결과를 보여주지 못했다. 측정부위에서 맥파속도와 최고 HU에 따른 혈관 석회화는 수축기 혈압(r = 0.365, p< 0.05)보다 맥압(r = 0.483, p< 0.01)이 더 높은 상관관계를 보여주었다. 그 외 혈청 protein, albumin, CRP (C-reactive protein) 등과는 상관관계가 없었다(data not shown).
또한 투석 환자에서 동맥 경화 및 혈관 석회화에 관련이 있는 각 위험인자들에 대하여 다중 회귀 분석을 시행하였다(Table 4).
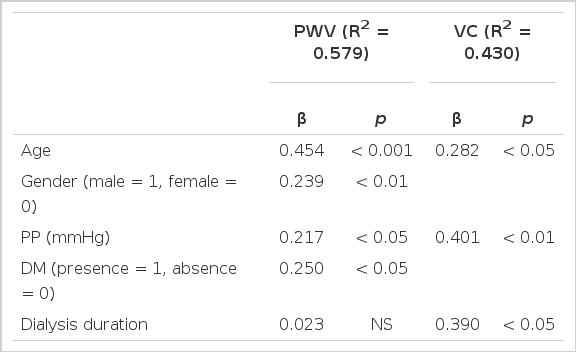
Multivariate regression analysis with variables for arterial stiffness and vascular calcification in patients undergoing dialysis
맥파속도는 연령이 많고, 당뇨, 남성에서, 맥압이 높을수록(β = 0.454, p< 0.001, β = 0.250, p< 0.05, β = 0.239, p< 0.05, β = 0.217, p< 0.05) 혈관 석회화 정도는 맥압, 투석기간, 연령(β = 0.401, p< 0.001, β = 0.390, p< 0.05, β = 0.282, p< 0.05) 순으로 기여도가 높았다.
하위집단 분석(Subgroup analysis)
당뇨를 동반한 투석군에서 맥압이 높고(66.9 ± 15.7 vs. 53.9 ± 20.2 mmHg, p< 0.05) 각 분절의 맥파속도(hfPWV 12.62 ± 2.92 vs. 10.47 ± 3.13 mmHg, p< 0.05; and baPWV 18.17 ± 4.57 vs. 17.46 ± 4.99 mmHg, p< 0.05)가 증가되었다(Table 5). 또한 혈관석회화에서 최고 HU (299.8 ± 276.4 vs. 510.0 ± 292.9 HU, p< 0.01) 및 석회화 수(2.02 ± 2.18 vs. 3.64 ± 2.50, p< 0.01)가 증가되었으나 연령, 성별, 흡연력, 투석기간, 혈액검사 및 칼슘-인 대사 표지자, 인 결합제의 누적 복용량 그리고 투석 적절도에서는 차이를 보이지 않았다(p= NS, respectively).
고 찰
혈관 경직도는 맥파속도 측정을 통해 유추하는데, 그 정도가 심할수록 맥파속도가 높게 나타난다. 본 연구에서 대조군인 고혈압군과 비교하여 투석군에서 hfPWV 및 baPWV 모두 증가되어 있었으며, 인 농도 및 칼슘-인의 곱이 증가되어 있었다. 이와 더불어 투석군에서 심한 혈관석회화를 보였다. 이러한 결과는 투석 환자에서 혈관경직도가 증가되어 있으며, 이의 원인기전에 혈관 석회화가 연관되어 있을 것임을 시사하는 소견이다.
혈관 석회화의 원인기전으로 칼슘-인 농도의 증가가 제시되어 왔으며[13,14], 임상연구에서 혈관석회화가 심혈관 손상과 연관되어 있음이 알려져 있다[15]. 따라서 본 연구 결과는 투석 환자에서 칼슘-인의 곱이 증가한 것이 혈관 석회화 및 이로 인한 혈관 경직도 증가를 유발하였을 것으로 유추하여 볼 수 있다.
혈관 석회화의 평가는 측정 부위와 방법에 따라 차이가 있으며 단순 방사선 및 전산화 단층촬영 등이 제시되고 있으나 명확한 지침은 없는 실정이다. 본 연구에서는 중심동맥 석회화를 평가하기 위해 복부 대동맥에서 전산화 단층촬영을 시행하였다. 혈액투석 환자에서 대동맥 석회화는 대부분에서 관찰되었으며 석회화의 개수 및 HU와 같은 반정량적인 방법에서도 고령, 투석기간 및 높은 맥압과 같은 위험인자와 연관성이 좋았다.
hfPWV는 대동맥과 같은 큰 중심동맥의 경직도를 반영하며, baPWV는 중심 및 말초동맥의 경직도를 반영한다[16]. 따라서 hfPWV는 대동맥 경직도를 평가하는 경-대퇴동맥(carotid-femoral) PWV (cfPWV)을 대체할 수 있으며, 대동맥 경직도를 대변하여준다. 본 구에서 분절에 따른 동맥 경직도 및 혈관 석회화와 각 요인들 간의 단변량 회귀분석에서 hfPWV가 baPWV 보다 각 위험인자들과 더 좋은 상관관계를 보여주었다. 이러한 소견은 대동맥 경직도의 변화에 연령, 맥압, 혈관 석회화, 성별, 당뇨병 등이 병인에 연관되어 있음을 시사한다. 투석환자에서 동맥 경직도 및 혈관 석회화가 연령 및 맥압과 높은 상관관계를 확인하였으나 칼슘-인 대사 이상과 같은 비전통적인 위험인자와 상관관계는 관찰되지 않았다. 이전의 보고[10,17]에서도 동맥 경직도와 혈관 석회화에 영향을 미치는 인자는 연관성은 유사했고, 기여도에서도 정도의 차이만 보여 본 연구와 대체로 유사한 결과를 보였다. 또한 혈관 석회화와 비전통적인 위험인자인 투석 기간이 의미 있는 상관관계를 보였으며[10], 석회화가 심한 군에서 유의하진 않았지만 인 결합제의 누적사용량이 많은 경향 등으로 미루어 말기 신질환의 이환에 따른 지속적인 칼슘-인 대사 이상, 인 결합제의 복용, 부갑상선 항진증, 투석액의 칼슘 농도 등이 영향을 미칠 가능성이 있어 추가적인 대규모, 전향적인 연구가 요구된다.
당뇨를 동반한 투석군에서 맥압이 높고, 맥파속도가 증가되었다. 하지만 전통적인 위험인자인 연령, 성별, 흡연력, 투석기간, 혈액검사 및 칼슘-인 대사 표지자, 인 결합제의 누적 복용량 그리고 투석 적절도에서는 차이를 보이지 않아, 당뇨병 자체가 혈관경직도의 위험인자가 될 수 있음을 시사하였다.
본 연구의 제한점으로 첫째, 소수의 환자를 대상으로 각 위험인자들이 유의한 차이를 보여 혈관 경직도 및 석회화에 영향을 미쳤을 가능성이 있었다. 또한 혈액투석 환자의 일부에서 고혈압이 동반되지 않은 대상자가 포함되어 표준화가 부족하였다. 둘째, 단면 연구로 진행되어 위험인자에 따른 변화를 확인할 수 없었다.
결론적으로 투석 환자에서 혈관경직도 증가의 위험인자로 고령, 당뇨, 남성 및 높은 맥압이 관여하며, 혈관 석회화의 위험인자는 고령, 투석기간 및 높은 맥압이 연관되어 있었다. 당뇨를 동반한 투석군에서 비당뇨군에 비교하여 혈관경직도가 증가되었다.