급성골수성백혈병의 차세대 염기서열 분석을 통한 분자유전학적 위험도 분류
Molecular Risk Stratification using Next-generation Sequencing in Acute Myeloid Leukemia
Article information
Trans Abstract
Chromosomal abnormalities are an important prognostic factor in cases of acute myeloid leukemia (AML). Molecular mutations have been reported to contribute to the pathogenesis and prognosis of AML. Next-generation sequencing (NGS) has revolutionized the speed and cost of genomic sequencing and enables the parallel analysis of many genes for molecular risk stratification. The molecular mutations currently included in risk stratification at AML diagnosis are c-kit, FLT3-ITD, NPM1, CEBPA (biallelic), RUNX1, ASLX1, and TP53. The importance of screening for mutations has been further emphasized by introducing novel therapeutic targets for molecular mutations, such as FLT3-TKD, IDH1, and IDH2. Molecular mutations are also used to evaluate measurable residual disease during treatment and to select the intensity of the treatment during consolidation and follow-up. Pretreatment leukemic marrow and blood should be stored at a biobank to perform NGS analysis in cases of AML at diagnosis. Samples from various time points during and after treatment should be obtained and stored under appropriate conditions.
서 론
급성골수성백혈병(acute myeloid leukemia, AML)은 성인에서 호발하는 혈액암이며, 우리나라에서 연간 1,300명가량이 AML로 진단된다[1]. AML의 치료는 관해유도항암치료(induction chemotherapy)와 공고치료(consolidation therapy)로 나뉘며, 일차 치료의 목표는 관해유도항암치료를 시행하여 완전관해(complete remission)에 도달하는 것이다. 완전관해에 도달한 후에는 재발률을 낮추기 위해 동종조혈모세포이식술을 시행 받아야 할 것인지를 결정하게 된다. 동종조혈모세포이식술은 재발률을 낮추는 데는 매우 효과적인 치료이지만 치료 강도가 매우 높아서 치료 연관 부작용으로 인한 사망률을 증가시키므로, 재발률이 높을 것으로 분류된 환자군을 선택하여 시행할 것을 권고한다[2]. AML은 전통적으로 진단 시 동반된 염색체 이상이 질환의 진단과 예후에 중요한 인자이다. 최근 분자유전학적 분석 방법의 발달로 분자돌연변이가 질환의 발병에 중요한 역할을 하는 것으로 밝혀지고, 이러한 분자돌연변이가 질환의 예후와 연관이 있는 것으로 알려져 있다[3].
차세대 염기서열 분석법(next-generation sequencing, NGS)은 수십-수백 개의 유전자를 하나의 패널로 구성하여 1회의 검사로 많은 유전자를 동시에 검사할 수 있으며, 생산된 유전자 결과를 분석하여 2-4주 내에 결과를 확인하여 환자의 치료를 결정할 수 있다. 진단 시 동반되는 염색체 이상은 중요한 예후 인자이지만, 50%가량의 환자에서 염색체 이상을 동반하지 않는 정상핵형(normal karyotype)을 보이며, 이 환자들은 광범위하게 중간위험군에 속하게 되고 다양한 임상 경과를 보이게 된다. 분자돌연변이 동반의 유무는 특히 정상 핵형의 환자들을 유전학적 위험도에 따라 세분화된 분류가 가능하도록 해주었다. NGS에 대한 자세한 검사 방법 및 우리나라에서의 현황, 질환별 유전자 패널의 구성에 대한 국가 의료보험의 기준은 이전 호에 소개된 논문을 참고하기 바란다[4]. AML에서 국가의료보험에서 지정한 NGS에 포함해야 할 필수 유전자 돌연변이는 CEBPA, FLT3, JAK2, KIT, NPM1, RUNX1, TP53, IDH1 및 IDH2이다.
현재 AML에서 진단 당시 위험도 분류에 포함된 분자돌연변이는 c-kit, FLT3-ITD, NPM1, CEBPA (biallelic), RUNX1, ASXL1 및 TP53이다. 이뿐만 아니라 추가적으로 분자돌연변이의 유무에 따라 치료를 결정하는 데 중요한 돌연변이는 FLT3-TKD, IDH1 및 IDH2이다. 분자돌연변이는 진단 시에 위험군 분류 및 치료약제 선택에 매우 중요할 뿐만 아니라, 치료 중 미세잔존질환(measurable residual disease)의 평가 및 재발 시에 분자돌연변이의 유무에 따라 표적치료제를 선택하는 것에도 이용되고 있다[5]. NGS 검사를 적절하게 시행하기 위해서는 무엇보다도 AML의 진단이나 재발 시점에서 검사가 가능하도록 적절한 골수 흡인 검체를 충분히 확보하고, 이를 냉동보존(cryopreservation)하여 향후 검사를 시행할 수 있도록 하는 것이 매우 중요하다.
본 론
AML의 NGS 검사는 위험도 분류에 이용되는 분자돌연변이 외에도, 추가적으로 생식세포 돌연변이(germline mutation) 혹은 clonal hematopoiesis of indeterminate potential과 같이 혈액암 발병과 관련이 있는 것으로 알려져 있는 돌연변이에 대한 유전자를 포함한 포괄적인 유전자 패널을 이용하여 검사를 시행할 것을 권고하고 있다. AML에서 흔히 보고되는 분자돌연변이들은 상호 배타적으로 관찰되거나 혹은 동시에 여러 돌연변이가 관찰되기도 하므로, 이들의 관계를 잘 이해하는 것이 관찰된 돌연변이의 의미를 해석하는 데 중요하다. 현재까지 AML의 위험도 분류에 이용되는 유전자 돌연변이의 각각의 의미는 다음과 같으며, 이들의 유전자간 위험도 분류법은 본론의 마지막에 설명하였다.
NPM1 돌연변이
NPM1은 세포핵 내의 셔틀단백질을 인코딩하는 유전자이다. AML에서 NPM1 돌연변이는 28-35%로 보고되며, 특히 정상핵형인 경우에서는 48-53%로 흔하게 관찰되는 것으로 알려져 있다[6-9]. NPM1 돌연변이가 동반된 경우는 완전관해율이 높으며, 전체 생존율도 예후가 좋은 염색체 이상이 동반된 AML과 유사한 생존율을 보이므로 예후가 좋은 유전자 돌연변이로 해석된다[7,8,10].
FLT3 돌연변이
FLT3는 조혈에 관여하는 티로신 키나제(tyrosine kinase)를 인코딩하는 유전자이며, internal tandem duplication (ITD)과 tyrosine kinase domain (TKD)인 두 가지 class로 분류된다. FLT3-ITD는 AML의 30%가량에서 관찰되고 FLT3-TKD (10%가량)보다 더 흔하게 관찰되며, 특히 정상핵형의 AML에서 FLT3-ITD 돌연변이가 동반되는 경우는 많은 연구에서 무진행 생존율이나 전체 생존율에서 예후가 불량한 것으로 보고하고 있다[6,9,11,12]. 최근의 연구에서는 FLT3-ITD 돌연변이의 유무보다는 allelic ratio (DNA 단편[fragment]을 분석하여 FLT3-ITD 아래 곡선의 면적을 FLT3-wild type 면적으로 나눈 비율)가 높은가(≥ 0.5) 혹은 낮은가(< 0.5)가 중요하며, FLT3-ITD의 allelic ratio와 NPM1 돌연변이의 동반 여부에 따라 AML의 분자유전학적 위험도가 분류된다[13-15].
FLT3-TKD 돌연변이는 FLT3-ITD와는 독립적으로 관찰되며, FLT3-TKD 돌연변이가 동반된 경우의 예후적 의미에 대해서는 논란의 여지가 있다. FLT3-TKD 돌연변이가 동반된 경우에 관해 유지 기간 및 전체 생존 기간이 짧은 것으로 보고한 연구도 있으나, 예후와 관련이 없거나 더 좋은 예후를 보이는 등 다양한 결과를 보고하고 있는데, 이는 어떠한 환자군을 연구 대상으로 하였는가에 따라 다른 결과를 보이는 것으로 해석된다[11,16,17].
FLT3 돌연변이를 표적으로 하는 키나제 억제제는 많은 연구가 보고되어 있으며, 현재까지 미국 식품의약국(Food and Drug Administration, FDA)의 승인을 받은 약제로는 일차 치료 및 재발 혹은 불응성 AML에서 각각 midostaurin과 gilteritinib이 있다. 새로이 진단된 FLT3-ITD 혹은 FLT3-TKD 돌연변이가 동반된 AML 환자를 대상으로 한 제3상 임상 연구(RATIFY trial)에서 표준 관해유도항암치료제에 다중 키나제 억제제(multitargeted kinase inhibitor)인 midostaurin (Rydapt®)을 추가한 경우 무진행 생존율(위험비 0.78)과 전체 생존율(위험비 0.78)의 향상을 보였다[18]. 이 연구 결과를 근거로 midostaurin은 AML의 일차 치료제로 2017년 미국 FDA 승인을 받게 되었고 우리나라에서도 사용 허가를 받게 되었다. Gilteritinib은 2세대 키나제 억제제로 FLT3에 더욱 선택적으로 강력히 작용하는 약물이다. FLT3 돌연변이가 동반된 재발 혹은 불응성 AML을 대상으로 한 제3상 임상 연구(ADMIRAL trial)에서 gilteritinib 단일약제로 치료한 군이 기존의 항암 치료군과 비교하여 전체 생존율이 향상됨을 보여 주었다[19]. 이 결과를 바탕으로 FLT3-ITD 혹은 FLT3-TKD 돌연변이가 동반된 재발 혹은 불응성 AML의 치료제로 gilteritinib이 2018년 미국 FDA 승인을 받았으며, 현재 우리나라에서는 gilteritinib이 Xospata® 약물명으로 재발 혹은 불응성 AML에서 단일약제요법으로 사용이 허가된 상태이다.
CEBPA 돌연변이
AML의 예후와 관련된 중요한 돌연변이 중 하나는 CEBPA이다. CEBPA 유전자는 과립구의 분화에 중요한 역할을 하는 전사인자이며, AML의 7-11%에서 돌연변이가 관찰된다[6,12]. CEBPA 이중(double 혹은 biallelic) 돌연변이가 동반된 경우는 단일 돌연변이나 돌연변이가 없는 경우에 비해 예후가 좋은 것으로 보고되며, 위험도 분류에서도 예후가 좋은 군으로 분류된다[9,11,12,20].
KIT 돌연변이
Core binding factor (CBF) AML은 t(8;21) 혹은 inv(16) 염색체 이상이 동반된 경우로 정의하며, 전체 AML의 10-15%에서 관찰되고 예후가 좋은 군으로 분류된다[21,22]. KIT 돌연변이는 CBF AML 환자의 20%에서 보고되며, t(8;21) 염색체 이상이 있는 환자군에서 KIT 돌연변이가 동반된 경우는 무진행 생존율 및 전체 생존율이 낮게 관찰된다[23,24]. 하지만 inv(16) 염색체 이상에 KIT 돌연변이가 동반된 경우 예후가 나쁜 것으로 보고된 연구가 있는 반면, 예후적으로 완전관해율이나 전체 생존율에 차이가 없다고 보고한 연구들이 있어 논란의 여지가 있다[23-26].
RUNX1 돌연변이
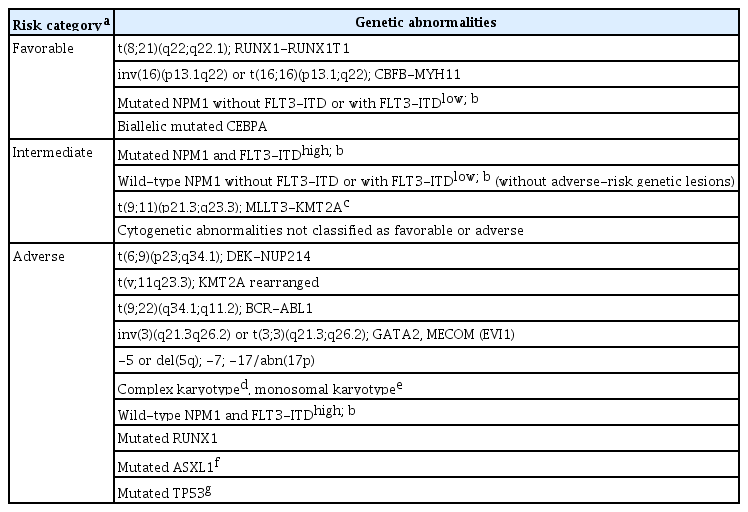
RUNX1은 골수전사인자를 인코딩하는 유전자로, AML의 10%에서 RUNX1 돌연변이가 관찰된다[27-29]. AML에서 RUNX1 돌연변이가 동반된 경우에는 예후가 불량한 것으로 알려져 있다[28,29]. 새로이 진단된 AML에서 RUNX1 돌연변이가 동반된 경우는 고령, 남자 및 골수형성이상증후군에서 진행한 이차 AML에서 더 흔하게 관찰이 된다[29]. RUNX1 돌연변이가 동반된 경우는 2017 European LeukemiaNet (ELN) 위험도 분류에서 예후가 나쁜 군으로 분류된다(Table 1).
ASXL1 돌연변이
ASXL1은 전사에 관여하는 enhancer 유전자의 단백질을 인코딩하는 유전자이며, AML의 5-36%에서 돌연변이가 보고된다[30,31]. ASXL1 돌연변이는 60세 이상 고령의 환자에서 더 흔하게 관찰되며, ASXL1 돌연변이가 동반된 경우 예후가 좋지 않은 것으로 알려져 있다[31].
TP53 돌연변이
TP53 돌연변이는 AML의 12-13%에서 관찰되며 고령에서 더 흔히 관찰된다[32,33]. TP53은 주로 예후가 좋지 않은 복합핵형(complex karyotype)에서 흔하게 동반이 되며(75-78%), 치료 연관(therapy-related) AML에서는 monosomal karyotype (X 혹은 Y 염색체를 제외한 한 개의 홑염색체 이상에, 추가하여 다른 홑염색체 이상이 동반되거나 혹은 CBF를 제외한 다른 염색체 구조적 이상이 동반된 경우)이나 5번 혹은 7번 염색체 이상이 있는 경우에 흔하게 관찰이 된다[33]. TP53 돌연변이가 동반된 AML은 완전관해율이 낮고 무진행 생존율 및 전체 생존율도 낮아서 예후가 매우 좋지 않은 것으로 알려져 있다[34,35].
분자돌연변이에 따른 위험군 분류
AML의 진단 시에 임상에서 가장 많이 이용되는 위험도 분류는 2017 ELN 위험도 분류이며(Table 1), National Comprehensive Cancer Network 권고안도 2017 ELN 위험도 분류를 채택하여 사용하고 있다[2,3]. 2017년 ELN 분류는 AML의 진단 시 동반되는 유전자 이상에 근거한 위험도 분류이며, 임상적 특징과 치료 예후를 반영하여 예후가 좋은 군(favorable), 중간 군(intermediate), 나쁜 군(adverse)과 같이 세 가지 위험군으로 분류한다[3]. 여러 연구에서 FLT3-ITD의 allelic ratio가 예후에 중요한 영향을 미치는 것으로 보고하고 있다. FLT3-ITD의 allelic ratio가 낮으면서(< 0.5) NPM1 돌연변이가 동반된 경우는 FLT3-ITD가 없으면서 NPM1 돌연변이가 동반된 경우와 유사하게 좋은 예후를 보이고 있어서, 이 두 경우는 예후가 좋은 군으로 분류한다. 반면에 NPM1 돌연변이의 동반없이 FLT3-ITD의 allelic ratio가 높은(≥ 0.5) 경우는 예후가 나쁜 군으로 분류된다. 하지만 FLT3-ITD의 allelic ratio 검사는 모든 기관에서 가능한 것이 아니므로, 정량 검사를 시행하기 어려운 경우에는 FLT3-ITD가 관찰되고 NPM1 돌연변이가 동반되지 않는다면 고위험군으로 간주한다[2]. AML에서 TP53 돌연변이 및 CBF AML을 제외한 AML에서 RUNX1 및 ASXL1 돌연변이가 관찰되는 경우는 독립적으로 불량한 예후를 보이고 있어 예후가 나쁜 군으로 분류한다(Table 1).
후성 유전자(epigenetic gene) 돌연변이 및 생식세포 돌연변이의 의미
위에서 언급한 이외의 유전자 돌연변이들도 많은 연구가 시행되고 있으며, 대표적인 유전자로는 후성 유전자 돌연변이에 해당하는 DNMT3A, IDH1, IDH2, TET2가 있다. 비록 예후인자로 사용되기에는 증거가 충분하지는 않지만, 후성 유전자 돌연변이에 대한 표적치료제의 연구가 활발히 진행되고 있다. DNMT3A 돌연변이는 AML의 18-22%에서 관찰되며, 정상핵형에서는 29-34%까지 보고된다[6,12,36-38]. IDH1 돌연변이는 AML의 6-9%에서 관찰되고 정상핵형에서는 8-16%로 더 흔하게 보고되며, 마찬가지로 IDH2도 AML의 8-12%에서 관찰되며, 정상핵형에서는 19%까지 더 빈번한 것으로 보고하고 있다[39-41]. 이들 돌연변이의 예후적 의의에 대해서는 동반되는 돌연변이에 따라 다양한 예후를 보고하고 있어 논란의 여지가 있다. IDH1 및 IDH2 돌연변이는 이를 표적으로 하는 소분자억제제(small molecule inhibitor)인 ivosidenib과 enasidenib이 소개되었으며, 재발성 혹은 불응성 AML 환자를 대상으로 FDA 승인을 받았다[42,43]. 이를 바탕으로 일차 치료 약제로 사용하는 임상 연구가 진행되었는데, IDH1 돌연변이를 표적으로 하는 ivosidenib은 제1상 임상시험에서 41.2% 환자에서 완전관해 혹은 부분 혈액학적 회복을 동반한 완전관해를 보여, 이 자료를 근거로 고강도 관해 유도항암치료가 어렵거나 혹은 75세 이상의 환자에서 AML의 일차 치료제로 2019년에 미국 FDA 승인을 받았다[44]. Enasidenib은 IDH2 돌연변이를 표적으로 하는 약제이며, 60세 이상 새로 진단받은 AML 환자를 대상으로 한 제1b/2상 임상시험의 하위 분석에서 43% 환자에서 완전관해 혹은 부분 혈액학적 회복을 동반한 완전관해를 보여 AML의 효과적인 일차 치료약제로의 역할이 기대되고 있다[45].
최근 혈액 질환의 가족력이 있는 경우에 가족 간에 유전되는 돌연변이가 보고되어 생식세포 돌연변이(germline mutation)에 대한 개념이 소개되었는데, 생식세포 돌연변이는 NGS를 이용한 진단 시 스크리닝 검사가 시행되면서 최근 진단되는 경우가 증가하게 되었다. 이러한 가족 간에 발생하는 돌연변이를 진단하는 것은 AML 환자와 환자의 가족을 적절히 관리하는 데 매우 중요하다. AML로 진단된 환자에서 혈액암의 가족력이 있거나 설명되지 않는 빈혈이나 백혈구 감소증 혹은 혈소판 감소증의 가족력이 있을 경우에는 생식세포 소인(germline predisposition) 골수구계종양에 대한 NGS 검사를 시행하기를 권고한다. 비교적 드물지 않게 보고되는 생식세포 소인 골수구계종양과 관련된 유전자 돌연변이는 CEBPA 돌연변이와 DDX41 돌연변이이며, 매우 드물게 MBD4, RUNX1 및 GATA2 돌연변이가 보고된다. 특히 이러한 돌연변이 유전자가 40-60%의 정량값으로 관찰되는 경우에는 생식세포 검사(germline test)를 시행하여 생식세포 돌연변이임을 진단하도록 권고한다. 하지만 이들 돌연변이가 관찰되는 경우에 적합한 치료 방법은 아직 확립되어 있지 않으므로 환자 개개인의 상황에 맞추어 치료를 계획해야 한다.
치료 후 미세잔존질환 평가로 인한 치료 결정
AML에서 미세잔존질환은 기존의 현미경을 이용한 형태학적 검사에서 관찰되지 않을 정도로 미세하게 백혈병 세포가 남아있는 것을 의미하는데, 실제로는 완전관해에 도달한 환자들이 여전히 많은 양의 백혈병 세포를 가지고 있을 수 있다. 치료 후 미세잔존질환의 평가는 여러 가지 방법이 사용될 수 있으며, 최근 NGS 방법도 미세잔존질환 평가에 이용하고자 연구가 활발히 되고 있다. AML 환자에서 항암 치료 후에 미세잔존질환이 남아 있는 경우에는 동종조혈모세포이식술을 시행하여 재발률을 낮출 수 있으며, 동종조혈모세포이식술의 전처치항암요법을 고강도 요법을 선택하는 등 치료 방법을 차별화하여 재발률을 낮출 수 있음을 보고하고 있다[46,47]. 또한 동종조혈모세포이식술 후에도 미세잔존질환이 관찰되는 경우는 그렇지 않은 군에 비해 재발률이 높으므로 이식편대백혈병효과를 유도하여 재발률을 감소시키거나 유지요법을 시행하는 방안이 제시되기도 한다[48,49]. 하지만 미세잔존질환의 유무를 평가하기 위한 적절한 검사 시점, 양성을 판정하기 위한 cut-off value, 시퀀싱 read depth를 얼마나 시행할 지와 같은 기술적인 문제를 포함하여 NGS를 이용한 미세잔존질환 평가를 이용한 치료 방법의 선택을 임상에 적용하기 위해서는 많은 연구가 필요한 상태이다.
결 론
최근 NGS가 임상에 도입되면서 진단 시 AML을 더욱 세분화하여 위험도를 분류하여 치료방침을 정할 수 있게 되었다. 현재 AML에 대해 분자돌연변이가 질환의 발병 및 진행에 중요한 역할을 하는 것이 밝혀지면서, 이를 표적으로 하는 임상 연구가 다양하게 진행되고 있다. 임상에서도 FLT3, IDH1 및 IDH2 돌연변이에 대한 표적치료제가 미국 FDA의 허가를 받은 상태이며, 우리나라에서는 FLT3 돌연변이를 표적으로 하는 표적치료제인 midostaurin과 gilteritinib이 사용 가능한 상태이다. 이뿐만 아니라 최근 AML의 치료에 소개되는 항대사 약물도 진단 시 분자돌연변이가 예후에 중요한 역할을 하는 것으로 밝혀지고 있어서, NGS를 통한 분자돌연변이의 중요성이 더욱 대두되고 있다. 이는 환자를 분자유전학적 특징을 반영하여 치료를 결정할 수 있도록 해주어 궁극적으로는 환자의 개인 맞춤 치료에 한 단계 다가갈 수 있도록 해줄 것이며, 현재에도 많은 연구가 진행 중이어서 앞으로 NGS를 이용한 맞춤 치료가 더욱 발전될 것으로 기대된다.