만성 복통과 철결핍빈혈로 인하여 소화기 질환으로 오인된 발작성 야간혈색소뇨증 1예
Paroxysmal Nocturnal Hemoglobinuria Presenting with Chronic Abdominal Pain and Iron Deficiency Anemia
Article information
Abstract
발작성 야간혈색소뇨증은 만성적인 혈관 내 용혈, 야간혈색소뇨, 혈전색전증과 이차적 골수부전이 특징인 드문 후천적 조혈모세포 질환이다. 만성 복통과 동반된 철결핍빈혈은 소화관 암, 염증성 장질환 등의 소화기 질환으로 오인될 수 있으나 표준 검사에도 원인을 알 수 없었던 경우에는 드문 원인 질환의 감별 진단의 하나로 발작성 야간혈색소뇨증을 고려할 수 있다. 저자들은 만성 복통 및 철결핍빈혈이 동반된 환자에서 드문 원인인 발작성 야간혈색소뇨증으로 진단한 경험을 하였기에 문헌고찰과 함께 보고하고자 한다.
Trans Abstract
Paroxysmal nocturnal hemoglobinuria (PNH) is a rare acquired disorder of hematopoietic stem cells characterized by chronic intravascular hemolysis, nocturnal hemoglobinuria, thromboembolic events and secondary bone marrow failure caused by uncontrolled complement activation. Generally, chronic abdominal pain and iron deficiency anemia are considered typical symptoms of gastrointestinal diseases, but are also common in PNH. We report a case of PNH presenting with chronic abdominal pain and iron deficiency anemia, along with a relevant literature review.
서 론
만성 복통은 수개월 혹은 수년간 지속되는 복통으로 대부분은 과민성대장증후군과 같은 기능성 장애에 해당하는 질환이 주요 원인이지만[1], 빈혈과 같은 검사실 이상 소견을 동반한 경우에는 기질적 원인을 찾기 위한 추가적 검사를 시행해야 한다. 만성 복통과 빈혈을 동반하는 대표적인 원인 질환은 염증성 장질환 혹은 소화관암 등과 같은 소화기 질환이며, 대부분은 병력 청취, 신체 검사, 혈액 검사, 내시경 및 영상의학적 검사를 통해 원인 감별이 가능하다. 하지만 명확한 원인을 찾지 못하는 경우도 종종 발생하고 있다. 이들 증상과 연관된 드문 질환으로 발작성 야간혈색소뇨증(paroxysmal nocturnal hemoglobinuria, PNH)이 있으며, 복통과 빈혈이 드물지 않게 동반된다고 알려져 있다[2]. 발작성 야간혈색소뇨증은 후천적 조혈모세포 질환으로 발생률은 인구 100만 명당 10명 이내로 드문 질환으로 알려져 있고[3], 증상은 다양하게 나타나며 많은 환자들은 원인을 알 수 없는 용혈성 빈혈과 피로감, 황달, 혈색소뇨 등을 호소한다. 이후 진행되면 골수 기능저하로 인한 빈혈의 악화와 다른 혈구 감소증을 일으키며, 복부나 뇌혈관에서 혈전증을 일으키는 것으로 알려져 있다[3]. 또한, 혈관 내 용혈로 인한 평활근 수축으로 인해 비특이적인 증상인 삼킴곤란과 복통, 발기장애 등이 발생하는 것으로 알려져 있고[4], 반복된 용혈 및 지속적인 혈색소뇨로 인해 철결핍빈혈이 유발되는 것으로 알려져 있다[5]. 저자들은 만성 복통 및 철결핍빈혈을 호소하는 젊은 성인 환자에서 혈뇨를 동반하지 않아 소화기 질환으로 오인하여 여러 검사를 시행하였으나 뚜렷한 원인을 찾지 못하던 중, 드문 원인인 발작성 야간혈색소뇨증을 진단하였기에 문헌고찰과 함께 보고하고자 한다.
증 례
환자: 25세 남자
주소: 반복되는 복통
현병력: 2년 전 시작된 반복적인 복통으로 경과 관찰 중, 2개월 전부터 지속되는 심한 복통이 있어 평가 및 치료를 위하여 외래 입원하였다.
과거력: 2년 전 상복부 통증과 빈혈로 위, 대장 내시경을 시행하였으며 얕은 위궤양 이외에 특이 소견은 없었다. 당시 혈액 검사에서 세망적혈구(reticulocyte) 상승 및 락트산탈수소효소(lactate dehydrogenase, LDH) 상승을 보여 쿰즈 검사(Coombs’ test)를 시행하였으나 음성이었다. 추가적으로 시행한 골수생검에서 저세포성 골수를 보이는 재생불량성 빈혈과는 달리, 정상 골수 소견에 적혈구 전구물질의 증가와 저장철 부족 소견으로 철결핍성 빈혈 의증으로 진단되어 철분제를 복용하며 추적 중이었다. 3년 전 고열을 동반한 장염으로 치료받은 과거력이 있었다.
사회력 및 가족력: 특이병력은 없었다.
신체 진찰 소견: 내원 당시 혈압 110/60 mmHg, 맥박 59회/분, 호흡수 20회/분, 체온 36.7℃였으며 피로감, 전신 쇠약감을 호소하였다. 복부진찰에서 장음은 정상이었고, 복부 압통 및 반발압통은 없었다. 장기비대 소견은 없었고 종괴는 촉지되지 않았다. 구강 궤양, 피부 자반은 없었다.
검사실 소견: 말초혈액 검사에서 백혈구 3,620/mm3와 혈색소 10.2 g/dL로 감소되어 있었고, 혈소판은 242,000/mm3로 정상범위였다. 혈액응고 검사는 정상범위였고, 생화학 검사에서는 LDH가 1,713 IU/L로 상승되어 있었고, 철(iron) 16 ug/dL (정상범위, 33-193 ug/dL)과 페리틴(ferritin)은 21 ng/mL (정상범위, 30-400 ng/mL)로 감소되어 있었으며, 그 밖에 총 빌리루빈 0.7 mg/dL, 직접 빌리루빈 0.18 mg/dL, 혈액요소질소(blood urea nitrogen) 12.3 mg/dL, 크레아티닌(creatinine) 0.70 mg/dL, 총철결합능(total iron binding capacity) 341 ug/dL (정상범위, 252-456 ug/dL), 평균 적혈구용적(mean corpuscular volume) 81.6 fL (정상범위, 80-94 fL), 평균 적혈구혈색소농도(mean corpuscular hemoglobin concentration) 32.2 g/dL (정상범위, 32-36 g/dL)로 모두 정상범위였다. 소변 검사에서 육안적 및 현미경적 혈뇨가 관찰되지 않았으며, 그 밖에 단백뇨, 농뇨, 소변 유로빌리노겐도 정상이었다. 혈청학적 검사에서 antineutrophil cytoplasmic antibody, anti-saccharomyces cerevisiae antibody 검사는 음성이었다.
영상 검사 소견: 염증성 장질환을 포함한 소화관 질환 진단 목적으로 시행한 복부 전산화단층촬영에서 특이 소견은 없었다. 위내시경에서는 경도의 홍반성 위염 이외에는 이상 소견이 없었으며, 소장캡슐내시경과 대장내시경에서는 말단부 공장에 림프여포성 비대(lymphofollicular hypertrophy) 이외에 특이 소견은 없었다.
치료 및 경과: 환자의 복통은 수액 및 보존적 치료로 호전되었다. 빈혈에 대한 원인을 평가하기 위해 시행한 혈액 검사에서 세망적혈구(reticulocyte) 상승 및 쿰즈 검사(Coombs’ test) 음성, 합토글로빈(haptoglobin) 감소 소견으로 용혈성 빈혈이 의심되었다. 복통과 용혈성 빈혈을 동반하는 질환인 발작성 야간혈색소뇨증이 의심되어, 감별을 위해 유세포분석 검사(flow cytometric analysis)를 시행하였고, 과립구(FLAER/CD24 deficiency 89.5%/89.5%)와 적혈구(CD59/CD55 deficiency 59.3%/45.0%)에서 발작성 야간혈색소뇨증 클론(clone)이 동정되어 발작성 야간혈색소뇨증으로 진단되었다(Fig. 1). 치료를 위하여 prednisolone 복용을 시작하였고, prednisolone 복용 1년 후부터 육안적 혈뇨 소견을 호소하였으며, 당시 외래에서 시행한 소변 검사에서는 육안적 및 현미경적 혈뇨는 관찰되지 않았다. 그 밖에 단백뇨, 농뇨도 동반되지 않았다. Prednisolone을 복용한 4년간 복통의 호전과 악화가 반복되었으며, 2014년 4월 및 2016년 10월에는 복통과 호흡곤란이 동반되어 혈전증 의심으로 복부 전산화단층촬영을 시행하였으나 특이 소견은 관찰되지 않았다. Prednisolone 복용 4년간 빈혈에 의한 피로감이 지속되고 복통의 호전 및 악화가 반복되며 혈뇨 지속적으로 호소하여 2017년 1월부터 혈관 내 용혈을 직접적으로 억제하는 에쿨리주맙(eculizumab)을 투여하며 경과 관찰 중이다(Table 1).
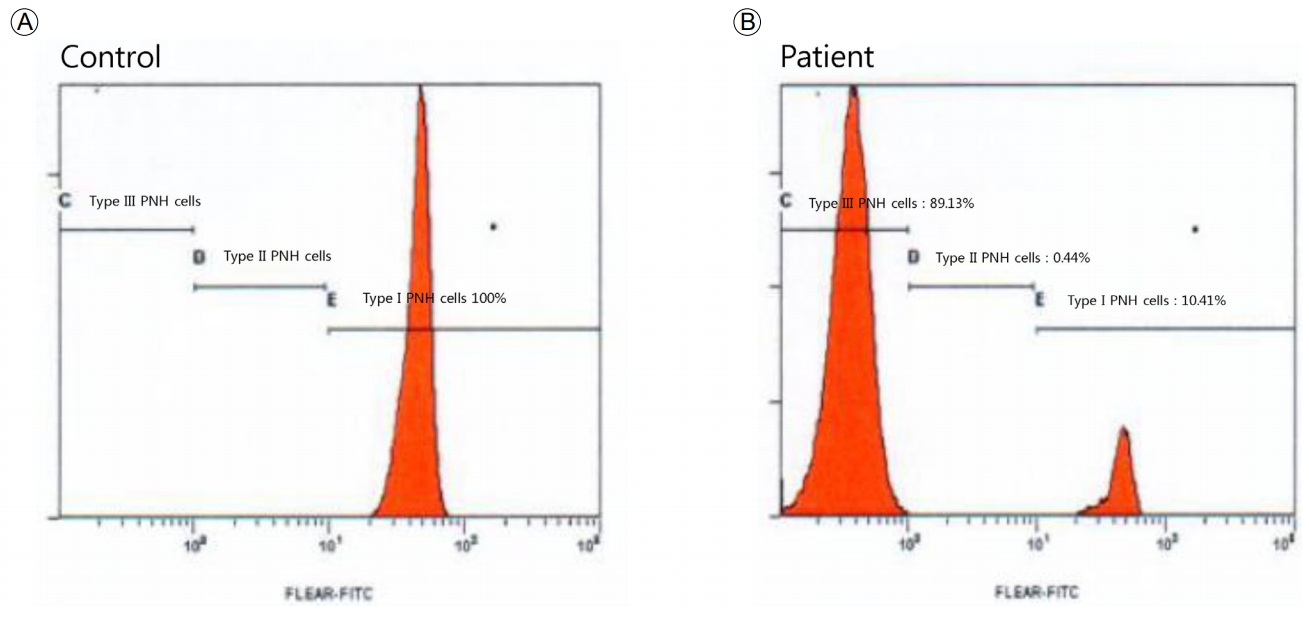
Flow cytometric analysis of granulocytes using FLAER. (A) In the control setting, there was no evidence of decreased (type II PNH cells) or absent (type III PNH cells) expression of FLAER. (B) In this patient, decreased (0.44%) and absent (89.13%) FLAER fractions were detected, suggesting that 89.5% of PNH granulocyte clones had a FLAER deficiency. FLAER, fluorescein-labeled proaerolysin; FITC, fluorescein isothiocyanate; PNH, paroxysmal nocturnal hemoglobinuria.
고 찰
만성 복통은 수개월 혹은 수년간 지속되는 복통으로 과민성대장증후군, 기능성 소화불량과 같은 기능성 장애에 해당하는 질환이 주요 원인으로 알려져 있다. 하지만 체중 감소, 전해질 불균형, 영양결핍 혹은 빈혈과 같은 증상이 동반되어 있다면 기질적 질환 동반 유무를 반드시 평가해 보아야 한다. 만성 복통이 빈혈과 함께 동반된 경우 염증성 장질환, 소화관종양 등의 질환을 우선 순위에 두고 환자를 평가하게 된다. 만성 복통 환자의 대부분은 병력 청취, 신체 검사, 혈액검사, 위장관 내시경 검사 및 영상의학적 검사를 통해 원인 감별이 가능하지만, 일부는 명확한 원인을 찾지 못하는 경우도 발생하고 있다. 원인이 명확하지 않은 젊은 환자들의 경우에는 대증적 치료를 유지하며 경과 관찰하는 것이 일반적이나, 50세 이상의 고령의 환자이거나 본 증례의 환자처럼 증상이 반복적으로 발생한다면 만성 복통을 유발할 수 있는 드문 원인들까지 포함하여 감별진단을 하여야 한다.
발작성 야간혈색소뇨증은 X 염색체에 존재하는 phosphadidylinositol glycan anchor biosynthesis (class A) gene의 돌연변이로 인하여 glycosylphosphatidylinostol (GPI)의 생성에 장애가 발생한다. 이는 적혈구 용혈을 방지하는 데 중요한 단백인 CD55, CD59가 적혈구 막에 결합하는 것을 방해하고, 이로 인해 보체 매개 용혈을 유발하게 된다. 임상 양상은 다양하게 나타나는데, 대부분의 환자들은 용혈성 빈혈과 관련한 증상인 피로, 황달, 혈뇨의 증상을 보이고 용혈에 의해 유리 혈색소가 혈장에 유리되어 혈전증을 유발하기도 한다. 혈전증은 다양한 원인에 의해 발생할 수 있으며 혈소판의 활성화, 유리 혈색소의 유독성, 일산화질소(nitric oxide, NO)의 고갈 등이 대표적인 것으로 알려져 있다. 혈전증은 발작성 야간혈색소뇨증과 관련한 사망 원인 중 가장 중요한 원인으로, 한국인을 대상으로 한 연구에서 그 발생률이 17.9%로 알려져 있으며[2], 보고자에 따라 40%까지도 발생할 수 있다고 알려져 있다[6]. 심부정맥 혈전증 및 폐색전증이 가장 흔한 발생 부위이나, 비전형적인 혈관의 동맥 및 정맥에서도 발생이 가능하다고 보고되고 있다. 비전형적인 혈관인 복강 내 혈관에 혈전이 생기는 경우, 갑작스러운 심한 복통이나 반복적인 복통이 발생할 수 있으며 혈전 발생 부위에 따라 다양한 증상이 발생할 수 있다[7]. 간정맥에 혈전이 발생하는 경우에는 버드-키아리 증후군으로 급·만성의 복통과 간부전, 사망에까지 이를 수 있고, 내장 혈관에 미세혈전이 발생할 경우에는 일과성 허혈로 인한 복통과 발열, 장폐색, 출혈 등의 증상이 나타날 수 있다. 장관의 허혈성 변화는 영상학적 검사에서 장벽의 부종이 관찰될 수 있으며, 내시경 검사에서는 장점막의 부종과 발적, 미란, 궤양이 관찰될 수 있다. 미세혈전의 경우, 보존적 치료를 시행할 수 있으나 혈전이 영상학적으로 진단된다면 항응고요법 및 혈전용해요법을 사용할 수 있고 장경색이 발생하는 경우, 수술적 절제술이 필요할 수 있다. 더불어 인간화 단일클론항체인 에쿨리주맙(eculizumab)이 혈전의 예방 및 치료에 효과적으로 알려져 있다[8]. 그 밖에 혈장 내 존재하는 유리 혈색소는 NO의 고갈을 발생시키게 되고, 이러한 NO의 고갈은 내장근의 긴장도를 높여 복통이나 삼킴곤란, 발기부전 등의 내장근의 이상 증상을 유발하여 반복적인 복통의 원인이 되기도 한다[4]. 발작성 야간혈색소뇨증의 진단에 과거에 많이 사용되었던 산성화 혈청용해시험(Ham’s test)이나 자당용해시험(sucrose hemolysis test)은 낮은 민감도와 정량분석의 제한으로 요즘은 거의 사용하지 않고 있으며, 현재는 확진을 위해서 유세포분석기를 이용하여 GPI anchor protein 결핍세포를 측정하고 있다. 유세포분석기를 이용한 진단 시 민감도와 특이도를 높이고 최근 용혈이나 수혈로 인한 위음성의 결과가 나오는 것을 방지하기 위하여 2개 이상 계열의 세포(예, red blood cell and white blood cell)에서 2개 이상의 단일클론항체(예, CD59 and CD55)를 사용하기를 권유하고 있다[3]. 진단은 3가지 범주로 분류할 수 있으며, 첫 번째로 기저에 다른 골수 질환이 없는 가운데 혈관 내 용혈이 동반된 경우로 유세포 분석기에서 40-99%가량의 발작성 야간혈색소뇨증 과립구(PNH granulocyte)를 포함하는 전통적 발작성 야간혈색소뇨증(classic PNH), 두 번째는 기저에 재생불량성 빈혈 혹은 골수형성이상 질환(myelodysplastic syndrome)같은 골수 질환이 있고, 혈관 내 용혈이 동반된 발작성 야간혈색소뇨증, 마지막으로 임상 증상 및 혈액학적 이상은 없으나 소수의 PNH 세포가 동반된 무증상 발작성 야간혈색소뇨증(subclinical PNH)으로 나눌 수 있다[4].
본 증례에서는 발작성 야간혈색소뇨증에서 동반되는 증상인 용혈성 빈혈과 만성 복통을 보였고, 철결핍빈혈이 동반되어 있었다. 용혈성 빈혈은 발작성 야간혈색소뇨증의 대표적인 임상 양상으로, 빈혈로 인한 피로의 증상은 80% 정도의 환자에서 발생한다고 보고하고 있고, 호흡곤란, 혈색소뇨 역시 각각 64%, 62%에서 발생한다고 보고하고 있다[4]. 철결핍빈혈은 반복된 용혈 및 지속적인 혈색소뇨로 인해 저장 철의 감소 및 고갈을 초래하여 유발되는 것으로 알려져 있다[5]. 복통은 10-46% 정도의 발작성 야간혈색소뇨증 환자에서 호소한다고 알려져 있으며, 본 증례의 만성 복통의 원인 역시 복강 내 미세 혈전에 의한 장허혈 및 혈장 내 NO의 고갈로 상승된 내장근의 긴장으로 인한 증상으로 보인다[2,4,7]. 내장근의 긴장도 상승으로 인해 여러 증상이 발생 가능하고 가장 흔한 증상은 식도의 연축으로 인한 삼킴곤란 혹은 흉통이며, 짧은 기간 동안의 쥐어짜는 듯한 복통을 일으키기도 한다고 보고하고 있다[4]. 하지만 본 증례처럼 문진 및 검사실 소견에서 혈뇨나 혈색소뇨 소견이 관찰되지 않는 경우에는 염증성 장질환, 특히 소장 크론병으로 인한 만성 복통과 철결핍성 빈혈로 판단할 수 있고 용혈성 빈혈은 염증성 장질환의 장외증상으로 드물게 0.2-1.7%까지 발생할 수 있어[9], 진단에 어려움이 발생할 수 있다.
발작성 야간혈색소뇨증의 치료는 과거 수혈과 스테로이드, 항응고제 등의 약물 치료로 이루어졌으나 효과적이지 못하였으며 현재는 전통적 발작성 야간혈색소뇨증(classic PNH) 환자에서 동종조혈모세포이식과 C5 보체에 부착하여 막공격 복합체(membrane attack complex) 형성에 필요한 C5a와 C5b로 분할되는 과정을 직접적으로 억제하는 인간화 단일클론 항체(humanized monoclonal antibody) 에쿨리주맙(eculizumab)이 사용되고 있다. 2007년 미국식품의약국 승인 후 치료제로 사용되고 있는 에쿨리주맙(eculizumab)은 빈혈로 인한 증상이 심하거나 수혈 의존적인 경우에 혈전증, 복통 등 다양한 증상에서 사용할 수 있으며, 그 효과 및 안정성이 여러 연구에서 입증되고 있다[10]. 본 증례에서도 에쿨리주맙(eculizumab) 사용 후 복통 및 혈색소뇨의 호전이 보였으며, LDH의 정상화 및 혈색소 상승 등의 혈액학적 호전 소견이 관찰되었다.
저자들은 혈뇨를 동반하지 않아 소화기 질환으로 오인된 만성 복통과 철결핍빈혈을 보인 발작성 야간혈색소뇨증 환자의 증례를 보고하며, 표준 검사에도 불구하고 원인을 알 수 없는 만성적인 복통과 빈혈이 함께 동반되었을 경우에 감별 진단의 하나로 드문 질환인 발작성 야간혈색소뇨증을 고려해 볼 수 있을 것으로 생각한다.
Acknowledgements
본 연구는 2020년 양산부산대학교병원 임상연구비 지원으로 이루어졌습니다.
