액상 전자담배와 폐질환
Pulmonary Disease Related to E-Cigarettes
Article information
Trans Abstract
The potential role of E-cigarettes in smoking cessation is debatable, and whether they are harmful remains controversial worldwide. However, several cases of E-cigarette or vaping-associated lung injury (EVALI) have been reported in the United States. In this review, we discuss and summarize EVALI cases.
서 론
전자담배는 2000년부터 전 세계적으로 사용이 점차 증가되어 왔다[1-4]. 국내에서는 전체 성인 흡연자의 약 7%가 전자담배를 사용하고 있는 것으로 보고되었고, 남성이 11%, 여성이 2%로 확인되었다. 특히 18세 미만의 청소년에서는 흡연자의 약 10%가 전자담배 경험이 있었고, 남성 15%, 여성 3%로 성인보다 높았다[5,6]. 2013년-2016년 국민건강영양조사 결과에 따르면 전자담배 사용 경험이 있는 인구는 일반 인구의 약 28% 이상이었고, 특히 40세 미만에서 43% 이상의 사용 경험을 보이는 것으로 확인되었다[4].
전자담배가 금연에 도움이 될 뿐 아니라, 궐련 담배에 비해 유해한 독성 물질의 흡입이 적다는 점을 근거로, 전자담배가 더 유용하다는 의견이 있어 전 세계적으로 큰 관심을 받아왔다. 하지만 아직 장기적 안전성이 확보되지 않았고, 니코틴 사용량이 오히려 증가되어 의존성이 증대될 수 있다는 주장도 있어, 액상형 전자담배의 유해성과 안전성 관련 논란은 지금까지 지속되고 있다. 이런 가운데 2019년 8월부터 미국을 중심으로 액상형 전자담배로 인한 폐질환(E-cigarette or vaping associated lung injury, EVALI) 보고 사례들이 급증하였다[7]. 이에 미국질병관리본부(Centers for Disease Control and Prevention, CDC)는 액상형 전자담배 사용 자제를 권고하였고, 국내에서도 2019년 10월 23일부터 보건복지부는 액상형 전자담배 사용 중단을 강력하게 권고하였다[8]. 본고에서는 전 세계적으로 큰 이슈가 되고 있는 EVALI 관련 내용들을 정리해 보고자 한다.
본 론
EVALI 국내·외 역학적 특성
2019년 12월까지 미국에서 EVALI로 추정 혹은 확정된 환자는 총 2,560여 명으로 확인되었으며, 55명이 사망하였다[8]. 모든 환자가 미국 본토 전역 내지 주변에서 발생하였고, 특정 지역이 아닌 50개의 주 전체에서 발생하였으며, 푸에르토리코(Puerto Rico), 버진 아일랜드(Virgin Island), 콜롬비아에서도 발생한 것으로 확인되었다[8]. 스페인에서 EVALI 환자 1명을 보고한 바 있는데, 이 환자는 미국인으로 일리노이 주거주자이나 스페인 여행 중 발생한 호흡기 증상으로 내원하여 진단되었다[9]. 국내에는 2019년 10월에 의심 환자가 신고되었으나, EVALI로 확진되어 사망한 환자는 현재까지 없는 것으로 보고되고 있다.
미국에서 전자담배 사용과 연관된 문제로 응급실에 방문한 환자를 2017년부터 조사한 결과, 2017년 이후 점차 증가하는 추세로 이어지다, 2019년 6월부터 급격하게 증가하였다. 이러한 경향성은 2019년 9월에 최고점에 이른 후 점차 감소하는 추세이나, 2019년 6월 이전의 응급실 방문율 미만까지 감소하지는 못하고 있다[7]. 2019년 12월 3일까지의 EVALI 환자들의 분포를 분석하였을 때 환자의 대부분은 남성(67%)이었고, 특히 35세 미만이 78%로 대부분을 차지하였으며, 평균 연령은 24세, 18세 미만이 16%를 차지하였다(Fig. 1) [8].
EVALI 정의 및 진단
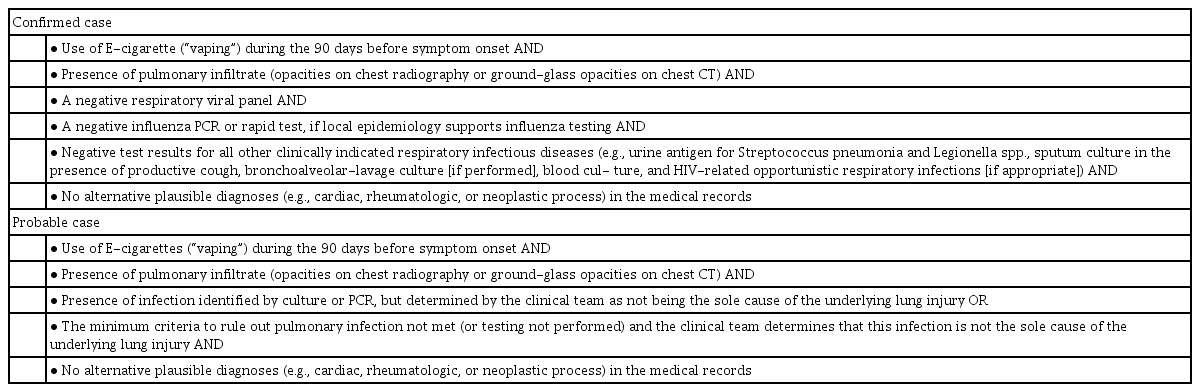
현재까지 EVALI를 명확하게 진단하기 위한 검사나 바이오마커(biomarker)는 없기 때문에, 임상가의 판단 및 다른 질환의 배제를 통해 진단된다. 미국 일리노이 주에서 발생한 25건과 위스콘신 주에서 발생한 28건을 포함, 최소 25개 이상의 주에서 보고된 사례들을 종합하여 미국 CDC에서 예비조사를 위한 EVALI 사례 정의를 정립하였다[10]. 현재 국내에서도 질병관리본부에서 이 기준을 준용하고 있다. EVALI 확진자(confirmed) 사례의 정의는 다음의 조건을 모두 충족하는 자로 질병관리본부에 발생 보고를 해야 한다. 환자는 주요 증상인 기침, 호흡곤란, 가슴통증 등의 호흡기 증상을 포함하여 전신 증상인 발열, 피로감, 체중 감소 또는 소화기계 증상인 오심, 구토, 설사의 증상이 발생하기 90일 이전에 액상형 전자담배를 사용한 경험이 있어야 한다. 동시에 흉부 X선 또는 흉부 전산화단층촬영(chest computed tomography)에서 이상 소견이 있으며, 폐감염이 배제되어야 하는데 최소한 호흡기 바이러스, 인플루엔자, 폐렴구균, 레지오넬라, 마이코플라스마 등의 초기 검사에 모두 음성을 보여야 한다. 또한 종양, 심장 질환, 류마티스 질환의 병력이 없어야 한다. EVALI로 추정되는(probable) 사례는 확진 사례와 다른 조건은 모두 동일하나, 초기 배양 및 PCR 검사 등에서 폐감염이 배제되지 않지만, 감염이 폐질환의 단독 원인이 아니라고 판단되는 경우이다(Table 1).
발생 원인
EVALI 사례가 점차 증가함에 따라, 미국 CDC에서는 원인 물질을 규명하기 위한 분석을 시작하였다. 2019년 8월부터 10월까지 수집한 정보를 통해 약 86%의 환자가 증상이 발생하기 3개월 전에 tetrahydrocarnnabinol (THC)이 포함된 제품을 사용한 것으로 확인되었다[11]. 이에 따라 미국 CDC와 Food and Drug Administration (FDA)은 THC가 포함된 액상 제품들을 분석하였고, 그 결과 vitamin E acetate나 중간사슬지방(medium chain triglycerides)과 같은 희석제, 금속 등을 포함한 여러 유해물질들이 검출되었다[11]. 원인 물질을 파악하기 위하여 EVALI 환자 총 29명의 bronchoalveolar-lavage (BAL) fluids 내에서 이러한 유해물질의 양을 분석하였고, 29명 전체 환자의 BAL fluids 내에서 vitamin E acetate가 검출되었다[12]. 뿐만 아니라 82%의 환자에서 THC 또는 THC 대사체가 확인되었고, 62% 환자에서 니코틴 대사체가 확인되었다[12]. 이러한 결과를 바탕으로 원인 물질을 확정하기 위하여 총 51명의 EVALI 환자들의 BAL fluids 내의 유해물질을 추가로 분석하였고, 총 99명의 정상인의 BAL fluids와 비교하였다[13]. 51명 중 총 48명의 환자(94%)에서 vitamin E acetate가 검출되었고, 47명 중 40명(85%)에서 THC 또는 THC 대사체가 BAL fluids에서 확인되었다[13]. Vitamin E acetate 이외에는 1명의 환자에서 니코틴 염(nicotine salts) 1명, 다른 1명의 환자에서 코코넛 오일(coconut oil)과 리모넨(limonene)이 EVALI 원인으로 판단되었다[9,13].
Vitamin E acetate는 영양제나 화장품에도 흔하게 사용되는 물질로, 경구로 섭취하거나 피부에 도포하는 경우에는 해롭지 않다고 잘 알려져 있다. 그러나 vitamin E acetate를 흡입하는 경우, 폐손상을 유발할 수도 있다[11,14,15]. 반면, 일부 연구에서는 vitamin E가 경구 섭취나 네뷸라이져를 흡입하였을 때 항산화 역할을 하여 미세먼지 또는 흡연으로 인한 폐손상을 줄여준다고 보고하고 있다[16,17]. 현재까지 EVALI 환자에서 vitamin E의 폐손상 기전은 다음과 같이 추정되고 있다. 1) 상당량의 vitamin E acetate (tocopherols)가 흡입되면 폐 계면활성제(lung surfactant)를 쉽게 통과하여 계면활성제를 젤(gel) 형태에서 액체(liquid)로 변화시키고 이는 계면활성제의 장력(tension)을 변화시켜 기능과 역할을 소실하게 하여 결국 호흡부전에 이르게 할 수 있다는 가설이다. 2) 가열된 vitamin E acetate는 ketene이라는 물질을 생산할 수 있는데, 이 물질이 반응성 화합물(reactive compound)로 농도에 따라 폐 자극 물질(lung irritant)이 될 수 있다는 가설이다[13].
임상 양상 및 경과
EVALI 환자들의 사례를 분석한 보고에 따르면 환자들이 가장 많이 호소하는 증상은 호흡곤란 및 기침의 호흡기 증상이며, 흉통을 호소하기도 한다. 환자들은 발열, 오한, 체중 감소, 피로감 등의 증상을 동반하는 경우가 흔하고 오심, 구토, 설사나 복통 등의 소화기 증상을 호소하기도 한다[10]. 환자들은 심박동수 100회 이상의 빈맥(tachycardia)을 보인 환자가 가장 많았고, 약 70%의 환자들이 산소포화도가 95% 미만으로 감소한 저산소증(hypoxia) 소견을 보였다. 빈호흡(tachypnea) 증상 또는 38℃ 이상의 발열을 보이는 환자도 30-40%에 해당하였다. 전체 90% 이상의 환자가 입원 치료를 받았고, 평균 입원기간은 6일 내외로 확인되었다[10]. 대부분의 환자(87%)가 최소 산소 치료를 받았으며, 50% 이상의 환자가 중환자실에서 치료를 받았고, 약 30% 이상의 환자가 인공호흡기 치료 및 기도 삽관을 받은 것으로 보고되었다[10]. 과거 동반 질환으로 가장 많은 비율을 차지한 것은 기분장애 또는 불안장애였고, 천식이 약 30%로 높은 비율을 보였다[10]. 환자들이 사용한 전자담배기기, 전자담배 사용 빈도, 사용한 액상 제품이 다양하며, 기저 건강상태가 다 다르기 때문에 경증 또는 중증의 임상 양상 내지 사망까지 다양한 임상 양상을 보인 것으로 추측되고 있다.
임상 검사 결과 및 병리 소견
EVALI 환자들의 혈액 검사 결과는 대부분 호중구성(neutrophil dominant) 염증세포 증가 소견을 보이며 erythrocyte sedimentation rate (ESR)가 상승되어 있다[10]. 약 50% 미만에서 간기능 검사(AST, ALT) 수치가 상승하며, 크레아티닌(creatinine)의 상승은 흔하지 않았다[10]. 영상학적 소견은 폐 하부 중심의 경화(basilar-predominant consolidation) 및 간유리(ground-grass opacity) 음영이었다[1,18,19]. 이러한 미만성 음영은 주로 폐의 중심부 부분에만 발생하였고, 가장자리 부위에는 발생하지 않았다(subpleural sparing) (Fig. 2) [19]. 영상학적 소견은 과민성 폐장염(hypersensitivity pneumonitis, HP), 미만성 폐포 출혈(diffuse alveolar hemorrhage, DAH), 급성 호산구 폐렴(acute eosinophilic pneumonia, AEP), 미만성 폐손상(diffuse alveolar damage), 기질화 폐렴(organizing pneumonia, OP), 지질성 폐렴(lipoid pneumonia), 거대세포 간질성 폐렴(giant cell interstitial pneumonia, GIP) 등 매우 다양한 형태로 보고된다[18]. 이러한 다양한 패턴은 폐손상의 기전이 환자마다 다양함을 의미하는데, 폐 상피세포와 폐 기질의 염증성 손상을 유발하는 공통의 기전 내에서 발생할 수 있는 다양한 급성 폐손상의 패턴을 모두 보여주는 것으로 판단된다[1].
일부 환자에서는 폐조직 병리 소견이 보고되었다[20,21]. 모든 조직 검사 결과에서 감염 질환은 배제되었으며, 급성 폐손상(acute lung injury patterns) 패턴을 보였다. 이러한 폐손상은 가열된 증기(heated vapor)로 인한 일종의 화상, 풍부한 오일 첨가물(oil-rich additives)로 인한 지방 축적(lipid accumulation), 증기 내 다양한 화합물에 대한 알레르기 반응, 과민반응 또는 독성 손상의 기전으로 발생하는 것으로 추측된다[22]. 가장 흔한 조직학적 소견은 fibroblast plugs, hyaline membranes, fibrinous exudates, type 2 pneumocyte hyperplasia, interstitial organization이었다[20,21,23]. 모든 환자의 air-space에서 포말성 대식세포(foamy macrophages)가 존재하였고, 폐포세포 액포화(pneumocyte vacuolization)가 관찰되었다. 조직은 대부분 호중구(neutrophils)가 우세(neutrophil dominant)하였으며 호산구(eosinophils)가 증가되어 있거나 육아종(granulomas)이 관찰되는 경우는 거의 없었다[21]. 대부분 조직에서 지질함유 대식세포(lipid-laden macrophage)가 관찰되지만, 이는 다른 감염성 질환이나 흡인, 약물 반응, 자가면역 질환과 관련하여 보일 수 있는 소견으로 EVALI에 특징적인 소견은 아니기 때문에 환자의 BAL fluids나 조직에서 지질 염색(lipid stains)을 시행하는 것을 최근에는 추천하지 않고 있다[20].
치료
EVALI 환자의 치료에 있어 가장 효과적인 치료는 전신스테로이드이다. 전신스테로이드 투약으로 환자들은 급격한 산소 요구량의 감소와 염증 지표 감소 소견을 보였다[1,10]. 전신스테로이드 투약 지침이나 가이드라인은 현재까지 명확히 제시되지 않고 있으나, 경험적으로 메틸프레드니솔론(methylprednisolone)을 기준으로 40 mg 8시간 간격으로 투약을 시작하고, 환자 임상 증상이 호전되면 서서히 감량하여 2-3주까지 유지하는 것으로 하고 있다[1]. 대부분의 환자가 빠르면 5일 이내 임상 증상의 호전을 보이는 것으로 보고되었다[1]. 외래진료에서 전신스테로이드를 투약하는 것은 아직까지 정립된 양식이 부족하며, 다른 감염 질환을 악화시킬 수 있어 주의가 필요하다[24]. EVALI 환자의 치료에 있어 금연, 인플루엔자 백신 접종 관련 교육도 필수적이다[24].
결 론
전자담배의 유효성과 안전성의 논란이 끝나지 않은 상황에서 미국을 중심으로 빠르게 확산된 EVALI 환자들은 대부분 액상형 전자담배를 통해 THC를 흡입한 것으로 확인되었고, 제품에 첨가된 vitamin E acetate가 가장 유력한 원인물질로 지목되고 있다. 대부분의 EVALI 환자들의 생체시료에서 vitamin E acetate가 검출된 것은 사실이지만, 이 vitamin E acetate가 폐손상의 직접적인 원인인지 기전이 명확하지 않다. 또한, EVALI의 발생 원인을 한 가지 물질로 단정짓기 어려울 수 있다. THC가 포함된 제품들은 비공식적인 경로로 판매되고 다양한 상품이 존재하기 때문에 아직 확인되지 못한 성분들도 존재할 수 있다. 뿐만 아니라 EVALI로 진행한 환자들의 위험인자와 고위험군에 대한 정보도 필요하다.
국내에서는 아직 EVALI로 확진되고 사망한 환자는 보고되지 않았으나, 앞으로 발생할 가능성에 대하여 충분히 이해하고 대처해야 할 것이다. 국내 액상형 전자담배 액상 물질 성분 분석 결과, 일부 제품에서 vitamin E acetate가 검출되었으며, 액상형 전자담배는 대부분 가향물질을 첨가하기 때문에 향후 폐질환 발생의 위험이 있다[8,25]. 또한 전자담배는 폐 상피세포의 손상을 유발하고, 이를 통한 호흡기 감염의 위험성이 증가될 수 있어 예방 및 주의가 필요하다[26,27]. 이러한 위험성과 관련된 연구뿐 아니라, 액상형 전자담배의 사용과 관련한 결론이 아직 내려지지 않은 상태로, 앞으로의 액상형 전자담배와 관련된 정책과 규정에 관련된 연구는 지속되어야 할 것이다.
국내 현황 요약
국내 보건복지부와 질병관리본부는 2019년 9월 20일부터 액상형 전자담배 사용 자제 권고를 시행하였고, 2019년 10월 23일부터 액상형 전자담배 사용 중단을 강력하게 권고하였다. 국내 의심사례는 2019년 11월 1일까지 총 2건이었다.
보고 사례는 모두 남성, 호흡기계 증상(기침, 호흡곤란)과 전신 증상(발열, 체중 감소, 식욕저하)을 보였고, 감염성 질환은 모두 배제되었다. 환자들은 모두 발병 2-4개월 전부터 국내 시판 액상형 전자담배를 사용하였으며, 호흡기 및 영상의학 전문가의 검토 후 1건만이 의심 사례에 부합하는 것으로 확인되었다.
식품의약품안전처는 2019년 10월 23일 국내 유통되는 153개 액상형 전자담배의 액상을 대상으로 THC, vitamin E acetate, 가향물질 3종(디아세틸, 아세토인, 2,3-펜탄디온) 등 총 7개 성분에 대한 분석을 시행하였다. THC는 모든 제품에서 검출되지 않았으나, 일부 제품에서 vitamin E acetate 성분과 폐질환을 유발할 수 있다고 알려진 가향물질이 검출되었다. 검출된 vitamin E acetate는 국내 제품의 경우 검출은 되었으나 0.1-8.4 ppm범위로 검출되어, 미국에서 검출된 농도인 23만-88만 ppm에 비해 현저하게 낮은 양이었다. 미국의 경우, THC를 희석하는 용도로 vitamin E acetate를 많이 사용하였기 때문에, 높은 양으로 검출된 것으로 추정하고 있다. 국내의 경우 THC 즉, 대마 사용은 금지되어 있다. 가향성분 3종에서는 흡입 시 폐질환의 가능성이 있는 디아세틸, 아세토인이 각각 29개, 30개 제품에서 검출된 것으로 보고하였다.
국내에서는 현재 폐손상의 원인물질이 확정되지 않았고, 추가 인체 유해성 연구가 진행 중인 점, 미국의 조치사항 등을 종합적으로 고려하여 현재의 액상형 전자담배 사용 중단 강력 권고 조치를 인체 유해성 연구가 발표되기 전까지 유지하기로 결정한 상태이다(2020년 상반기 예정). 또한 정부는 담배의 정의 확대법안, 담배 성분 제출 의무화 법안, 가향 물질 첨가 금지 법안 등 담배 안전관리 강화를 위한 핵심 법안의 의결을 위해 노력 중이다.