 |
 |
| Korean J Med > Volume 94(5); 2019 > Article |
|
Abstract
The major guidelines for lipid-lowering therapy (LLT) have been revised recently. Although ‚Äúhigher cardiovascular risk-aggressive LLT with greater absolute clinical benefit‚ÄĚ is the main idea underlying all guidelines, there are some differences in the details among them. The US guidelines recommend pharmacological LLT based on a patient‚Äôs risk category, independently of their low-density lipoprotein-cholesterol (LDL-C) level. However, the European and Korean guidelines consider the patient‚Äôs risk category and LDL-C at the same time. Lifestyle modifications are suggested in parallel in all guidelines. The newest US guidelines have characteristically revived target LDL-C values in some patient groups and indications for non-statin drugs (ezetimibe and PCSK9 inhibitors), whereas the European and Korean guidelines have maintained target LDL-C values as usual. It is universally accepted that statins are the first-line agent. Adding ezetimibe, bile acid sequestrants, or PCSK9 inhibitors is recommended as a second line treatment. Appreciating the trend and background of the newest LLT guidelines will be essential to maximize cardiovascular prevention in patients.
ž≤īÍ≥Ąž†ĀžĚł Í≥†žßÄŪėąž¶Ě žĻėŽ£Ć žßÄžĻ®(žßÄžßąÍįēŪēė žĻėŽ£Ć žßÄžĻ®)žĚÄ 30ŽÖĄ ŽāīžôłžĚė žó≠žā¨ÍįÄ žěąŽäĒŽćį, 2000ŽÖĄŽĆÄ žĚīŪõĄžĚė žěĄžÉĀžčúŪóė žěźŽ£ĆŽ•ľ ŽįėžėĀŪēėžó¨ 2010ŽÖĄ žĚīŪõĄžóź žĄłÍ≥Ą ÍįĀžßĞ󟞥ú žßÄžĻ®žĚī Íįúž†ēŽźėžóąŽč§. ŪäĻŪěą ŽĮłÍĶ≠žóźžĄúŽäĒ 2013ŽÖĄÍ≥ľ 2018ŽÖĄžóź žßÄžĻ®žĚė žÉąŽ°úžöī ŪĆźžĚī ŽįúŪĎúŽźėžóąŽäĒŽćį, ŪÉÄ ÍĶ≠ÍįÄžĚė žßÄžĻ®žĚīŽāė ŽĮłÍĶ≠žĚė žĚīž†Ą žßÄžĻ®Í≥ľŽŹĄ ŽßéžĚī Žč¨ŽĚľž†łžĄú žßÄžĻ®žĚĄ Ž≥īŽäĒ ŽŹÖžěźŽď§žĚī ž°įÍłą ŪėľŽěĞ䧎ü¨žöł žąėŽŹĄ žěąŽč§. ÍĶ≠ŽāīžóźžĄúŽäĒ ŪēúÍĶ≠žßÄžßąŽŹôŽß•Í≤ĹŪôĒŪēôŪöƞ󟞥ú 2018ŽÖĄžóź žßÄžĻ®žĚė žĶúžč†ŪĆźžĚĄ ŽįúŪĎúŪēėžėÄŽč§. ŪēúÍĶ≠ žßÄžĻ®žĚī ÍĶ≠Žāīžôł žó¨Žü¨ ž°įÍĪīžĚĄ ŽįėžėĀŪēú Í≤ÉžĚīÍłįŽäĒ ŪēėŽāė, žôłÍĶ≠žĚė ŽĆÄŪĎúž†ĀžĚł žĶúžč† žßÄžĻ®žĚĄ žēĄŽäĒ Í≤ÉŽŹĄ ž§ĎžöĒŪēėÍłį ŽēĆŽ¨łžóź Ž≥łÍ≥†žóźžĄúŽäĒ ŽĮłÍĶ≠, žú†ŽüĹ, ŪēúÍĶ≠žĚė žĄł ÍįÄžßÄ žßÄžĻ®žĚĄ ŪēĶžč¨žā¨Ūē≠ žúĄž£ľŽ°ú ŽĻĄÍĶźŪēėŽ©į Íłįžą†ŪēėŽ†§Í≥† ŪēúŽč§.
ÍĶ≠ž†úž†ĀžúľŽ°ú ŽĆÄŪĎúž†ĀžĚł Í≥†žßÄŪėąž¶Ě žĻėŽ£Ć žßÄžĻ®žĚÄ ŽĮłÍĶ≠žč¨žě•ŪēôŪöĆ(American College of Cardiology/American Heart Association) žßÄžĻ®Í≥ľ žú†ŽüŞ訞ě•ŪēôŪöĆ/ŽŹôŽß•Í≤ĹŪôĒŪēôŪöĆ(European Society of Cardiology/European Atherosclerosis Society) žßÄžĻ®žĚīŽč§. ŽĮłÍĶ≠ žßÄžĻ®žĚÄ 2018ŽÖĄžóź Íįúž†ēŽźėžóąÍ≥†[1], žú†ŽüĹžĚÄ 2016ŽÖĄ žßÄžĻ®žĚī ž†úžĚľ žĶúÍ∑ľ žßÄžĻ®žĚīŽč§[2]. žöįŽ¶¨ŽāėŽĚľžóźžĄúŽäĒ ŪēúÍĶ≠žßÄžßąŽŹôŽß•Í≤ĹŪôĒŪēôŪöĆ žĻėŽ£Ć žßÄžĻ®žĚī 2018ŽÖĄžóź Íįúž†ēŽźėžóąŽč§[3].
ŽĮłÍĶ≠ žßÄžĻ®žĚÄ ž†ÄŽįÄŽŹĄ žßĎ讎įĪ žĹúŽ†ąžä§ŪÖĆŽ°§(low-density lipoprotein-cholesterol, LDL-C) žąėžĻėžôÄ ÍīÄÍ≥ĄžóÜžĚī žč¨ŪėąÍīÄ žúĄŪóėŽŹĄžóź ŽĒįŽĚľ ž†ēŪēīžßÄŽäĒ Ūôėžěź Í∑łŽ£Ļžóź ŽĒįŽĚľ žēĹŽ¨ľ žĻėŽ£Ć žčúžěϞ̥ Í≤įž†ēŪēėŽäĒ Í≤ÉžĚī 2013ŽÖĄŪĆź žĚīŪõĄ ž†úžĚľ ŪĀį ŪäĻžßēžĚīŽĚľ Ūē† žąė žěąŽč§. žú†ŽüĹžßÄžĻ®žĚÄ Í≥ĄžāįŽźú žč¨ŪėąÍīÄ žúĄŪóėŽŹĄžôÄ LDL-C ŽĎź ÍįÄžßÄŽ•ľ ÍįÄžßÄÍ≥† žēĹŽ¨ľ žĻėŽ£Ć žčúžěϞ̥ Í≤įž†ēŪēėŽäĒ Í≤ÉžĚī ŽĮłÍĶ≠ žßÄžĻ®Í≥ľžĚė žį®žĚīžĚīŽč§. ŪēúÍĶ≠ žßÄžĻ®žĚÄ 2004ŽÖĄžóź ŽįúÍįĄŽźú ŽĮłÍĶ≠žĚė National Cholesterol Education Program Adult Treatment Panel III Íįúž†ēŪĆźžĚĄ ž†ĀÍ∑Ļ žįłÍ≥†Ūēėžó¨ Í≥†žēąŪēėžėÄžúľŽāė[4], žßÄÍłąžĚė ŽĮłÍĶ≠ žßÄžĻ® Ž™®žĖϞɹžôÄŽäĒ Íŧ Žč§Ž•īŽč§. žč¨ŪėąÍīÄ žúĄŪóėŽŹĄŽ•ľ žúĄŪóėžĚłžěźžĚė žĘÖŽ•ėžôÄ ÍįúžąėŽ°ú ŪĆźŽč®ŪēėÍ≥†, LDL-CŽ•ľ Í≥†Ž†§Ūēėžó¨ žēĹŽ¨ľ žĻėŽ£ĆŽ•ľ Í≤įž†ēŪēėŽäĒŽćį, ŪÉÄ žßÄžĻ®žóź ŽĻĄŪēėžó¨ Žćú Ž≥Ķžě°ŪēėŽč§(Table 1). Ž¨ľŽ°† žĖīŽäź ŽāėŽĚľ žßÄžĻ®žĚīŽĚľ ŪēėŽćĒŽĚľŽŹĄ žĶúÍ∑ľ 20žó¨ ŽÖĄÍįĄ žßÄžßąÍįēŪēė žĻėŽ£Ćžóź ŽĆÄŪēú žó¨Žü¨ ŽĆÄÍ∑úŽ™® žěĄžÉĀžĚĄ ÍłįžīąŽ°ú ŪēėžėÄÍłį ŽēĆŽ¨łžóź, ‚Äúžč¨ŪėąÍīÄ žúĄŪóėŽŹĄÍįÄ ŽÜížĚĄžąėŽ°Ě, žĻėŽ£Ćžóź ŽĒįŽ•ł ž†ąŽĆÄ žĚīŽďĚžĚī ŪĀ¨ŽĮÄŽ°ú ÍįēŪēú žßÄžßąÍįēŪēė žĻėŽ£ĆÍįÄ ŪēĄžöĒŪēėŽč§‚ÄĚŽĚľŽäĒ ŽľąŽĆÄŽäĒ Í≥ĶŪÜĶž†ĀžĚīŽ©į(Fig. 1), žĄłŽ∂Äžā¨Ūē≠žĚī žēĹÍįĄ Žč§Ž•īŽč§Í≥† žĚīŪēīŪē† žąė žěąŽč§.
žúĄžóźžĄú žĖłÍłČŪēėžėÄŽďĮžĚī žßÄžßąÍįēŪēė žĻėŽ£Ć žó¨Ž∂ÄžôÄ žēĹŽ¨ľ žĻėŽ£Ć žó¨Ž∂ÄŽ•ľ Í≤įž†ēŪē† ŽēĆ ž≤ę Žč®Í≥ĄŽäĒ žč¨ŪėąÍīÄ žúĄŪóėŽŹĄŽ•ľ ŪŹČÍįÄŪēėŽäĒ Í≤ÉžĚīŽč§. žč¨ŪėąÍīÄ žúĄŪóėŽŹĄÍįÄ ŽÜížúľŽ©ī ÍįēŪēú žĻėŽ£Ć, ž§ĎÍįĄžĚīŽ©ī ž§ĎÍįĄ ž†ēŽŹĄžĚė žĻėŽ£ĆÍįÄ ŪēĄžöĒŪēėÍ≥†, žúĄŪóėŽŹĄÍįÄ ŽāģžúľŽ©ī žēĹŽ¨ľ žĻėŽ£ĆÍįÄ Ž∂ąŪēĄžöĒŪē† ŽēĆÍįÄ ŽßéŽč§. ŽĮłÍĶ≠ žßÄžĻ®žĚÄ 2001-2004ŽÖĄÍĻĆžßÄŽäĒ žú†ŽüĹ žßÄžĻ®Í≥ľ Žßąžį¨ÍįÄžßÄŽ°ú žúĄŪóėŽŹĄžóź ŽĒįŽĚľ ŪôėžěźÍĶįžĚĄ ŽāėŽąĄžóąžúľŽ©į žúĄŪóėŽŹĄŽ•ľ žłĶŪôĒŪē† ŽēĆ žúĄŪóėžĚłžěź(risk factor)žĚė žĘÖŽ•ėžôÄ ÍįúžąėŽ•ľ Íłįž§ÄžúľŽ°ú ŪēėžėÄŽč§. ŪēėžßÄŽßĆ 2013ŽÖĄ žßÄžĻ®Ž∂ÄŪĄį žúĄŪóėŽŹĄ žłĶŪôĒŽ≥īŽč§ŽäĒ Í≥†žúĄŪóė ŪôėžěźÍĶįžĚĄ Ž™á ÍĶį žßÄž†ēŪēėžó¨ ž†ĀÍ∑Ļž†ĀžĚł žßÄžßąÍįēŪēė žĻėŽ£ĆŽ•ľ Í∂ĆÍ≥†ŪēėÍ≥† žěąŽč§: žó¨ÍłįžóźŽäĒ 1) žĚīžį® žėąŽį©žóź ŪēīŽčĻŽźėŽäĒ žěĄžÉĀž†Ā ž£ĹžÉĀÍ≤ĹŪôĒžĄĪ žč¨ŪėąÍīÄ žßąŪôė(atherosclerotic cardiovascular disease, ASCVD) Ūôėžěź, 2) LDL-CÍįÄ 190 mg/dL žĚīžÉĀžĚł žč¨Ūēú Í≥†žĹúŽ†ąžä§ŪÖĆŽ°§Ūėąž¶Ě Ūôėžěź, 3) ŽčĻŽá®Ž≥Ď Ūôėžěź, 4) pooled cohort equation (PCE)žúľŽ°ú Í≥ĄžāįŪēú žč¨ŪėąÍīÄ žúĄŪóėŽŹĄÍįÄ ŽÜížĚÄ ŪôėžěźÍįÄ ŪŹ¨Ūē®ŽźúŽč§. 2018ŽÖĄ žĶúžč† žßÄžĻ®žóźžĄúŽäĒ žĚīŽüį Í≥†žúĄŪóė ŪôėžěźÍĶįžĚė ŽľąŽĆÄŽäĒ žú†žßÄŪēėžėÄžúľŽāė, 1) ASCVD ŪôėžěźÍĶįžóź ŽĆÄŪēú ž∂ĒÍįÄž†ĀžúľŽ°ú žłĶŪôĒŪēėžó¨ ‚ÄúžīąÍ≥†žúĄŪóė ASCVDÍĶį‚ÄĚžúľŽ°ú Ž∂ĄŽ•ėŪēėÍ≥† žĚīŽď§žóź ŽĆÄŪēėžó¨ žĻėŽ£Ć Ž™©ŪĎúžĻėŽ•ľ ŽćĒ žóĄÍ≤©ŪēėÍ≤Ć ž†Āžö©ŪēėžėÄÍ≥†, 2) PCEŽ°ú Í≥ĄžāįŪēú žč¨ŪėąÍīÄ žúĄŪóėŽŹĄÍįÄ ž§ĎŽďĪŽŹĄžĚł ŪôėžěźžóźžĄú ž∂ĒÍįÄž†ĀžĚł žúĄŪóėžĚłžěź ž°īžě¨ žó¨Ž∂ÄŽ•ľ Í≥†Ž†§Ūēėžó¨ žēĹŽ¨ľ žĻėŽ£ĆŽ•ľ Í≤įž†ēŪēėŽŹĄŽ°Ě ŪēėžėÄŽäĒŽćį, ž°įÍłą Ž≥Ķžě°ŪēėŽč§[1].
žú†ŽüĹ žßÄžĻ®žĚÄ žúĄŪóėžĚłžěźžôÄ European risk scoring system (SCORE)žĚĄ ÍłįžīąŽ°ú ŪôėžěźÍĶįžĚĄ Ž∂ĄŽ•ėŪēėŽäĒŽćį, Í≥†žúĄŪóėÍĶįžóźžĄúŽäĒ ŽĎė ž§Ď žĖīŽäź ž°įÍĪīžĚĄ žā¨žö©ŪēīŽŹĄ žÉĀÍīÄžóÜŽč§. ŽĄ§ ÍįÄžßÄ ŪôėžěźÍĶįžúľŽ°ú Ž∂ĄŽ•ėŪēėŽäĒŽćį, 1) žīąÍ≥†žúĄŪóėÍĶį ŪėĻžĚÄ SCORE 10ž†ź žĚīžÉĀ, 2) Í≥†žúĄŪóėÍĶį ŪėĻžĚÄ SCORE 5ž†ź žĚīžÉĀ 10ž†ź ŽĮłŽßĆ, 3) SCORE 1ž†ź žĚīžÉĀ 5ž†ź ŽĮłŽßĆ, 4) SCORE 1ž†ź ŽĮłŽßĆžĚīŽč§. žīąÍ≥†žúĄŪóėÍĶįžĚÄ Žč§žĚĆ ž°įÍĪī ž§Ď Ūēú Íįú žĚīžÉĀ Ž≥īžú†žěźžĚłŽćį, žč¨ŪėąÍīÄ žßąŪôė, ŪĎúž†Āžě•Íłį žÜźžÉĀžĚī žěąŽäĒ ŽčĻŽá®Ž≥Ď, ž§Ďž¶Ě ŽßĆžĄĪ žč†žßąŪôė(glomerular filtration rate [GFR] < 30)žĚīŽč§. Í≥†žúĄŪóėÍĶįžĚÄ Žč®žĚľ žúĄŪóėžĚłžěźÍįÄ žč¨Ūēú ž†ēŽŹĄžĚł Í≤Ĺžöį, ŪĎúž†Āžě•Íłį žÜźžÉĀžĚī žóÜŽäĒ ŽčĻŽá®Ž≥ĎžĚė ŽĆĎ觞ąė, ž§ĎŽďĪŽŹĄ ŽßĆžĄĪ žč†žßąŪôė(GFR 30-59)žĚīŽč§. SCOREŽäĒ Í≥ĄžāįŪē† ŽēĆ žĚīžö©ŪēėŽäĒ Ž≥ÄžąėÍįÄ ŽĮłÍĶ≠žĚė ž†ĄŪÜĶž†Ā žúĄŪóėŽŹĄ ž†źžąėžĚł Framningham žúĄŪóėŽŹĄ ž†źžąėŽāė PCEžôÄ ŽĻĄžä∑ŪēėžßÄŽßĆ, ÍįôžßÄŽäĒ žēäŽč§(Table 2) [2].
ŪēúÍĶ≠ žßÄžĻ®žĚÄ žúĄŪóėžĚłžěź žĘÖŽ•ėžôÄ Íįúžąėžóź ŽĒįŽĚľ ŪôėžěźÍĶįžĚĄ Ž∂ĄŽ•ėŪēėŽ©į, 2004ŽÖĄ ŽĮłÍĶ≠ žßÄžĻ®žĚĄ žįłÍ≥†ŪēīžĄú Í≥†žēąŪēėžėÄŽč§. 1) žīąÍ≥†žúĄŪóėÍĶįžĚÄ ž£ĹžÉĀÍ≤ĹŪôĒžĄĪ žč¨ŪėąÍīÄ, ŽáĆŪėąÍīÄ, ŽßźžīąŪėąÍīÄ žßąŪôė, 2) Í≥†žúĄŪóėÍĶįžĚÄ Í≤ĹŽŹôŽß• žßąŪôė, ŽĆÄŽŹôŽß•Ž•ė, ŽčĻŽá®Ž≥Ď, 3) ž§Ďž¶ĚŽŹĄ žúĄŪóėÍĶįžĚÄ žúĄŪóėžĚłžěź 2Íįú žĚīžÉĀ, 4) ž†ÄžúĄŪóėÍĶįžĚÄ žúĄŪóėžĚłžěź 0-1ÍįúžĚł Í≤ĹžöįŽ°ú ž†ēžĚėŪēúŽč§. žĶúžč† žßÄžĻ®ŽĀľŽ¶¨ ŽĻĄÍĶźŪē† Í≤ĹžöįžóźŽäĒ ŽĮłÍĶ≠Ž≥īŽč§ŽäĒ žú†ŽüĹžßÄžĻ®žĚė ÍĶ¨ž°įžóź ŽćĒ ÍįÄÍĻĚŽč§Í≥† Ūē† žąė žěąŽč§.
ŽĮłÍĶ≠ žßÄžĻ®žĚÄ žÉĚŪôúžäĶÍīÄ ÍĶźž†ēžóź ŽĆÄŪēėžó¨ žĄ§Ž™ÖŪēī ŽÜďžēėžúľŽāė, ŪôėžěźÍĶįžóź ŽĒįŽĚľ Žč¨Ž¶¨ ž†Āžö©ŪēėžßÄŽäĒ žēäŽäĒŽč§. žú†ŽüĹ žßÄžĻ®žĚÄ ŪôėžěźÍĶįÍ≥ľ LDL-C žąėžĻėžóź ŽĒįŽĚľ žÉĚŪôúžäĶÍīÄ ÍĶźž†ē žčúžěϞ̥ Í≤įž†ēŪēėŽäĒŽćį, žėąžĽ®ŽĆÄ žīąÍ≥†žúĄŪóėÍĶįžĚÄ LDL-C žąėžĻėžôÄ žÉĀÍīÄžóÜžĚī, Í≥†žúĄŪóėÍĶįžĚÄ LDL-C 70Ž∂ÄŪĄį, ž§ĎŽďĪŽŹĄ žúĄŪóėÍĶįžĚÄ LDL-C 100Ž∂ÄŪĄį, ž†ÄžúĄŪóėÍĶįžĚÄ LDL-C 190Ž∂ÄŪĄįžĚīŽč§. ŪēúÍĶ≠ žßÄžĻ®žóźžĄúŽäĒ žēĹŽ¨ľ žĻėŽ£Ć žčúžěĎž†źžĚÄ ŪôėžěźÍĶįŽßąŽč§ Žč§Ž•īžßÄŽßĆ, žÉĚŪôúžäĶÍīÄ ÍĶźž†ēžĚÄ Ūôėžěź ž†Ąž≤īžóź Í∂ĆÍ≥†ŪēėÍ≥† žěąŽč§. žÉĚŪôúžäĶÍīÄ ÍĶźž†ēžĚÄ ŪĀ¨Í≤Ć žčĚžā¨ ž°įž†ąÍ≥ľ žöīŽŹôžúľŽ°ú ÍĶ¨žĄĪŽźėŽäĒŽćį, žó¨ÍłįžóźŽäĒ žó≠ŽĆÄ ŽĮłÍĶ≠ žčĚžā¨ žßÄžĻ®žĚĄ žÜĆÍįúŪēúŽč§. ŽĮłÍĶ≠ žčĚžā¨ žßÄžĻ®žĚÄ Íįúž†ē ŽēĆŽßąŽč§ žēĹÍįĄžĒ© žąėž†ēŽźėžóąŽäĒŽćį, ŪēĶžč¨ž†ĀžĚł Žāīžö©žĚĄ ž†ēŽ¶¨ŪēėžėÄŽč§(Table 3). Žč®, ŪēúÍĶ≠žĚłŽď§žĚė žčĚžā¨ Žāīžö©žĚī žĄúÍĶ¨žôÄ žÉĀŽčĻŪěą Žč§Ž•īÍ≥†, žĄłŽĆÄŽ≥Ą žį®žĚīŽŹĄ ŪĀī žąė žěąžúľŽĮÄŽ°ú žč§ž†ú žßĄŽ£ĆžčúžóźŽäĒ ŪôėžěźŽßąŽč§ ÍįúŽ≥ĄŪôĒŽźú ÍĶźžú°Í≥ľ Í∂ĆÍ≥†Ž•ľ ŪēėŽäĒ Í≤ÉžĚī ŪēĄžöĒŪē† Í≤ÉžĚīŽč§.
žĖłÍłČŪēėžėĎ觞čúŪĒľ ŽĮłÍĶ≠ žßÄžĻ®žĚÄ žēĹŽ¨ľ žĻėŽ£Ć ŽĆÄžÉĀ ŪôėžěźÍĶįžĚĄ žúĄŪóėŽŹĄžóź ŽĒįŽĚľ žĚīŽ¶ĄžĚĄ Ž∂ôžĚīžßÄ žēäžúľŽ©į, žĻėŽ£Ć ŽĆÄžÉĀ ŪôėžěźÍĶįžóźžĄúŽäĒ žēĹŽ¨ľ žĻėŽ£ĆŽ•ľ žčúžěĎŪēėŽäĒ LDL-C žąėžĻėÍįÄ ŽĒįŽ°ú žóÜŽč§. ž¶Č, LDL-C žąėžĻėÍįÄ ŽāģŽćĒŽĚľŽŹĄ ŪēīŽčĻ ŪôėžěźÍĶįžóźžĄúŽäĒ žēĹŽ¨ľ žĻėŽ£ĆŽ•ľ Í∂ĆÍ≥†ŪēėÍ≥† žěąŽč§. ŽįėŽĆÄŽ°ú žú†ŽüĹÍ≥ľ ŪēúÍĶ≠žĚÄ ŪôėžěźÍĶįžĚĄ žúĄŪóėŽŹĄŽ•ľ ÍłįžīąŽ°ú ŪôėžěźÍĶį žĚīŽ¶ĄžĚĄ Ž∂ôžĚīŽ©į, žúĄŪóėÍĶįžóź ŽĒįŽĚľžĄú žēĹŽ¨ľ žĻėŽ£Ć žčúžěĎž†źžĚĄ ž†ēŪēī ŽÜďžēėŽäĒŽćį, žĚī žł°Ž©īžĚÄ žú†ŽüĹÍ≥ľ ŪēúÍĶ≠ žßÄžĻ®žĚī žÉĀŽčĻŪěą ŽĻĄžä∑ŪēėŽč§. žėąžĽ®ŽĆÄ, žú†ŽüĹ žßÄžĻ®žóźžĄúŽäĒ žīąÍ≥†žúĄŪóėÍĶįžóźžĄú LDL-C 70 žĚīžÉĀžóźžĄú žēĹŽ¨ľ žĻėŽ£ĆŽ•ľ žčúžěĎŪēėŽ©į < 70žĚł Í≤Ĺžöį žēĹŽ¨ľ žĻėŽ£ĆŽäĒ Í≥†Ž†§ÍįÄŽä•ŪēėŽč§Í≥†(žĄ†ŪÉĚžā¨Ūē≠) ŽźėžĖī žěąŽč§. Í≥†žúĄŪóėÍĶįžóźžĄúŽäĒ 100 žĚīžÉĀŽ∂ÄŪĄį žēĹŽ¨ľ žĻėŽ£ĆŽ•ľ Í∂ĆÍ≥†ŪēėŽ©į < 100žĚł Í≤Ĺžöį žēĹŽ¨ľ žĻėŽ£ĆŽäĒ žĄ†ŪÉĚžā¨Ūē≠žĚīŽč§. žīąÍ≥†žúĄŪóėÍĶįÍ≥ľ Í≥†žúĄŪóėÍĶįžóźžĄú ŪēúÍĶ≠ žßÄžĻ®žĚė žēĹŽ¨ľ žĻėŽ£Ć žčúžěĎž†źžĚÄ žú†ŽüĹÍ≥ľ ÍįôŽč§. ŪēúÍĶ≠ žßÄžĻ®žóźžĄú ž§ĎŽďĪŽŹĄžôÄ ž†ÄžúĄŪóėÍĶįžĚÄ LDL-CÍįÄ ÍįĀÍįĀ 130, 160 žĚīžÉĀžĚľ ŽēĆ žēĹŽ¨ľ žĻėŽ£ĆŽ•ľ Í∂ĆÍ≥†ŪēúŽč§. Í∑łŽü¨Žāė žú†ŽüĹ žßÄžĻ®žóźžĄúŽäĒ ž§ĎŽďĪŽŹĄžôÄ ž†ÄžúĄŪóėÍĶį Ž™®ŽĎźžóźžĄú žēĹŽ¨ľžĻėŽ£ĆŽäĒ žĄ†ŪÉĚ žā¨Ūē≠žĚīŽ©į žĚīÍ≤ÉŽŹĄ LDL-CÍįÄ ÍįĀÍįĀ 100Í≥ľ 190 žĚīžÉĀžĚľ ŽēĆŽ°ú ž†úŪēúŪēėŽäĒ Í≤ÉžúľŽ°ú Ž≥īžēĄ žú†ŽüĹ žßÄžĻ®žóźžĄúŽäĒ ž§ĎŽďĪŽŹĄ žĚīŪēėžóźžĄúŽäĒ žēĹŽ¨ľžĚĄ Žćú žďįŽ†§Í≥† ŪēėŽäĒ Í≤ÉžĚī ŪäĻžßēžĚīŽč§(Table 4).
ŽĮłÍĶ≠ žßÄžĻ®žĚÄ žĚīž†ĄŪĆź(2013ŽÖĄ)žóźžĄú LDL-CžĚė žĻėŽ£Ć Ž™©ŪĎúžĻėŽ•ľ ŽöúŽ†∑ŪēėÍ≤Ć ž†úžčúŪēėžßÄŽäĒ žēäžēėžúľŽāė, žä§ŪÉÄŪčī ÍįēŽŹĄŽ•ľ Í≥†ÍįēŽŹĄ, ž§ĎÍįĄ ÍįēŽŹĄ ŽďĪžúľŽ°ú ŽāėŽąĄžĖī ÍįĀÍįĀžĚė ÍįēŽŹĄŽ•ľ žďł Í≤Ĺžöį LDL-CÍįÄ 50% žĚīžÉĀ ŽėźŽäĒ 30% žĚīžÉĀ ÍįēŪēėŽź† Í≤ÉžúľŽ°ú žėąžÉĀŪēėžėÄŽč§. ŽĮłÍĶ≠ žßÄžĻ®žĚė žĶúžč†ŪĆź(2018ŽÖĄ)žóźžĄúŽäĒ žä§ŪÉÄŪčī ÍįēŽŹĄžĚė Ž∂ĄŽ•ėŽ•ľ žú†žßÄŪēėžó¨ Ž™áŽ™á ŪôėžěźÍĶįžóźžĄú ÍįĀÍįĀžĚė ÍįēŽŹĄžóź ŽĒįŽ•ł LDL-C ÍįēŪēėžú®žĚĄ ž†úžčúŪēėŽäĒ ŽŹôžčúžóź, Žč§Ž•ł žßÄžĻ®žóźžĄú žīąÍ≥†žúĄŪóėÍĶįžúľŽ°ú Ž∂ĄŽ•ėŽźėŽäĒ ASCVD Ūôėžěźžóź ŽĆÄŪēīžĄúŽäĒ 2013ŽÖĄ ŪĆźžóź žóÜžóąŽćė LDL-C žĻėŽ£Ć Ž™©ŪĎúžĻėžĚł < 70žĚĄ ŽźėžāīŽ†§ŽÉąŽč§. ŪĚ•ŽĮłŽ°úžöī ž†źžĚÄ žĚī Ž™©ŪĎúžĻėžóź ŽĮłŽč¨Žźú ŪôėžěźŽ•ľ ž§Ďžč¨žúľŽ°ú ŽĻĄžä§ŪÉÄŪčīÍ≥Ą žēĹŽ¨ľžĚł žóźž†úŪčįŽĮłŽłĆžôÄ PCSK9 žĖĶž†úž†ú Í∂ĆÍ≥†ÍįÄ ž∂ĒÍįÄŽźú Í≤ÉžĚīŽč§. žú†ŽüĹ žßÄžĻ®žĚÄ LDL-C žĻėŽ£Ć Ž™©ŪĎúžĻėŽ•ľ ž†ĄŪÜĶž†Ā ŪėēžčĚžúľŽ°ú ŪŹ¨Ūē®ŪēėÍ≥† žěąžúľŽ©į ŽĻĄÍĶźž†Ā Žč®žąúŪēúŽćį, žīąÍ≥†žúĄŪóėÍĶįžóźžĄú < 70Í≥ľ 50% ÍįēŪēė ŽŹôžčú Žč¨žĄĪ, Í≥†žúĄŪóėÍĶįžóźžĄú < 100Í≥ľ 50% ÍįēŪēė ŽŹôžčú Žč¨žĄĪ, ž§ĎŽďĪŽŹĄ žĚīŪēė žúĄŪóėÍĶįžóźžĄúŽäĒ < 115Ž•ľ ž†úžčúŪēėÍ≥† žěąŽč§. ŪēúÍĶ≠žĚÄ žú†ŽüĹ žßÄžĻ®Í≥ľ ŽĻĄžä∑ŪēėžßÄŽßĆ LDL-C žąėžĻėŽßĆ ž†úžčúŪēėŽ©į, žīąÍ≥†žúĄŪóėÍĶį, Í≥†žúĄŪóėÍĶį, ž§ĎŽďĪŽŹĄ žúĄŪóėÍĶį, ž†ÄžúĄŪóėÍĶįžóźžĄú ÍįĀÍįĀ < 70, < 100, < 130, < 160žĚĄ Ž™©ŪĎúŽ°ú ŪēėÍ≥† žěąŽč§(Table 5).
ŽĮłÍĶ≠ žßÄžĻ®žĚī ŽįĒŽ°ú ž†ĄŪĆź(2013ŽÖĄ)žóźžĄúŽäĒ žä§ŪÉÄŪčī žôłžĚė žēĹŽ¨ľžĚĄ ž†Ąž†ĀžúľŽ°ú ž†úžôłŪēėžėÄžóąŽäĒŽćį, žĚīŽ≤ą ŪĆź(2018ŽÖĄ)žóźŽäĒ žä§ŪÉÄŪčī ÍīÄŽ†® Žāīžö©žĚī ŽĆÄŽ∂ÄŽ∂ĄžĚīÍłįŽäĒ ŪēėžßÄŽßĆ žĚľŽ∂Ä žÉĀŪô©žóź žóźž†úŪčįŽĮłŽłĆžôÄ PCSK9 žĖĶž†úž†úŽ•ľ Í∂ĆÍ≥†ŪēėÍ≥† žěąŽč§. ÍįĀ žßÄžĻ®žóźžĄúŽäĒ ÍłįŽ≥łž†ĀžúľŽ°ú LDL-C žĻėŽ£Ć Ž™©ŪĎúŽ•ľ Žč¨žĄĪŪēėÍłį žúĄŪēīžĄú ŽāīžēĹ ÍįÄŽä•Ūēú žĶúÍ≥†žö©ŽüČ žä§ŪÉÄŪčī žā¨žö©žĚĄ Í∂ĆÍ≥†ŪēėŽ©į, žä§ŪÉÄŪčī Ž∂ÄžěĎžö©žĚī ŽįúžÉĚŪēėÍĪįŽāė žĶúÍ≥† žö©ŽüȞ̥ žďįÍ≥†ŽŹĄ Ž™©ŪĎúžĻė Žč¨žĄĪžóź žč§ŪĆ®Ūēú Í≤Ĺžöį žóźž†úŪčįŽĮłŽłĆ, Žčīž¶ôžāį žąėžßÄŽ•ľ žä§ŪÉÄŪčīžóź Ž≥ĎŪē© ŪėĻžĚÄ Žč®ŽŹÖ Ūą¨žó¨ŪēėŽäĒ Í≤ɞ̥ žõźžĻôžúľŽ°ú ŪēúŽč§. Žč®, žīąÍ≥†žúĄŪóėÍĶį ŪôėžěźžóźžĄú Ž™©ŪĎúžĻė Žč¨žĄĪžóź žč§ŪĆ®Ūē† Í≤Ĺžöį žä§ŪÉÄŪčīžóź PCSK9 žĖĶž†úž†úŽ•ľ Ž≥ĎŪē© Ūą¨žó¨ŪēėŽäĒ Í≤ÉžĚÄ žĄ†ŪÉĚ žā¨Ūē≠žúľŽ°ú ŪŹ¨Ūē®ŽźúŽč§. žĚīŽüį žā¨Ūē≠Žď§žĚÄ ŽĮłÍĶ≠, žú†ŽüĹ, ŪēúÍĶ≠ žßÄžĻ®žóź ŽĆÄž≤īž†ĀžúľŽ°ú Í≥ĶŪÜĶž†ĀžĚłŽćį, ŽĮłÍĶ≠ žßÄžĻ®žĚÄ žēĹž†ú Í∂ĆÍ≥†žóź ŽĆÄŪēú žĄ§Ž™ÖžĚī Žč§žÜĆ ž†ĀŽč§(Table 6). Í≥†ž§ĎžĄĪžßÄŽį©Ūėąž¶Ěžóź ŽĆÄŪēú ž°įž†ą žēĹž†úŽäĒ Ž≥ł Í≥†žóźžĄúŽäĒ žěźžĄłŪěą Žč§Ž£®žßÄ žēäÍ≤†Žč§.
žĶúÍ∑ľ Íĺłž§ÄŪěą ž¶ĚÍįÄŪēėŽäĒ ŪôėžěźÍĶį ž§Ď ŽĆÄŪĎúž†ĀžúľŽ°ú ŽÖłžĚłÍ≥ľ ŽßĆžĄĪ žč†žßąŪôė ŪôėžěźÍįÄ žěąŽč§. žĚī ŽĎź ž°įÍĪīžĚÄ žč¨ŪėąÍīÄ žúĄŪóėŽŹĄžĚė ž£ľžöĒ žúĄŪóė žĚłžěźžĚīŽ©į, žĚľžį®žėąŽį© ŽĆÄžÉĀžĚľ Í≤Ĺžöį žĚīŽ°†ž†ĀžúľŽ°ú ž†ĀÍ∑Ļž†Ā žßÄžßą ÍįēŪēė žĻėŽ£ĆÍįÄ ŪēĄžöĒŪēėŽč§Í≥† Ūē† žąė žěąŽč§. ŪēėžßÄŽßĆ žĚī ŽĎź ŪôėžěźÍĶįžĚÄ žó¨Žü¨ ÍįÄžßÄ žĚīžú†Ž°ú žĚłŪēėžó¨, žēĹŽ¨ľžĻėŽ£Ć žĚīŽďĚžóź ŽĆÄŪēú žěĄžÉĀžčúŪóė ž¶ĚÍĪįÍįÄ ŽßéžßÄ žēäŽč§. ŽėźŪēú žĚīŽď§žĚÄ Žč§žĖĎŪēú žßąŪôėžĚī ŪĚĒŪěą ŽŹôŽįėŽźėŽ©į Žč§žēĹž†ú Ž≥Ķžö© ÍįÄŽä•žĄĪŽŹĄ ŽÜíÍłį ŽēĆŽ¨łžóź, žēĹŽ¨ľ Ž∂ÄžěĎžö© ŽĻąŽŹĄŽŹĄ ŽÜížēĄžßą žąė žěąžĖīžĄú žĻėŽ£Ć žĚīŽď̞󟞥ú žĻėŽ£Ć žúĄŪēīŽ•ľ ŽļÄ žč§žĚīŽďĚ(net benefit)žĚī Ž≥ĄŽ°ú žóܞ̥ žąėŽŹĄ žěąÍłį ŽēĆŽ¨łžóź žč¨Ūēú Í≥†Ž†Ļ ŽďĪžóźžĄúŽäĒ ž†ĀÍ∑Ļž†ĀžĚł žßÄžßąÍįēŪēė žĻėŽ£Ćžóź žĚėŽ¨łžĚĄ ž†úÍłįŪēėÍłįŽŹĄ ŪēúŽč§. ŪēúŪéł, Ūą¨žĄĚ ž§ĎžĚł ŽßĆžĄĪ žč†žßąŪôė Ūôėžěźžóź ŽĆÄŪēú Ž™á ÍįÄžßÄ žóįÍĶ¨žóźžĄúŽäĒ žĻėŽ£Ć žĚīŽďĚžĚī ŽāėŪÉÄŽāėžßÄ žēäžēĄžĄú, Ūą¨žĄĚ ž§ĎžĚł ŪôėžěźžóźžĄúŽäĒ žä§ŪÉÄŪčī Ž≥Ķžö©žĚĄ žÉąŽ°ú žčúžěĎŪēėŽäĒ Í≤ɞ̥ Í∂ĆÍ≥†ŪēėžßÄ žēäŽäĒŽč§.
ŪēúÍĶ≠žĚłžóźžĄú žßÄžßąÍįēŪēė žĻėŽ£ĆŽ•ľ ŪēėžėĞ̥ ŽēĆ žĖĽžĚĄ žąė žěąŽäĒ žĚīŽďĚžĚī ŽĮłÍĶ≠žĚīŽāė žú†ŽüĹ žā¨ŽěĆŽď§Í≥ľ ÍįôžĚĄžßÄ, Žč§Ž•ľžßÄžóź ŽĆÄŪēú ž†ēŪôēŪēú žěźŽ£ĆŽäĒ žóÜŽč§. Žč®, ŽĮłÍĶ≠žĚīŽāė žú†ŽüĹžĚė žúĄŪóėŽŹĄ ž†źžąėÍįÄ ŪēúÍĶ≠žĚłžóźžĄú žč¨ŪėąÍīÄ žúĄŪóėŽŹĄŽ•ľ Í≥ľŽĆÄŪŹČÍįÄŪē† žąė žěąŽč§ŽäĒ Ž≥īÍ≥†ÍįÄ žěąÍłį ŽēĆŽ¨łžóź[5], ŪäĻŪěą žĚľžį®žėąŽį© ŽĆÄžÉĀžěźžóźžĄú žßÄžßąÍįēŪēė žĻėŽ£ĆžĚė ž†ąŽĆÄžĚīŽďĚžĚī žÉĀŽĆÄž†ĀžúľŽ°ú žěϞ̥ ÍįÄŽä•žĄĪžĚÄ žěąŽč§. ŪēúŪéł žĄúžĖĎ žā¨ŽěĆŽ≥īŽč§ ŽćĒ žēĹŪēú ÍįēŽŹĄžĚė žä§ŪÉÄŪčīžĚĄ Ūą¨žó¨ŪēėžėĞ̥ ŽēĆ žßÄžßąÍįēŪēėŽāė žěĄžÉĀž†Ā žĚīŽďĚžĚī ŽĻĄžä∑Ūē† Í≤ÉžĚīŽĚľŽäĒ ž∂Ēžł°žĚÄ žěąžúľŽāė žó≠žčú ž¶ĚÍĪįŽäĒ Ž∂Äž°ĪŪēėŽč§. Žč®, žĶúžč† ŽĮłÍĶ≠ žßÄžĻ®žóźžĄúŽŹĄ žĚľŽ≥ł ŽďĪ ŽŹôžēĄžčúžēĄžĚłžóźžĄú žēĹŽ¨ľ žĻėŽ£Ć Ž∂ÄžěĎžö©žĚĄ ž°įžč¨ŪēėŽĚľŽäĒ žĖłÍłČžĚī žěąÍłį ŽēĆŽ¨łžóź[1], ŪēúÍĶ≠žĚłžóźžĄú Ūôėžěź ÍįúžĚł ŪäĻžĄĪžĚĄ Í≥†Ž†§Ūēėžó¨ žä§ŪÉÄŪčī žö©ŽüȞ̥ žÜĆŪŹ≠ ž§ĄžĚīŽäĒ Í≤ÉŽŹĄ Í≥†Ž†§Ūē† žąė žěąžĚĄ Í≤ÉžĚīŽč§.
ž£ľžöĒ žßÄžĻ®ŽßąŽč§ žēĹÍįĄ žį®žĚīŽäĒ žěąžúľŽāė, žĶúžč† žßÄžĻ®žóźžĄúŽäĒ ŽčĻŽá®Ž≥ĎžĚÄ ž°įÍĪī žóÜžĚī ŪėĻžĚÄ LDL-C 100 žĚīžÉĀŽ∂ÄŪĄį žēĹŽ¨ľ žĻėŽ£ĆŽ•ľ ŪēėŽĚľŽäĒ Í≤ÉžĚī ŪÜĶžÉĀž†ĀžĚł Í∂ĆÍ≥†žā¨Ūē≠žĚīŽč§. ŪēėžßÄŽßĆ ÍĶ≠Žāī žěźŽ£ĆŽ•ľ Ž≥īŽ©ī ŽčĻŽá®Ž≥Ď ŪôėžěźžóźžĄú žä§ŪÉÄŪčī ž≤ėŽį©Ž•†žĚÄ žßÄžĻ®žóź ŽĒįŽ•ł ŽĆÄžÉĀ Ūôėžěźžóź Ūõ®žĒ¨ Ž™Ľ ŽĮłžĻúŽč§Í≥† Ž≥īÍ≥†ŽźúŽč§[6]. ŽčĻŽá®Ž≥Ď Ūôėžěźžóź ŽĆÄŪēú žĚī žĻėŽ£Ć ÍįĄÍ∑ĻžĚī žßÄžßąÍįēŪēė žĻėŽ£ĆžóźžĄú ŪĚĒŪēú Ž¨łž†ú ž§Ď ŪēėŽāėŽ°ú Ž≥īžĚłŽč§.
IMPROVE-IT žóįÍĶ¨žóźžĄú žä§ŪÉÄŪčī/žóźž†úŪčįŽĮłŽłĆ Ž≥ĶŪē©ž†úžĚė žěĄžÉĀž†Ā žĚīŽďĚžĚī žĶúžīąŽ°ú Ž≥īÍ≥†ŽźėÍ≥†, žĚīŪõĄ žä§ŪÉÄŪčī/žóźž†úŪčįŽĮłŽłĆ Ž≥ĶŪē©ž†úÍįÄ žó¨Žü¨ ÍįÄžßÄ ž∂ĒÍįÄŽ°ú ž∂úžčúŽźėŽ©īžĄú ÍĶ≠ŽāīžóźžĄúŽŹĄ žĚīŽüį ž†úŪėēžóź ŽĆÄŪēú ž≤ėŽį©žĚī ŽäėžĖīŽāėÍ≥† žěąŽč§. ŪēėžßÄŽßĆ žĶúžč† žßÄžĻ®Žď§žóźžĄú Ž≥īŽďĮžĚī žßÄžßąÍįēŪēė žĻėŽ£ĆžóźžĄú žĚľžį®ž†Ā Í∂ĆÍ≥† žēĹž†úŽäĒ žä§ŪÉÄŪčīžĚīŽ©į, Í≥†žö©ŽüČ žä§ŪÉÄŪčīžúľŽ°úŽŹĄ Ž™©ŪĎúžĻėžóź ŽŹĄŽč¨ŪēėžßÄ Ž™ĽŪēėÍĪįŽāė Ž∂ÄžěĎžö© Í≤ĹŪóėžěźžóźžĄú Ž≥ĎŪē©žöĒŽ≤ēžĚĄ žā¨žö©ŪēėŽäĒ Í≤ÉžĚī ŽįĒŽěĆžßĀŪēėŽč§ŽäĒ Í≤ɞ̥ ÍłįžĖĶŪē† ŪēĄžöĒÍįÄ žěąŽč§.
žē장ú žĖłÍłČŪēėžėÄžßÄŽßĆ žßÄžßąÍįēŪēėžĚė žĻėŽ£Ć ŪēĄžöĒžĄĪÍ≥ľ Í∑ł ÍįēŽŹĄŽäĒ ÍįúŽ≥ĄŪôėžěźžĚė žč¨ŪėąÍīÄ žúĄŪóėŽŹĄžóź ŽĒįŽĚľ Í≤įž†ēŽźėŽ©į, ŽĆÄŪĎúž†ĀžúľŽ°ú Í≥†ÍįēŽŹĄ žä§ŪÉÄŪčīžĚī ŪēĄžöĒŪēú ŪôėžěźÍĶįžĚÄ žč¨ŪėąÍīÄ žßąŪôė(ŪėϞ訞¶Ě, žč¨Í∑ľÍ≤ĹžÉČž¶Ě, ŪóąŪėąžĄĪ ŽáĆž°łž§Ď ŽďĪ) Í≥ľÍĪįŽ†•žĚī žěąŽäĒ ŪôėžěźžĚīŽč§. ÍįĄŪėĻ ž†Äžö©ŽüČ žä§ŪÉÄŪčīŽßĆ Ž≥Ķžö©Ūēėžó¨ŽŹĄ LDL-C žĻėŽ£Ć Ž™©ŪĎúžĻėžóź žČĹÍ≤Ć ŽŹĄŽč¨ŽźėžóąŽč§ÍĪįŽāė žč¨žßÄžĖī žēŞ̥ žēą Ž®ĻžĖīŽŹĄ LDL-CÍįÄ < 70žĚł Ūôėžěźžóź ŽĆÄŪēīžĄúŽäĒ Í≥†žö©ŽüČ žä§ŪÉÄŪčī Ž≥Ķžö©žĚī ÍļľŽ†§žßą žąė žěąžúľŽ©į, žč§ž†ú žßĄŽ£ĆžóźžĄúŽŹĄ žĚīŽüį žĚľžĚī ž†ĀžßÄ žēäžĚĄ Í≤ÉžĚīŽč§. ŪēėžßÄŽßĆ ŽßéžĚÄ žěĄžÉĀžčúŪóėžóź ÍłįžīąŪēú žĶúžč† žßÄžĻ®žóźžĄú žĚīŽüį ŪôėžěźžóźžĄú LDL-C žąėžĻėžôÄ ÍīÄÍ≥ĄžóÜžĚī Í≥†ÍįēŽŹĄ žä§ŪÉÄŪčīžĚĄ Í∂ĆÍ≥†ŪēėÍ≥† žěąŽäĒŽćį, ŽĒįŽĚľžĄú žĻėŽ£Ćžóź ŽĒįŽ•ł ŪôėžěźžĚė žĚīŽď̞̥ žúĄŪēėžó¨ Íľ≠ žĚīŽ•ľ ŽĒįŽ•īŽäĒ Í≤ÉžĚī žĘčžúľŽ¶¨ŽĚľ žÉĚÍįĀŽźúŽč§.
žßÄžßąÍįēŪēė žĻėŽ£ĆŽäĒ žč¨ŪėąÍīÄ žßąŪôėžĚė žĚľ, žĚīžį® žėąŽį©žĚė ŪēĶžč¨žĚīŽ©į, ÍĶ≠Žāīžôł žĶúžč† žßÄžĻ®žĚė ž£ľžöĒ žā¨Ūē≠žĚĄ žąôžßÄŪēėŽäĒ Í≤ÉžĚī žĘčŽč§. Í≥†žúĄŪóėÍĶįžóźžĄú ÍįēŪēú žĻėŽ£ĆŽ•ľ ŪēėŽ©ī žěĄžÉĀž†Ā žĚīŽďĚžĚī ŪĀ¨Žč§ŽäĒ žõźžĻôžĚĄ ÍłįžīąŽ°ú Ūēėžó¨ žĚľžį® žēĹŽ¨ľŽ°ú žä§ŪÉÄŪčīžĚĄ žā¨žö©ŪēėÍ≤Ć ŽźėŽ©į, Í≤Ĺžöįžóź ŽĒįŽĚľ ŽĻĄžä§ŪÉÄŪčī žēĹŽ¨ľžĚĄ Ž≥ĎŪē©Ūē† žąė žěąŽč§. ŪäĻž†ē ŪôėžěźÍĶįžĚė žĻėŽ£ĆŽį©žĻ®žĚĄ ÍłįžĖĶŪēėÍ≥† ŪĚĒŪěą žÉĚÍłł žąė žěąŽäĒ žė§Ž•ėžóź ž£ľžĚėŪēėŽ©ī ŪôėžěźžóźÍ≤Ć ŽćĒ ŽßéžĚÄ ŽŹĄžõĞ̥ ž§Ą žąė žěąžĚĄ Í≤ÉžĚīŽč§.
REFERENCES
1. Grundy SM, Stone NJ, Bailey AL, et al. 2018 AHA/ACC/AACVPR/AAPA/ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA guideline on the management of blood cholesterol: a report of the american college of cardiology/american heart association task force on clinical practice guidelines. Circulation 2019;139:e1082‚Äďe1143.
2. Catapano AL, Graham I, De Backer G, et al. 2016 ESC/EAS guidelines for the management of dyslipidaemias. Eur Heart J 2016;37:2999‚Äď3058.


3. Rhee EJ, Kim HC, Kim JH, et al. 2018 guidelines for the management of dyslipidemia. Korean J Intern Med 2019;34:723‚Äď771.

4. Grundy SM, Cleeman JI, Merz CN, et al. Implications of recent clinical trials for the national cholesterol education program adult treatment panel III guidelines. Circulation 2004;110:227‚Äď239.


The need for stratified lipid-lowering therapy is based on the relationship between higher cardiovascular risk, aggressive lipid-lowering therapy, and greater absolute clinical benefit. In this figure, the more centrally located patient group has a higher cardiovascular risk and obtains more clinical benefit from lipid-lowering therapy. DM, diabetes mellitus.
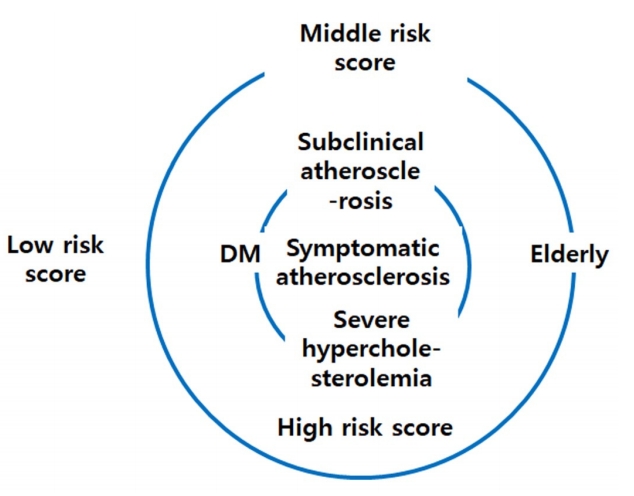
Figure 1.
Table 1.
Major points of the latest US, European, and Korean guidelines for lipid-lowering therapy
Table 2.
Risk stratification of the latest guidelines
| 2018 American | 2016 European | 2018 Korean | |
|---|---|---|---|
| Major points | Specific patient groups for LLT | Combination of specific patient groups and risk score for LLT | Specific patient groups or number of risk factors for LLT |
| Very high- risk groupa | -- | CVD, DM with target organ damage, severe CKD, or SCORE ‚Č• 10% | CAD, atherosclerotic ischemic stroke or TIA, and PAD |
| High risk groupa | -- | Markedly elevated single RFs, most other DM, moderate CKD, or SCORE > 5% and < 10% | Carotid artery disease, abdominal aortic aneurysm, DM |
| Moderate risk group | -- | SCORE ‚Č• 1% and < 5% | Number of RFs ‚Č• 2 |
| Low risk group | -- | SCORE < 1% | Number of RFs 0‚Äď1 |
Table 3.
American diet recommendations
Table 4.
Starting points for pharmacological treatments in the latest guidelines
Table 5.
LDL-C target value
| 2018 American | 2016 European | 2018 Korean | |
|---|---|---|---|
| Major points | Suggests statin intensity rather than specific LDL-C targets except for ASCVD; < 70 for ASCVD | Depending on the risk category | Depending on the risk category |
| Very high risk groupa | -- | < 70 plus 50% reduction | < 70 |
| High risk groupa | -- | < 100 plus 50% reduction | < 100 |
| Moderate risk group | -- | < 115 | < 130 |
| Low risk group | -- | < 115 | < 160 |
Table 6.
Recommended levels for pharmacological agents in the latest guidelines
-
METRICS

-
- 1 Crossref
- 0 Scopus
- 21,743 View
- 1,871 Download



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



